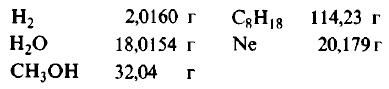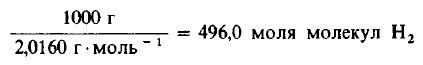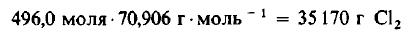материал по химии (8 класс) на тему
Проверить усвоение учащимися понятий о количестве вещества и единицах его измерения: моль, ммоль, кмоль; умение пользоваться периодической системой химических элементов Д.И. Менделеева для определения относительных атомной и молекулярной масс; умение показать взаимосвязь физико – химических величин: массы, количества вещества и числа частиц; развивать навыки учащихся производить расчеты с использованием понятий: количество вещества, молярная масса, молярный объем, постоянная Авогадро; способствовать развитию у школьников интереса к химической наук
- Скачать:
- Предварительный просмотр:
- Задачи на количество вещества 8 класс химия с решением и уравнением
- 1 Определение относительной молекулярной массы Мг
- 2 Определение массовой доли элемента в соединении
- 3 Определение числа молекул в порции вещества
- 4 Определение массы атома в граммах
- 5 Определение молярной массы
- 6 Определение массового отношения элементов в соединении
- 7 Определение объема, который занимает порция газа при н.у.
- 8 Определение теплового эффекта реакции
- 9 Определение максимального выхода продукта реакции
- 10 Определение реального выхода продукта реакции
- 11 Определение выхода продукта по стехиометрическим соотношениям
- 12 Определение содержания основного компонента (или содержания примеси) в исходном веществе
- 13 Определение выхода реакции, когда одно из исходных веществ взято в избытке
- 14 Определение состава газовой смеси (в объемных процентах)
- 15 Определение объема газа, расходуемого на проведение реакции с другими газами
- 16 Определение молекулярной формулы вещества по относительной плотности его паров
- 17 Определение состава газовой смеси
- 18 Определение состава солей в растворе
- 19 Приготовление раствора с заданной массовой долей растворенного вещества
- 20 Приготовление раствора с заданной массовой долей растворенного вещества
- 21 Приготовление раствора с заданной массовой долей растворенного вещества
- 22 Приготовление раствора с заданной массовой долей растворенного вещества
- 23 Приготовление раствора с заданной молярной концентрацией
- 24 Определение формулы органического вещества по данным о массе продуктов реакции
- 25 Определение молекулярной формулы органического вещества по данным о продукте реакции
- 2 Комментарии
- Добавить комментарий Отменить ответ
- Школьные предметы:
- Поиск конспекта
- Новые конспекты
- О проекте
- Задачи на количество вещества 8 класс химия с решением и уравнением
- Урок 5. Моль и молярная масса
- Единица измерения количества вещества
- Молярная масса вещества
- Задачи на количество вещества
Скачать:
| Вложение | Размер |
|---|---|
| kolichestvo_veshchestva.doc | 47 КБ |
Предварительный просмотр:
Решение задач по теме «Количество вещества»
Какова молярная (киломолярная, миллимолярная) масса водорода?
/Ответ: 2 г/моль, 2 кг/кмоль, 2 мг/ммоль./
Сколько молекул водорода содержится в 1моль водорода, в 1кмоль, в 1ммоль?
/Ответ: 6 * 10 23 молекул, 6 * 10 26 молекул, 6 * 10 20 молекул./
Какой объем займут при нормальных условиях 3г водорода? /Ответ: 33,6 л./
Сколько будут весить 12 * 10 20 молекул водорода, 12 * 10 23 молекул,
12 * 10 26 молекул? /Ответ: 4мг, 4г, 4кг./
Какой объем займут 12 * 10 20 молекул водорода, 12 * 10 23 молекул,
12 * 10 26 молекул? / Ответ: 44,8мл, 44,8л, 44,8м 3 ./
Какова молярная (киломолярная, миллимолярная) масса кислорода?
/Ответ: 32г/моль, 32кг/кмоль, 32мг/ммоль./
Сколько молекул кислорода содержится в 2 моль вещества, в 2 кмоль, в 2 ммоль?
/Ответ: 12*10 23 молекул, 12*10 26 молекул, 12*10 20 молекул./
Какой объем займут при н. у. 16г кислорода? /Ответ: 11,2 л/
Какую массу будут иметь 9*10 20 молекул кислорода (9*10 23 , 9*10 26 молекул)?
/Ответ: 48 мг, 48г, 48кг./
Какой объем займут 9*10 20 молекул кислорода (9*10 23 , 9*10 26 молекул)?
/Ответ: 33,6 мл, 33,6 л, 33,6 м 3/ .
Какова миллимолярная, молярная, киломолярная масса озона?
/Ответ : 48 мг/ммоль, 48 г/моль, 48 кг/ кмоль./
Сколько молекул озона содержится в 3 моль его (в 3 ммоль, в 3 кмоль)?
/Ответ: 18*10 23 молекул, 18*10 20 молекул, 18*10 26 молекул./
Какой объем займут при н.у. 48 г озона? /Ответ: 22,4 л./
Какую массу будут иметь 3*10 23 молекул, 3*10 20 молекул, 3*10 26 молекул озона?
/Ответ: 24г, 24 мг, 24кг./
Какой объем займут 6*10 20 молекул, 6*10 23 молекул, 6*10 26 молекул озона?
Задачи на количество вещества 8 класс химия с решением и уравнением
Ключевые слова: решение 25 типовых задач по химии, определение массы, доли, числа,
1 Определение относительной молекулярной массы Мг
Задача Какова относительная молекулярная масса Мг нитробензола С6Н5NO2? Какова молекулярная масса этого вещества в а.е.м.?
2 Определение массовой доли элемента в соединении
Задача Какова масса в граммах 1 атома 131 I ?
3 Определение числа молекул в порции вещества
Задача Сколько молекул воды содержится в 1 капле воды массой 0,03 г?
4 Определение массы атома в граммах
Задача Какова массовая доля фосфора в фосфате кальция Са3(РO4)2 ?
Ответ: ω = 0.2 или 20%
5 Определение молярной массы
Задача Какова молярная масса вещества, если масса 2.5 моль этого вещества равна 250 г?
6 Определение массового отношения элементов в соединении
Задача Каково массовое отношение углерода, водорода и кислорода в глюкозе С6Н1206 ?
7 Определение объема, который занимает порция газа при н.у.
Задача Какой объем (н.у.) занимают 66 г С02?
8 Определение теплового эффекта реакции
Задача Молярная теплота сгорания угля на воздухе 393.5 кДж/моль. Сколько теплоты выделится при полном сгорании 1 кг угля?
9 Определение максимального выхода продукта реакции
Задача Сколько максимально литров (н.у.) водорода можно получить, используя 45.5 г цинка и избыток соляной кислоты?
10 Определение реального выхода продукта реакции
Задача При прокаливании 15,8 г перманганата калия КМnО4 получено 0,896 л (н.у.) кислорода. Каков выход кислорода в данном случае?
11 Определение выхода продукта по стехиометрическим соотношениям
Задача Сколько граммов азотной кислоты HNO3 максимально можно получить из 44.8 л (н.у.) азота?
12 Определение содержания основного компонента (или содержания примеси) в исходном веществе
Задача Каково содержание (в процентах) СаСО3 в образце известняка, при длительном прокаливании 400 г которого получено 78,4 л С02 (н.у.)?
13 Определение выхода реакции, когда одно из исходных веществ взято в избытке
Задача Сколько граммов поваренной соли NaCI можно получить, если смешать два раствора, один из которых содержит 29,2 г HCI, а другой 44 г NaOH?
14 Определение состава газовой смеси (в объемных процентах)
Задача 20 л (н.у.) аммиака пропустили через нагретую до 350°С трубку с железным катализатором. Объем полученной газовой смеси (н.у.) равен 25 л. Каков состав полученной газовой смеси (в объемных процентах) ?
15 Определение объема газа, расходуемого на проведение реакции с другими газами
Задача Какой минимальный объем кислорода, содержащего 10 объемн. % озона, необходим для полного сжигания 4 л пропана С3Н8 ?
16 Определение молекулярной формулы вещества по относительной плотности его паров
Задача Относительная плотность паров углеводорода по воздуху 2,69. Массовая доля водорода в соединении 7,69%. Какова молекулярная формула углеводорода?
17 Определение состава газовой смеси
Задача Относительная плотность 30 л смеси метана СН4 и азота N2 по гелию равна 5. Сколько литров метана и азота взято для приготовления смеси?
18 Определение состава солей в растворе
Задача В растворе смешали 9,8 г H2S04 и 6,5 г NaOH. Какие соли и в каких количествах образовались?
19 Приготовление раствора с заданной массовой долей растворенного вещества
Задача Сколько граммов сахарозы надо растворить в 250 г воды, чтобы получить раствор с массовой долей сахарозы 0,3 (30%)?
20 Приготовление раствора с заданной массовой долей растворенного вещества
Задача : Сколько граммов медного купороса CuS04 • 5Н20 надо добавить к 300 г 2%-го раствора сульфата меди, чтобы получить 5%-ный раствор ?
21 Приготовление раствора с заданной массовой долей растворенного вещества
Задача Сколько миллилитров воды нужно добавить к 100 мл 30%-го раствора соляной кислоты с плотностью 1,15 г/мл, чтобы получить раствор с массовой долей НCl 5%?
22 Приготовление раствора с заданной массовой долей растворенного вещества
Задача Сколько граммов ВаО надо добавить к 100 г воды, чтобы получить 5%-ный раствор?
23 Приготовление раствора с заданной молярной концентрацией
Задача Сколько граммов сульфата натрия Na2S04* 10Н20 необходимо для приготовления 0,5 л раствора с молярной концентрацией 0,02 моль/л?
24 Определение формулы органического вещества по данным о массе продуктов реакции
Задача При полном сгорании 6,0 г органического вещества получено 8,8 г С02 и 3.6 г воды. Плотность паров органического вещества по водороду равна 30. Какова молекулярная формула вещества?
25 Определение молекулярной формулы органического вещества по данным о продукте реакции
Задача При обработке 14,8 г одноосновной карбоновой кислоты избытком цинка получено 2,24 л водорода. Какова молекулярная формула кислоты?
Автор задач: С.С.Бердоносов
Решение 25 типовых задач по химии. Выберите дальнейшие действия:
2 Комментарии
Спасибо! Все задачи решены в одном ключе (используются одни и те же приемы), что ускоряет их понимание и использование.
Благодарю! Помогли вспомнить решение нужной мне задачи. 17. 03 21г.
Добавить комментарий Отменить ответ
Школьные предметы:
Поиск конспекта
Новые конспекты
О проекте
Сайт «УчительPRO» — некоммерческий школьный проект учеников, их родителей и учителей. Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie и других пользовательских данных в целях функционирования сайта, проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт.
Возрастная категория: 12+
(с) 2021 Учитель.PRO — Копирование информации с сайта только при указании активной ссылки на сайт!
Задачи на количество вещества 8 класс химия с решением и уравнением
Урок посвящен закреплению умений производить расчеты по уравнению реакции с учетом количественных соотношений участников реакции.
I. Алгоритмы решения задач по уравнению химических реакций
Внимательно изучите алгоритмы и запишите в тетрадь, решите самостоятельно предложенные задачи
- Используя алгоритм, решите самостоятельно следующие задачи:
1. Вычислите количество вещества оксида алюминия, образовавшегося в результате взаимодействия алюминия количеством вещества 0,27 моль с достаточным количеством кислорода (4Al +3O2=2Al2O3).
2. Вычислите количество вещества оксида натрия, образовавшегося в результате взаимодействия натрия количеством вещества 2,3 моль с достаточным количеством кислорода (4Na+O2=2Na2O).
Алгоритм №1
Вычисление количества вещества по известному количеству вещества, участвующего в реакции
Пример. Вычислите количество вещества кислорода, выделившегося в результате разложения воды количеством вещества 6 моль.
Последовательность выполнения действий
1. Записать условие задачи
2. Вычислить молярные массы веществ,
о которых, идёт речь в задаче
3. Запишем уравнение реакции
и расставим коэффициенты
4. Над формулами веществ запишем
количества веществ из условия задачи,
а под формулами –
стехиометрические коэффициенты,
отображаемые уравнением реакции
5. Для вычисления искомого количества вещества,
6. Записываем ответ
- Используя алгоритм, решите самостоятельно следующие задачи:
1. Вычислите массу серы, необходимую для получения оксида серы (IV) количеством вещества 4 моль (S+O2=SO2).
2. Вычислите массу лития, необходимого для получения хлорида лития количеством вещества 0,6 моль (2Li+Cl2=2LiCl).
Алгоритм №2
Вычисление массы вещества по известному количеству другого вещества, участвующего в реакции
Пример: Вычислите массу алюминия, необходимого для получения оксида алюминия количеством вещества 8 моль.
Последовательность выполнения действий
Оформление решения задачи
1. Записать условие задачи
2. Вычислить молярные массы веществ,
о которых, идёт речь в задаче
3. Запишем уравнение реакции
и расставим коэффициенты
4. Над формулами веществ запишем
количества веществ из условия задачи,
а под формулами –стехиометрические коэффициенты, отображаемые уравнением реакции
5. Вычислим количества вещества, массу которого требуется найти. Для этого составим соотношение.
6. Вычисляем массу вещества, которую требуется найти
7. Записываем ответ
- Используя алгоритм, решите самостоятельно следующие задачи:
1. Вычислите количество вещества сульфида натрия, если в реакцию с натрием вступает сера массой 12,8 г (2Na+S=Na2S).
2. Вычислите количество вещества образующейся меди, если в реакцию с водородом вступает оксид меди (II) массой 64 г (CuO + H2 = Cu + H2O).
Алгоритм №3
Вычисление количества вещества по известной массе другого вещества, участвующего в реакции
Пример. Вычислите количество вещества оксида меди (I), если в реакцию с кислородом вступает медь массой 19,2г.
Последовательность выполнения действий
1. Записать условие задачи
2. Вычислить молярные массы веществ, о которых, идёт речь в задаче
3. Найдём количество вещества, масса которого дана в условии задачи
4. Запишем уравнение реакции
и расставим коэффициенты
5. Над формулами веществ запишем
количества веществ из условия задачи, а под формулами –стехиометрические коэффициенты, отображаемые уравнением реакции
6. Для вычисления искомого количества вещества, составим соотношение
7. Запишем ответ
- Используя алгоритм, решите самостоятельно задачу:
1. Вычислите массу кислорода, необходимую для реакции с железом массой 112 г (3Fe + 4O2=Fe3O4).
Алгоритм №4
Пример. Вычислите массу кислорода, необходимую для сгорания фосфора, массой 0,31г.
Последовательность выполнения действий
1. Записать условие задачи
2. Вычислить молярные массы веществ,
о которых, идёт реь в задаче
3. Найдём количество вещества, масса которого дана в условии задачи
4. Запишем уравнение реакции и расставим коэффициенты
5. Над формулами веществ запишем
количества веществ из условия задачи, а под формулами –стехиометрические коэффициенты, отображаемые уравнением реакции
6. Вычислим количества вещества, массу которого необходимо найти
7. Найдем массу вещeства, которую требуется вычислить
8. Запишем ответ
II. Задачи для самостоятельного решения
1. Вычислите количество вещества оксида алюминия, образовавшегося в результате взаимодействия алюминия количеством вещества 0,27 моль с достаточным количеством кислорода (4Al +3O2=2Al2O3).
2. Вычислите количество вещества оксида натрия, образовавшегося в результате взаимодействия натрия количеством вещества 2,3 моль с достаточным количеством кислорода (4Na+O2=2Na2O).
3. Вычислите массу серы, необходимую для получения оксида серы (IV) количеством вещества 4 моль (S+O2=SO2).
4. Вычислите массу лития, необходимого для получения хлорида лития количеством вещества 0,6 моль (2Li+Cl2=2LiCl).
5. Вычислите количество вещества сульфида натрия, если в реакцию с натрием вступает сера массой 12,8 г (2Na+S=Na2S).
6. Вычислите количество вещества образующейся меди, если в реакцию с водородом вступает оксид меди (II) массой 64 г (CuO + H2 = Cu + H2O).
Урок 5. Моль и молярная масса
В уроке 5 «Моль и молярная масса» из курса «Химия для чайников» рассмотрим моль как единицу измерения количества вещества; дадим определение числу Авогадро, а также научимся определять молярную массу и решать задачи на количество вещества. Базой для данного урока послужат основы химии, изложенные в прошлых уроках, так что если вы изучаете химию с нуля, то рекомендую их просмотреть хотя бы мельком.
Единица измерения количества вещества
До этого урока мы обсуждали лишь индивидуальные молекулы и атомы, а их массы мы выражали в атомных единицах массы. В реальной жизни с индивидуальными молекулами работать невозможно, потому что они ничтожно малы. Для этого химики взвешивают вещества ни в а.е.м., а в граммах.
Чтобы перейти от молекулярной шкалы измерения масс в лабораторную шкалу, используют единицу измерения количества вещества под названием моль. 1 моль содержит 6,022·10 23 частиц (атомов или молекул) и является безразмерной величиной. Число 6,022·10 23 носит название Число Авогадро, которое определяется как число частиц, содержащихся в 12 г атомов углерода 12 C. Важно понимать, что 1 моль любого вещества содержит всегда одно и то же число частиц (6,022·10 23 ).
Как уже было сказано, термин «моль» применяется не только к молекулам, но также и к атомам. Например, если вы говорите о моле гелия (He), то это означает, что вы имеет количество равное 6,022·10 23 атомов . Точно так же, 1 моль воды (H2O) подразумевает количество равное 6,022·10 23 молекул . Однако чаще всего моль применяют именно к молекулам.
Молярная масса вещества
Молярная масса – это масса 1 моля вещества, выраженная в граммах. Молярную массу одного моля любого химического элемента без труда находят из таблицы Менделеева, так как молярная масса численно равна атомной массе, но размерности у них разные (молярная масса имеет размерность г/моль). Запишите и запомните формулы для вычисления молярной массы, количества вещества и числа молекул:
- Молярная масса формула M=m/n
- Количество вещества формула n=m/M
- Число молекул формула N =NA·n
где m — масса вещества, n — количество вещества (число молей), М — молярная масса, N — число молекул, NA — число Авогадро. Благодаря молярной массе вещества химики могут вести подсчет атомов и молекул в лаборатории просто путем их взвешивания. Этим и удобно использование понятия моль.
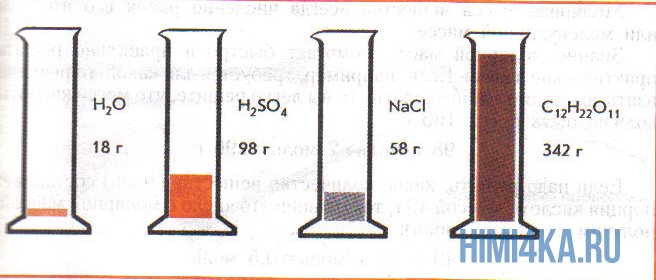
На рисунке изображены четыре колбы с различными веществами, но в каждой из них всего 1 моль вещества. Можете перепроверить, используя формулы выше.
Задачи на количество вещества
Пример 1. Сколько граммов Н2, Н2O, СН3ОН, октана (С8Н18) и газа неона (Ne) содержится в 1 моле?
Решение: Молекулярные массы (в атомных единицах массы) перечисленных веществ приведены в таблице Менделеева. 1 моль каждого из названных веществ имеет следующую массу:
Поскольку массы, указанные в решении примера 1, дают правильные относительные массы взвешиваемых молекул, указанная масса каждого из перечисленных веществ содержит одинаковое число молекул. Этим и удобно использование понятия моля. Нет даже необходимости знать, чему равно численное значение моля, хотя мы уже знаем, что оно составляет 6,022·10 23 ; эта величина называется числом Авогадро и обозначается символом NA. Переход от индивидуальных молекул к молям означает увеличение шкалы измерения в 6,022·10 23 раз. Число Авогадро представляет собой также множитель перевода атомных единиц массы в граммы: 1 г = 6,022·10 23 а.е.м. Если мы понимаем под молекулярной массой массу моля вещества, то ее следует измерять в граммах на моль; если же мы действительно имеем в виду массу одной молекулы, то она численно совпадает
с молекулярной массой вещества, но выражается в атомных единицах массы на одну молекулу. Оба способа выражения молекулярной массы правильны.
Пример 2. Сколько молей составляют и сколько молекул содержат 8 г газообразного кислорода O2?
Решение: Выписываем из таблицы Менделеева атомную массу атома кислорода (O), которая равна 15,99 а.е.м, округляем до 16. Так как у нас молекула кислорода, состоящая из двух атомов O, то ее атомная масса равна 16×2=32 а.е.м. Хорошо, а теперь переводим ее в молярную массу: 32 а.е.м = 32 г/моль. Это означает, что 1 моль (6,022·10 23 молекул) O2 имеет массу 32 грамма. Ну и в заключении по формулам выше находим количество вещества (моль) и число молекул, содержащихся в 8 граммах O2:
- n = m / M = 8г / 32г/моль = 0,25 моль
- N = NA × n = 6,022·10 23 × 0,25 = 1,505·10 23 молекул
Пример 3. 1 молекула Н2 реагирует с 1 молекулой Сl2, в результате чего образуются 2 молекулы газообразного хлористого водорода НСl. Какую массу газообразного хлора необходимо использовать, чтобы он полностью прореагировал с 1 килограммом (кг) газообразного водорода?
Решение: Молекулярные массы H2 и Cl2 равны 2,0160 и 70,906 г/моль соответственно. Следовательно, в 1000 г H2 содержится
Даже не выясняя, сколько молекул содержится в одном моле вещества, мы можем быть уверены, что 496 моля Cl2 содержат такое же число молекул, как и 496,0 моля, или 1000 г, H2. Сколько же граммов Cl2 содержится в 496 молях этого вещества? Поскольку молекулярная масса Cl2 равна 70,906 г/моль, то
Пример 4. Сколько молекул H2 и Cl2 принимает участие в реакции, описанной в примере 3?
Решение: В 496 молях любого вещества должно содержаться 496 моля × 6,022·10 23 молекул/моль, что равно 2,99·10 26 молекул.
Чтобы наглядно показать, сколь велико число Авогадро, приведем такой пример: 1 моль кокосовых орехов каждый диаметром 14 сантиметров (см) мог бы заполнить такой объем, какой занимает наша планета Земля. Использование молей в химических расчетах рассматривается в следующей главе, но представление об этом пришлось ввести уже здесь, поскольку нам необходимо знать, как осуществляется переход от молекулярной шкалы измерения масс к лабораторной шкале.
Надеюсь урок 5 «Моль и молярная масса» был познавательным и понятным. Если у вас возникли вопросы, пишите их в комментарии.