Как металл взаимодействует с сильным окислителем
- Общая характеристика элемента
- Физические и химические свойства цинка
- Реакция серной кислоты с цинком и получение водорода
- Реакция концентрированной серной кислоты с цинком
- Цинк. Химия цинка и его соединений
- Положение в периодической системе химических элементов
- Электронное строение цинка и свойства
- Физические свойства
- Нахождение в природе
- Способы получения
- Качественные реакции
- Химические свойства
- Оксид цинка
- Способы получения
- Химические свойства
- Гидроксид цинка
- Способы получения
- Химические свойства
- Соли цинка
- Нитрат и сульфат цинка
- Комплексные соли цинка
- Гидролиз солей цинка
- Цинкаты
- Сульфид цинка
- Упражнения типа «мысленный эксперимент» по химии цинка (тренажер задания 32 ЕГЭ по химии)
- Как реагирует цинк с соляной кислотой?
- Физические свойства металла
- Химические свойства цинка
- Реакция цинка и соляной кислоты
- Десятки экспериментов у вас дома
- Положение в периодической системе химических элементов
- Электронное строение цинка и свойства
- Физические свойства
- Нахождение в природе
- Способы получения
- Качественные реакции
- Цинк и соляная кислота
- Цинк как минерал
- Цинк в теле
- Цинк как типичный щелочной металл
- Реакция цинка с соляной кислотой
Общая характеристика элемента
Цинк располагается во второй группе, побочной подгруппе периодической системы Менделеева и является переходным металлом. Порядковый номер элемента — 30, масса — 65,37. Электронная конфигурация внешнего слоя атома — 4s2. Единственная и постоянная степень окисления равна «+2». Для переходных металлов характерно образование комплексных соединений, в которых они выступают в качестве комплексообразователя с разными координационными числами. Это относится и к цинку. Существует 5 устойчивых в природе изотопов с массовыми числами от 64 до 70. При этом изотоп 65Zn является радиоактивным, период его полураспада составляет 244 дня.
Цинк — это серебристо-голубой металл, который на воздухе быстро покрывается защитной оксидной пленкой, скрывающей его блеск. При удалении оксидной пленки цинк проявляет свойства металлов — сияние и характерный яркий блеск. В природе цинк содержится в составе многих минералов и руд. Самые распространенные: клейофан, цинковая обманка (сфалерит), вюрцит, марматит, каламин, смитсонит, виллемит, цинкит, франклинит.
В составе смешанных руд цинк встречается со своими постоянными спутниками: таллием, германием, индием, галлием, кадмием. В земной коре содержится 0,0076% цинка, а 0,07 мг/л этого металла содержится в морской воде в виде солей. Формула цинка как простого вещества — Zn, химическая связь — металлическая. У цинка гексагональная плотная кристаллическая решетка.
Физические и химические свойства цинка
Температура плавления цинка — 420 °С. При нормальных условиях это хрупкий металл. При нагревании до 100-150 °С ковкость и пластичность цинка повышается, возможно изготовление из металла проволоки и прокатка фольги. Температура кипения цинка — 906 °С. Этот металл — отличный проводник. Начиная от 200 °С, цинк легко растирается в серый порошок и теряет пластичность. У металла хорошая теплопроводность и теплоемкость. Описанные физические параметры позволяют использовать цинк в соединениях с другими элементами. Латунь — наиболее известный сплав цинка.
При обычных условиях поверхность цинка мгновенно покрывается оксидом в виде серо-белого тусклого налета. Он образуется из-за того, что кислород воздуха окисляет чистое вещество. Цинк как простое вещество реагирует с халькогенами, галогенами, кислородом, фосфором, щелочами, кислотами, аммонием (его солями), аммиаком. Цинк не взаимодействует с азотом, водородом, бором, углеродом и кремнием. Химически чистый цинк не реагирует с растворами кислот и щелочей. Цинк — металл амфотерный, и при реакциях со щелочами образует комплексные соединения — гидроксоцинкаты. Нажмите здесь, чтобы узнать, какие опыты на изучение свойств цинка можно провести дома.
Реакция серной кислоты с цинком и получение водорода
Взаимодействие разбавленной серной кислоты с цинком — основной лабораторный способ получения водорода. Для этого используется чистый зерненый (гранулированный) цинк либо технический цинк в виде обрезков и стружек.
Если взяты очень чистые цинк и серная кислота, то водород выделяется медленно, особенно в начале реакции. Поэтому к остывшему после разбавления раствору иногда добавляют немного раствора медного купороса. Осевшая на поверхности цинка металлическая медь ускоряет реакцию. Оптимальный способ разбавить кислоту для получения водорода — разбавить водой концентрированную серную кислоту плотностью 1,19 в соотношении 1:1.
Реакция концентрированной серной кислоты с цинком
В концентрированной серной кислоте окислителем является не катион водорода, а более сильный окислитель — сульфат-ион. Он не проявляет себя как окислитель в разбавленной серной кислоте из-за сильной гидратации, и, как следствие, малоподвижности.
То, как концентрированная серная кислота будет реагировать с цинком, зависит от температуры и концентрации. Уравнения реакций:
Zn + 2H₂SO₄ = ZnSO₄ + SO₂ + 2H₂O
3Zn + 4H₂SO₄ = 3ZnSO₄ + S + 4H₂O
4Zn + 5H₂SO₄ = 4ZnSO₄ + H₂S + 4H₂O
Концентрированная серная кислота является сильным окислителем благодаря степени окисления серы (S⁺⁶). Она взаимодействует даже с малоактивными металлами, то есть с металлами до и после водорода, и, в отличие от разбавленной кислоты, никогда не выделяет водород при этих реакциях. В реакциях концентрированной серной кислоты с металлами всегда образуются три продукта: соль, вода и продукт восстановления серы. Концентрированная серная кислота — это такой сильный окислитель, что окисляет даже некоторые неметаллы (уголь, серу, фосфор).
Цинк. Химия цинка и его соединений
Положение в периодической системе химических элементов
Цинк расположены в побочной подгруппе II группы (или в 12 группе в современной форме ПСХЭ) и в четвертом периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение цинка и свойства
Электронная конфигурация цинка в основном состоянии :
+30Zn 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2
2s 
3s 

Характерная степень окисления цинка в соединениях +2.
Физические свойства
Цинк при нормальных условиях — хрупкий переходный металл голубовато-белого цвета (быстро тускнеет на воздухе, покрываясь тонким слоем оксида цинка).
Температура плавления цинка 420°С, температура кипения 906°С, плотность 7,13 г/см 3 .
Нахождение в природе
Среднее содержание цинка в земной коре 8,3·10 -3 мас.%. Основной минерал цинка: сфалерит (цинковая обманка) ZnS..
Цинк играет важную роль в процессах, протекающих в живых организмах.
В природе цинк как самородный металл не встречается.
Способы получения
Цинк получают из сульфидной руды. На первом этапе руду обогащают, повышая концентрацию сульфидов металлов. Сульфид цинка обжигают в печи кипящего слоя:
2ZnS + 3O2 → 2ZnO + 2SO2
Чистый цинк из оксида получают двумя способами.
При пирометаллургическом способе , который использовался издавна, оксид цинка восстанавливают углём или коксом при 1200—1300 °C:
ZnO + С → Zn + CO
Далее цинк очищают от примесей.
В настоящее время основной способ получения цинка — электролитический (гидрометаллургический) . При этом сульфид цинка обрабатывают серной кислотой:
При это получаемый раствор сульфата цинка очищают от примесей (осаждением их цинковой пылью) и подвергают электролизу.
При электролизе чистый цинк осаждается на алюминиевых катодах, с которых его удаляют и подвергают плавлению в индукционных печах. Таким образом можно получить цинк с высокой чистотой (до 99,95 %).
Качественные реакции
Качественная реакция на ионы цинка — взаимодействие избытка солей цинка с щелочами . При этом образуется белый осадок гидроксида цинка.
Например , хлорид цинка взаимодействует с гидроксидом натрия:
ZnCl2 + 2NaOH → Zn(OH)2 + 2NaCl
При дальнейшем добавлении щелочи амфотерный гидроксид цинка растворяется с образованием комплексной соли тетрагидроксоцинката:
Обратите внимание , если мы поместим соль цинка в избыток раствора щелочи, то белый осадок гидроксида цинка не образуется, т.к. в избытке щелочи соединения цинка сразу переходят в комплекс:
Химические свойства
1. Цинк – сильный восстановитель . Цинк – довольно активный металл, но на воздухе он устойчив, так как покрывается тонким слоем оксида, предохраняющим его от дальнейшего окисления. При нагревании цинк реагирует со многими неметаллами .
1.1. Цинк реагируют с галогенами с образованием галогенидов:
Реакция цинка с иодом при добавлении воды:
1.2. Цинк реагирует с серой с образованием сульфидов:
Zn + S → ZnS
1.3. Цинк реагируют с фосфором . При этом образуется бинарное соединение — фосфид:
1.4. С азотом цинк непосредственно не реагирует.
1.5. Цинк непосредственно не реагирует с водородом, углеродом, кремнием и бором.
1.6. Цинк взаимодействует с кислородом с образованием оксида:
2Zn + O2 → 2ZnO
2. Цинк взаимодействует со сложными веществами:
2.1. Цинк реагирует с парами воды при температуре красного каления с образованием оксида цинка и водорода:
Zn 0 + H2 + O → Zn +2 O + H2 0
2.2. Цинк взаимодействуют с минеральными кислотами (с соляной, фосфорной и разбавленной серной кислотой и др.). При этом образуются соль и водород.
Например , цинк реагирует с соляной кислотой :
Zn + 2HCl → ZnCl2 + H2↑
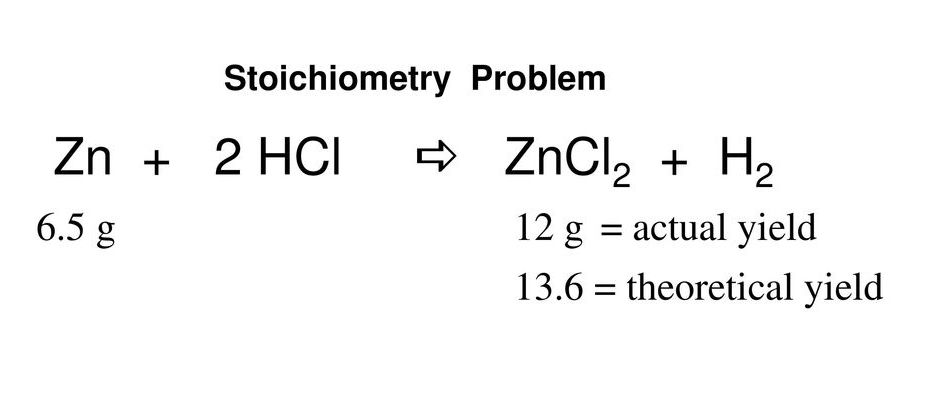
Демонстрация количества выделения водорода при реакции цинка с кислотой:
Цинк реагирует с разбавленной серной кислотой:
2.3. Цинк реагирует с концентрированной серной кислотой . В зависимости от условий возможно образование различных продуктов. При нагревании гранулированного цинка с концентрированной серной кислотой образуются оксид серы (IV), сульфат цинка и вода:
Порошковый цинк реагирует с концентрированной серной кислотой с образованием сероводорода, сульфата цинка и воды:
2.4. Аналогично: при нагревании гранулированного цинка с концентрированной азотной кислотой образуются оксид азота (IV) , нитрат цинка и вода :
При нагревании цинка с очень разбавленной азотной кислотой образуются нитрат аммония , нитрат цинка и вода :
2.5. Цинк – амфотерный металл, он взаимодействует с щелочами. При взаимодействии цинка с раствором щелочи образуется тетрагидроксоцинкат и водород:
Zn + 2KOH + 2H2O = K2[Zn(OH)4] + H2
Цинк реагирует с расплавом щелочи с образованием цинката и водорода:
В отличие от алюминия, цинк растворяется и в водном растворе аммиака:
2.6. Цинк вытесняет менее активные металлы из оксидов и солей .
Например , цинк вытесняет медь из оксида меди (II):
Zn + CuO → Cu + ZnO
Еще пример : цинк восстанавливает медь из раствора сульфата меди (II):
CuSO4 + Zn = ZnSO4 + Cu
И свинец из раствора нитрата свинца (II):
Восстановительные свойства цинка также проявляются при взаимодействии его с сильными окислителями: нитратами и сульфитами в щелочной среде, перманганатами, соединениями хрома (VI):
Оксид цинка
Способы получения
Оксид цинка можно получить различными методами :
1. Окислением цинка кислородом:
2Zn + O2 → 2ZnO
2. Разложением гидроксида цинка при нагревании:
3. Оксид цинка можно получить разложением нитрата цинка :
Химические свойства
Оксид цинка — типичный амфотерный оксид . Взаимодействует с кислотными и основными оксидами, кислотами, щелочами.
1. При взаимодействии оксида цинка с основными оксидами образуются соли-цинкаты.
Например , оксид цинка взаимодействует с оксидом натрия:
2. Оксид цинка взаимодействует с растворимыми основаниями (щелочами). При этом в расплаве образуются соли—цинкаты, а в растворе – комплексные соли . При этом оксид цинка проявляет кислотные свойства.
Например , оксид цинка взаимодействует с гидроксидом натрия в расплаве с образованием цинката натрия и воды:
Оксид цинка растворяется в избытке раствора щелочи с образованием тетрагидроксоцинката:
3. Оксид цинка не взаимодействует с водой.
ZnO + H2O ≠
4. Оксид цинка взаимодействует с кислотными оксидами . При этом образуются соли цинка. В этих реакциях оксид цинка проявляет основные свойства.
Например , оксид цинка взаимодействует с оксидом серы (VI) с образованием сульфата цинка:
5. Оксид цинка взаимодействует с растворимыми кислотами с образованием солей.
Например , оксид цинка реагирует с соляной кислотой:
ZnO + 2HCl = ZnCl2 + H2O
6. Оксид цинка проявляет слабые окислительные свойства .
Например , оксид цинка при нагревании реагирует с водородом и угарным газом:
ZnO + С(кокс) → Zn + СО
ZnO + СО → Zn + СО2
7. Оксид цинка — твердый, нелетучий. А следовательно, он вытесняет более летучие оксиды (как правило, углекислый газ) из солей при сплавлении.
Например , из карбоната бария:
Гидроксид цинка
Способы получения
1. Гидроксид цинка можно получить пропусканием углекислого газа, сернистого газа или сероводорода через раствор тетрагидроксоцинката натрия:
Чтобы понять, как протекает эта реакция, можно использовать несложный прием: мысленно разбить исходное вещество Na2[Zn(OH)4] на составные части: NaOH и Zn(OH)2. Далее мы определяем, как реагирует углекислый газ с каждым из этих веществ, и записываем продукты их взаимодействия. Т.к. Zn(OH)2 не реагирует с СО2, то мы записываем справа Zn(OH)2 без изменения.
2. Гидроксид цинка можно получить действием недостатка щелочи на избыток соли цинка.
Например , хлорид цинка реагирует с недостатком гидроксида калия с образованием гидроксида цинка и хлорида калия:
Химические свойства
1. Гидроксид цинка реагирует с растворимыми кислотами .
Например , гидроксид цинка взаимодействует с азотной кислотой с образованием нитрата цинка:
2. Гидроксид цинка взаимодействует с кислотными оксидами .
Например , гидроксид цинка взаимодействует с оксидом серы (VI) с образованием сульфата цинка:
3. Гидроксид цинка взаимодействует с растворимыми основаниями (щелочами). При этом в расплаве образуются соли—цинкаты, а в растворе – комплексные соли . При этом гидроксид цинка проявляет кислотные свойства.
Например , гидроксид цинка взаимодействует с гидроксидом калия в расплаве с образованием цинката калия и воды:
Гидроксид цинка растворяется в избытке щелочи с образованием тетрагидроксоцинката:
4. Г идроксид цинка разлагается при нагревании :
Соли цинка
Нитрат и сульфат цинка
Нитрат цинка при нагревании разлагается на оксид цинка, оксид азота (IV) и кислород:
Сульфат цинка при сильном нагревании разлагается аналогично — на оксид цинка, сернистый газ и кислород:
Комплексные соли цинка
Для описания свойств комплексных солей цинка — гидроксоцинкатов, удобно использоваться следующий прием: мысленно разбейте тетрагидроксоцинкат на две отдельные частицы — гидроксид цинка и гидроксид щелочного металла.
Например , тетрагидроксоцинкат натрия разбиваем на гидроксид цинка и гидроксид натрия:
Na2[Zn(OH)4] разбиваем на NaOH и Zn(OH)2
Свойства всего комплекса можно определять, как свойства этих отдельных соединений.
Таким образом, гидроксокомплексы цинка реагируют с кислотными оксидами .
Например , гидроксокомплекс разрушается под действием избытка углекислого газа. При этом с СО2 реагирует NaOH с образованием кислой соли (при избытке СО2), а амфотерный гидроксид цинка не реагирует с углекислым газом, следовательно, просто выпадает в осадок:
Аналогично тетрагидроксоцинкат калия реагирует с углекислым газом:
А вот под действием избытка сильной кислоты осадок не выпадает, т.к. амфотерный гидроксид цинка реагирует с сильными кислотами.
Например , с соляной кислотой:
Правда, под действием небольшого количества ( недостатка ) сильной кислоты осадок все-таки выпадет, для растворения гидроксида цинка кислоты не будет хватать:
Аналогично с недостатком азотной кислоты выпадает гидроксид цинка:
Если выпарить воду из раствора комплексной соли и нагреть образующееся вещество, то останется обычная соль-цинкат:
Гидролиз солей цинка
Растворимые соли цинка и сильных кислот гидролизуются по катиону. Гидролиз протекает ступенчато и обратимо, т.е. чуть-чуть:
I ступень: Zn 2+ + H2O = ZnOH + + H +
II ступень: ZnOH + + H2O = Zn(OH )2 + H +
Более подробно про гидролиз можно прочитать в соответствующей статье.
Цинкаты
Соли, в которых цинк образует кислотный остаток (цинкаты) — образуются из оксида цинка при сплавлении с щелочами и основными оксидами:
Для понимания свойств цинкатов их также можно мысленно разбить на два отдельных вещества.
Например, цинкат натрия мы разделим мысленно на два вещества: оксид цинка и оксид натрия.
Na2ZnO2 разбиваем на Na2O и ZnO
Тогда нам станет очевидно, что цинкаты реагируют с кислотами с образованием солей цинка :
Под действием избытка воды цинкаты переходят в комплексные соли:
Сульфид цинка
Сульфид цинка — так называемый «белый сульфид». В воде сульфид цинка нерастворим, зато минеральные кислоты вытесняют из сульфида цинка сероводород (например, соляная кислота):
ZnS + 2HCl → ZnCl2 + H2S
Под действием азотной кислоты сульфид цинка окисляется до сульфата:
(в продуктах также можно записать нитрат цинка и серную кислоту).
Концентрированная серная кислота также окисляет сульфид цинка:
При окислении сульфида цинка сильными окислителями в щелочной среде образуется комплексная соль:
Z nS + 4NaOH + Br2 = Na2[Zn(OH)4] + S + 2NaBr
Упражнения типа «мысленный эксперимент» по химии цинка (тренажер задания 32 ЕГЭ по химии)
- Оксид цинка растворили в растворе хлороводородной кислоты и раствор нейтрализовали, добавляя едкий натр. Выделившееся студенистое вещество белого цвета отделили и обработали избытком раствора щелочи, при этом осадок полностью растворился. нейтрализация полученного раствора кислотой, например, азотной, приводит к повторному образованию студенистого осадка. Напишите уравнения описанных реакций.
- Цинк растворили в очень разбавленной азотной кислоте и в полученный раствор добавили избыток щелочи, получив прозрачный раствор. Напишите уравнения описанных реакций.
- Соль, полученную при взаимодействии оксида цинка с серной кислотой, прокалили при температуре 800°С. Твердый продукт реакции обработали концентрированным раствором щелочи, и через полученный раствор пропустили углекислый газ. Напишите уравнения описанных реакций.
- Нитрат цинка прокалили, продукт реакции при нагревании обработали раствором едкого натра. Через образовавшийся раствор пропустили углекислый газ до прекращения выделения осадка, после чего обработали избытком концентрированного нашатырного спирта, при этом осадок растворился. Напишите уравнения описанных реакций.
- Цинк растворили в очень разбавленной азотной кислоте, полученный раствор осторожно выпарили и остаток прокалили. Продукты реакции смешали с коксом и нагрели. Напишите уравнения описанных реакций.
- Несколько гранул цинка растворили при нагревании в растворе едкого натра. В полученный раствор небольшими порциями добавляли азотную кислоту до образования осадка. Осадок отделили, растворили в разбавленной азотной кислоте, раствор осторожно выпарили и остаток прокалили. Напишите уравнения описанных реакций.
- В концентрированную серную кислоту добавили металлический цинк. образовавшуюся соль выделили, растворили в воде и в раствор добавили нитрат бария. После отделения осадка в раствор внесли магниевую стружку, раствор профильтровали, фильтрат выпарили и прокалили. Напишите уравнения описанных реакций.
- Сульфид цинка подвергли обжигу. Полученное твердое вещество полностью прореагировало с раствором гидроксида калия. Через полученный раствор пропустили углекислый газ до выпадения осадка. Осадок растворили в соляной кислоте. Напишите уравнения описанных реакций.
- Некоторое количество сульфида цинка разделили на две части. Одну из них обработали соляной кислотой, а другую подвергли обжигу на воздухе. При взаимодействии выделившихся газов образовалось простое вещество. Это вещество нагрели с концентрированной азотной кислотой, причем выделился бурый газ. Напишите уравнения описанных реакций.
- Цинк растворили в растворе гидроксида калия. Выделившийся газ прореагировал с литием, а к полученному раствору по каплям добавили соляную кислоту до прекращения выпадения осадка. Его отфильтровали и прокалили. Напишите уравнения описанных реакций.
Как реагирует цинк с соляной кислотой?
Физические свойства металла
Цинк — это хрупкий металл серебристо-голубого цвета, он очень ковок и пластичен.
Кристаллы этого металла похожи на иголки, поэтому, вероятнее всего, название тридцатого элемента происходит от немецкого zinke, что переводится как «зубец». Цинк настолько хрупкий, что если согнуть палочку этого металла при нормальной температуре, можно услышать хруст, даже более отчетливый, чем у олова. При температурах 100–150 °С цинк становится тягучим и используется для соединения деталей между собой. Но если температура воздействия на цинк поднимется, к примеру, до 210 °С, серебристый металл вновь станет хрупким.
Химические свойства цинка
Тридцатый элемент таблицы Менделеева является мощным восстановителем. При высоких температурах металл сгорает и тем самым образует атмосферный белый оксид цинка. Реакция сопровождается голубым пламенем:
При горении цинк весьма бурно реагирует с серой. Взаимодействие сопровождается красивым зеленоватым пламенем:
С галогенами цинк реагирует в присутствии влаги:
Также цинк реагирует с парами воды при 600–800 °С с образованием водорода и оксида цинка:
Zn + 2H₂O = ZnO + H₂
Если опустить кусочек цинка в разбавленную серную кислоту, пойдет выделение пузырьков водорода:
H₂SO₄ + Zn = ZnSO₄ + H₂↑
Цинк — тяжелый металл (например, по сравнению с литием), поэтому такой металл не всплывает на поверхность под действием пузырьков.
Реакция цинка и соляной кислоты
Рассмотрим взаимодействие серебристого металла с соляной кислотой. С НСl цинк реагирует также медленно, с образованием небольших пузырьков и выделением водорода. В результате реакции получается хлорид цинка ZnCl₂:
Zn + HCl → ZnCl₂ + H₂
Десятки экспериментов у вас дома
Один из самых интересных и амбициозных образовательных химических проектов
Положение в периодической системе химических элементов
Цинк расположены в побочной подгруппе II группы (или в 12 группе в современной форме ПСХЭ) и в четвертом периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение цинка и свойства
Электронная конфигурация цинка в основном состоянии :
+30Zn 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2
2s 
3s 
Характерная степень окисления цинка в соединениях +2.
Физические свойства
Цинк при нормальных условиях — хрупкий переходный металл голубовато-белого цвета (быстро тускнеет на воздухе, покрываясь тонким слоем оксида цинка).
Температура плавления цинка 420°С, температура кипения 906°С, плотность 7,13 г/см 3 .
Нахождение в природе
Среднее содержание цинка в земной коре 8,3·10 -3 мас.%. Основной минерал цинка: сфалерит (цинковая обманка) ZnS..
Цинк играет важную роль в процессах, протекающих в живых организмах.
В природе цинк как самородный металл не встречается.
Способы получения
Цинк получают из сульфидной руды. На первом этапе руду обогащают, повышая концентрацию сульфидов металлов. Сульфид цинка обжигают в печи кипящего слоя:
2ZnS + 3O2 → 2ZnO + 2SO2
Чистый цинк из оксида получают двумя способами.
При пирометаллургическом способе , который использовался издавна, оксид цинка восстанавливают углём или коксом при 1200—1300 °C:
ZnO + С → Zn + CO
Далее цинк очищают от примесей.
В настоящее время основной способ получения цинка — электролитический (гидрометаллургический) . При этом сульфид цинка обрабатывают серной кислотой:
При это получаемый раствор сульфата цинка очищают от примесей (осаждением их цинковой пылью) и подвергают электролизу.
При электролизе чистый цинк осаждается на алюминиевых катодах, с которых его удаляют и подвергают плавлению в индукционных печах. Таким образом можно получить цинк с высокой чистотой (до 99,95 %).
Качественные реакции
Качественная реакция на ионы цинка — взаимодействие избытка солей цинка с щелочами . При этом образуется белый осадок гидроксида цинка.
Например , хлорид цинка взаимодействует с гидроксидом натрия:
ZnCl2 + 2NaOH → Zn(OH)2 + 2NaCl
При дальнейшем добавлении щелочи амфотерный гидроксид цинка растворяется с образованием комплексной соли тетрагидроксоцинката:
Обратите внимание , если мы поместим соль цинка в избыток раствора щелочи, то белый осадок гидроксида цинка не образуется, т.к. в избытке щелочи соединения цинка сразу переходят в комплекс:
Цинк находится в группе элементов из периодической таблицы, называемой переходными металлами. Эти металлы имеют переменную реакционную способность и различаются в природе в элементарной форме. Цинк встречается в природе как в элементарной форме – как блестящий серый металл, так и в виде соли. Люди и многие другие организмы зависят от определенного количества неметаллического цинка, то есть цинка в форме соли, для поддержания клеточной функции.
Соли, в которых цинк образует кислотный остаток (цинкаты) — образуются из оксида цинка при сплавлении с щелочами и основными оксидами:
Для понимания свойств цинкатов их также можно мысленно разбить на два отдельных вещества.
Например, цинкат натрия мы разделим мысленно на два вещества: оксид цинка и оксид натрия.
Na2ZnO2 разбиваем на Na2O и ZnO
Тогда нам станет очевидно, что цинкаты реагируют с кислотами с образованием солей цинка :
Нитрат цинка при нагревании разлагается на оксид цинка, оксид азота (IV) и кислород:
Сульфат цинка при сильном нагревании разлагается аналогично — на оксид цинка, сернистый газ и кислород:
Под действием избытка воды цинкаты переходят в комплексные соли:
Сульфид цинка — так называемый «белый сульфид». В воде сульфид цинка нерастворим, зато минеральные кислоты вытесняют из сульфида цинка сероводород (например, соляная кислота):
ZnS + 2HCl → ZnCl2 + H2S
Под действием азотной кислоты сульфид цинка окисляется до сульфата:
(в продуктах также можно записать нитрат цинка и серную кислоту).
Концентрированная серная кислота также окисляет сульфид цинка:
При окислении сульфида цинка сильными окислителями в щелочной среде образуется комплексная соль:
Z nS + 4NaOH + Br2 = Na2[Zn(OH)4] + S + 2NaBr
Растворимые соли цинка и сильных кислот гидролизуются по катиону. Гидролиз протекает ступенчато и обратимо, т.е. чуть-чуть:
I ступень: Zn 2+ + H2O = ZnOH + + H +
II ступень: ZnOH + + H2O = Zn(OH )2 + H +
Для описания свойств комплексных солей цинка — гидроксоцинкатов, удобно использоваться следующий прием: мысленно разбейте тетрагидроксоцинкат на две отдельные частицы — гидроксид цинка и гидроксид щелочного металла.
Например , тетрагидроксоцинкат натрия разбиваем на гидроксид цинка и гидроксид натрия:
Na2[Zn(OH)4] разбиваем на NaOH и Zn(OH)2
Свойства всего комплекса можно определять, как свойства этих отдельных соединений.
Таким образом, гидроксокомплексы цинка реагируют с кислотными оксидами .
Например , гидроксокомплекс разрушается под действием избытка углекислого газа. При этом с СО2 реагирует NaOH с образованием кислой соли (при избытке СО2), а амфотерный гидроксид цинка не реагирует с углекислым газом, следовательно, просто выпадает в осадок:
Аналогично тетрагидроксоцинкат калия реагирует с углекислым газом:
А вот под действием избытка сильной кислоты осадок не выпадает, т.к. амфотерный гидроксид цинка реагирует с сильными кислотами.
Например , с соляной кислотой:
Правда, под действием небольшого количества ( недостатка ) сильной кислоты осадок все-таки выпадет, для растворения гидроксида цинка кислоты не будет хватать:
Аналогично с недостатком азотной кислоты выпадает гидроксид цинка:
Если выпарить воду из раствора комплексной соли и нагреть образующееся вещество, то останется обычная соль-цинкат:
1. Гидроксид цинка реагирует с растворимыми кислотами .
Например , гидроксид цинка взаимодействует с азотной кислотой с образованием нитрата цинка:
2. Гидроксид цинка взаимодействует с кислотными оксидами .
Например , гидроксид цинка взаимодействует с оксидом серы (VI) с образованием сульфата цинка:
3. Гидроксид цинка взаимодействует с растворимыми основаниями (щелочами). При этом в расплаве образуются соли—цинкаты, а в растворе – комплексные соли . При этом гидроксид цинка проявляет кислотные свойства.
Например , гидроксид цинка взаимодействует с гидроксидом калия в расплаве с образованием цинката калия и воды:
Гидроксид цинка растворяется в избытке щелочи с образованием тетрагидроксоцинката:
4. Г идроксид цинка разлагается при нагревании :
Оксид цинка можно получить различными методами :
1. Окислением цинка кислородом:
2Zn + O2 → 2ZnO
2. Разложением гидроксида цинка при нагревании:
3. Оксид цинка можно получить разложением нитрата цинка :
Оксид цинка — типичный амфотерный оксид . Взаимодействует с кислотными и основными оксидами, кислотами, щелочами.
1. При взаимодействии оксида цинка с основными оксидами образуются соли-цинкаты.
Например , оксид цинка взаимодействует с оксидом натрия:
2. Оксид цинка взаимодействует с растворимыми основаниями (щелочами). При этом в расплаве образуются соли—цинкаты, а в растворе – комплексные соли . При этом оксид цинка проявляет кислотные свойства.
Например , оксид цинка взаимодействует с гидроксидом натрия в расплаве с образованием цинката натрия и воды:
Оксид цинка растворяется в избытке раствора щелочи с образованием тетрагидроксоцинката:
3. Оксид цинка не взаимодействует с водой.
ZnO + H2O ≠
4. Оксид цинка взаимодействует с кислотными оксидами . При этом образуются соли цинка. В этих реакциях оксид цинка проявляет основные свойства.
Например , оксид цинка взаимодействует с оксидом серы (VI) с образованием сульфата цинка:
5. Оксид цинка взаимодействует с растворимыми кислотами с образованием солей.
Например , оксид цинка реагирует с соляной кислотой:
ZnO + 2HCl = ZnCl2 + H2O
6. Оксид цинка проявляет слабые окислительные свойства .
Например , оксид цинка при нагревании реагирует с водородом и угарным газом:
ZnO + С(кокс) → Zn + СО
ZnO + СО → Zn + СО2
7. Оксид цинка — твердый, нелетучий. А следовательно, он вытесняет более летучие оксиды (как правило, углекислый газ) из солей при сплавлении.
Например , из карбоната бария:
Цинк и соляная кислота
Хотя не все металлы реагируют с соляной кислотой или HCl, некоторые делают. Способность металла реагировать с HCl зависит от так называемой активности металла, когда металлы с высокой активностью реагируют с HCl. Активность металлического цинка достаточно высока, чтобы позволить ему вступать в реакцию с HCl, которая производит газ H2 и хлорид соединения, или ZnCl2, объясняет д-р Мартин Зильберберг в своей книге «Химия: молекулярная природа материи и изменений».
Цинк как минерал
Вы принимаете цинк в любое время, когда потребляете определенные продукты, особенно мясо и моллюски. Цинк играет важную роль в качестве основного минерала, объясняет доктор Лаурали Шервуд книга «Физиология человека». Ряду ваших ферментов требуется цинк для того, чтобы функционировать, где фермент является химическим веществом, которое помогает протекать быстрее, чем в противном случае. Многие из метаболических ферментов, которые вы используете для обработки питательных веществ, зависят от цинка .
Цинк в теле
Пока у вас HCl в желудке – он помогает в переваривании пищи – вы не производите ни H2, ни ZnCl2, когда потребляете цинк в пище. Это потому, что цинк вы взятие через продукты питания или дополнения не в металлической форме. Вместо этого оно имеет потеряли некоторые из его электронов, образуя положительно заряженные частицы, называемые ионами цинка. Тело не использует металлический цинк, а цинк в пище не реагирует с HCl.
Цинк как типичный щелочной металл
Цинк – это типичный представитель металлов, в нормальном состоянии имеет голубовато-серый цвет, легко окисляется на воздухе, приобретая на поверхности оксидную пленку (ZnO).
Как типичный амфотерный металл цинк взаимодействует с кислородом воздуха: 2Zn+O2=2ZnO – без температуры, с образованием оксидной пленки. При нагревании образуется белый порошок.
Сам оксид реагирует с кислотами с образованием соли и воды:
С растворами кислот. Если цинк обычной чистоты, то уравнение реакции HCl Zn ниже.
Zn+2HCl= ZnCl2+H2↑ – молекулярное уравнение реакции.
Zn (заряд 0) + 2H (заряд +) + 2Cl (заряд -) = Zn (заряд +2) + 2Cl (заряд -)+ 2H (заряд 0) – полное Zn HCl ионное уравнение реакции.
Zn + 2H(+) = Zn(2+) +H2 – С.И.У. (сокращенное ионное уравнение реакции).
Реакция цинка с соляной кислотой
Данное уравнение реакции HCl Zn относится к типу окислительно-восстановительных. Это можно доказать тем, что у Zn и H2 в ходе реакции изменился заряд, наблюдалось качественное проявление реакции, а также наблюдалось присутствие окислителя и восстановителя.
В данном случае H2 является окислителем, так как с. о. водорода до начала реакции была “+”, а после стала “0”. Он участвовал в процессе восстановления, отдавая 2 электрона.
Zn является восстановителем, он участвует в окислении, принимая 2 электрона, повышая с.о. (степень окисления).
Также это реакция замещения. В ходе нее участвовало 2 вещества, простое Zn и сложное – HCl. В результате реакции образовалось 2 новых вещества, а также одно простое – H2 и одно сложное – ZnCl2. Так как Zn расположен в ряду активности металлов до H2, он вытеснил его из вещества, которое реагировала с ним.