| Йодид серебра I | |
|---|---|
  | |
| Хим. формула | AgI |
| Рац. формула | AgI |
| Молярная масса | 234.77 г/моль |
| Плотность | 5.675 г/см³ |
| Температура | |
| • плавления | 558 °C |
| • кипения | 1506 °C |
| Энтальпия | |
| • образования | −62,4 кДж/моль |
| Рег. номер CAS | 7783-96-2 |
| PubChem | 24563 |
| Рег. номер EINECS | 232-038-0 |
| SMILES | |
| Номер ООН | 3077 |
| ChemSpider | 22969 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Йодид серебра (Йодистое серебро) — неорганическое соединение с формулой AgI. Это жёлтое вещество, чувствительное к действию света, используется в фотографии, находит применение в качестве антисептика в медицине, а также в качестве дождеобразующего реагента.
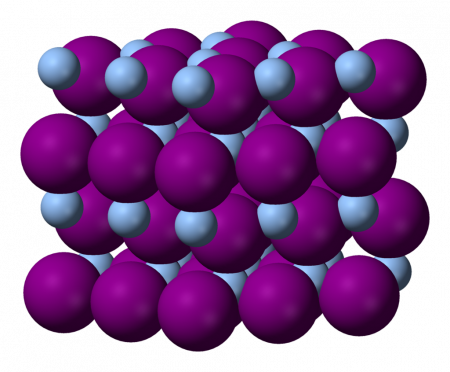
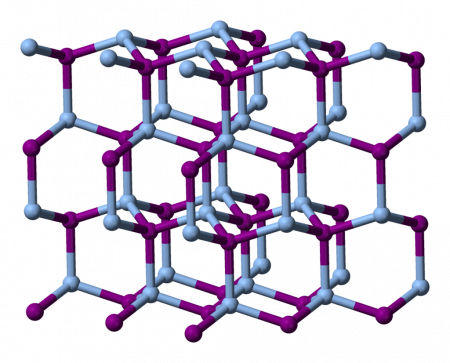
Йодид серебра практически не растворяется в воде благодаря своей кристаллической структуре. Она существует в трёх известных разновидностях, меняющихся с изменением температуры.
Одна из них очень схожа по строению с таковой у льда, поэтому введение небольшого количества йодида вызывает образование очагов конденсации в облаках, тем самым вызывая выпадение осадков. По некоторым оценкам, для этой цели используется около 50 тонн вещества в год — при том, что однократно расходуется от 10 до 50 граммов.
Йодид серебра токсичен, при контакте или вдыхании концентрированных паров возможно отравление. Симптомы: головная боль, слабость, анемия, потеря веса, раздражение слизистых оболочек. При длительном контакте или вдыхании может развиться аргирия.
- Получение
- Реакция взаимодействия серебра и йода
- Реакция взаимодействия серебра и йода
- Реакция взаимодействия оксида серебра (I) и азотной кислоты
- Реакция взаимодействия меди и оксида азота (II)
- Реакция термического разложения гидроксида молибдена (III)
- Выбрать язык
- Популярные записи
- Предупреждение.
- Йодид натрия: способы получения и химические свойства
- Способ получения
- Качественная реакция
- Химические свойства
Получение
При комнатной температуре, воздействием йодоводородом или йодидом калия или йодидом натрия на нитрат серебра, йодид серебра выпадет в осадок.
AgNO3 + HI ⟶ AgI ↓ + HNO3 , AgNO3 + KI ⟶ AgI ↓ + KNO3 , AgNO3 + NaI ⟶ AgI ↓ + NaNO3
Медная пластина, покрытая тонким слоем серебра, тщательно отполированная до зеркального блеска, помещается в специальный ящик, полированной стороной вниз. Снизу ящика под пластиной помещается чашка с кристаллическим йодом. При подогреве йод начинает возгоняться и пары его сублимируются на полированной серебряной пластине. Йод вступает в реакцию с серебром, и пластина покрывается тонким слоем йодистого серебра, становясь светочувствительной. Дагеротипия
Реакция взаимодействия серебра и йода
Реакция взаимодействия серебра и йода
Уравнение реакции взаимодействия серебра и йода:
Реакция взаимодействия серебра и йода.
В результате реакции образуется йодид серебра (I).
Реакция протекает при условии: при температуре 150-200 °C.
Формула поиска по сайту: 2Ag + I2 → 2AgI.
Реакция взаимодействия оксида серебра (I) и азотной кислоты
Реакция взаимодействия меди и оксида азота (II)
Реакция термического разложения гидроксида молибдена (III)
Выбрать язык
Популярные записи
Предупреждение.
Все химические реакции и вся информация на сайте предназначены для использования исключительно в учебных целях — только для решения письменных, учебных задач. Мы не несем ответственность за проведение вами химических реакций.
Химические реакции и информация на сайте
не предназначены для проведения химических и лабораторных опытов и работ.
Йодид натрия: способы получения и химические свойства
Йодид натрия NaI — соль щелочного металла натрия и йодоводородной кислоты. Белый, при хранении на свету желтеет из-за окисления. Плавится без разложения, при дальнейшем нагревании разлагается. Хорошо растворяется в воде (гидролиза нет).
Относительная молекулярная масса Mr = 149,90; относительная плотность для тв. и ж. состояния d = 3,667; tпл = 661º C;
Способ получения
1. Йодид натрия можно получить путем взаимодействия горячего гидроксида натрия, пероксида водорода и йода, образуются йодид натрия, газ кислород и вода:
если гидроксид натрия будет холодным и к нему вместе с йодом добавить газ сероводород, то в результате данной реакции произойдет образование йодида натрия, осадка серы и воды:
2NaOH + I2 + H2S = 2NaI + S↓ + 2H2O
2. При температуре 150–200º C, в результате взаимодействия натрия и брома, образуется йодид натрия:
2Na + I2 = 2NaI
3. Разбавленный раствор гидроксида натрия реагирует с йодидом железа в атмосфере азота . При этом образуются йодид натрия и осадок гидроксид железа:
2NaOH + FeI2 = 2NaI + Fe(OH)2↓
Качественная реакция
Качественная реакция на йодид натрия — взаимодействие его с нитратом серебра, в результате реакции происходит образование осадка желтого цвета:
1. При взаимодействии с нитратом серебра , йодид натрия образует нитрат натрия и осадок йодид серебра:
NaI + AgNO3 = NaNO3 + AgI↓
Химические свойства
1. Йодид натрия разлагается при температуре выше 1400º C с образованием натрия и йода:
2NaI = 2Na + I2
2. Йодид натрия вступает в реакцию с простыми веществами :
2.1. Холодный йодид натрия взаимодействует с хлором. В результате реакции происходит образование хлорида натрия и осадка йода:
2NaI + Cl2 = 2NaCl + I2↓
2.2. Холодный йодид натрия взаимодействует с бромом. В результате реакции происходит образование бромида натрия и осадка йода:
2NaI + Br2 = 2NaBr + I2↓
3. Йодид натрия способен вступать в реакцию со сложными веществами :
3.1. Йодид натрия реагирует с кислотами-окислителями :
3.1.1. Твердый йодид натрия реагирует с серной кислотой при 30 — 50º С. Взаимодействие данных веществ приводит к образованию осадка йода, газа сероводорода, воды и гидросульфата натрия:
3.1.2. При кипении, в результате взаимодействия твердого йодида натрия и концентрированной азотной кислоты образуются осадок йод, газ оксид азота (IV), вода и нитрат натрия:
4. Йодид натрия способен вступать в реакцию с соединениями железа (III) :
NaI + FeCl3 = FeCl2 + I2↓ + NaCl


