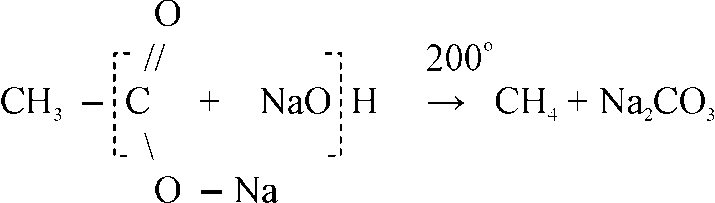Постановка опытов и текст – к.п.н. Павел Беспалов.
Получение метана
Метан в лаборатории получают прокаливанием безводного ацетата натрия с натронной известью. Натронная известь представляет собой смесь гидроксида натрия с гидроксидом кальция. Тщательно перемешаем натронную известь с ацетатом натрия и поместим в пробирку. Закроем пробирку пробкой с газоотводной трубкой. Нагреем смесь. Через некоторое время начинает выделяться метан
CH3COONa + NaOH = CH4 + Na2CO3
Оборудование: пробирка, газоотводная трубка, промывалка, кристаллизатор, цилиндр, горелка, штатив.
Техника безопасности. Соблюдать правила работы с горючими газами и нагревательными приборами. Не допускать попадания натронной извести на кожу.
Горение метана и изучение его физических свойств
Заполним метаном цилиндр. Метан представляет собой бесцветный газ, мало растворимый в воде. Он легче воздуха, поэтому легко улетучивается из открытого цилиндра. При поджигании метан загорается. При сгорании метана образуются углекислый газ и водяные пары.
CH4 + 2О2 = СО2 + 2 Н2О
Оборудование: пробирка, газоотводная трубка, промывалка, кристаллизатор, цилиндр, горелка, штатив.
Техника безопасности. Соблюдать правила работы с горючими газами и нагревательными приборами. Не допускать попадания натронной извести на кожу.
Взрыв метана с кислородом
Для полного сгорания метана на один объем метана нужно взять два объема кислорода (см. уравнение реакции). Пластиковую бутылку, разделенную метками на три равные части, заполним способом вытеснения воды одной частью метана и двумя частями кислорода. При поджигании смеси происходит взрыв — полное сгорание метана в кислороде.
CH4 + 2О2 = СО2 + 2 Н2О
Оборудование: пробирка, газоотводная трубка, промывалка, кристаллизатор, цилиндр, горелка, штатив.
Техника безопасности. Соблюдать правила работы с горючими газами и нагревательными приборами.
Отношение метана к раствору перманганата калия и бромной воде
Получаем метан прокаливанием безводного ацетата натрия с натронной известью. Пропустим метан через раствор перманганата калия. Никаких видимых изменений не наблюдаем. Бромная вода также не изменяет своей окраски. Метан стоек к окислителям и не вступает в реакцию с бромом при данных условиях.
Оборудование: пробирка, газоотводная трубка, промывалка, кристаллизатор, цилиндр, горелка, штатив.
Техника безопасности. Соблюдать правила работы с горючими газами и нагревательными приборами.
Горение жидких углеводородов
Возьмем для опыта гексан и керосин.
Молекула гексана содержит шесть атомов углерода. Керосин – это смесь молекул алканов, в составе которых от двенадцати до восемнадцати атомов углерода. Подожжем небольшие количества гексана и керосина. Гексан загорается сразу: алканы с небольшой молекулярной массой загораются легко.
Поджечь керосин оказывается немного труднее, появляется коптящее пламя. В виде копоти выделяется несгоревший углерод. Большинство алканов горят коптящим пламенем из-за высокого содержания углерода. Мы убедились в том, что алканы с небольшой молекулярной массой загораются легче, чем алканы с большой молекулярной массой.
Оборудование: фарфоровые чашки, лучина, огнезащитная прокладка.
Техника безопасности. Соблюдать правила работы с горючими жидкостями. Работать с небольшими количествами жидких углеводородов (не более 2 мл).
Горение твердых углеводородов (на примере парафина)
Парафин – смесь твердых алканов, содержащих в своем составе от 16 до 40 атомов углерода. Твердый парафин на воздухе загорается с трудом. Кипящий парафин на воздухе самовозгорается. Нагреем парафин до кипения. Выливаем кипящий парафин из пробирки в кристаллизатор, наполненный водой. Кипящий парафин, смешиваясь с воздухом, загорается. При горении парафина образуются углекислый газ и водяные пары.
Оборудование: пробирка, зажим пробирочный, горелка, кристаллизатор.
Техника безопасности. Соблюдать правила работы с горючими веществами. Не наклоняться над кипящим парафином. Не допускать попадание парафина на одежду, кожу.
Установление качественного состава предельных углеводородов
Общим методом определения углерода и водорода в органических соединениях является окисление веществ оксидом двухвалентной меди. При этом углерод окисляется до углекислого газа, а водород до воды. Оксид меди (II) восстанавливается до меди или до оксида одновалентной меди, имеющих красный цвет
С18Н38 + СuО = 18СО2 + 19 Н2О + 55Сu
Углекислый газ обнаруживают при помощи известковой воды. Известковая вода мутнеет от углекислого газа.
Ca (OH)2 + CO2 = CaCO3 ↓ + H2O
Воду обнаруживают безводным сульфатом меди (II). Под действием воды белый сульфат меди (II) переходит в голубой кристаллогидрат — медный купорос
CuSO4 + 5H2O = CuSO4 * 5 H2O
Оборудование: пробирка с газоотводной трубкой, стакан, штатив, горелка.
Техника безопасности. Соблюдать правила работы с нагревательными приборами.
Определение содержания хлора в органических соединениях
Качественно определить содержание галогена в органическом соединении можно при помощи медной проволоки. При нагревании с оксидом меди (II) галогенсодержащие вещества сгорают с образованием летучих соединений, окрашивающих пламя в сине-зеленый цвет. Эта качественная реакция на галогены в органических соединениях называется пробой Бейльштейна. Для проведения пробы медную проволоку прокаливают в пламени горелки, опускают в жидкость или касаются твердого вещества и вновь вносят в пламя горелки. Появление сине-зеленого окрашивания, свидетельствует о наличии галогена в органическом соединении. Испытаем диметиламин хлорид и убедимся в том, что в его составе присутствует галоген — хлор.
Оборудование: горелка, медная спираль.
Техника безопасности. Соблюдать правила работы с нагревательными приборами.
- Опыт 10. Получение метана из ацетата натрия и его свойства
- По теме лабораторной работы
- Метан: способы получения и свойства
- Гомологический ряд метана
- Строение метана
- Изомерия метана
- Химические свойства метана
- 1. Реакции замещения
- 1.1. Галогенирование
- 1.2. Нитрование метана
- 2. Реакции разложения метана (д егидрирование, пиролиз)
- 3. Окисление метана
- 3.1. Полное окисление – горение
- 3.2. Каталитическое окисление
- Получение метана
- 1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
- 2. Водный или кислотный гидролиз карбида алюминия
- 3. Декарбоксилирование солей карбоновых кислот (реакция Дюма)
- 4. Синтез Фишера-Тропша
- 5. Получение метана в промышленности
Опыт 10. Получение метана из ацетата натрия и его свойства
Опыт 10. Получение метана из ацетата натрия и его свойства.
В пробирку, снабженную пробкой с газоотводной трубкой, поместить смесь, состоящую из одной частя обезвоженного тонкоизмельченного ацетата натрия и двух частей натронной извести (NaOH в СаО). Общий объем смеси 3. 4 см (около 1/3нагреть ее в пламени горелки.
Поджечь метан у выхода газоотводной трубки через 1. 2 минуты после выделения газа, т. е. после того, как улетучится гремучая смесь (будьте осторожны: смесь взрывоопасна!). Обратите внимание на то, что метан горит светящимся пламенем.
Выделяющийся метан пропустить через растворы бромной воды и KMnO4. Изменяется ли окраска последних, почему? Напишите уравнения реакций образования метана и горения метана.
Опыт 11. Бромирование гексана.
В сухую пробирку поместить 1 мл гексана и несколько капель бромной волы (Br2). Содержимое пробирки перемешать на холоде. Отметить, исчезает ли окраска брома. Нагреть содержимое пробирки до исчезновения окраски. Реакция сопровождается выделением HBr.
Объясните наблюдаемое явление, напишите уравнение соответствующей реакции и предложите радикальный цепной механизм бромирования гексана.
Опыт 12. Получение этилена и его свойства.
В коническую колбу на 50 мл, снабженную пробкой с газоотводной трубкой, поместить 4. 5 мл заранее приготовленной смеси (1 часть этилового спирта и 5 частей серной кислоты) и добавить немного песку, который необходим для обеспечения равномерного кипения. Конец газоотводной трубки опустить в пробирку с 4. 5 мл бромной воды. Нагреть колбу со смесью в пламени горелки. Во избежание затягивания раствора бромной воды при перерывах в нагревании следует сначала удалить пробирку с раствором бромной воды, а затем прекратить нагревание. Убедившись, что бромная вода быстро обесцвечивается, немедленно опустить конец газоотводной трубки в заранее приготовленную пробирку с 3. 4 мл раствора KMnO4. Продолжая нагревание колбы, обратить внимание на быстрое обесцвечивание розового раствора KMnO4. При этом этилен окисляется, образуя двухатомный спирт — этиленгликоль, а раствор буреет за счет выделяющегося диоксида марганца.
Заканчивая опыт (после пропускания этилена через бромную воду и раствор перманганата калия), этилен можно поджечь у конца газоотводной трубки. Он горит несветящимся пламенем.
При взаимодействии этилового спирта и концентрированной серной кислоты выделяется вода и образуется сложный эфир:
CH3—CH2—ОН + HO—SO3H

Этиловый эфир серной кислоты
При нагревании сложного эфира серная кислота регенерируется и выделяется газообразный этилен:
Таким образом, серная кислота в итоге отнимает от этилового спирта молекулу воды. Напишите уравнения реакций: взаимодействия этилена с бромом и предложите цепной ионный механизм бромирования этилена, окисления этилена перманганатом калия, горения этилена.
Опыт 13. Получение ацетилена и исследование его свойств.
В сухую пробирку поместить кусочек карбида кальция и прилить воду, быстро закрыть пробирку пробкой с газоотводной трубкой и выделяющийся газ пропустить последовательно в пробирки с бромной водой, раствором KMnO4 и аммиачным раствором оксида серебра.
После обесцвечивания растворов в первых двух пробирках и выпадения осадка в третьей пробирке поджечь газ у конца отводной трубки. Ацетилен горит коптящим пламенем. Образовавшийся в третьей пробирке осадок отфильтровать, высушить, положить на асбестовую сетку включенной электроплитки и отойти на безопасное расстояние. При высыхании фильтра и осадка при дальнейшем подогреве происходит громкий взрыв ацетиленида серебра.
Напишите уравнения реакций получения ацетилена, взаимодействия ацетилена с бромом, окисления ацетилена раствором KMnO4, которое происходит с образованием промежуточного соединения — щавелевой кислоты, окисляющейся далее до диоксида углерода и уравнение реакции ацетилена с аммиачным раствором оксида серебра-[Ag(NH3)2]OH.
По теме лабораторной работы
Лабораторная работа № 1
Тема: Получение метана и изучение его свойств.
Цель: изучить свойства метана; опытным путем исследовать их.
Реактивы и оборудование: прибор для получения газа, заправленный смесью ацетата натрия и натронной извести, металлический штатив, держалка, кристаллизатор, штатив с пробирками, раствор перманганата калия, раствор йодной воды, стакан, спиртовка, спички.
Краткие теоретические и учебно-методические материалы
по теме лабораторной работы
Предельными или насыщенными углеводородами называют ациклические углеводороды, в которых все валентности атомов углерода, не затраченные на образование углерод – углеродных (С — С) связей, насыщены атомами водорода. Ациклические соединения – вещества, имеющие прямую или разветвленную, но обязательно открытую (незамкнутую) цепь углеродных атомов. Первым членом класса предельных углеводородов является метан – СН4. Предельные углеводороды образуют гомологический ряд. Гомологическим рядом называют ряд органических соединений, сходных по своему химическому строению, имеющих общие методы получения, обладающих близкими химическими и закономерно изменяющимися физическими свойствами.
Общая формула предельных углеводородов CnH2n +2. Метан представляет собой газ (tкип. = -111 о С, tпл. = -192 о С), легче воздуха.
Молекулы предельных углеводородов содержат ковалентные связи. Вследствие малой химической активности предельные углеводороды получили название парафинов (от латинского выражения: лишенные сродства, с трудом вступающие в реакции). Парафины настолько малоактивны, что даже с очень активными химическими реагентами (О2, галогены) вступают во взаимодействие только после предварительного возбуждения реагирующих веществ – нагревания или под действием яркого (или ультрафиолетового) света.
В молекулах предельных углеводородов атомы углерода либо связаны между собой простыми связями (С – С связи) либо с атомами водорода
(С – Н связи). Поэтому при химических реакциях могут разрываться или
С – С или С – Н связи. Наиболее важными реакциями, характеризующими химические свойства предельных углеводородов, являются реакции замещения атомов водорода на
атомы галогенов. Образуются моно-, ди-, три- и полигалогензамещенные предельных углеводородов.
Гомологи метана могут расщепляться не только с разрывом С – Н связей и отщеплением водорода (дегидрогенизация), но и с разрывом С – С связей (крекинг). При этом образуется смесь предельных и непредельных соединений, например:
В лаборатории для получения метана и его гомологов пользуются разложением солей органических кислот при прокаливании их со щелочами:
Другим лабораторным способом получения предельных углеводородов служит реакция Вюрца – нагревание моногалогенпроизводных предельных углеводородов с металлическим натрием:
В этой реакции происходит «удвоение» радикалов, входящих в состав галогенпроизводного, т.е. из С3Н7Cl можно получить С6Н14 и т.д.
ХОД РАБОТЫ
Опыт №1.Получение метана
Метан в лаборатории получают прокаливанием безводного ацетата натрия с натронной известью. Натронная известь представляет собой смесь гидроксида натрия с гидроксидом кальция. Возьмем натронную известь и ацетат натрия, тщательно перемешаем и поместим в пробирку. Закроем пробирку пробкой с газоотводной трубкой. Нагреем смесь. Через некоторое время начинает выделяться метан
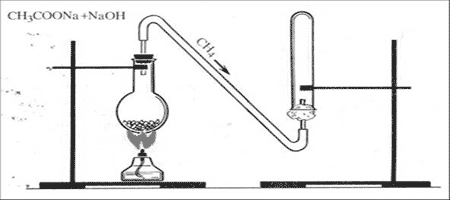
Поджигаем метан. Он горит почти бесцветным пламенем. При горении метана образуется углекислый газ и вода.
Опыт №2.Горение метана и изучение его физических свойств
Заполним метаном цилиндр. Метан представляет собой бесцветный газ, мало растворимый в воде. Он легче воздуха, поэтому легко улетучивается из открытого цилиндра. При поджигании метан загорается. При сгорании метана образуются углекислый газ и водяные пары.
Метан: способы получения и свойства
Метан CH4 – это предельный углеводород, содержащий один атом углерода в углеродной цепи. Бесцветный газ без вкуса и запаха, легче воды, нерастворим в воде и не смешивается с ней.
Гомологический ряд метана
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Самый первый представитель гомологического ряда алканов – метан CH4, или Н–СH2–H.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Строение метана
В молекуле метана встречаются связи C–H. Связь C–H ковалентная слабополярная. Это одинарная σ-связь. Атом углерода в метане образует четыре σ-связи. Следовательно, гибридизация атома углерода в молекуле метана– sp 3 :
При образовании связи С–H происходит перекрывание sp 3 -гибридной орбитали атома углерода и s-орбитали атома водорода:
Четыре sp 3 -гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109 о 28′ друг к другу:
Это соответствует тетраэдрическому строению молекулы.
| Например, в молекуле метана CH4 атомы водорода располагаются в пространстве в вершинах тетраэдра, центром которого является атом углерода |
Изомерия метана
Для метана не характерно наличие изомеров – ни структурных (изомерия углеродного скелета, положения заместителей), ни пространственных.
Химические свойства метана
Метан – предельный углеводород, поэтому он не может вступать в реакции присоединения.
Для метана характерны реакции:
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для метана характерны только радикальные реакции.
Метан устойчив к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагирует с концентрированными кислотами, щелочами, бромной водой.
1. Реакции замещения
Для метана характерны реакции радикального замещение.
1.1. Галогенирование
Метан реагирует с хлором и бромом на свету или при нагревании.
При хлорировании метана сначала образуется хлорметан:
Хлорметан может взаимодействовать с хлором и дальше с образованием дихлорметана, трихлорметана и тетрахлорметана:
| Химическая активность хлора выше, чем активность брома, поэтому хлорирование протекает быстро и неизбирательно. |
Бромирование протекает более медленно.
Реакции замещения в алканах протекают по свободнорадикальному механизму.
Свободные радикалы R∙ – это атомы или группы связанных между собой атомов, которые содержат неспаренный электрон.
Первая стадия. Инициирование цепи.
Под действием кванта света или при нагревании молекула галогена разрывается на два радикала:
Свободные радикалы – очень активные частицы, которые стремятся образовать связь с каким-либо другим атомом.
Вторая стадия. Развитие цепи.
Радикал галогена взаимодействует с молекулой алкана и отрывает от него водород.
При этом образуется промежуточная частица – алкильный радикал, который в свою очередь взаимодействует с новой нераспавшейся молекулой хлора:
Третья стадия. Обрыв цепи.
При протекании цепного процесса рано или поздно радикалы сталкиваются с радикалами, образуя молекулы, радикальный процесс обрывается.
Могут столкнуться как одинаковые, так и разные радикалы, в том числе два метильных радикала:
1.2. Нитрование метана
Метан взаимодействует с разбавленной азотной кислотой по радикальному механизму, при нагревании до 140 о С и под давлением. Атом водорода в метане замещается на нитрогруппу NO2.
Например. При нитровании метана образуется преимущественно нитрометан:2. Реакции разложения метана (д егидрирование, пиролиз)При медленном и длительном нагревании до 1500 о С метан разлагается до простых веществ: Если процесс нагревания метана проводить очень быстро (примерно 0,01 с), то происходит межмолекулярное дегидрирование и образуется ацетилен: Пиролиз метана – промышленный способ получения ацетилена. 3. Окисление метанаАлканы – малополярные соединения, поэтому при обычных условиях они не окисляются даже сильными окислителями (перманганат калия, хромат или дихромат калия и др.). 3.1. Полное окисление – горениеАлканы горят с образованием углекислого газа и воды. Реакция горения алканов сопровождается выделением большого количества теплоты. Уравнение сгорания алканов в общем виде: При горении алканов в недостатке кислорода может образоваться угарный газ СО или сажа С. Промышленное значение имеет реакция окисления метана кислородом до простого вещества – углерода: Эта реакция используется для получения сажи. 3.2. Каталитическое окисление
Продукт реакции – так называемый «синтез-газ». Получение метана1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)Это один из лабораторных способов получения алканов. При этом происходит удвоение углеродного скелета. Реакция больше подходит для получения симметричных алканов. Получить таким образом метан нельзя. 2. Водный или кислотный гидролиз карбида алюминияЭтот способ получения используется в лаборатории для получения метана. 3. Декарбоксилирование солей карбоновых кислот (реакция Дюма)Реакция Дюма — это взаимодействие солей карбоновых кислот с щелочами при сплавлении. R–COONa + NaOH → R–H + Na2CO3 Декарбоксилирование — это отщепление (элиминирование) молекулы углекислого газа из карбоксильной группы (-COOH) или органической кислоты или карбоксилатной группы (-COOMe) соли органической кислоты. При взаимодействии ацетата натрия с гидроксидом натрия при сплавлении образуется метан и карбонат натрия: 4. Синтез Фишера-ТропшаИз синтез-газа (смесь угарного газа и водорода) при определенных условиях (катализатор, температура и давление) можно получить различные углеводороды: Это промышленный процесс получения алканов. Синтезом Фишера-Тропша можно получить метан: 5. Получение метана в промышленностиВ промышленности метан получают из нефти, каменного угля, природного и попутного газа . При переработке нефти используют ректификацию, крекинг и другие способы. |