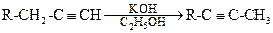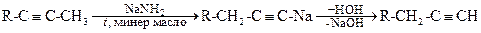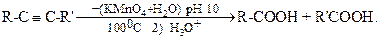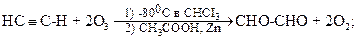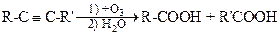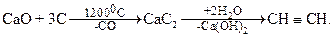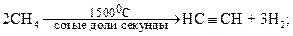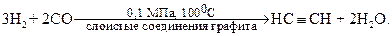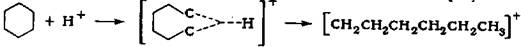Фаворский установил, что изомеризация терминального алкина в алкин с внутренней тройной связью протекает при 170 0 С в присутствии спиртового раствора щелочи.
Если же алкины с неконцевой тройной связью нагревать в минеральном масле при 120-160 0 С с амидом натрия, то они быстро и практически необратимо превращаются в Na-производные терминальных алкинов.
Реакции алкинов с разрушением связи Сsp-Н
Алкины, имеющие атомы водорода при sp-гибридизированном атоме углерода (концевая тройная связь) являются СН-кислотами, причем более сильными, чем алканы, алкены, аммиак, но более слабыми, чем вода, спирт.
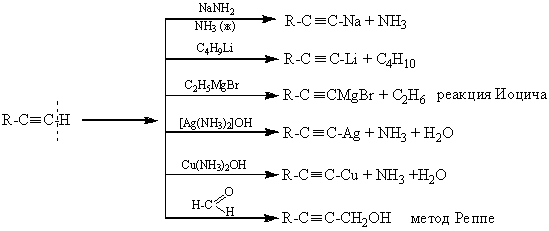
При действии очень сильных оснований алкины, имеющие концевую (торсионную) связь, полностью ионизируются и образуют соли, которые называют ацетиленидами.
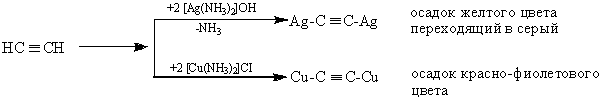
Если реакции протекают с ацетиленом, то возможно замещение двух атомов водорода.
Полученные ацетилениды щелочных металлов разлагаются водой.
В отличие от ацетиленидов щелочных и щелочноземельных металлов ацетилениды меди и серебра устойчивы к действию воды и разрушаются с выделением ацетилена только под действием сильных кислот. Однако в сухом виде они неустойчивы и взрываются при нагревании, трении, ударе.
Ацетилиниды нашли применение в органическом синтезе для получения производных ацетилена.
Окисление алкинов
Окисление алкинов в жестких условиях сильными окислителями, например, раствор KMnO4, концентрированной HNO3, при нагревании приводит к расщеплению углеродного скелета:
В нейтральной среде реакция протекает с образованием дикетона:
Озонирование алкинов зависит от условия проведения реакции:
а) при низких температурах образуются диальдегид-глиоксаль
б) при нагревании
образуется смесь карбоновых кислот.
Ацетилен горит в атмосфере кислорода с образованием пламени с температурой 2800 0 С
Его используют для сварки и резки металлов.
Ацетилен образует с воздухом взрывчатые смеси в широких пределах (от 5 до 80% ацетилена).
Получение алкинов
1. Карбидный метод
2. Пиролиз метана, этилена
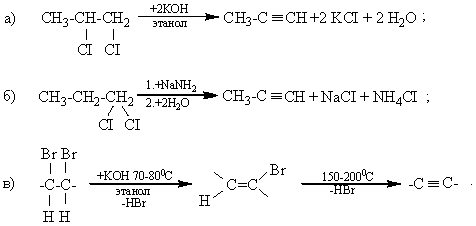
3. Дегидрогалогенирование дигалогенопроизводных
4. Из оксида углерода и водорода
5. Из ацетиленидов
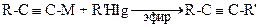
где М: К, Na, Li, Ag, MgCI.
6. Дегалогенирование тетрабромпроизводных алканов
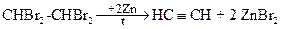
Дата добавления: 2016-02-16 ; просмотров: 2766 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Видео:Реакции изомеризации углеводородовСкачать

Реакции, сопровождающие изомеризацию
Реакция изомеризации сопровождается рядом побочных реакций — крекинга, гидрокрекинга и диспро-порционирования; так, молекула н-гексана может подвергаться гидрокрекингу в следуюшие продукты:
Необходимо отметить, что основным направлением реакций гидрокре-кинга является превращение н-гексана в пропан и бутан, реакция с образовани-ем метана практически не имеет места. Реакция диспропорционирования про-исходит с образованием парафиновых углеводородов с более низкой и высокой молекулярной массой:
При протекании реакции диспропорционирования парафиновых углево-дородов на морденитсодержащих цеолитных катализаторах в продуктах реакции не обнаруживаются углеводороды с молекулярной массой выше исходного, так как имеет место реакция их гидрокрекинга
Поэтому основная реакция при осуществлении диспропорционирования гексанов на цеолитном катализаторе в среде водорода приближенно соответст-вует суммарному уравнению
О механизме реакции диспропорционирования парафиновых углеводоро-дов существуют различные точки зрения: для алюмоплатиновых катализаторов, модифицированных хлором, предполагают следующее протекание реакций :
Карбкатион в кислотной системе находится в равновесии с олефинами (I), которые совместно с карбкатионом могут подвергаться алкилированию (II) и реакции крекинга (III). Гексен, образующийся по уравнению (III), может алки-лироваться с С5-карбкатионом до С11 -карбкатиона (по схеме 11), последний подвергается крекингу и т. д. В случае гексанов и гептанов реакции диспропор-ционирования могут протекать значительно быстрее, так как более высокомо-лекулярные карбкатионы могут присутствовать в более высоких концентраци-ях. Результатом высокой концентрации высших олефинов будет гидридный пе-ренос от олефина к карбкатиону, что приведет к образованию аллильных ионов карбония и в свою очередь, к дезактивации катализатора. Реакцию диспропор-ционирования можно подавить, снизив концентрацию карбкатиона и, следова-тельно, концентрацию олефинов. Добавление водорода может сдвинуть равно-весие по уравнению
Уменьшение концентрации карбкатиона приводит к снижению скорости диспропорционирования. Существует мнение, что на цеолитсодержащих ката-лизаторах, в частности на мордените в катионзамешенных формах (Н, Мо, Са, Sr), диспропорционирование протекает за счет реакций трансметилирования. По некоторым данным, наиболее существенную роль играют отщепление и масс-межмолекулярный перенос С2-фрагментов. Ряд исследователей высказы-ваются за механизм реакций по схеме конденсация — крекинг, т. е. без образова-ния низкомолекулярных алкилирующих агентов.
В промышленных процессах изомеризации н-пентана и н-гексана на ка-тализаторах Pt-А12O3-F, Pt-А12O3-CI, Pt-HM-А12O3 найден баланс между реак-циями изомеризации, гидрокрекинга и диспропорционирования, который по-зволяет осуществить процесс с высокой селективностью; в случае изомериза-ции гептанов не достигнуто удовлетворительных результатов.
При осуществлении процессов изомеризации пентан-гексановых фрак-ций, выкипающих до 70oС, в состав их помимо пентанов и гексанов входят вы-сококипящие парафиновые углеводороды, нафтеновые и ароматические угле-водороды (бензол, метилциклопентан, циклогексан, гептаны).
В процессе изомеризации на платиновых катализаторах эти углеводороды подвергаются превращениям в соответствии с условиями термодинамического равновесия для каждого углеводорода по нижеследующим реакциям:
Влияние нафтенов на активность катализаторов в реакции изомеризации парафинов различается в зависимости от природы катализатора и условий осу-ществления реакции. В процессе высокотемпературной изомеризации на алю-моплатиновом катализаторе, промотированном фтором, нафтены, пока их мас-совая доля не превышает 15%, практически не оказывают влияния на глубину изомеризации парафинового углеводорода.
В процессе низкотемпературной изомеризации на алюмоплатиновом ка-тализаторе, промотированном хлором, в присутствии нафтенов скорость реак-ции снижается. В случае осуществления реакции изомеризации н-гексана в жидкой фазе на сверхкислотных катализаторах влияние нафтеновых углеводо-родов специфично. Как следует из рассмотрения результатов, представленных на рис. 5.24, циклогексан оказывает промотирующее действие на скорость изо-меризации н-гексана на HF-SbF5; в противоположность этому реакции крекинга и диспропорционирования подавляются.
Рис. 5.24 Влияние циклогексана на константу скорости образования 2,2-диметил-бутана и образование побочных продуктов при изомеризации н-гексана: Т=50°C; РН2 =0,4МПа; мольноеотношение С6Н14: MF5=10, HF:MF5=10; время реакции 30 мин.
Влияние циклогексана на скорость реакции изомеризации н-парафина и побочных реакций уменьшается по мере увеличения содержания циклогексана в исходном сырье. Для объяснения полученных результатов было изучено пре-вращение циклогексана в присутствии HF — SbF5, которое показало, что помимо изомеризации циклогексана в метилциклопентан наблюдается образование изо-гексанов в количествах до 8% (рис. 5.25).
Рис. 5.25 Кривые накопления метилциклопентана (1) и изогексанов (2) при изомеризации циклогексана: Т=50°C; РН2 =0.4 MПa; мольное отношение С6Н12:MF5=15, HF:MF5=10.
На основании полученных результатов превращение циклогексана в при-сутствии HF — SbF5 можно представить следующим образом: при протолизе С-
С-связи циклогексана образуется циклогексониевый ион, который, расщепля-ясь, дает гексильный катион:
В результате этой реакции катализатор переходит в R-форму — раствор C6H13SbF6- в HF. Следующим актом является образование циклогексильного иона, который претерпевает перегруппировку в метилциклопентильный катион и отрывает гидрид-ион от нейтральной молекулы углеводорода:
Из представленной схемы видно, что изомеризация циклогексана сопро-вождается образованием изогексанов. Реакция протекает до тех пор, пока все гексильные катионы в комплексе R+MF6- не будут замещены на циклогексиль-ный или метилодклопентильный ион С6Н11+, что хорошо согласуется с экспе-риментальными результатами. Водород не участвует в образовании гексанов, скорость реакции не изменяется в отсутствие водорода (табл. 3).
Таблица 5.10 Превращение циклогексана на сверхкислотном катализаторе HF-SbF5 Условия: температура 50oС; мольное отношение С6Н12:MF5=15, HF:MF5=10; время контакта 60 мин.
Отсюда можно сделать вывод, что влияние нафтенов на превращение па-рафиновых углеводородов определяется характером взаимодействия нафтенов с катализатором. В сверхкислотных средах HF — SbF5 нафтены образуют ком-плекс RMF6, как и парафиновые углеводороды. Скорость образования этого комплекса для различных углеводородов неодинакова и убывает в ряду С6Н12 ≈

Нафтеновые углеводороды являются более сильными органическими ос-нованиями, чем парафины, поэтому присутствие их в сырье должно снижать возможность прямого присоединения карбкатиона по s -связи парафинов, кото-рое ведет к образованию продуктов распада и циклических углеводородов.
Можно предположить также, что образование продуктов крекинга и дис-пропорционирования протекает по механизму, включающему участие олефи-нов; в этом случае роль нафтенов должна сводиться к алкилированию непредельных соединений.
На алюмоплатиновых катализаторах, промотированных фтором, взаимного влияния пентанов и гексанов при изомеризации не наблюдается. В случае проведения реакции на алюмоплатиновом катализаторе, промотированном хлором, и на морденитсодержащих катализаторах с увеличением содержания пентанов в сырье увеличивается выход изогексанов, в том числе и 2,2-диметилбутана.
Показано, что при смешении н-пентана и н-гексана скорость изомеризации н-пентана снижается, в то время как скорость изомеризации н-гексана уве-личивается (рис. 5.26). Эти результаты соответствуют гипотезе о том, что н-гексан адсорбируется сильнее, чем н-пентан. Так как молекулы н-пентана и н-гексана достаточно малы, чтобы не задерживаться в порах морденита, то диффузия в порах не должна оказывать влияние на константу скорости реакции. Следовательно, единственное объяснение наблюдаемого явления — это преимущественная адсорбция н-гексана на активных центрах морденита. Статистический анализ показывает, что модель, соответствующая преимущественной адсорбции н-гексана, более корректна.
Рис. 5.26. Изомеризация н-пентана, н-гексана и их смесей на Pt-НM — А12О3: Т=140°С, РН2 =2,2 МПа: мольное отношение Н2 : углеводород = 10.
Приведенные здесь данные имеют большое практическое значение. При выборе состава сырья, оценке результатов и показателей изомеризации парафи-новых углеводородов в различных процессах необходимо учитывать углеводо-родный состав сырья, в особенности содержание пентанов и нафтенов; увеличение содержания пентанов всегда приводит к более благоприятному протека-нию процесса изомеризации, в частности к более высокому октановому числу получаемого изомеризата.
Вопрос о влиянии водорода на протекание реакции изомеризации пара-финовых углеводородов на рассмотренных катализаторах обсуждался в ряде работ, но до сих пор не получил однозначного толкования .
На алюмоплатиновом катализаторе, промотированном фтором, реакция изомеризации парафиновых углеводородов не происходит в отсутствие водорода; если катализатор модифицирован хлором, реакция в начальный период протекает и в отсутствие водорода (то же явление имеет место и на фторидах металлов V и VI групп, активированных фтороводородом), но с течением вре-мени ее скорость постепенно уменьшается.
Чтобы реакция изомеризации на металлсодержащем катализаторе проте-кала постоянно, ее необходимо осуществлять в среде водорода. Это связано с явлениями адсорбции и диссоциации водорода на металле и переноса частиц водорода с металла на носитель. Имеют место также явления конкурентной ад-сорбции водорода и промежуточных ненасыщенных соединений на поверхно-сти катализатора, при этом часть этих соединений вытесняется водородом с по-верхности катализатора, что также обеспечивает его стабильную работу.
Несмотря на различный механизм превращения парафиновых углеводо-родов на всех рассмотренных катализаторах, для них наблюдается общность кинетических закономерностей н торможение реакции изомеризации парафи-новых углеводородов избытком водорода. Для всех катализаторов зависимость скорости реакции от парциального давления водорода носит экстремальный характер после достижения определенной концентрации водорода на поверхности катализатора. Величина и положение максимума зависят от типа катализатора, температуры и молекулярной массы парафинового углеводорода.
При низком давлении водорода скорость реакции изомеризации опреде-ляется скоростью образования промежуточных ненасыщенных соединений, ко-торые десорбируются в газовую фазу путем вытеснения их с поверхности ката-лизатора водородом. Таким образом, возрастание скорости реакции изомериза-ции при увеличении парциального давления водорода от нуля до определенной величины связано с явлениями ограничения избыточных концентраций проме-жуточных ненасыщенных соединений; тем самым водород препятствует обра-зованию из них прочно адсорбированных соединений на поверхности катализа-тора. С увеличением парциального давления водорода выше определенного промежуточные соединения и водород начинают конкурировать за участки по-верхности, ответственные за .протекание реакции, и дальнейшее увеличение давления водорода приводит к уменьшению скорости реакции.
В случае осуществления реакции на алюмоплатиновых катализаторах, промотированньах фтором и хлором, и на металлцеолитных катализаторах ско-рости реакций гидрокрекинга и диспропорционирования имеют максимальное значение в отсутствие водорода, постепенно уменьшаются при увеличении парциального давления водорода до некоторого предела и увеличиваются при дальнейшем его повышении.
Итак, существует оптимальное соотношение концентрации водорода и углеводорода на поверхности катализатора, при котором устанавливается рав-новесие между процессами регенерации поверхности катализатора водородом и адсорбционным вытеснением молекул углеводорода водородом с поверхности катализатора и ограничением протекания побочных. реакций. Определение об-ласти оптимального соотношения очень важно для выбора технологических па-раметров процесса, определяющих активность, селективность и стабильность катализатора. Было показано, что в случае осуществления реакции изомериза-ции н-гексана на HF-SbF5 с увеличением парциального давления водорода ско-рость реакций гидрокрекинга и диспропорционирования н-гексана снижается, одновременно несколько снижается и скорость его изомеризации (рис.5.27).
Рис. 5.27. Зависимость константы скорости образования 2,2-диметилбутана (I) и выхода побочных продуктов (2) от парциального давления водорода при изо-меризации н-гексана: Т=50oС; мольное отношение С6Н14- SbF5 =10:1; HF: SbF5 =10: 1; время реакции 60 мин.
Согласно взглядам Ола, взаимодействие карбкатиона и молекулы пара-финового углеводорода протекает через образование промежуточного пентако-
В присутствии катализаторов НС1 — А1С13 и HF — ВF3 ингибирование во-дородом реакции гидрокрекинга и диспропорционирования, а также реакции изомеризации объясняется снижением концентрации карбкатионов по реакции


Эта реакция конкурирует с реакциями (I) — (III). Таким образом, водород снижает скорости реакций изомеризации, гидрокрекинга и диспропорциониро-вания парафиновых углеводородов в присутствии сверхкислот. Как уже упоми-налось, высказано предположение об участии водорода в медленной стадии реакции изомеризации адсорбированных фрагментов на кислотных центрах ката-лизатора.
Видео:Как решать ОРГАНИЧЕСКИЕ ЦЕПОЧКИ? Основные типы химических реакцийСкачать

ИЗОМЕРИЗАЦИЯ
ИЗОМЕРИЗАЦИЯ – превращение одного изомера в другой (см. ИЗОМЕРИЯ). Изомеризация приводит к получению соединения с иным расположением атомов или групп, но при этом не происходит изменение состава и молекулярной массы соединения. В литературе изомеризацию часто называют перегруппировкой, в некоторых случаях, в соответствии с традицией, это именные реакции.
Наиболее известный катализатор перестройки углеводородного скелета – AlCl3, в присутствии этого катализатора осуществляют превращение линейных углеводородов в разветвленные (см. рис. 1, реакция 1), проводят перестройку циклических углеводородов (см. рис. 1, реакция 2), получают из полициклических соединений углеводородные каркасы (см. рис. 1, реакция 3). Этот же катализатор приводит к перемещению функциональных групп в молекуле (см. рис. 1, реакция 4)
Рис. 1. Изомеризация углеводородного скелета и перемещение функциональных групп
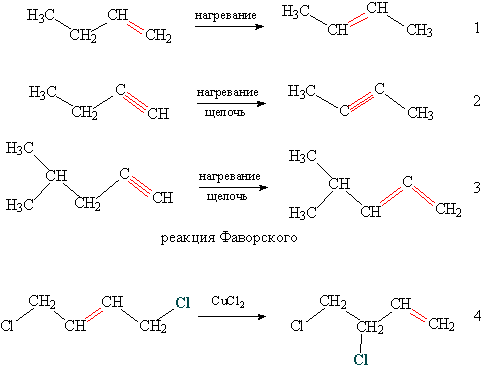
Изменение положения кратных связей проходит при нагревании, часто в присутствии щелочи (см. рис. 2, реакции 1, 2), возможно также перераспределение кратных связей, когда тройная связь переходит в две двойные связи – реакция Фаворского (см. рис. 2, реакция 3). У галогенированных ненасыщенных соединений происходит одновременное перемещение кратной связи и атома галогена (см. рис. 2, реакция 4).
Рис. 2. Перемещение кратных связей и атомов галогена
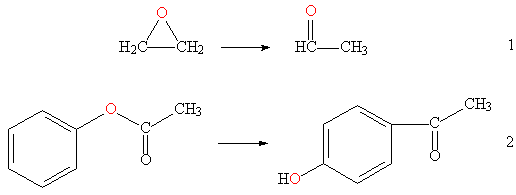
Изомеризация кислородсодержащих соединений часто приводят к изменению природы функциональной группы, например, превращение простой эфирной связи в альдегидную группу (см. рис. 3, реакция 1), или в гидроксильную (см. рис. 3, реакция 2).
Рис. 3. Изомеризация О-содержащих соединений.
Существуют примеры изомеризации N- и Р-содержащих соединений, проходящей обычно с участием атома кислорода. В подобных перестройках молекул помимо перемещения O, N и P-атомов происходит изменение положения некоторых атомов водорода или органических групп.
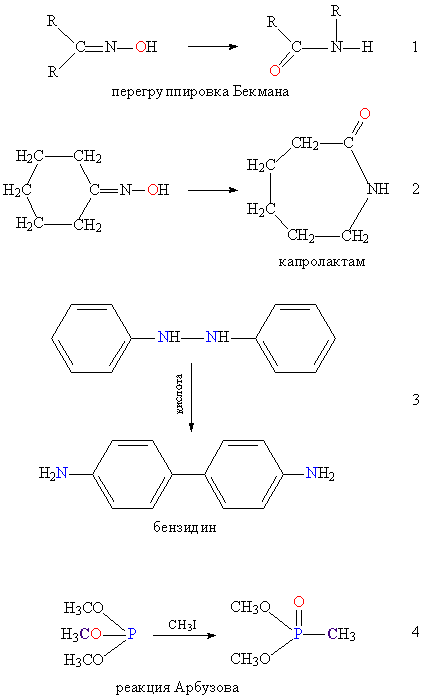
При перегруппировке Бекмана (см. рис. 4, реакция 1) гидроксильная группа превращается в карбонильную. Другой вариант перегруппировки Бекмана (см. рис. 4, реакция 2) сопровождается расширением цикла.
При бензидиновой перегруппировке происходит миграция атомов азота и водорода (см. рис. 4, реакция 3)
Реакция Арбузова превращает трехвалентный атом фосфора в пятивалентный, одновременно происходит образование Р-С – связи (см. рис. 4, реакция 4).
Рис. 4. Изомеризация O, N и Р-содержащих соединений
Изомеризация обычно идет в том направлении, которое приводит к соединению, более стабильному в условиях данного опыта. Некоторые изомеризационные процессы при изменении типа катализатора или условий опыта обратимы.
Изомеризацию оптических изомеров изучает специальный раздел химии – динамическая стереохимия (См. также ВАЛЬДЕНОВСОЕ ОБРАЩЕНИЕ.).
Видео:ВСЕ ПРО АЛКАНЫ за 8 минут: Химические Свойства и ПолучениеСкачать

Применение изомеризации.
Переработка нефтяных продуктов (пиролиз, крекинг) обычно сопровождается изомеризацией линейных углеводородов в соединения с разветвленной цепью, которые имеют более высокое октановое число. Из продукта изомеризации хлорированного бутена (см. рис. 2, реакция 4) получают бензостойкий каучук хлоропрен.
Перегруппировку Бекмана применяют для промышленного синтеза капролактама (см. рис. 4, реакция 2), из которого получают поликапролактам (капрон). Бензидиновую перегруппировку (см. рис. 4, реакция 3) используют для получения соединений, применяемых в производстве азокрасителей. Реакция Арбузова (см. рис. 4, реакция 4) позволяет получать соединения со связью С-Р, на основе которых производят пестициды.
Реакции и методы исследования органических соединений. М., 1954
Олехнович Л.П. Многообразие строения и форм молекул органических соединений. Соросовский Образовательный Журнал. 1997, № 2
🔥 Видео
Уравнивание реакций горения углеводородовСкачать

ОВР и Метод Электронного Баланса — Быстрая Подготовка к ЕГЭ по ХимииСкачать

Химические свойства алканов. 1 часть. 10 класс.Скачать

Составление уравнений химических реакций. 1 часть. 8 класс.Скачать

7 ВАЖНЕЙШИХ РЕАКЦИЙ, которые тебе нужно знать (Алкины)Скачать

Химические свойства алканов | Химия ЕГЭ для 10 класса | УмскулСкачать

ВСЯ ПРАВДА ПРО УДАЛЕНИЕ КАТАЛИЗАТОРА! Это должен знать каждый!Скачать

Реакции присоединения | Химия 10 класс | УмскулСкачать

Химическая кинетика. Скорость химической реакции | ХимияСкачать

КАК определить ЗАБИТЫЙ КАТАЛИЗАТОР | Признаки неисправности КАТАЛИЗАТОРА #1Скачать

Влияние концентрации на скорость химических реакций. 10 класс.Скачать

Изменение мощности двигателя после удаления катализатораСкачать

Видеоурок по химии "Типы химических реакций в органической химии"Скачать

Химическое равновесие. Константа равновесия. 10 класс.Скачать

Реакции присоединения в органике, которые протекают против правила Марковникова | Химия ЕГЭ | УмскулСкачать

25. Схема реакции и химическое уравнениеСкачать

Установка каталитической изомеризацииСкачать