- РАЗДЕЛ 7. ОБМЕН УГЛЕВОДОВ
- VIII. Катаболизм глюкозы
- Анаэробный гликолиз АТФ: схема и реакции
- Основные отличия дихотомического анаэробного распада глюкозы и аэробного гликолиза
- Реакции анаэробного гликолиза
- Промежуточный обмен глюкозы в организме
- Глюконеогенез. Роль печени в углеводном обмене.
- Основные пути метаболизма глюкозы
- Анаэробный распад глюкозы (гликолиз): значение анаэробного распада глюкозы. Эффект Пастера
- Энергетический эффект цикла Кребса
- Таблица 9 Энергетический эффект цикла Кребса
- Бескислородное окисление глюкозы включает два этапа
- Первый этап гликолиза
- Второй этап гликолиза
- Глюкоза крайне важна для энергетики клеток
- Глюкоза – это субстрат для получения энергии
- Глюкоза – это источник оксалоацетата
РАЗДЕЛ 7. ОБМЕН УГЛЕВОДОВ
VIII. Катаболизм глюкозы
Катаболизм глюкозы — основной поставщик энергии для процессов жизнедеятельности организма.
А. Основные пути катаболизма глюкозы
Окисление глюкозы до СО2 и Н2О (аэробный распад). Аэробный распад глюкозы можно выразить суммарным уравнением:
Этот процесс включает несколько стадий (рис. 7-33).
Рис. 7-33. Аэробный распад глюкозы. 1-10 — реакции аэробного гликолиза; 11 — малат-аспартатный челночный механизм транспорта водорода в митохондрии; 2 (в кружке) — стехиометрический коэффициент.
✵ Аэробный гликолиз — процесс окисления глюкозы с образованием двух молекул пирувата;
✵ Общий путь катаболизма, включающий превращение пирувата в ацетил-КоА и его дальнейшее окисление в нитратном цикле;
✵ ЦПЭ на кислород, сопряжённая с реакциями дегидрирования, происходящими в процессе распада глюкозы.
В определённых ситуациях обеспечение кислородом тканей может не соответствовать их потребностям. Например, на начальных стадиях интенсивной мышечной работы при стрессе сердечные сокращения могут не достигать нужной частоты, а потребности мышц в кислороде для аэробного распада глюкозы велики. В подобных случаях включается процесс, который протекает без кислорода и заканчивается образованием лактата из пировиноградной кислоты. Этот процесс называют анаэробным распадом, или анаэробным гликолизом. Анаэробный распад глюкозы энергетически малоэффективен, но именно этот процесс может стать единственным источником энергии для мышечной клетки в описанной ситуации. В дальнейшем, когда снабжение мышц кислородом будет достаточным в результате перехода сердца на ускоренный ритм, анаэробный распад переключается на аэробный. Пути катаболизма глюкозы и их энергетический эффект показаны на рис. 7-34.
Рис. 7-34. Пути катаболизма глюкозы. 1 — аэробный гликолиз; 2, 3 — общий путь катаболизма; 4 — аэробный распад глюкозы; 5 — анаэробный распад глюкозы (в рамке); 2 (в кружке) — стехиометрический коэффициент.
Б. Аэробный гликолиз
Аэробным гликолизом называют процесс окисления глюкозы до пировиноградной кислоты, протекающий, в присутствии кислорода. Все ферменты, катализирующие реакции этого процесса, локализованы в цитозоле клетки.
1. Этапы аэробного гликолиза
В аэробном гликолизе можно выделить 2 этапа.
1. Подготовительный этап, в ходе которого глюкоза фосфорилируется и расщепляется на две молекулы фосфотриоз. Эта серия реакций протекает с использованием 2 молекул АТФ.
2. Этап, сопряжённый с синтезом АТФ. В результате этой серии реакций фосфотриозы превращаются в пируват. Энергия, высвобождающаяся на этом этапе, используется для синтеза 10 моль АТФ.
2. Реакции аэробного гликолиза
Превращение глюкозо-6-фосфата в 2 молекулы глицеральдегид-3-фосфата
Глюкозо-6-фосфат, образованный в результате фосфорилирования глюкозы с участием АТФ, в ходе следующей реакции превращается в фруктозо-6-фосфат. Эта обратимая реакция изомеризации протекает под действием фермента глюкозофосфатизомеразы.
Затем следует ещё одна реакция фосфорилирования с использованием фосфатного остатка и энергии АТФ. В ходе этой реакции, катализируемой фосфофруктокиназой, фруктозо-6-фосфат превращается в фруктозо-1,6- бисфосфат. Данная реакция, так же, как гексокиназная, практически необратима, и, кроме того, она наиболее медленная из всех реакций гликолиза. Реакция, катализируемая фосфофруктокиназой, определяет скорость всего гликолиза, поэтому, регулируя активность фосфофруктокиназы, можно изменять скорость катаболизма глюкозы.
Фруктозо-1,6-бисфосфат далее расщепляется на 2 триозофосфата: глицеральдегид-3-фосфат и дигидроксиацетонфосфат. Реакцию катализирует фермент фруктозобисфосфатальдолаза, или просто альдолаза. Этот фермент катализирует как реакцию альдольного расщепления, так и альдольной конденсации, т. е. обратимую реакцию. Продукты реакции альдольного расщепления — изомеры. В последующих реакциях гликолиза используется только глицеральдегид-3-фосфат, поэтому дигидроксиацетонфосфат превращается с участием фермента триозофосфатизомеразы в глицероальдегид-3-фосфат (рис. 7-35).
Рис. 7-35. Превращение глюкозо-6-фосфата в триозофосфаты.
В описанной серии реакций дважды происходит фосфорилирование с использованием АТФ. Однако расходование двух молекул АТФ (на одну молекулу глюкозы) далее будет компенсировано синтезом большего количества АТФ.
Превращение глицеральдегид-3-фосфата в пируват
Эта часть аэробного гликолиза включает реакции, связанные с синтезом АТФ. Наиболее сложной в данной серии реакций является реакция превращения глицеральдегид-3-фосфата в 1,3- бисфосфоглицерат. Это превращение — первая реакция окисления в ходе гликолиза. Реакцию катализирует глицеральдегцд-3-фосфатдегидрогеназа, которая является NAD-зависимым ферментом. Значение данной реакции заключается не только в том, что образуется восстановленный кофермент, окисление которого в дыхательной цепи сопряжено с синтезом АТФ, но также и в том, что свободная энергия окисления концентрируется в макроэргической связи продукта реакции. Глицеральдегид-3-фосфатдегидрогеназа содержит в активном центре остаток цистеина, сульфгидрильная группа которого принимает непосредственное участие в катализе. Окисление глицеральдегид-3-фосфата приводит к восстановлению NAD и образованию с участием Н3РО4 высокоэнергетической ангидридной связи в 1,3-бис- фосфоглицерате в положении 1. В следующей реакции высокоэнергетический фосфат передаётся на АДФ с образованием АТФ. Фермент, катализирующий это превращение, назван по обратной реакции фосфоглицераткиназой (киназы называются по субстрату, находящемуся в уравнении реакции по одну сторону с АТФ). Данная серия реакций показана на рис. 7-36.
Рис. 7-36. Превращение глицеральдегид-3-фосфата в 3-фосфоглицерат.
Образование АТФ описанным способом не связано с дыхательной цепью, и его называют субстратным фосфорилированием АДФ. Образованный 3-фосфоглицерат уже не содержит макроэргической связи. В следующих реакциях происходят внутримолекулярные перестройки, смысл которых сводится к тому, что низкоэнергетический фосфоэфир переходит в соединение, содержащее высокоэнергетический фосфат. Внутримолекулярные преобразования заключаются в переносе фосфатного остатка из положения 3 в фосфоглицерате в положение 2. Затем от образовавшегося 2-фосфоглицерата отщепляется молекула воды при участии фермента енолазы. Название дегидратирующего фермента дано по обратной реакции. В результате реакции образуется замещённый енол — фосфоенолпируват. Образованный фосфоенолпируват — макроэргическое соединение, фосфатная группа которого переносится в следующей реакции на АДФ при участии пируваткиназы (фермент также назван по обратной реакции, в которой происходит фосфорилирование пиру- вата, хотя подобная реакция в таком виде не имеет места).
Превращение фосфоенолпирувата в пируват — необратимая реакция. Это вторая в ходе гликолиза реакция субстратного фосфорилирования. Образующаяся енольная форма пирувата затем неферментативно переходит в более термодинамически стабильную кетоформу. Описанная серия реакций представлена на рис. 7-37.
Рис. 7-37. Превращение 3-фосфоглицерата в пируват.
Схема 10 реакций, протекающих при аэробном гликолизе, и дальнейшее окисление пирувата представлены на рис. 7-33.
3. Окисление цитоплазматического NАDН в митохондриальной дыхательной цепи. Челночные системы
NADH, образующийся при окислении глицер- альдегид-3-фосфата в аэробном гликолизе, подвергается окислению путём переноса атомов водорода в митохондриальную дыхательную цепь. Однако цитозольный NADH не способен передавать водород на дыхательную цепь, потому что митохондриальная мембрана для него непроницаема. Перенос водорода через мембрану происходит с помощью специальных систем, называемых «челночными». В этих системах водород транспортируется через мембрану при участии пар субстратов, связанных соответствующими дегидрогеназами, т.е. с обеих сторон митохондриальной мембраны находится специфическая дегидрогеназа. Известны 2 челночные системы. В первой из этих систем водород от NADH в цитозоле передаётся на дигидроксиацетонфосфат ферментом глицерол-3-фосфатдегидрогеназой (NAD-зависимый фермент, назван по обратной реакции). Образованный в ходе этой реакции глицерол-3-фосфат, окисляется далее ферментом’ внутренней мембраны митохондрий — глицерол-3-фосфатдегидрогеназой (FAD- зависимым ферментом). Затем протоны и электроны с FADH2 переходят на убихинон и далее по ЦПЭ (рис. 7-38).
Рис. 7-38. Глицерофосфатная челночная система. 1 — глицеральдегид-3-фосфатдегидрогеназа; 2 — глицерол-3-фосфатдегидрогеназа (цитозольный фермент, назван по обратной реакции); 3 — глицерол-3-фосфатдегидрогеназа (митохондриальный флавиновый фермент).
Глицеролфосфатная челночная система работает в клетках белых мышц и гепатоцитов. Однако в клетках сердечных мышц митохондриальная глицерол-3-фосфатдегидрогеназа отсутствует. Вторая челночная система, в которой участвуют малат, цитозольная и митохондриальная малат- дегидрогеназы, является более универсальной. В цитоплазме NADH восстанавливает оксалоа- цетат в малат (рис. 7-39, реакция 1), который при участии переносчика проходит в митохондрии, где окисляется в оксалоацетат NAD-зави- симой малатдегидрогеназой (реакция 2). Восстановленный в ходе этой реакции NAD отдаёт водород в митохондриальную ЦПЭ. Однако образованный из малата оксалоацетат выйти самостоятельно из митохондрий в цитозоль не может, так как мембрана митохондрий для него непроницаема. Поэтому оксалоацетат превращается в аспартат, который и транспортируется в цитозоль, где снова превращается в оксалоацетат. Превращения оксалоацетата в аспартат и обратно связаны с присоединением и отщеплением аминогруппы (реакции трансаминирования, см. раздел 9). Эта челночная система называется малат-аспартатной (рис. 7-39). Результат её работы — регенерация цитоплазматического NAD + из NADH.
Рис. 7-39. Малат-аспартатная челночная система. 1,2 — окислительно-восстановительные реакции, обеспечивающие транспорт водорода из цитозоля в митохондрии на ЦПЭ; 3, 4 — транслоказы, обеспечивающие транспорт α-кетоглутарата, аспартата и глутамата и через мембрану митохондрий.
Обе челночные системы существенно отличаются по количеству синтезированного АТФ. В первой системе соотношение P/О равно 2, так как водород вводится в ЦПЭ на уровне KoQ. Вторая система энергетически более эффективна, так как передаёт водород в ЦПЭ через митохондриальный NAD + и соотношение Р/О близко к 3.
4. Баланс АТФ при аэробном гликолизе и распаде глюкозы до СO2 и Н2O
Выход АТФ при аэробном гликолизе
На образование фруктозо-1,6-бисфосфата из одной молекулы глюкозы требуется 2 молекулы АТФ (реакции 1 и 3 на рис. 7-33). Реакции, связанные с синтезом АТФ, происходят после распада глюкозы на 2 молекулы фосфотриозы, т. е. на втором этапе гликолиза. На этом этапе происходят 2 реакции субстратного фосфорилирования и синтезируются 2 молекулы АТФ (реакции 7 и 10). Кроме того, одна молекула глицеральдегид-3-фосфата дегидрируется (реакция 6), а NADH передаёт водород в митохондриальную ЦПЭ, где синтезируется 3 молекулы АТФ путём окислительного фосфорилирования. В данном случае количество АТФ (3 или 2) зависит от типа челночной системы. Следовательно, окисление до пирувата одной молекулы глицеральдегид-3-фосфата сопряжено с синтезом 5 молекул АТФ. Учитывая, что из глюкозы образуются 2 молекулы фосфотриозы, полученную величину нужно умножить на 2 и затем вычесть 2 молекулы АТФ, затраченные на первом этапе. Таким образом, выход АТФ при аэробном гликолизе составляет (5 x2) — 2 = 8 АТФ.
Выход АТФ при аэробном распаде глюкозы до конечных продуктов
В результате гликолиза образуется пируват, который далее окисляется до СO2 и Н2O в ОПК, описанном в разделе 6. Теперь можно оценить энергетическую эффективность гликолиза и ОПК, которые вместе составляют процесс аэробного распада глюкозы до конечных продуктов (табл. 7-4).
Таблица 7-4. Этапы аэробного распада глюкозы
Анаэробный гликолиз АТФ: схема и реакции
Основные отличия дихотомического анаэробного распада глюкозы и аэробного гликолиза
Аэробный распад глюкозы можно выразить суммарным уравнением:
С6Н12О6 + 6О2 → 6СО2 + Н2О + 2880 кДж/моль.
Этот процесс включает несколько стадий:
1. Аэробный гликолиз — процесс окисления глюкозы с образованием двух молекул пирувата; Аэробным гликолизом называют процесс окисления глюкозы до пировиноградной кислоты, протекающий в присутствии кислорода. Все ферменты, катализирующие реакции этого процесса, локализованы в цитозоле клетки.
2. Общий путь катаболизма, включающий превращение пирувата в ацетил-КоА и его дальнейшее окисление в цитратом цикле;
3. Цепь переноса электронов на кислород, сопряжённая с реакциями дегидрирования, происходящими в процессе распада глюкозы.
Анаэробным гликолизом называют процесс расщепления глюкозы с образованием в качестве конечного продукта лактата. Этот процесс протекает без использования кислорода и поэтому не зависит от работы митохондриальной дыхательной цепи.
АТФ образуется за счёт реакций субстратного фосфорилирования.
Суммарное уравнение процесса:
С6Н1206 + 2Н3Р04 + 2АДФ = 2С3Н6О3 + 2АТФ + 2Н2O.
Реакции анаэробного гликолиза
При анаэробном гликолизе (рис.14) в цитозоле протекают все 10 реакций, идентичных аэробному гликолизу. Лишь 11-я реакция, где происходит восстановление пирувата цитозольным NADH, является специфической для анаэробного гликолиза (рис.15).
Восстановление пирувата в лактат катализирует лактатдегидрогеназа (реакция обратимая, и фермент назван по обратной реакции). С помощью этой реакции обеспечивается регенерация NAD+ из NADH без участия митохондриальной дыхательной цепи в иситуациях, связанных с недостаточным снабжением клеток кислородом.
Роль акцептора водорода от NADH (подобно кислороду в дыхательной цепи) выполняет пируват. Таким образом, значение реакции восстановления пирувата заключается не в образовании лактата, а в том, что данная цитозольная реакция обеспечивает регенерацию NAD+.
К тому же лактат не является конечным продуктом метаболизма, удаляемым из организма. Это вещество выводится в кровь и утилизируется, превращаясь в печени в глюкозу, или при доступности кислорода превращается в пируват, который вступает в общий путь катаболизма, окисляясь до СО2 и Н2О.
Промежуточный обмен глюкозы в организме
Глюконеогенез. Роль печени в углеводном обмене.
Одним из этапов обмена углеводов в организме является межуточный обмен – окисление углеводов в тканях организма до образования конечных продуктов – СО2 и Н2О.
Процесс окисления Гл идет по двум основным путям:
1. Анаэробный гликолиз.
2. Аэробный гликолиз.
Распад Гл в анаэробных условиях и при непрямом превращении протекает почти одинаково до образования пировиноградной кислоты (ПК).
В анаэробных условиях ПК восстанавливается в молочную кислоту (МК), которая в печени участвует в образовании гликогена или ресинтезируется через цикл Кори в Гл.
В крови здоровых людей содержание МК составляет 0,6-1,7 ммоль/л.
В аэробных условиях при участии пируватдегидрогеназного комплекса и 5 коферментов (тиаминдифосфата, рибофлавина, пантотеновой и липоевой кислот, никотинамида) происходит окисление пировиноградной кислоты до ацетил-КoА, который затем подвергается дальнейшим превращениям в цикле Кребса, конечными продуктами которого является СО2 и Н2О и 38 молекул АТФ.
Основные пути метаболизма глюкозы




Гликолиз – это серия реакций, в результате которых глюкоза распадается на 2 молекулы пирувата (аэробный гликолиз) или две молекулы лактата (анаэробный гликолиз).
Все реакции гликолиза (10-11 реакций) протекают в цитозоле и характерны для всех органов и тканей.
Анаэробный гликолиз – это процесс окисления глюкозы, в результате которого происходит расщепление глюкозы с образованием 2 молекул лактата.
Главным путем распада глюкозы, ведущим к освобождению энергии, является дихотомический путь.
В реакциях этого пути получить из глюкозы энергию можно двумя путями:
1) Путем анаэробного распада глюкозы (анаэробный гликолиз) до молочной кислоты.
Многоступенчатые реакции можно выразить суммарным уравнением: глюкоза → 2лактат + 134 кДж.
Часть этой энергии расходуется на образование 2 молекул АТФ, остальная рассеивается в виде тепла.
2) Путем аэробного распада глюкозы (аэробный гликолиз) до конечных продуктов – СО2 и Н2О.
Многоступенчатые реакции можно выразить суммарным уравнением: Глюкоза + 6О2 → 6СО2 + 6Н2О + 2850 кДж.
При этом 60% образующейся энергии запасается в виде АТФ. Аэробный путь экономически выгоднее, при равных количествах используемой глюкозы, этот путь дает почти в 20 раз больше АТФ.
Аэробный распад глюкозы осуществляется почти всеми тканями нашего организма, исключение – эритроциты, их жизнедеятельность поддерживается путем гликолиза.
Анаэробный распад глюкозы (гликолиз): значение анаэробного распада глюкозы. Эффект Пастера
АНАЭРОБНЫЙ ГЛИКОЛИЗ – процесс расщепления глюкозы с образованием конечного продукта лактата. Он протекает без использования кислорода и поэтому не зависит от работы митохондриальной дыхательной цепи.
АТФ образуется за счет субстратного фосфорилирования (2 АТФ). Протекает в мышцах, в первые минуты мышечной работы, в эритроцитах (в которых отсутствуют митохондрии), а также в разных органах в условиях ограниченного снабжения их кислородом, в том числе в опухолевых клетках. Этот процесс служит показателем повышенной скорости деления клеток при недостаточной обеспеченности их системой кровеносных сосудов.
Сходство анаэробного и аэробного гликолиза заключается в том, что до стадии образования ПВК эти процессы протекают одинаково при участии тех же ферментов.




ПВК 2 НАДН2 2НАД лактат
Энергетический баланс анаэробного окисления глюкозы: образование 2 АТФ.
Основное физиологическое значение – использование энергии, которая освобождается в этом процессе для синтеза АТФ.
Метаболиты гликолиза используются для синтеза новых соединений (фр-6-фосфат и глицеральдегид-3-фосфат участвуют в образовании рибозо-5-фосфата – структурного компонента нуклеозидов; 3-фосфоглицерат включается в синтез аминокислот: серин, глицин, цистеин).
ЭФФЕКТ ПАСТЕРА. Заключается в угнетении дыханием (О2) анаэробного гликолиза, т.е. происходит переключение с аэробного гликолиза на анаэробное окисление.
Если ткани снабжены О2, то 2НАДН2, образовавшийся в процессе центральной реакции оксидоредукции, окислится в дыхательной цепи, поэтому ПВК не превращается в лактат, а в ацетил-КоА, который вовлекается в ЦТК.
Биосинтез глюкозы (глюконеогенезе) из аминокислот, глицерина и молочной кислоты. Значение глюконеогенеза для детского организма.
Взаимосвязь гликолиза в мышцах и глюконеогенеза в печени (цикл Кори). Гормональная регуляция.
Это процесс синтеза глюкозы из веществ неуглеводной природы. Процесс протекает в печени и менее интенсивно в корковом веществе почек, а также в слизистой кишечника. Эти ткани могут обеспечивать синтез 80-100 г глюкозы в сутки.
Первичные субстраты – лактат, аминокислоты, глицерол. Их включение в глюконеогенез зависит от физиологического состояния организма:
глицерол – высвобождается при гидролизе жиров в период голодания или при длительной физической нагрузке;
аминокислоты – образуются в результате распада мышечных белков и включаются в глюконеогенез при длительном голодании или продолжительной мышечной работе.
Если гликолиз протекает в цитозоле, а часть реакций глюконеогенеза происходит в митохондриях.
Процесс идет обратно анаэробному гликолизу за исключением 3-х необратимых реакций:
1. Пируваткиназная – образование фосфоенолпирувата из ПВК происходит в ходе 2-х реакций, первая из кот. протекает в митохондриях. ПВК транспортируется в матрикс митохондрий и там карбоксилируется с образованием оксалацетата (ЩУК). Фермент-пируваткарбоксилаза, коферментом которым является биотин. Реакция протекает с использование АТФ.
Затем оксалацетат (в цитозоле) превращается в фосфоенолпируват входе реакции, катализируемой фосфоенолпируваткарбоксилазой – ГТФ-зависимым ферментом ( -СО2, ГТФ → ГДФ).
2. Фосфофруктокиназная: ФР-1,6-дифосфат →Фр-6-фосфат под действием фермента фруктозо-1,6-бифосфатаза.
3. Гексокиназная: Гл-6-фосфат→ Глюкоза под действием фермента Гл-6-фосфатазы.
ЗНАЧЕНИЕ – поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок.
РЕГУЛЯЦИЯ: инсулин – тормозит синтез ферментов; глюкокортикоиды – индуцируют синтез ферментов; СТГ – повышает активность ферментов глюконеогенеза.
(взаимосвязь гликолиза в мышцах и глюконеогенеза в печени).
Регуляция постоянного уровня глюкозы в крови.
2. Обеспечивает утилизацию лактата.
3. Предотвращает накопление лактата (снижение рН — лактоацидоз).
4. Экономичное использование углеводов организмом.
5. Регуляция обмена углеводов осуществляется на уровне тканей – кровь, печень, мышцы.
Анаэробный гликолиз – это процесс окисления глюкозы до лактата, протекающий в отсутствии О2.
Анаэробный гликолиз отличается от аэробного только наличием последней 11 реакции, первые 10 реакций у них общие.
Этапы:
1) Подготовительный, в нем затрачивается 2 АТФ. Глюкоза фосфорилируется и расщепляется на 2 фосфотриозы;
2) 2 этап сопряжён с синтезом АТФ. На этом этапе фосфотриозы превращаются в ПВК.
Энергия этого этапа используется для синтеза 4 АТФ и восстановления 2НАДН2, которые в анаэробных условиях восстанавливают ПВК до лактата.
Энергетический баланс:2АТФ = -2АТФ + 4АТФ
Общая схема:
Происходит окисление 1 глюкозы до 2 молекул молочной кислоты с образованием 2 АТФ (сначала 2 АТФ затрачиваются, затем 4 образуются).
В анаэробных условиях гликолиз является единственным источником энергии. Суммарное уравнение: С6Н12О6 + 2Н3РО4 + 2АДФ → 2С3Н6О3 + 2АТФ + 2Н2О.
Реакции:
Общие реакции аэробного и анаэробного гликолиза
1) Гексокиназав мышцах фосфорилирует в основном глюкозу, меньше – фруктозу и галактозу.Ингибитор глюкозо-6-ф, АТФ. Активатор адреналин. Индуктор инсулин.
Глюкокиназа фосфорилирует глюкозу.
Активна в печени, почках. Не ингибируется глюкозо-6-ф. Индуктор инсулин.
2) Фосфогексозоизомераза осуществляет альдо-кетоизомеризацию открытых форм гексоз.
3) Фосфофруктокиназа 1 осуществляет фосфорилирование фруктозы-6ф.
Реакция необратима и самая медленная из всех реакций гликолиза, определяет скорость всего гликолиза. Активируется: АМФ, фруктозо-2,6-дф, фруктозо-6-ф, Фн. Ингибируется: глюкагоном, АТФ, НАДН2, цитратом, жирными кислотами, кетоновыми телами. Индуктор реакции инсулин.
4) Альдолаза А действует на открытые формы гексоз, образует несколько изоформ.
В большинстве тканей содержится Альдолаза А.
В печени и почках – Альдолаза В.
6) 3-ФГА дегидрогеназа катализирует образование макроэргической связи в 1,3-ФГК и восстановление НАДН2.
7) Фосфоглицераткиназа осуществляет субстратное фосфорилирование АДФ с образованием АТФ.
8) Фосфоглицератмутаза осуществляет перенос фосфатного остатка в ФГК из положения 3 положение 2.
9) Енолаза отщепляет от 2-ФГК молекулу воды и образует высокоэнергетическую связь у фосфора.
Ингибируется ионами F-.
10) Пируваткиназа осуществляет субстратное фосфорилирование АДФ с образованием АТФ.
Активируется фруктозо-1,6-дф, глюкозой. Ингибируется АТФ, НАДН2, глюкагоном, адреналином, аланином, жирными кислотами, Ацетил-КоА.
Индуктор: инсулин, фруктоза.
Образующаяся енольная форма ПВК затем неферментативно переходит в более термодинамически стабильную кетоформу.
Реакция анаэробного гликолиза
11) Лактатдегидрогеназа. Стоит из 4 субъединиц, имеет 5 изоформ.
Лактат не является конечным продуктом метаболизма, удаляемым из организма.
Из анаэробной ткани лактат переноситься кровью в печень, где превращаясь в глюкозу (Цикл Кори), или в аэробные ткани (миокард), где превращается в ПВК и окисляется до СО2 и Н2О.
Энергетический эффект цикла Кребса
Регуляция гликолиза Ключевые ферменты:
1).Гексокиназа аллостерически ингибируется гл-6-фосфатом. Синтез глюкокиназы индуцируется инсулином.
2).Фосфофруктокиназа. Ситез индуцируется инсулином. Аллостерические активаторы — АМФ, фруктозо-2,6-дифосфат, ингибиторы — АТФ, цитрат.
3).Пирувтакиназа. Ситез индуцируется инсулином. Активатор — Фр-1,6-фф, ингибиторы — АТФ, аланин, ацетилКоА.
Глюконеогенез
Суммарное уравнение:
2ПВК + 4АТФ + 2ГТФ + 2НАДН + 2Н+ + 6Н2О = глюкоза + 4АДФ + 2ГДФ + 6Ф + 2НАД+
На синтез молекулы глюкозы из двух молекул пирувата расходуется 4АТФ и 2ГТФ.
Процесс окисления ЖК поставляет энергию для глюконеогенеза. Для восстановительных этапов требуется две молекулы НАДН.
Пируваткарбоксилаза, катализирующая первую реакцию, имеет аллостерического активатора — ацетилКоА.
Регуляция глюконеогенеза
1).Репрессируется после приёма богатой углеводами пищи (под действием инсулина) и индуцируется при голодании, стрессе, диабете (под действием глюкокортикоидов).
2).Процесс окисления ЖК стимулирует глюконеогенез.
Стимуляция осуществляется через увеличение уровня ацетил-КоА.
3).Реципрокная взаимосвязь:
-ацетилКоА ингибирует пируватДГ и активирует пируваткарбоксилазу.
-АТФ активирует фруктозодифосфатазу, АМФ — ингибирует.
-фруктозо-2,6-дифосфат активирует фосфофруктокиназу-1 и ингибирует фруктозодифосфатазу-1.
Расчет энергетического эффекта гликолиза.
Гликолиз — это анаэробный процесс.
При расчете энергетического эффекта биохимического процесса в анаэробных условиях следует учитывать:
- 1) затраты АТФ (как правило, в фосфотрансферазных реакциях);
- 2) образование АТФ в процессах субстратного фосфорилирования.
В первом этапе гликолиза происходит затрата 2 моль АТФ: на фосфорилирование глюкозы и на фосфорилирование глюкозо-6-фосфата.
Еще раз заострим внимание на том, что из 1 моль глюкозы образуется 2 моль 3-фосфоглицеринового альдегида, который вступает во второй этап гликолиза.
Во втором этапе гликолиза можно найти две реакции субстратного фосфорилирования, в которых образуется 2 моль АТФ при распаде 1 моль 3-фосфоглицеринового альдегида. Следовательно, при распаде 2 моль 3-фосфоглицеринового альдегида образуется 4 моль АТФ.
Суммируя полученное и затраченное количество АТФ, получаем суммарный энергетический эффект гликолиза — 2 моль АТФ.
Расчет энергетического эффекта полного распада глюкозы в аэробных условиях.
При расчете энергетического эффекта биохимического процесса в аэробных условиях следует учитывать:
- 1) затраты АТФ;
- 2) образование АТФ в процессах субстратного фосфорилирования;
- 3) фосфорилирование АДФ, сопряженное с работой электронотранспортной цепи.
Процессы полного распада глюкозы до оксида углерода (IV) и воды разделим на этапы и проведем расчет энергетического эффекта каждого этапа.
Первый этап гликолиза — на этом этапе затрачиваются 2 моль АТФ.
2. Второй этап гликолиза — 4 моль АТФ получаются в реакциях субстратного фосфорилирования. Фермент 3-фосфоглицеральде-гидцегидрогеназа катализирует отщепление 2 атомов водорода от молекулы субстрата, поставляя их в электронотранспортную цепь; результатом сопряжения окисления с фосфорилированием АДФ является образование 3 моль АТФ на каждый моль 3-фосфоглицеринового альдегида.
Поскольку из 1 моль глюкозы образуется 2 моль 3-фосфоглицеринового альдегида, в данном процессе образуется 6 моль АТФ.
3. Окислительное декарбоксилирование ПВК дает 6 моль АТФ, так как в электронотранспортную цепь водороды поставляют 2 моль НАД.
4. В цикле Кребса нет затрат АТФ и отсутствуют реакции субстратного фосфорилирования. Однако имеются четыре дегидрогеназные реакции, и в одной реакции образуется ГГФ, которая по выходу энергии эквивалентна АТФ.
Выход АТФ на отдельных стадиях цикла Кребса суммирован в таблице 9.
Таблица 9 Энергетический эффект цикла Кребса
| Фермент | Кофермент | Выход АТФ, моль |
| Изоцитратдегидрогеназа | НАД | |
| α-Кетоглутаратдегидрогеназный комплекс | НАД | |
| Сукцинаттиокиназа | ГДФ | |
| Сукцинатдегидрогеназа | ФАД | |
| Малатдегидрогеназа | НАД | |
| Всего |
Итак, при распаде 1 моль ацетил-КоА образуется 12 моль АТФ, следовательно, из 2 моль ацетил-КоА — 24 моль АТФ.
Суммируя энергетические эффекты всех этапов распада глюкозы в аэробных условиях, получаем 38 моль АТФ.
Основные метаболические пути превращения углеводов и жиров в печени показаны на рис.
Метаболизм глюкозо-6-фосфата может идти по 5 направлениям.
1. Образование свободной глюкозы, которая поступает в кровоток и доставляется в другие ткани.
3. Расщепление до ацетил-СоА, из которого могут синтезироваться холестерол, жирные кислоты и далее триацилглицеролы и фосфолипиды.
4. Ацетил-СоА может быть окислен в цикле лимонной кислоты до СО2 и Н2О с накоплением энергии в виде АТФ.
Пентозофосфатный путь, в ходе которого образуются NADPH и рибозо-5-фосфат.
Рис. 8. Пути превращения углеводов и жиров в печени
Для жирных кислот возможны тоже 5 путей превращения.
Окисление до ацетил-СоА и далее в цикле лимонной кислоты до СО2 + Н2О с образованием энергии АТФ.
2. Образование кетоновых тел через ацетил-СоА. Кетоновые тела переносятся кровью в периферические ткани, где окисляются в цикле лимонной кислоты.
Биосинтез холестерола через ацетил-СоА.
4. Биосинтез липопротеидов плазмы крови.
5. Часть жирных кислот выходит из печени, альбумином крови доставляется в периферические ткани, где используются в качестве топлива.
Таким образом, метаболизм углеводов и жиров в печени обладает исключительной гибкостью.
Метаболические пути углеводов и жиров пересекаются на уровне ацетил-СоА.
Биосинтез белка — сложный многостадийный процесс синтеза полипептидной цепи из аминокислот, происходящий на рибосомахс участием молекул мРНК и тРНК. Процесс биосинтеза белка требует значительных затрат энергии.
Биосинтез белка происходит в два этапа. В первый этап входит транскрипция и процессинг РНК, второй этап включает трансляцию. Во время транскрипции фермент РНК-полимераза синтезирует молекулу РНК, комплементарную последовательности соответствующего гена (участка ДНК).
Терминатор в последовательности нуклеотидов ДНК определяет, в какой момент транскрипция прекратится. В ходе ряда последовательных стадий процессинга из мРНК удаляются некоторые фрагменты, и редко происходит редактирование нуклеотидных последовательностей.
После синтеза РНК на матрице ДНК происходит транспортировка молекул РНК в цитоплазму. В процессе трансляции информация, записанная в последовательности нуклеотидов переводится в последовательность остатков аминокислот.
Процессинг РНК (посттранскрипционные модификации РНК) — совокупность процессов в клетках эукариот, которые приводят к превращению первичного транскрипта РНК в зрелую РНК.
Между транскрипцией и трансляцией молекула мРНК претерпевает ряд последовательных изменений, которые обеспечивают созревание функционирующей матрицы для синтеза полипептидной цепочки. К 5΄-концу присоединяется кэп, а к 3΄-концу поли-А хвост, который увеличивает длительность жизни иРНК.
У прокариот мРНК может считываться рибосомами в аминокислотную последовательность белков сразу после транскрипции, а у эукариот она транспортируется из ядра в цитоплазму, где находятся рибосомы.
Скорость синтеза белков выше у прокариот и может достигать 20 аминокислот в секунду[1].
Процесс синтеза белка на основе молекулы мРНК называется трансляцией.
Во время начальной стадии биосинтеза белков, инициации, обычно метиониновый кодон узнаётся малой субъединицей рибосомы, к которой при помощи белковых факторов инициации присоединена метиониновая транспортная РНК (тРНК).
После узнавания стартового кодона к малой субъединице присоединяется большая субъединица и начинается вторая стадия трансляции — элонгация. При каждом движении рибосомы от 5′ к 3′ концу мРНК считывается один кодон путём образования водородных связей между тремя нуклеотидами (кодоном) мРНК и комплементарным ему антикодоном транспортной РНК, к которой присоединена соответствующая аминокислота. Синтезпептидной связи катализируется рибосомальной РНК (рРНК), образующей пептидилтрансферазный центр рибосомы.
Рибосомальная РНК катализирует образование пептидной связи между последней аминокислотой растущего пептида и аминокислотой, присоединённой к тРНК, позиционируя атомы азота и углерода в положении, благоприятном для прохождения реакции.
Ферментыаминоацил-тРНК-синтетазы присоединяют аминокислоты к их тРНК. Третья и последняя стадия трансляции, терминация, происходит при достижении рибосомой стоп-кодона, после чего белковыефакторы терминации гидролизуют последнюю тРНК от белка, прекращая его синтез.
Таким образом, в рибосомах белки всегда синтезируются от N- к C-концу.
Как любой синтетический процесс, синтез белка — это эндотермическая реакция и, значит, требует энергозатрат.
Биосинтез белка представляет цепь синтетических реакций: 1) синтез и-РНК; 2) соединение аминокислот с т-РНК; 3) «сборку белка». Все эти реакции требуют больших энергетических затрат — до 24, 2 ккал/моль. Энергия для синтеза белка доставляется реакцией расщепления АТФ.
Значение: процесс синтеза полипептидной цепи из аминокислотных остатков, происходящий на рибосомах клеток живых организмов с участием молекул РНК и РНК.
Образование белков специфичных данной клетке для дальнейшего его использования.
Функция ДНК — хранение генетической информации в ядре клетки.
1. информационная РНК (и-РНК) — считывание генетической информации;
2. матричная РНК (м-РНК) — участие в биосинтезе белка (трансляции);
3. транспортная РНК (т-РНК) — доставка аминокислот в полисому для биосинтеза белка (трансляции) и адапторная роль («перевод с языка» нуклеотидов на «язык» аминокислот»);
рибосомная РНК — входит в состав рибосом, участвует в биосинтезе белков.
Первичная структура ДНК и РНК представляет собой последовательность нуклеотидных звеньев, соединенных между собой с помощью фосфодиэфирных мостиков, связывающих С—3′ предыдущего нуклетидного звена и С-5′ последующего нуклеотидного звена. Полимерная цепь, таким образом, состоит из чередующихся пентозных и фосфатных остатков, а гетероциклические основания являются «боковыми группами», присоединенными к пентозным остаткам.
Нуклеоти́ды — фосфорные эфиры нуклеозидов, нуклеозидфосфаты.
Свободные нуклеотиды, в частности АТФ, цАМФ, АДФ, играют важную роль в энергетических и информационных внутриклеточных процессах, а также являются составляющими частями нуклеиновых кислот и многих коферментов.
Нуклеотиды принадлежат к наиболее сложным метаболитам. Их биосинтез требует много времени и высоких затрат энергии (см. с. 190). Поэтому понятно, что нуклеотиды не полностью разрушаются, а по большей части снова участвуют в синтезе. Прежде всего это относится к пуриновым основаниям аденину и гуанину, В организме высших животных около 90% пуриновых оснований снова превращаются в нуклеозидмонофосфаты, связываясь с фосфорибозилдифосфатом (PRPP) (ферменты [1] и [2]).
Участие пиримидиновых оснований в ресинтезе весьма незначительно.
Анаэробный гликолиз — это восстановление пировиноградной кислоты до молочной кислоты (лактата) в анаэробном процессе, поэтому в микробиологии его называют молочнокислым брожением. Лактат является метаболическим тупиком и далее ни во что не превращается, единственная возможность утилизовать лактат — это окислить его обратно в пируват.
Многие клетки организма способны к анаэробному окислению глюкозы. Для эритроцитов он является единственным источником энергии. Клетки скелетной мускулатуры за счет бескислородного расщепления глюкозы способны выполнять мощную, быструю, интенсивную работу, как, например, бег на короткие дистанции, напряжение в силовых видах спорта.
Вне физических нагрузок бескислородное окисление глюкозы в клетках усиливается при гипоксии — при различного рода анемиях, при нарушении кровообращения в тканях независимо от причины.
Бескислородное окисление глюкозы включает два этапа
Анаэробное превращение глюкозы локализуется в цитозоле и включает два этапа из 11 ферментативных реакций.
Первый этап гликолиза
Первый этап гликолиза — подготовительный, здесь происходит затрата энергии АТФ, активация глюкозы и образование из нее триозофосфатов.
Первая реакция гликолиза сводится к превращению глюкозы в реакционно-способное соединение за счет фосфорилирования 6-го, не включенного в кольцо, атома углерода. Эта реакция является первой в любом превращении глюкозы, катализируется гексокиназой.
Вторая реакция необходима для выведения еще одного атома углерода из кольца для его последующего фосфорилирования (фермент изомераза). В результате образуется фруктозо-6-фосфат.
Третья реакция — фермент фосфофруктокиназа фосфорилирует фруктозо-6-фосфат с образованием почти симметричной молекулы фруктозо-1,6-дифосфата. Эта реакция является главной в регуляции скорости гликолиза.
В четвертой реакции фруктозо-1,6-дифосфат разрезается пополам фруктозо-1,6-дифосфат-альдолазой с образованием двух фосфорилированных триоз-изомеров — альдозы глицеральдегида (ГАФ) и кетозы диоксиацетона (ДАФ).
Пятая реакция подготовительного этапа — переход глицеральдегидфосфата и диоксиацетонфосфата друг в друга при участии триозофосфатизомеразы. Равновесие реакции сдвинуто в пользу диоксиацетонфосфата, его доля составляет 97 %, доля глицеральдегидфосфата — 3 %.
Эта реакция, при всей ее простоте, определяет дальнейшую судьбу глюкозы:
- при нехватке энергии в клетке и активации окисления глюкозы диоксиацетонфосфат превращается в глицеральдегидфосфат, который далее окисляется на втором этапе гликолиза:
- при достаточном количестве АТФ, наоборот, глицеральдегидфосфат изомеризуется в диоксиацетонфосфат, и последний отправляется на синтез жиров.
Второй этап гликолиза
Второй этап гликолиза — это освобождение энергии, содержащейся в глицеральдегидфосфате, и запасание ее в форме АТФ.
Шестая реакция гликолиза (фермент глицеральдегидфосфат-дегидрогеназа) — окисление глицеральдегидфосфата и присоединение к нему фосфорной кислоты приводит к образованию макроэргического соединения 1,3-дифосфоглицериновой кислоты и НАДН.
В седьмой реакции (фермент фосфоглицераткиназа) энергия фосфоэфирной связи, заключенная в 1,3-дифосфоглицерате тратится на образование АТФ. Реакция получила дополнительное название — реакция субстратного фосфорилирования, что уточняет источник энергии для получения макроэргической связи в АТФ (от субстрата реакции) в отличие от окислительного фосфорилирования (от электрохимического градиента ионов водорода на мембране митохондрий).
Восьмая реакция — синтезированный в предыдущей реакции 3-фосфоглицерат под влиянием фосфоглицератмутазы изомеризуется в 2-фосфоглицерат.
Девятая реакция — фермент енолаза отрывает молекулу воды от 2-фосфоглицериновой кислоты и приводит к образованию макроэргической фосфоэфирной связи в составе фосфоенолпирувата.
Десятая реакция гликолиза — еще одна реакция субстратного фосфорилирования — заключается в переносе пируваткиназой макроэргического фосфата с фосфоенолпирувата на АДФ и образовании пировиноградной кислоты.
Последняя реакция бескислородного окисления глюкозы, одиннадцатая — образование молочной кислоты из пирувата под действием лактатдегидрогеназы. Важно то, что эта реакция осуществляется только в анаэробных условиях. Эта реакция необходима клетке, так как НАДН, образующийся в 6-й реакции, в отсутствие кислорода не может окисляться в митохондриях.
У плода и детей первых месяцев жизни преобладает анаэробный распад глюкозы, в связи с чем концентрация молочной кислоты в крови у них выше чем у взрослых.
Глюкоза крайне важна для энергетики клеток
Глюкоза – это субстрат для получения энергии
Энергетика любой клетки нашего организма основана на окислении глюкозы. Окисление глюкозы происходит по двум направлениям:
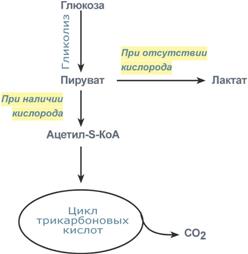 Пути метаболизма пирувата в присут- |
- Окисление с образованием пентоз: рибозы, рибулозы, ксилулозы. Этот путь называется пентозофосфатный шунт и не связан с получением энергии
- Окисление с получением энергии.
Второй путь, т.е. тот по которому глюкоза окисляется для получения энергии, называется гликолиз (греч. glykos — сладкий и греч. lysis — растворение). Конечным продуктом гликолиза является пировиноградная кислота (пируват).
В зависимости от дальнейшей судьбы пирувата различают аэробное и анаэробное окисление глюкозы. Целью обоих типов окисления является получение АТФ .
В аэробном процессе пировиноградная кислота превращается в ацетил-SКоА (реакции ПВК-дегидрогеназы) и далее сгорает в реакциях цикла трикарбоновых кислот до СО2 (реакции ЦТК).
Общее уравнение аэробного окисления глюкозы:
В анаэробном процессе пировиноградная кислота восстанавливается до молочной кислоты (лактата). Лактат является метаболическим тупиком и далее ни во что не превращается, единственная возможность утилизовать лактат – это окислить его обратно в пируват. В микробиологии анаэробный гликолиз называют молочнокислым брожением.
Суммарное уравнение анаэробного гликолиза имеет вид:
Глюкоза – это источник оксалоацетата
После того как пируват синтезировался, он необязательно превращается в ацетил-SКоА или молочную кислоту. Существенное значение имеет его способность карбоксилироваться в оксалоацетат , особенно эта реакция активна в печени. Наличие избытка оксалоацетата «подталкивает» реакции цикла трикарбоновых кислот (доступность субстрата), ускоряет связывание ацетильной группы, ее окисление и производство энергии.
При голодании отсутствие глюкозы в клетках и активация глюконеогенеза в гепатоцитах, ухудшение окисления глюкозы до пирувата при сахарном диабете влечет за собой недостаточное количество оксалоацетата. Это сопровождается гипоэнергетическим состоянием клетки и активацией синтеза кетоновых тел в печени.
























