Химия | 5 — 9 классы
Составьте уравнения возможных реакций между металлами и растворами кислот : 1) Ca + HB = 2) AU + HBr = 3) Na + H3PO4 = 4) Ag + HCl = 5) Zn + Hi = 6) Na + Hi = 7) Al + Hi = 8) Hg + HCl = 9) Cu + HBr =.
Са + 2НВr — — > ; CaBr₂ + H₂
Au + HBr — — > ; реакция не идет, т.
К. золото стоит после Н₂
6Na + 2H₃PO₄ — — > ; 2Na₃PO₄ + 3H₂
Ag + HCl — — > ; реакция не идет, т.
К. серебро стоит после Н₂
Zn + 2Hi — — > ; Zni₂ + H₂
2Na + 2Hi — — > ; 2Nai + H₂
2Al + 6Hi — — > ; 2Ali₃ + 3H₂
Hg + HCl — — > ; реакция не идет, т.
К. ртуть стоит после Н₂
Сu + HBr — — > ; реакция не идет, т.
К. медь стоит после Н₂.
- Как изменяется сила кислот в ряду HF — HCL — HBr — HI?
- Помогите закончить уравнения возможных реакций и расставить коэффиценты Na + H2CO3 ; Ca + H2S ; Na + H2SO3 ; Zn + HBr ; Al + H2SO4 ; Ba + H3PO4 ; Ag + HCL ; Al + HBr?
- Приведите примеры по два металла, которые не вытесняют водород из раствора HCl?
- HCl + MgBr = MgCl + HBr — коэффиценты?
- Сила галогеноводородных кислот возрастает в ряду 1) HCl , HBr , HI 2) HI, HBr, HF 3) HBr , HI , HCl 4) HI, HCl, HBr?
- Решите уравнение Fe + HCl = CuO + HCl = ZnO + HCl = Ca(OH)2 + HCL = Na2CO3 + HCL = NH3 + HCl = KCl + Pb(No3) = HgSo4 + HBr = HI + KOH = HI + SnSO4 = Al2O3 + HF = K2CO3 + HBr =?
- Напишите пожалуйста качественные реакции на анионы кислот : HCl, HBr, HI, H2SO4, HNO3, H3PO4, H2S?
- Как из HBr получить HCl?
- Срочно дам 60 баллов?
- ЧТО ИЗ ПЕРЕЧИСЛЕННОГО НИЖЕ ЯВЛЯЕТСЯ ОДНООСНОВНОЙ КИСЛОТОЙ : HClO₄, H₂SO₄, H₃PO4, HPO₃, H₂SO₃, HNO₃, HCl, HNO₂, HClO₃, H₂SiO₃, HCL, HBr?
- Составить уравнения возможных реакций между металлами и растворами кислот
- Химические свойства металлов
- Ряд активности металлов
- Общие химические свойства металлов
- Взаимодействие с неметаллами
- Взаимодействие с водой
- Взаимодействие с кислотами
- Взаимодействие с солями
- Взаимодействие с аммиаком
- Взаимодействие с органическими веществами
- Взаимодействие металлов с оксидами
- Вопросы для самоконтроля
- Подведем итоги
Как изменяется сила кислот в ряду HF — HCL — HBr — HI?
Как изменяется сила кислот в ряду HF — HCL — HBr — HI.
Помогите закончить уравнения возможных реакций и расставить коэффиценты Na + H2CO3 ; Ca + H2S ; Na + H2SO3 ; Zn + HBr ; Al + H2SO4 ; Ba + H3PO4 ; Ag + HCL ; Al + HBr?
Помогите закончить уравнения возможных реакций и расставить коэффиценты Na + H2CO3 ; Ca + H2S ; Na + H2SO3 ; Zn + HBr ; Al + H2SO4 ; Ba + H3PO4 ; Ag + HCL ; Al + HBr.
Приведите примеры по два металла, которые не вытесняют водород из раствора HCl?
Приведите примеры по два металла, которые не вытесняют водород из раствора HCl.
Составьте уравнения реакций.
HCl + MgBr = MgCl + HBr — коэффиценты?
HCl + MgBr = MgCl + HBr — коэффиценты.
Сила галогеноводородных кислот возрастает в ряду 1) HCl , HBr , HI 2) HI, HBr, HF 3) HBr , HI , HCl 4) HI, HCl, HBr?
Сила галогеноводородных кислот возрастает в ряду 1) HCl , HBr , HI 2) HI, HBr, HF 3) HBr , HI , HCl 4) HI, HCl, HBr.
Решите уравнение Fe + HCl = CuO + HCl = ZnO + HCl = Ca(OH)2 + HCL = Na2CO3 + HCL = NH3 + HCl = KCl + Pb(No3) = HgSo4 + HBr = HI + KOH = HI + SnSO4 = Al2O3 + HF = K2CO3 + HBr =?
Решите уравнение Fe + HCl = CuO + HCl = ZnO + HCl = Ca(OH)2 + HCL = Na2CO3 + HCL = NH3 + HCl = KCl + Pb(No3) = HgSo4 + HBr = HI + KOH = HI + SnSO4 = Al2O3 + HF = K2CO3 + HBr =.
Напишите пожалуйста качественные реакции на анионы кислот : HCl, HBr, HI, H2SO4, HNO3, H3PO4, H2S?
Напишите пожалуйста качественные реакции на анионы кислот : HCl, HBr, HI, H2SO4, HNO3, H3PO4, H2S.
Как из HBr получить HCl?
Как из HBr получить HCl?
Срочно дам 60 баллов?
Срочно дам 60 баллов!
Составьте уравнения возможных реакций между металлами и растворами кислот : А) Zn + HCl →… Б) Hg + HBr→ … В) Na + Н2SO4→ … Г) Mg + H2SO4→ … Составьте уравнения реакций между кислотами и оксидами металлов : А) CaО + Н2SO4→ … Б) Fe2O3 + HNO3→ … В) BaО + НCl→ … Вычислите объем водорода (н.
У. ), который выделится при взаимодействии 6, 5 г цинка с соляной кислотой.
ЧТО ИЗ ПЕРЕЧИСЛЕННОГО НИЖЕ ЯВЛЯЕТСЯ ОДНООСНОВНОЙ КИСЛОТОЙ : HClO₄, H₂SO₄, H₃PO4, HPO₃, H₂SO₃, HNO₃, HCl, HNO₂, HClO₃, H₂SiO₃, HCL, HBr?
ЧТО ИЗ ПЕРЕЧИСЛЕННОГО НИЖЕ ЯВЛЯЕТСЯ ОДНООСНОВНОЙ КИСЛОТОЙ : HClO₄, H₂SO₄, H₃PO4, HPO₃, H₂SO₃, HNO₃, HCl, HNO₂, HClO₃, H₂SiO₃, HCL, HBr?
Если вам необходимо получить ответ на вопрос Составьте уравнения возможных реакций между металлами и растворами кислот : 1) Ca + HB = 2) AU + HBr = 3) Na + H3PO4 = 4) Ag + HCl = 5) Zn + Hi = 6) Na + Hi = 7) Al + Hi = 8) Hg + HCl = 9) Cu + HBr =?, относящийся к уровню подготовки учащихся 5 — 9 классов, вы открыли нужную страницу. В категории Химия вы также найдете ответы на похожие вопросы по интересующей теме, с помощью автоматического «умного» поиска. Если после ознакомления со всеми вариантами ответа у вас остались сомнения, или полученная информация не полностью освещает тематику, создайте свой вопрос с помощью кнопки, которая находится вверху страницы, или обсудите вопрос с посетителями этой страницы.
Mr(Al(NO3)2) = 27 + (14 + 16 * 2) * 3 = 27 + 138 = 165 Mr(Cu(OH)2) = 64 + (16 + 1) * 2 = 64 + 34 = 98 Mr(Fe) = 56.
1) 27 + 14×3 + 16×3×3 = 213 3)56.
А) Cx Hy 12x : y = 3 : 1 12x = 3y x : y = 3 : 12 x : y = 1 : 4 x = 1 ; y = 4 Ответ : СН4 б) по такому же принципу.
Предметное стекло, капля чистой воды, черная тушь, покровное стекло, микроскоп.
Привет! Полиэтилен при н. У. находится в состоянии твердого вещества. Пока = ).
1, 5 Зад. 1. 4 Зад. 2. 3 Зад. 3. 4 Зад. 4 2 Зад. 5 3.
А) 2SO2 + O2 → 2SO3 б) 2H2O → 2H2↑ + O2↑ в) 2Ca + O2 → 2CaO г) 2NH3 → N2↑ + 3H2↑.
Железо является металлом средней активности. 1. Железо реагирует с кислородом и другими неметаллами : 3Fe + 2O₂⇒ Fe₃O₄ 2Fe + 3Cl₂ ⇒ 2FeCl₃ 2. Железо реагирует с влажным воздухом(H₂O + O₂), а при высокой температуре и с водяными парами 4Fe + 6H₂O + ..
X — 5 Y — 4 Z — 6 T — 2 Все. Надеюсь помогла.
Применяется второй закон Ньютона : F = ma F = 75 Н m = 500 кг a = F / m a = 75 / 500 = 0, 15 м / с².
Составить уравнения возможных реакций между металлами и растворами кислот
Вопрос по химии:
4. Составьте уравнения возможных реакций между металлами и растворами кислот 1) Ca + HCl→________________________________________________ 2) Au + HBr→________________________________________________ 3) Na + H3PO4→______________________________________________ 4) Ag + HCl→________________________________________________ 5) Zn + HI→__________________________________________________ 6) Na + HI→_________________________________________________ 7) Al + HI→__________________________________________________ 8) Hg + HCl→________________________________________________ 9) Cu + HBr→________________________________________________
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок — бесплатно!
Химические свойства металлов
О чем эта статья:
8 класс, 9 класс, ЕГЭ/ОГЭ
Металлы — это химические элементы, атомы которых способны отдавать электроны с внешнего энергетического уровня, превращаясь в положительные ионы (катионы) и проявляя восстановительные свойства.
В окислительно-восстановительных реакциях металлы способны только отдавать электроны, являясь сильными восстановителями. В роли окислителей выступают простые вещества — неметаллы (кислород, фосфор) и сложные вещества (кислоты, соли и т. д.).
Металлы в природе встречаются в виде простых веществ и соединений. Активность металла в химических реакциях определяют, используя электрохимический ряд, который предложил русский ученый Н. Н. Бекетов. По химической активности выделяют три группы металлов.
Ряд активности металлов
Металлы средней активности
Общие химические свойства металлов
Взаимодействие с неметаллами
Щелочные металлы сравнительно легко реагируют с кислородом, но каждый металл проявляет свою индивидуальность:
оксид образует только литий
натрий образует пероксид
калий, рубидий и цезий — надпероксид
Остальные металлы с кислородом образуют оксиды:
2Zn + O2 = 2ZnO (при нагревании)
Металлы, которые в ряду активности расположены левее водорода, при контакте с кислородом воздуха образуют ржавчину. Например, так делает железо:
С галогенами металлы образуют галогениды:
Медный порошок реагирует с хлором и бромом (в эфире):
При взаимодействии с водородом образуются гидриды:
Взаимодействие с серой приводит к образованию сульфидов (реакции протекают при нагревании):
Реакции с фосфором протекают до образования фосфидов (при нагревании):
Основной продукт взаимодействия металла с углеродом — карбид (реакции протекают при нагревании).
Из щелочноземельных металлов с углеродом карбиды образуют литий и натрий:
Калий, рубидий и цезий карбиды не образуют, могут образовывать соединения включения с графитом:
С азотом из металлов IA группы легко реагирует только литий. Реакция протекает при комнатной температуре с образованием нитрида лития:
Взаимодействие с водой
Все металлы I A и IIA группы реагируют с водой, в результате образуются растворимые основания и выделяется H2. Литий реагирует спокойно, держась на поверхности воды, натрий часто воспламеняется, а калий, рубидий и цезий реагируют со взрывом:
Металлы средней активности реагируют с водой только при условии, что металл нагрет до высоких температур. Результат данной реакции — образование оксида.
Неактивные металлы с водой не взаимодействуют.
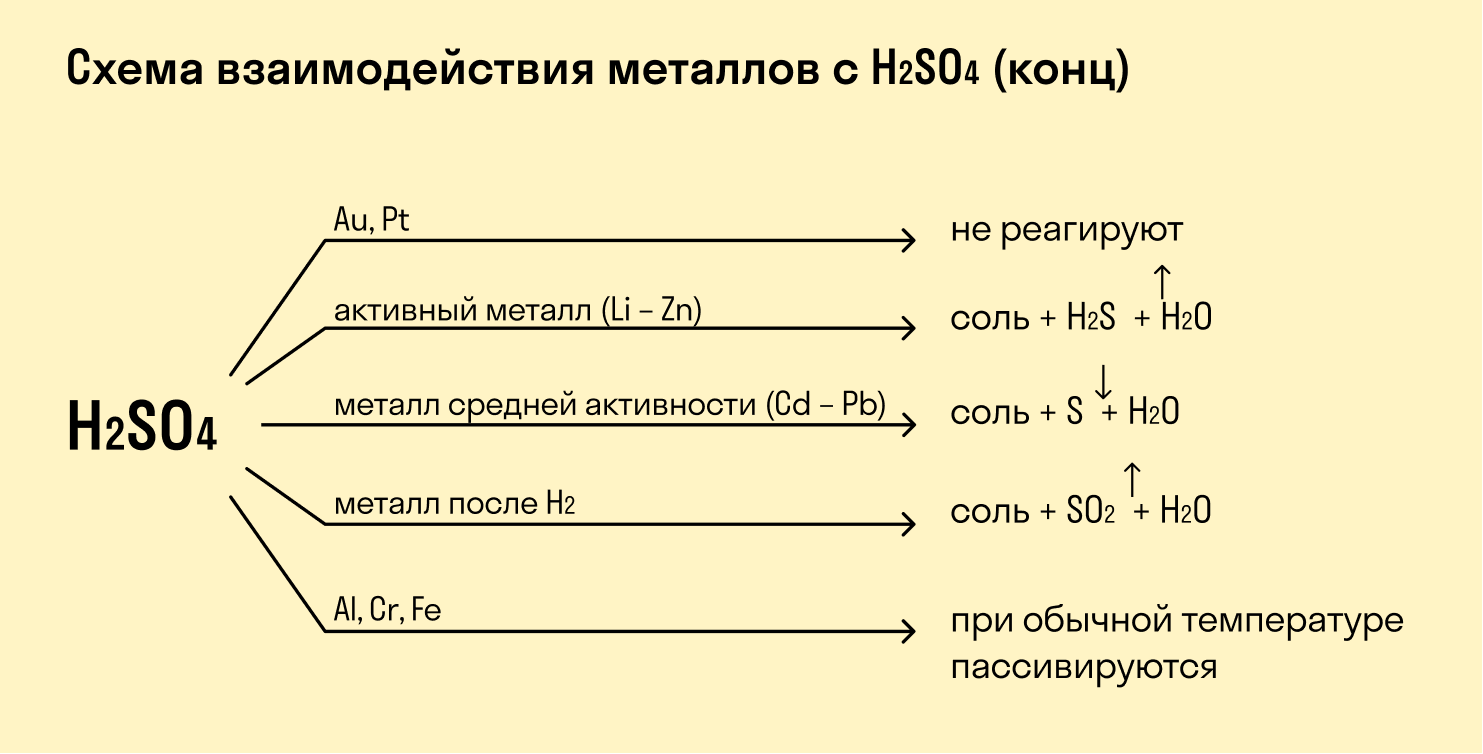
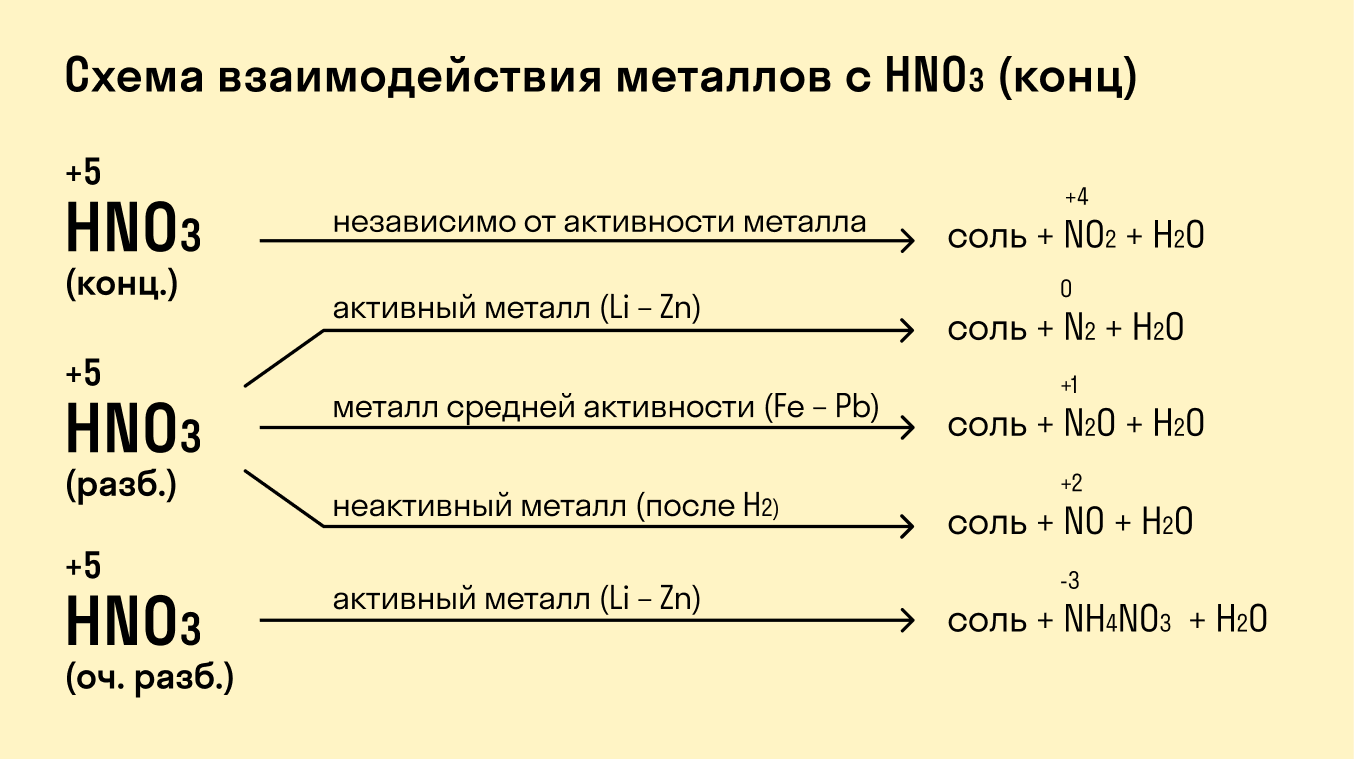
Взаимодействие с кислотами
Если металл расположен в ряду активности левее водорода, то происходит вытеснение водорода из разбавленных кислот. Данное правило работает в том случае, если в реакции с кислотой образуется растворимая соль.
2Na + 2HCl = 2NaCl + H2
При взаимодействии с кислотами-окислителями, например, азотной, образуется продукт восстановления кислоты, хотя протекание реакции также неоднозначно.
Металлы IА группы:
Металлы IIА группы
Такие металлы, как железо, хром, никель, кобальт на холоде не взаимодействуют с серной кислотой, но при нагревании реакция возможна.
Взаимодействие с солями
Металлы способны вытеснять из растворов солей другие металлы, стоящие в ряду напряжений правее, и могут быть вытеснены металлами, расположенными левее:
Zn + CuSO4 = ZnSO4 + Cu
На металлы IА и IIА группы это правило не распространяется, так как они реагируют с водой.
Реакция между металлом и солью менее активного металла возможна в том случае, если соли — как вступающие в реакцию, так и образующиеся в результате — растворимы в воде.
Взаимодействие с аммиаком
Щелочные металлы реагируют с аммиаком с образованием амида натрия:
Взаимодействие с органическими веществами
Металлы IА группы реагируют со спиртами и фенолами, которые проявляют в данном случае кислотные свойства:
Также они могут вступать в реакции с галогеналканами, галогенпроизводными аренов и другими органическими веществами.
Взаимодействие металлов с оксидами
Для металлов при высокой температуре характерно восстановление неметаллов или менее активных металлов из их оксидов.
3Са + Cr2O3 = 3СаО + 2Cr (кальциетермия)
Вопросы для самоконтроля
С чем реагируют неактивные металлы?
С чем связаны восстановительные свойства металлов?
Верно ли утверждение, что щелочные и щелочноземельные металлы легко реагируют с водой, образуя щелочи?
Методом электронного баланса расставьте коэффициенты в уравнении реакции по схеме:
Mg + HNO3 → Mg(NO3)2 + NH4NO3 + Н2O
Как металлы реагируют с кислотами?
Подведем итоги
От активности металлов зависит их химические свойства. Простые вещества — металлы в окислительно-восстановительных реакциях являются восстановителями. По положению металла в электрохимическом ряду можно судить о том, насколько активно он способен вступать в химические реакции (т. е. насколько сильно у металла проявляются восстановительные свойства).
Напоследок поделимся таблицей, которая поможет запомнить, с чем реагируют металлы, и подготовиться к контрольной работе по химии.