- We are checking your browser. gomolog.ru
- Why do I have to complete a CAPTCHA?
- What can I do to prevent this in the future?
- Практическая работа «Получение аммиака и изучение его свойств»
- Просмотр содержимого документа «Практическая работа «Получение аммиака и изучение его свойств»»
- Реакция взаимодействия гидроксида кальция и хлорида аммония
- Ca(OH)2 + 2NH4Cl CaCl2 + 2NH3 + 2H2O
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 702de37b6ba697ac • Your IP : 87.119.247.227 • Performance & security by Cloudflare
Практическая работа «Получение аммиака и изучение его свойств»
Материал может быть использован в 9 классе при изучении темы «Азот и фосфор». Разработка включает: экспериментальные задания, форму отчета и задания для самоконтроля.
Просмотр содержимого документа
«Практическая работа «Получение аммиака и изучение его свойств»»
Практическая работа № 4 9 класс
«Получение аммиака и изучение его свойств»
Цель: Получить аммиак и ознакомиться со свойствами водного раствора аммиака.
Оборудование: лабораторный штатив, сухие пробирки, пробка с газоотводной трубкой, ступка, ложки для сыпучих веществ, спиртовка, спички, стакан с водой.
Реактивы: кристаллический гидроксид кальция, кристаллический хлорид аммония, раствор соляной кислоты, раствор фенолфталеина или универсальн. индикатор.
II. Выполнение работы, оформление отчета
Уравнения реакций в молекулярном, полном и сокращенном ионном виде
1.Получение аммиака и исследование его физических свойств.
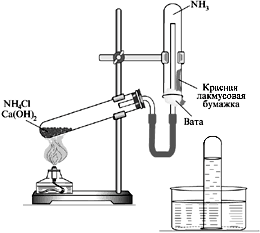
Получаем аммиак нагреванием смеси гидроксида кальция и хлорида аммония в пробирке
Собираем аммиак в пробирку дном .
Разрыхление реакционной массы.
Образование тумана.
Индикаторная бумага окрасилась в .
О выделении какого газа свидетельствуют наблюдения ?
Написать уравнение реакции:
Физические свойства аммиака. . Аммиак . воздуха, поэтому сухая пробирка – приемник находится дном. .
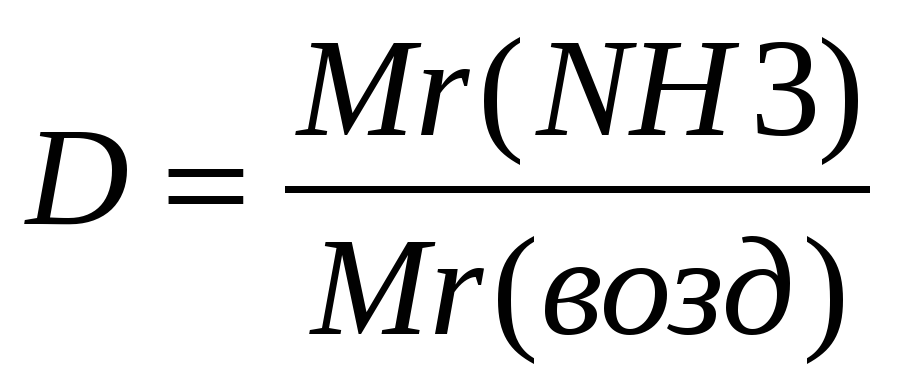
2. Исследование химических свойств аммиака
1. Растворение аммиака в воде.
.Изучение кислотно-основных свойств водного раствора аммиака.
3. Взаимодействие с кислотами:
Сняв с газоотводной трубки прибора пробирку, помещаем её в химический стакан с водой.
Убираем из стакана пробирку и в образовавшийся раствор добавляем индикатор … (указать название)
В стакан с водным раствором аммиака в присутствии индикатора вливают 1мл раствора соляной кислоты
Пробирка наполняется водой.
Над раствором образуется … .
Написать уравнение реакции, назвать образующееся вещество:
Аммиак . растворим в воде. Продукт взаимодействия аммиака с водой называется . . Относится к классу . . Механизм образования химической связи в катионе . . Тип реакции . .
Почему изменилась первоначальная окраска раствора?
Название продукта взаимодействия гидроксида аммония с соляной кислотой . . К какому классу относится продукт реакции? .
4. Окислительно-восстановительные свойства аммиака
На основе электронного баланса написать уравнение реакции, определить окислитель и восстановитель:
а) Горение аммиак без катализатора
б) Горение аммиак в присутствии катализатора
Какие вещества образуются в процессе горения аммиака а) без катализатора; б) в присутствии катализатора?
1) Какая масса хлорида аммония получится при взаимодействии 3 моль аммиака с соляной кислотой?
2) Какой объем кислорода потребуется для сжигания 34 г аммиака?
3) Закончите уравнения химических реакций, дайте названия продуктам реакций:
Реакция взаимодействия гидроксида кальция и хлорида аммония
Ca(OH)2 + 2NH4Cl  CaCl2 + 2NH3 + 2H2O
CaCl2 + 2NH3 + 2H2O
Реакция взаимодействия гидроксида кальция и хлорида аммония с образованием хлорида кальция, аммиака и воды. Реакция протекает при температуре около 200°C.
Лабораторный метод получения аммиака.


 CaCl2 + 2NH3 + 2H2O
CaCl2 + 2NH3 + 2H2O