Химия | 10 — 11 классы
Составьте уравнения реакций восстановления :
1)меди из оксида меди(2), углеродом и оксидов углерода(2)
2)кадмия из оксида кадмия и марганца из оксида марганца(4)водородом
3) железа из оксида железа(3) и хрома из оксида хрома(3) алюминием.
1)a) CuO + C = Cu + CO b) CuO + CO = Cu + CO2
2)a) CdO + H2 = Cd + H2O b) MnO2 + 2H2 = Mn + 2H2O
3)a) Fe2O3 + 2Al = 2Fe + Al2O3 b) Cr2O3 + 2Al = 2Cr + Al2O3.
- Допишите уравнения реакций 1) Оксид кальция + вода 2) Оксид меди + вода 3) Оксид хрома + КОН 4) Оксид углерода (IV) + KOH 5) Оксид меди (II) + H2SO4?
- Напишите уравнения реакций :восстановления алюминием свинца из его высшего оксида ;________________________________________________________________________________ 2) восстановления водородом молибден?
- С какимми веществами при комнатной температуре реагирует концентрированая серная кислота а)алюминия и оксидами алюминия б)железа и оксидом железа (III) в)цинком и оксидам меди (II) г) углеродом и окси?
- Составьте уравнения реакций восстановления меди из оксида меди (II) углеродом и оксидом углерода (II)?
- Составьте формулы следующих оксидов : оксид хрома(III), оксид углерода(IV), оксид магния, оксид серы(VI), оксид азота(V), оксид калия, оксид марганца(VI)?
- Составьте формулы след?
- Напишите уравнения реакций :1) восстановления железа их оксида железа(III) оксидом углерода(II)2) восстановления марганца из оксида марганца(IV) алюминием3) восстановления титана из оксида титана(IV) ?
- Напишите уравнения реакций восстановления углём свинца из оксида свинца(2), железа — из оксида железа (3), меди из оксида меди(1)?
- Напишите по 3 уравнения реакций получения : оксида меди (II), оксида углерода (IV), оксида алюминия?
- Составить и написать формулы следующих оксидов II вариант?
- Оксид меди (II)
- Оксид меди (II)
- Способы получения оксида меди (II)
- Химические свойства оксида меди (II)
- Напишите уравнения реакций восстановления оксидом углерода 2 меди из cu2o
- ГДЗ химия 11 класс Радецкий, дидактический материал, тема 5, раб 1, вариант 2, 1 задание. Напишите уравнения реакций
- 💥 Видео
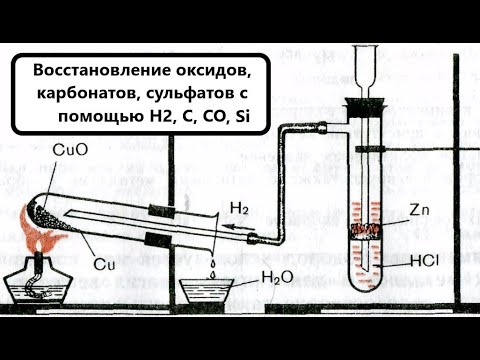
Видео:Восстановление металлов из оксидов водородом, углеродом, угарным газом, кремнием. BaSO4 + H2 / + CСкачать
Допишите уравнения реакций 1) Оксид кальция + вода 2) Оксид меди + вода 3) Оксид хрома + КОН 4) Оксид углерода (IV) + KOH 5) Оксид меди (II) + H2SO4?
Допишите уравнения реакций 1) Оксид кальция + вода 2) Оксид меди + вода 3) Оксид хрома + КОН 4) Оксид углерода (IV) + KOH 5) Оксид меди (II) + H2SO4.
Видео:ОВР и Метод Электронного Баланса — Быстрая Подготовка к ЕГЭ по ХимииСкачать

Напишите уравнения реакций :восстановления алюминием свинца из его высшего оксида ;________________________________________________________________________________ 2) восстановления водородом молибден?
Напишите уравнения реакций :
восстановления алюминием свинца из его высшего оксида ;
________________________________________________________________________________ 2) восстановления водородом молибдена из его высшего оксида ; ________________________________________________________________________________
3) восстановления углем (С) меди из оксида меди(I) ; _________________________________________________________________________________ 4) получения хрома из оксида хрома (III) алюминотермическим способом.
Видео:Химические уравнения // Как Составлять Уравнения Реакций // Химия 9 классСкачать

С какимми веществами при комнатной температуре реагирует концентрированая серная кислота а)алюминия и оксидами алюминия б)железа и оксидом железа (III) в)цинком и оксидам меди (II) г) углеродом и окси?
С какимми веществами при комнатной температуре реагирует концентрированая серная кислота а)алюминия и оксидами алюминия б)железа и оксидом железа (III) в)цинком и оксидам меди (II) г) углеродом и оксидам углерода (IV).
Видео:Практическая работа № 2. Опыт 2.2. Изучение взаимодействия оксида углерода(IV) со щелочью.Скачать

Составьте уравнения реакций восстановления меди из оксида меди (II) углеродом и оксидом углерода (II)?
Составьте уравнения реакций восстановления меди из оксида меди (II) углеродом и оксидом углерода (II).
Видео:9 класс. Оксиды углерода.Скачать

Составьте формулы следующих оксидов : оксид хрома(III), оксид углерода(IV), оксид магния, оксид серы(VI), оксид азота(V), оксид калия, оксид марганца(VI)?
Составьте формулы следующих оксидов : оксид хрома(III), оксид углерода(IV), оксид магния, оксид серы(VI), оксид азота(V), оксид калия, оксид марганца(VI).
Видео:Составление уравнений химических реакций. 1 часть. 8 класс.Скачать

Составьте формулы след?
Составьте формулы след.
Веществ : Оксид азота1 ; Оксид серебра ; Оксид цинка ; Оксид магния ; Оксид бора ; Оксид углерода 4 ; Оксид серы 6 ; Оксид алюминия ; Оксид марганца 4 ; Оксид марганца 6 ; Оксид меди 1 ; Оксид ванадия 5 ; Оксид железа 3 ; Оксид золота 3 ; Оксид вольфрама 6 ; Сульфид алюминия.
Видео:ОКСИДЫ ХИМИЯ — Что такое Оксиды? Химические свойства Оксидов | Реакция ОксидовСкачать

Напишите уравнения реакций :1) восстановления железа их оксида железа(III) оксидом углерода(II)2) восстановления марганца из оксида марганца(IV) алюминием3) восстановления титана из оксида титана(IV) ?
Напишите уравнения реакций :
1) восстановления железа их оксида железа(III) оксидом углерода(II)
2) восстановления марганца из оксида марганца(IV) алюминием
3) восстановления титана из оксида титана(IV) водородом.
Видео:ОКСИДЫ, КИСЛОТЫ, СОЛИ И ОСНОВАНИЯ ХИМИЯ 8 класс / Подготовка к ЕГЭ по Химии - INTENSIVСкачать

Напишите уравнения реакций восстановления углём свинца из оксида свинца(2), железа — из оксида железа (3), меди из оксида меди(1)?
Напишите уравнения реакций восстановления углём свинца из оксида свинца(2), железа — из оксида железа (3), меди из оксида меди(1).
Видео:Как Решать Задачи по Химии // Задачи с Уравнением Химической Реакции // Подготовка к ЕГЭ по ХимииСкачать

Напишите по 3 уравнения реакций получения : оксида меди (II), оксида углерода (IV), оксида алюминия?
Напишите по 3 уравнения реакций получения : оксида меди (II), оксида углерода (IV), оксида алюминия.
Видео:8 класс. Составление уравнений химических реакций.Скачать

Составить и написать формулы следующих оксидов II вариант?
Составить и написать формулы следующих оксидов II вариант.
Оксид углерода (IV), оксид железа (III), оксид кальция, оксид кремния, оксид марганца (II), оксид хрома (VI), оксид серы (IV).
Вы зашли на страницу вопроса Составьте уравнения реакций восстановления :1)меди из оксида меди(2), углеродом и оксидов углерода(2)2)кадмия из оксида кадмия и марганца из оксида марганца(4)водородом3) железа из оксида железа(3) и ?, который относится к категории Химия. По уровню сложности вопрос соответствует учебной программе для учащихся 10 — 11 классов. В этой же категории вы найдете ответ и на другие, похожие вопросы по теме, найти который можно с помощью автоматической системы «умный поиск». Интересную информацию можно найти в комментариях-ответах пользователей, с которыми есть обратная связь для обсуждения темы. Если предложенные варианты ответов не удовлетворяют, создайте свой вариант запроса в верхней строке.
Mr Al(oh)3 = 27 + 48 + 3 = 78г / моль Mr Na2S2O3 = 46 + 64 + 48 = 158 Mr Chcl3 = 12 + 1 + 106. 5 = 119. 5 Ca(oh)2 = 40 + 32 + 2 = 74 Al(oh)j2 = 27 + 16 + 1 + 127 = 171 27÷171 = 0. 15 17÷171 = 0. 09 127÷177 = 0. 71 K2so3 = 78 + 32 + 48 = 158 78÷1..
Номер 1. А) M(Al(oh)3) = 27 + (16 + 1) * 3 = 27 + 51 = 78 b) M(Na2S2O3) = 23 * 2 + 32 * 2 + 16 * 3 = 46 + 64 + 48 = 158 c) M(CHCl3) = 12 + 1 + 35? 5 * 3 = 13 + 106, 5 = 119, 5 Номер 2. M(N2) = 14 г. ⇒ n(N2) = 14 г. : 28 г / моль = 0, 5 моль m(Ca..
Ca(NO3)2 Атома Кислорода в веществе 6 штук, поэтому мы 0, 15 моль умножаем на 6 0, 15х6 = 0, 9 моль Ответ : 0, 9 моль Если помог нажми кнопку Спасибо)).
Видео:Окислительно-восстановительные реакции в ЕГЭ по химииСкачать

Оксид меди (II)
Оксид меди (II)
Оксид меди (II) CuO – твердое кристаллическое вещество черного цвета.
Способы получения оксида меди (II)
Оксид меди (II) можно получить различными методами :
1. Термическим разложением гидроксида меди (II) при 200°С :
2. В лаборатории оксид меди (II) получают окислением меди при нагревании на воздухе при 400–500°С:
2Cu + O2 → 2CuO
3. В лаборатории оксид меди (II) также получают прокаливанием солей (CuOH)2CO3, Cu(NO3)2:
Химические свойства оксида меди (II)
Оксид меди (II) – основный оксид (при этом у него есть слабо выраженные амфотерные свойства) . При этом он является довольно сильным окислителем.
1. При взаимодействии оксида меди (II) с сильными и растворимыми кислотами образуются соли.
Например , оксид меди (II) взаимодействует с соляной кислотой:
СuO + 2HBr = CuBr2 + H2O
CuO + 2HCl = CuCl2 + H2O
2. Оксид меди (II) вступает в реакцию с кислотными оксидами.
Например , оксид меди (II) взаимодействует с оксидом серы (VI) с образованием сульфата меди (II):
3. Оксид меди (II) не взаимодействует с водой.
4. В окислительно-восстановительных реакциях соединения меди (II) проявляют окислительные свойства:
Например , оксид меди (II) окисляет аммиак :
3CuO + 2NH3 → 3Cu + N2 + 3H2O
Оксид меди (II) можно восстановить углеродом, водородом или угарным газом при нагревании:
СuO + C → Cu + CO
Более активные металлы вытесняют медь из оксида.
Например , алюминий восстанавливает оксид меди (II):
3CuO + 2Al = 3Cu + Al2O3
Видео:Химические уравнения - Как составлять уравнения реакций // Составление Уравнений Химических РеакцийСкачать

Напишите уравнения реакций восстановления оксидом углерода 2 меди из cu2o
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
ПРОВЕРЬТЕ СВОИ ЗНАНИЯ
Упражнение 1 И магний, и медь взаимодействуют с:
1) раствором нитрата свинца (II);
2) разбавленной серной кислотой;
3) хлором;
4) с раствором гидроксида калия.
Ответ: 3)
Mg + Cl2 = MgCl2
Cu + Cl2 = CuCl2
Упражнение 2 Химическая реакция возможна между:
1) оксидом фосфора (V) и раствором гидроксида натрия;
2) оксидом меди (II) и водой;
3) растворами хлорида натрия и сульфата калия;
4) гидроксидом железа (III) и магнием.
Ответ: 1)
P2O5 + 6NaOH = 2Na3PO4 + 3H2O
Упражнение 3 Сульфат меди (II) в растворе не реагирует с:
1) железом;
2) гидроксидом натрия;
3) хлоридом бария;
4) нитратом цинка.
Ответ: 4)
1) CuSO4 + Fe = FeSO4 + H2O
2) CuSO4 + 2NaOH = Na2SO4 + Cu(OH)2↓
3) CuSO4 + BaCl2 = CuCl2 + BaSO4↓
4) не реагирует, т.к. образуются растворимые вещества.
Упражнение 4 И гидроксид калия, и серная кислота могут взаимодействовать с:
1) алюминием;
2) хлором;
3) оксидом магния;
4) нитратом бария.
Ответ: 1)
1) 2Al + 2KOH + 6H2O = 2K[Al(OH)4] + 3H2↑
K[Al(OH)4] т етрагидроксоалюминат натрия ― комплексная соль голубого цвета.
Упражнение 5 С оксидом натрия реагирует каждое из двух веществ:
1) кислород и вода;
2) оксид углерода(IV) и оксид бария;
3) калий и азотная кислота;
4) вода и оксид фосфора (V).
Ответ: 4)
Na2O + H2O = 2NaOH
3Na2O + P2O5 = 2Na3PO4
Упражнение 6 Разбавленная серная кислота не взаимодействует с:
1) оксидом кремния;
2) магнием;
3) оксидом алюминия;
4) карбонатом калия.
Ответ: 1)
Разбавленная серная кислота реагирует с оксидами (кроме оксида кремния), с металлами, стоящие в ряду напряжений до водорода, из солями с образованием осадка, воды или газа.
Упражнение 8 Установите соответствие между исходными веществами и продуктами реакции.
| Исходные вещества | Продукты реакции |
| А) Na2SO3 + HCl ⟶ Б) H2S + NaOH ⟶ В) Na2SO3 + O2 ⟶ | 1) Na2SO 4 2) NaCl + H2SO4 3) NaCl + SO2 + H2O 4) Na2SO3 + H2O 5) Na2S + H2O |
Ответ А)―3, Б)―5, В)―1
А) Na2SO3 + 2HCl = 2NaCl + SO2 + H2O
Б) H2S + 2NaOH = Na2S + 2H2O
В) 2Na2SO3 + O2 = 2Na2SO4
Упражнение 2 Дана цепочка превращений: Na2CO3 + HCl → X1 → CaCO3 + HNO3 → X2. Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для первого превращения составьте сокращённое ионное уравнение.
Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
2Na + + CO3 2- + 2H + + 2Cl — = 2Na + + 2Cl — + H2O + CO2↑
2H + + CO3 2- = H2O + CO2↑
CO2 + Ca(OH)2 = CaCO3↓ + H2O
CaCO3 + 2HNO3 = Ca(NO3)2 + H2O + CO2↑
Видео:РЕАКЦИИ ИОННОГО ОБМЕНА, ИОННОЕ УРАВНЕНИЕ - Урок Химия 9 класс / Подготовка к ЕГЭ по ХимииСкачать

ГДЗ химия 11 класс Радецкий, дидактический материал, тема 5, раб 1, вариант 2, 1 задание. Напишите уравнения реакций
Напишите уравнения реакций: а) получения железа из оксида железа(Ш) алюминотермическим способом; б) получения меди из оксида меди(II) путём восстановления углём; в) получения вольфрама из его высшего оксида путём восстановления водородом. Реакцию в разберите как окислительновосстановительную: обозначьте степени окисления атомов и расставьте коэффициенты, определив их методом электронного баланса.
💥 Видео
Решение задач на термохимические уравнения. 8 класс.Скачать

Все реакции с металлами за 1 урок | ЕГЭ по химии 2024 | Екатерина СтрогановаСкачать

Как уравнивать окислительно-восстановительные реакции?Скачать

Уравнения химический реакций на ОГЭ: как составлять без ошибок?Скачать

Окислительно-восстановительные реакции. Видеоурок по химии 9 классСкачать

Уравнивание реакций горения углеводородовСкачать

ЖЕЛЕЗО и его соединения для ЕГЭ ПОЛНОСТЬЮ | Самые завальные реакции | ЕГЭ по химии 2023Скачать







