Специфичность пептидов и белков определяется двумя важнейшими характеристиками — аминокислотным составом и аминокислотной последовательностью. Аминокислотный состав пептидов и белков — это природа и количественное соотношение входящих в них α-аминокислот. Аминокислотный состав устанавливается путем анализа пептидных и белковых гидролизатов в основном хроматографическими методами. В настоящее время такой анализ осуществляется с помощью аминокислотных анализаторов.
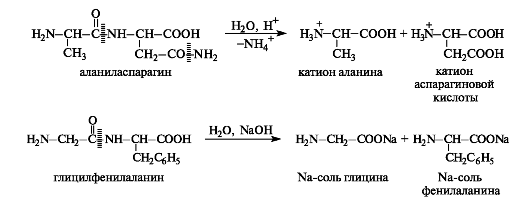
Амидные связи способны гидролизоваться как в кислой, так и щелочной среде. Пептиды и белки гидролизуются с образованием либо более коротких цепей — это так называемый частичный гидролиз, либо смеси аминокислот (в ионной форме) — полный гидролиз. Гидролиз пептидов может происходить в кислой или щелочной среде, а также под действием ферментов. Ферментативный гидролиз важен тем, что протекает селективно, т.е. позволяет расщеплять строго определенные участки пептидной цепи.
Обычно гидролиз осуществляют в кислой среде, так как в условиях щелочного гидролиза многие аминокислоты неустойчивы. Следует отметить, что гидролизу подвергаются также амидные группы аспарагина и глутамина.
Первичную структуру пептидов и белков определяют путем последовательного отщепления аминокислот с какого-либо конца цепи и их идентификации.
Видео:Гидролиз солей. 9 класс.Скачать

Схема гидролиза трипептида
Скачать
презентацию
Схема гидролиза трипептида.
Слайд 21 из презентации ««Аминокислоты и белки» химия». Размер архива с презентацией 1327 КБ.
Видео:Пептидная связь. Образование пептидной связи. Запись структурной формулы пептида.Скачать

Химия 10 класс
«Влияние железа на организм» — Биологическая роль железа. Влияние железа на жизнедеятельность организма человека. Железо не только основа всего мира, самый главный металл. Избыток железа отрицательно влияет на здоровье человека. Нервные расстройства. Необходимо для процессов роста организма. Железо–важнейший микроэлемент. Повышенная чувствительность к холоду. Железо в продуктах растительного происхождения. Сколько железа требуется человеку.
«Химическая промышленность мира» — Лидеры по производству серной кислоты. Химическая промышленность. Фосфорные удобрения. Принцип размещения. Азотные удобрения. Полимерные материалы. Крупнейшие транснациональные корпорации. Значение химической промышленности. Лидеры по производству. Минеральные удобрения. Калийные удобрения. Основная химия. Химическая промышленность мира.
«Использование алюминия» — Принимает участие в построении эпителиальной и соединительной тканях. Тема: Алюминий на кухне. Какую вы используете посуду? Изучить химические свойства алюминия. Опрос. Знаете ли вы о недостатках алюминиевых кастрюль? Основным поступлением алюминия в организм является пища. Методы Исследования: Подготовить памятки с рекомендациями «Советы хозяйкам». Алюминий играет важную биологическую роль в жизни человека.
««Амины» 10 класс» — Основные свойства аминов. Строение. Амины. Изомерия аминов. Задание. Аммиак. Ацетилен. Что такое амины. Классификация аминов. Химические свойства аминов. Горение. Номенклатура аминов. Химические свойства. Физические свойства.
«Крахмал» — Качественная реакция на крахмал. Гидролиз крахмала. Полисахариды. Биосинтез крахмала. Физические свойства крахмала. Промышленное значение крахмала. Спасибо за внимание. Значение крахмала для организма человека. Биологическое значение крахмала. Молекула крахмала.
«Задачи по химии для 10 класса» — Выведите молекулярную формулу. Определяем простейшую формулу соединения: n(S). Массовая доля кислорода. Решение задач. Выведите молекулярную формулу альдегида. Определите молекулярную формулу алкана. Массовая доля углерода. Вывести формулу соединения. Относительная плотность углеводорода по водороду. Определить химическую формулу соединения. Найдите молекулярную формулу углеводорода. Определяем молярную массу соединения.
Всего в теме «Химия 10 класс» 58 презентаций
Видео:Трипептиды как составлять (РязГМУ 2 семестр последний коллок)Скачать

Практические задания к зачету по дисциплине «Органическая химия». Варианты 1-4/1а-4а
Страницы работы
Содержание работы
В А Р И А Н Т N 1
1. Напишите строение трипептида Асп-Фен-Ала. Укажите пептидные связи, N- и С-конец в молекуле. В какой области рН находится ИЭТ данного трипептида?
2. О-гликозиды. Получение, строение, гидролиз. Галактозамин – строение, значение. Напишите формулу по Колли-Толленсу и Хеуорзсу. Мальтоза, цокло-оксотаутомерия.
3. Построить участок молекулы РНК со следующей последовательностью оснований в мононуклеотидах: Г-Ц-У.
4. Напишите схему гидролиза фосфатидилсерина, содержащего остатки пальмитиновой и линоленовой кислот в щелочной среде. Церамид, строение, биологическая роль.
В А Р И А Н Т N 2
1. Напишите строение трипептида Лиз-Мет-Тре. Укажите пептидные связи, N- и С-конец в молекуле. В какой области рН находится ИЭТ данного трипептида?
2. Химические свойства моносахаридов: реакции карбонильной и гидроксильной групп. Глюкоза и ее эпимеры (напишите строение в открытой и циклической форме по Хеуорзсу). Декстраны, строение, биологическая роль.
3. Нуклеотиды: пуриновые и пиримидиновые. Кислотный и щелочной гидролиз.
4. Напишите схему реакции этерификации глицерина соответствующими кислотами для получения диолеоиллинолеоилглицерина. Дайте определение иодного числа. Напишите соответствующее уравнение реакции. Фосфатидилхолин, щелочной гидролиз.
В А Р И А Н Т N 3
1. Напишите строение трипептида Гис-Сер-Арг. Укажите пептидные связи, N- и С-конец в молекуле. В какой области рН находится ИЭТ данного трипептида?
2. Сахароза, строение, свойства, биологическая роль. Полисахариды, классификация. Гликоген, строение, биологическая роль.
3. N-гликозиды пуриновые и пиримидиновые.
4. Напишите схему кислотного гидролиза кефалина, содержащего остатки пальмитиновой и линоленовой кислот. Покажите схему β-окисления пальмитиновой кислоты.
В А Р И А Н Т N 4
1. Напишите строение трипептида Тир-Глу-Лей. Укажите пептидные связи, N- и С-конец в молекуле. В какой области рН находится ИЭТ данного трипептида?
2. Восстановление моносахаридов (ксилит, сорбит, пульцит, маннит). Лактоза, строение, цикло-оксотаутомерия, биологическая роль, гидролиз.
3. Комплементарность (показать образование водородных связей между комплементарными основаниями). ДНК, биологическая роль.
4. Напишите строение фосфатидилхолина, содержащего стеариновую и олеиновую кислоты. Обозначьте полярную и неполярную части. Способно ли данное соединение подвергаться пероксидному окислению? Ответ подтвердите соответствующей схемой пероксидного окисления.
В А Р И А Н Т N 1а
1. Напишите строение трипептида Асп-Тир-Вал. Укажите пептидные связи, N- и С-конец в молекуле. В какой области рН находится ИЭТ данного трипептида?
2. Сахароза, строение, свойства, биологическая роль. Полисахариды, классификация. Гликоген, строение, биологическая роль.
3. Построить участок молекулы РНК со следующей последовательностью оснований в мононуклеотидах: А-У-Г.
4. Напишите схему гидролиза фосфатидилсерина, содержащего остатки пальмитиновой и линоленовой кислот в щелочной среде. Церамид, строение, биологическая роль.
В А Р И А Н Т N 2а
1. Напишите строение трипептида Мет-Иле-Лиз Укажите пептидные связи, N- и С-конец в молекуле. В какой области рН находится ИЭТ данного трипептида?
2. Восстановление моносахаридов (ксилит, сорбит, пульцит, маннит). Лактоза, строение, цикло-оксотаутомерия, биологическая роль, гидролиз.
3. Нуклеотиды: пуриновые и пиримидиновые. Кислотный и щелочной гидролиз.
4. Напишите схему реакции этерификации глицерина соответствующими кислотами для получения олеоиларахидоиллиноленоилглицерина. Дайте определение иодного числа. Напишите соответствующее уравнение реакции. Фосфатидилхолин, щелочной гидролиз.
В А Р И А Н Т N 3а
1. Напишите строение трипептида Арг-Три-Лей. Укажите пептидные связи, N- и С-конец в молекуле. В какой области рН находится ИЭТ данного трипептида?
2. О-гликозиды. Получение, строение, гидролиз. Галактозамин – строение, значение. Напишите формулу по Колли-Толленсу и Хеуорзсу. Мальтоза, цикло-оксотаутомерия.
3. Комплементарность (показать образование водородных связей между комплементарными основаниями). ДНК, биологическая роль.
4. Напишите схему кислотного гидролиза кефалина, содержащего остатки стеариновой и линолевой кислот. Покажите схему β-окисления пальмитиновой кислоты (один цикл).
В А Р И А Н Т N 4а
1. Напишите строение трипептида Гис-Тир-Фен. Укажите пептидные связи, N- и С-конец в молекуле. В какой области рН находится ИЭТ данного трипептида?
2. Химические свойства моносахаридов: реакции карбонильной и гидроксильной групп. Глюкоза и ее эпимеры (напишите строение в открытой и циклической форме по Хеуорзсу). Декстраны, строение, биологическая роль.
3. N-гликозиды пуриновые и пиримидиновые.
4. Напишите строение фосфатидилхолина, содержащего пальмитиновую и линоленовую кислоты. Обозначьте полярную и неполярную части. Способно ли данное соединение подвергаться пероксидному окислению? Ответ подтвердите соответствующей схемой пероксидного окисления на примере олеиновой кислоты.
🎥 Видео
Образование пептидов. Запись структурной формулы пептидаСкачать

Задача на определение формулы трипептида. Биохимия.Скачать

Определение pI (изоэлектрической точки) пептидов. Биохимия.Скачать

ГИДРОЛИЗ СОЛЕЙ | 9 класс | Кратко и понятноСкачать

Пептидная связь. 11 класс.Скачать

Гидролиз пептидов 🧪 #химия #егэ2023 #соткаСкачать

Совместный гидролиз за 12 минут | ХИМИЯ ЕГЭ | СОТКАСкачать

Составление уравнений реакций горения. 11 класс.Скачать

Щелочь + соль = ??? | Опыты для ЕГЭ и ОГЭ по химииСкачать

Кислотный и щелочной гидролиз бинарных соединений | Химия ЕГЭ 2023 | УмскулСкачать

13.3. Сложные эфиры: Химические свойстваСкачать

25. Схема реакции и химическое уравнениеСкачать

Гидролиз | Химия ЕГЭ | УмскулСкачать

Все реакции гидролиза в ЕГЭ за 2 часа | Химия ЕГЭ 2022 | УмскулСкачать

Переваривание и всасывание белков (катаболизм белков) | БиохимияСкачать

Совместный гидролиз в реакциях ионного обмена: за что?! | Химия ЕГЭ | УмскулСкачать

Реакции преципитации. Реакция двойной иммунодиффузииСкачать