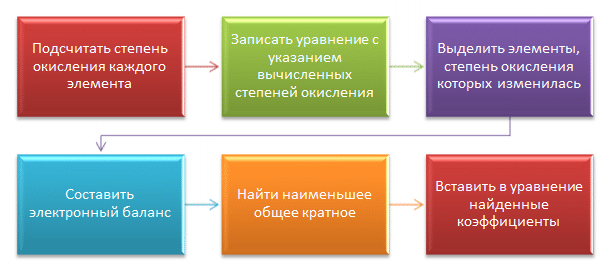
Спецификой многих ОВР является то, что при составлении их уравнений подбор коэффициентов вызывает затруднение.
Для облегчения подбора коэффициентов чаще всего используют метод электронного баланса и ионно-электронный метод (метод полуреакций). Рассмотрим применение каждого из этих методов на примерах.
- Метод электронного баланса
- Ионно-электронный метод (метод полуреакций)
- Метод электронного баланса в доступном изложении
- Применение метода электронного баланса по шагам. Пример «а»
- Пример «б»
- Пример «в»
- Применение метода электронного баланса для расстановки коэффициентов в неорганических реакциях. Случаи, когда индекс при химическом элементе вносится в электронный баланс. Расстановка коэффициентов методом электронного баланса, если в уравнении более 2 элементов меняют степени окисления
Метод электронного баланса
В его основе метода электронного баланса лежит следующее правило: общее число электронов, отдаваемое атомами-восстановителями, должно совпадать с общим числом электронов, которые принимают атомы-окислители .
В качестве примера составления ОВР рассмотрим процесс взаимодействия сульфита натрия с перманганатом калия в кислой среде.
1) Составить схему реакции:
Записать исходные вещества и продукты реакции, учитывая, что в кислой среде MnO4 — восстанавливается до Mn 2+ (см. схему):
Найдем степень окисления элементов:
Из приведенной схемы понятно, что в процессе реакции происходит увеличение степени окисления серы с +4 до +6. S +4 отдает 2 электрона и является восстановителем. Степень окисления марганца уменьшилась от +7 до +2, т.е. Mn +7 принимает 5 электронов и является окислителем.
3) Составить электронные уравнения и найти коэффициенты при окислителе и восстановителе.
S +4 – 2e — = S +6 | 5 восстановитель, процесс окисления
Mn +7 +5e — = Mn +2 | 2 окислитель, процесс восстановления
Чтобы число электронов, отданных восстановителем, было равно числу электронов, принятых восстановителем, необходимо:
- Число электронов, отданных восстановителем, поставить коэффициентом перед окислителем.
- Число электронов, принятых окислителем, поставить коэффициентом перед восстановителем.
Таким образом, 5 электронов, принимаемых окислителем Mn +7 , ставим коэффициентом перед восстановителем, а 2 электрона, отдаваемых восстановителем S +4 коэффициентом перед окислителем:
4) Уравнять количества атомов элементов, не изменяющих степень окисления
Соблюдаем последовательность: число атомов металлов, кислотных остатков, количество молекул среды (кислоты или щелочи). В последнюю очередь подсчитывают количество молекул образовавшейся воды.
Итак, в нашем случае число атомов металлов в правой и левой частях совпадают.
По числу кислотных остатков в правой части уравнения найдем коэффициент для кислоты.
В результате реакции образуется 8 кислотных остатков SO4 2- , из которых 5 – за счет превращения 5SO3 2- → 5SO4 2- , а 3 – за счет молекул серной кислоты 8SO4 2- — 5SO4 2- = 3SO4 2- .
Таким образом, серной кислоты надо взять 3 молекулы:
Аналогично, находим коэффициент для воды по числу ионов водорода, во взятом количестве кислоты
6H + + 3O -2 = 3H2O
Окончательный вид уравнения следующий:
Признаком того, что коэффициенты расставлены правильно является равное количество атомов каждого из элементов в обеих частях уравнения.
Ионно-электронный метод (метод полуреакций)
Реакции окисления-восстановления, также как и реакции обмена, в растворах электролитов происходят с участием ионов. Именно поэтому ионно-молекулярные уравнения ОВР более наглядно отражают сущность реакций окисления-восстановления.
При написании ионно-молекулярных уравнений, сильные электролиты записывают в виде ионов, а слабые электролиты, осадки и газы записывают в виде молекул (в недиссоциированном виде).
При написании полуреакций в ионной схеме указывают частицы, подвергающиеся изменению их степеней окисления, а также характеризующие среду, частицы:
H + — кислая среда, OH — — щелочная среда и H2O – нейтральная среда.
Пример 1.
Рассмотрим пример составления уравнения реакции между сульфитом натрия и перманганатом калия в кислой среде.
1) Составить схему реакции:
Записать исходные вещества и продукты реакции:
2) Записать уравнение в ионном виде
В уравнении сократим те ионы, которые не принимают участие в процессе окисления-восстановления:
SO3 2- + MnO4 — + 2H + = Mn 2+ + SO4 2- + H2O
3) Определить окислитель и восстановитель и составить полуреакции процессов восстановления и окисления.
В приведенной реакции окислитель — MnO4 — принимает 5 электронов восстанавливаясь в кислой среде до Mn 2+ . При этом освобождается кислород, входящий в состав MnO4 — , который, соединяясь с H + образует воду:
MnO4 — + 8H + + 5e — = Mn 2+ + 4H2O
Восстановитель SO3 2- — окисляется до SO4 2- , отдав 2 электрона. Как видно образовавшийся ион SO4 2- содержит больше кислорода, чем исходный SO3 2- . Недостаток кислорода восполняется за счет молекул воды и в результате этого происходит выделение 2H + :
SO3 2- + H2O — 2e — = SO4 2- + 2H +
4) Найти коэффициенты для окислителя и восстановителя
Необходимо учесть, что окислитель присоединяет столько электронов, сколько отдает восстановитель в процессе окисления-восстановления:
MnO4 — + 8H + + 5e — = Mn 2+ + 4H2O |2 окислитель, процесс восстановления
SO3 2- + H2O — 2e — = SO4 2- + 2H + |5 восстановитель, процесс окисления
5) Просуммировать обе полуреакции
Предварительно умножая на найденные коэффициенты, получаем:
2MnO4 — + 16H + + 5SO3 2- + 5H2O = 2Mn 2+ + 8H2O + 5SO4 2- + 10H +
Сократив подобные члены, находим ионное уравнение:
2MnO4 — + 5SO3 2- + 6H + = 2Mn 2+ + 5SO4 2- + 3H2O
6) Записать молекулярное уравнение
Молекулярное уравнение имеет следующий вид:
Пример 2.
Далее рассмотрим пример составления уравнения реакции между сульфитом натрия и перманганатом калия в нейтральной среде.
В ионном виде уравнение принимает вид:
Также, как и предыдущем примере, окислителем является MnO4 — , а восстановителем SO3 2- .
В нейтральной и слабощелочной среде MnO4 — принимает 3 электрона и восстанавливается до MnО2. SO3 2- — окисляется до SO4 2- , отдав 2 электрона.
Полуреакции имеют следующий вид:
MnO4 — + 2H2O + 3e — = MnО2 + 4OH — |2 окислитель, процесс восстановления
SO3 2- + 2OH — — 2e — = SO4 2- + H2O |3 восстановитель, процесс окисления
Запишем ионное и молекулярное уравнения, учитывая коэффициенты при окислителе и восстановителе:
Пример 3.
Составление уравнения реакции между сульфитом натрия и перманганатом калия в щелочной среде.
В ионном виде уравнение принимает вид:
В щелочной среде окислитель MnO4 — принимает 1 электрон и восстанавливается до MnО4 2- . Восстановитель SO3 2- — окисляется до SO4 2- , отдав 2 электрона.
Полуреакции имеют следующий вид:
MnO4 — + e — = MnО2 |2 окислитель, процесс восстановления
SO3 2- + 2OH — — 2e — = SO4 2- + H2O |1 восстановитель, процесс окисления
Запишем ионное и молекулярное уравнения, учитывая коэффициенты при окислителе и восстановителе:
Необходимо отметить, что не всегда при наличии окислителя и восстановителя, возможно самопроизвольное протекание ОВР. Поэтому для количественной характеристики силы окислителя и восстановителя и для определения направления реакции пользуются значениями окислительно-восстановительных потенциалов.
Еще больше примеров составления окислительно-восстановительных реакций приведены в разделе Задачи к разделу Окислительно-восстановительные реакции. Также в разделе тест Окислительно-восстановительные реакции
Метод электронного баланса в доступном изложении
Задача.
Методом электронного баланса подберите коэффициенты в схемах следующих окислительно-восстановительных реакций с участием металлов:
Применение метода электронного баланса по шагам. Пример «а»
(в сумме, опять же, получим ноль, как и должно быть)
Теперь перейдем ко второй части уравнения.
Для AgNO3 степень окисления серебра +1 кислорода -2, следовательно степень окисления азота равна:
Для NO степень окисления кислорода -2, следовательно азота +2
Для H2O степень окисления водорода +1, кислорода -2
Шаг 2. Запишем уравнение в новом виде, с указанием степени окисления каждого из элементов, участвующих в химической реакции.
Ag 0 + H +1 N +5 O -2 3 → Ag +1 N +5 O -2 3 + N +2 O -2 + H +1 2O -2
- В первоначальном уравнении перед Ag ставим тройку, что потребует такого же коэффициента перед AgNO3
- Теперь у нас возник дисбаланс по количеству атомов азота. В правой части их четыре, в левой — один. Поэтому ставим перед HNO3 коэффициент 4
- Теперь остается уравнять 4 атома водорода слева и два — справа. Решаем это путем применения коэффииента 2 перед H2O
Пример «б»
Для H2SO4 степень окисления водорода +1 кислорода -2 откуда степень окисления серы 0 — (+1)*2 — (-2)*4 = +6
Для CaSO4 степень окисления кальция равна +2 кислорода -2 откуда степень окисления серы 0 — (+2) — (-2)*4 = +6
Для H2S степень окисления водорода +1, соответственно серы -2
Ca 0 +H +1 2S +6 O -2 4 → Ca +2 S +6 O -2 4 + H +1 2S -2 + H +1 2O -2
Ca 0 — 2e = Ca +2 (коэффициент 4)
S +6 + 8e = S -2
Пример «в»
Для Be(NO3)2 степень окисления бериллия +2, кислорода -2, откуда степень окисления азота ( 0 — (+2) — (-2)*3*2 ) / 2 = +5
Be 0 + H +1 N +5 O -2 3 → Be +2 (N +5 O -2 3)2 + N +2 O -2 + H +1 2O -2
Be 0 — 2e = Be +2 (коэффициент 3)
N +5 +3e = N +2 (коэффициент 2)
Применение метода электронного баланса для расстановки коэффициентов в неорганических реакциях. Случаи, когда индекс при химическом элементе вносится в электронный баланс. Расстановка коэффициентов методом электронного баланса, если в уравнении более 2 элементов меняют степени окисления
Применение метода электронного баланса для расстановки коэффициентов в неорганических реакциях. Случаи, когда индекс при химическом элементе вносится в электронный баланс. Расстановка коэффициентов методом электронного баланса, если в уравнении более 2 элементов меняют степени окисления.
Решение заданий части С ЕГЭ требует от учащихся комплекса знаний и умений.
Давайте разберемся, что нужно знать и уметь ученику, чтобы успешно выполнить задание С1.
1. Уметь расставлять степени окисления элементов в молекулярных формулах веществ.
2. Уметь составлять электронный баланс, то есть определять количество и направление перехода электронов.
3. Уметь расставлять коэффициенты.
Именно этим трем пунктам будет посвящено наше первое занятие.
Однако, помимо этого, есть еще более сложные умения: прогнозировать продукты окислительно-восстановительных процессов, исходя из данных реагентов, или реагенты, исходя из продуктов. Этому будут посвящены наши дальнейшие занятия.
Умение 1: расставлять степени окисления элементов в молекулярных формулах веществ.
Это умение не является простым. Для того, чтобы определить степени окисления элементов, нужны определенные знания и способы их применения.
Какие это знания?
1. Электроотрицательность – способность атомов притягивать к себе общие электронные пары. Притягивая к себе электроны, атомы приобретают частичный отрицательный заряд. Наиболее электроотрицательными являются неметаллы: фтор, кислород и азот. Металлы, как правило, смещают электроны от себя, приобретая положительный заряд. Сравнить электроотрицательность разных элементов можно с помощью ряда электроотрицательности, или по положению в периодической системе.
2. Степень окисления. Понятие степени окисления весьма формально: это заряд, который приобрел бы атом, если бы все связи в молекуле стали ионными. Можно объяснить степень окисления несколько иначе: как число электронов, смещенных к атому ( – ) или от атома (+). Для того, чтобы воспользоваться этим определением степени окисления, потребуются графические (структурные) формулы, которые ученики не всегда могут построить правильно. Этот метод хорош в органической химии, и мы к нему обязательно обратимся на следующем занятии.
При определении степени окисления в неорганических веществах чаще всего пользуются алгебраическим методом и находят усредненное значение степени окисления. Именно поэтому иногда степень окисления выражается нецелыми числами. Степень окисления каждого отдельного атома должна быть целым числом (потому что смещается целое количество электронов).
3. Значение степени окисления некоторых элементов.
Ученики должны знать, что:
· Степень окисления элементов в простых веществах равна 0.
· Фтор в соединениях имеет степень окисления – 1.
· Металлы 1-2 группы главной подгруппы в соединениях имеют степень окисления +№ группы. (В принципе, можно сказать, что бор и алюминий тоже имеют степень окисления +№ группы, так как в школьном курсе с другими степенями окисления этих элементов мы не сталкиваемся. Но строго говоря, у алюминия, галлия, индия и таллия есть соединения, в которых они проявляют степень окисления +1)
· Водород в большинстве соединений проявляет степень окисления +1, и только в гидридах (соединениях с металлами) может быть – 1.
· Кислород чаще всего проявляет степень окисления – 2. Однако, в соединениях с фтором может быть +1 или +2, в соединениях с активными металлами и водородом может проявлять степень окисления – 1 (пероксиды), и дробные степени окисления (надпероксиды и озониды).
Как ученику понять, что в этом соединении у кислорода(или другого элемента) нетипичная степень окисления? Для этого достаточно расставлять степени окисления именно в том порядке, в котором я здесь их привожу, то есть сначала у атомов фтора, потом у атомов металлов 1, 2, 3 групп главных подгрупп, потом у водорода, потом у кислорода. Например, КО3. Расставлять степени окисления нужно с калия, так как у него возможна единственная степень окисления +1, тогда у кислорода – 1/3. N2H4 – расставлять степени окисления следует с водорода, так как он соединен с неметаллом, то проявляет степень окисления +1, значит, у азота степень окисления – 2. HOF – сначала определим степень окисления фтора – 1, потом водорода +1, степень окисления кислорода оказывается 0.
· Все остальные неметаллы могут проявлять переменные степени окисления от (№ группы – 8) – низшая степень окисления до + № группы – высшая степень окисления. Если атом неметалла является в молекуле наиболее электроотрицательным, то его степень окисления скорее всего будет низшей (№ группы – 8).
· Металлы побочных подгрупп и главных подгрупп 4 – 6 групп могут иметь только положительные степени окисления в соединениях, причем у элементов побочных подгрупп номер группы не всегда соответствует высшей степени окисления (например, медь +2, золото +3, железо +6, никель +2, кобальт +3 и т. д.). Степень окисления этих элементов можно определить только по формуле.
Алгебраический метод определения степени окисления исходит из того, что молекула в целом электронейтральна, то есть сумма степеней окисления всех элементов равна нулю.
Например, определим степени окисления элементов в молекуле серной кислоты H2SO4. Так как водород в этой молекуле не связан с металлом, то его степень окисления +1(на 2 атома водорода приходится +2), кислород не связан с фтором, перед нами явно не пероксид и не озонид, поэтому его степень окисления – 2 (на 4 атома кислорода приходится –8). Обозначим степень окисления серы за х. Тогда +2–8+х = 0; х = +6.
Этот метод хорош и для определения степени окисления элементов в ионах. Например, ортофосфат-анион PO43–.
У кислорода степень окисления – 2, на 4 атома кислорода приходится –8, пусть степень окисления фосфора х, тогда сумма степеней окисления равна заряду иона, то есть: х–8 = –3, откуда х = +5
Вот несколько другой подход:
Определим, какой элемент в молекуле наиболее электроотрицательный и отделим его. Это кислород, у него будет низшая степень окисления (№ группы – 8) = 6 – 8 = –2. Умножим индекс 4 на степень окисления –2, получится –8. Значит, на оставшуюся часть молекулы приходится +8. Из них +2 приходится на водород, значит, на серу остается +6.
 |

Если в формуле используются скобки, это может вызвать затруднения у учащихся. Здесь можно предложить несколько вариантов определения степени окисления.
Например, ортофосфат кальция. Первый вариант заключается в том, что нужно раскрыть скобки: Ca3(PO4)2 или Ca3P2O8, дальше можно действовать любым из указанных выше способов. Степени окисления кальция и кислорода очевидны, следует найти только степень окисления фосфора. Второй вариант заключается в том, что нужно определить степень окисления фосфора в соответствующей кислоте.
Третий вариант – найти степени окисления в ионе PO4 3 –
В формулах, где степень окисления не является постоянной у 2 элементов, нужно ориентироваться с помощью зарядов ионов.
Например, Fe2(SO4)3. Индекс у сульфат — иона показывает заряд железа. Дальше – любым из выше перечисленных способов.
FeSO4 – заряд сульфат — иона – 2, значит, у железа +2. И т. д.
Умение 2: составлять электронный баланс, то есть определять количество и направление перехода электронов.
Вы наверняка сталкивались с тем, что иногда путаете, отдает элемент электроны или принимает, окислитель он или восстановитель. Каждый учитель ищет рациональные способы запоминания понятий «окислитель», «восстановитель», «окисление», «восстановление», пытается добиться усвоения и безошибочного применения учащимися этих понятий.
Опять же начнем с обязательных знаний:
1. Окисление – процесс отдачи электронов. (Небольшой мнемонический приём: Окисление – Отдача, начинаются с одной буквы)
Восстановление – процесс принятия электронов.
2. Окисление происходит с восстановителем. Значит, восстановитель отдает электроны, окисляется, его степень окисления повышается.
Восстановление происходит с окислителем. Значит, окислитель принимает электроны, восстанавливается, его степень окисления понижается.
(Здесь я хочу вам предложить юмористический приём запоминания, связанный с одушевлением атомов. Восстановитель – созидатель, меценат, он отдает свои электроны, в результате приобретает «положительную репутацию» в обществе, то есть повышает степень окисления. А окислитель – вор, отбирает электроны у других элементов, в результате его «репутация» падает (степень окисления понижается). А рассуждать можно так: степень окисления понизилась, значит, репутация упала, это «плохой» герой нашей истории, окислитель, он отбирает электроны у других. И, наоборот: степень окисления повысилась, репутация возросла, значит, это положительный герой, он жертвует свои электроны, это восстановитель)
Кому не нравится такой подход, предлагаю графический метод:
Сколько электронов принимает или отдает атом элемента, можно посчитать по координатной прямой.
А теперь логический метод. Положительная степень окисления атома – это нехватка отрицательных частиц – электронов, отрицательная – избыток электронов. Например, S+4 ®S – 2 . Рассуждаем так: до реакции атому серы не хватало 4 электронов, после реакции появилось 2 лишних. Это значит, что он приобрел 6 электронов (4 – для того, чтобы стать нейтральной частицей, и ещё 2 – чтобы приобрести отрицательную степень окисления).
После того, как учащиеся научатся определять количество и направление перехода электронов, и записывать это в виде электронного баланса, можно переходить к расстановке коэффициентов.
Умение 3: расставлять коэффициенты методом электронного баланса.
Здесь мне хотелось бы рассмотреть два достаточно распространенных примера:
Cu + HNO3 ® Cu(NO3)2 + NO + H2O
1) Определяем степени окисления всех элементов;
2) Выбираем те элементы, у которых изменилась степень окисления;
3) Составляем электронный баланс

N +5 +3e ® N+2 2 окислитель
Число принятых и отданных электронов переносим крест-накрест и сокращаем. Это множители, которые позволяют осуществить закон сохранения: число принятых электронов должно быть равно числу отданных электронов.
Теперь эти множители нужно внести в схему реакции, они должны стать коэффициентами. Перед атомами меди в левой и правой части уравнения нужно поставить коэффициент 3. В этом действии можно не сомневаться, так как медь в левой и правой части встречается только по одному разу.
3 Cu + HNO3 ® 3Cu(NO3)2 + NO + H2O
А вот с азотом возникает вопрос: к какому из атомов азота относится коэффициент 2? Ответ: к тому, степень окисления которого в уравнении встречается единожды, то есть +2. Ставим коэффициент 2 перед NO.
3 Cu + HNO3 ® 3Cu(NO3)2 + 2NO + H2O
Дальше сравниваем левую и правую часть схемы и достраиваем коэффициенты в таком порядке: в правой части после выставления коэффициентов из баланса перед всеми атомами азота есть коэффициенты, пересчитаем азот в правой части – 8, ставим этот коэффициент перед азотной кислотой.
Теперь в левой части поставлен коэффициент перед водородом, число его атомов 8. Ставим в правую часть перед водой 4.
Осталось сравнить число атомов кислорода в левой и правой части уравнения. Если равно – коэффициенты расставлены правильно, если нет – ищем ошибку.
KMnO4 + K2SO3 + H2SO4 ® MnSO4 + K2SO4 + H2O
1) Определяем степени окисления всех элементов;
2) Выбираем те элементы, у которых изменилась степень окисления;
3) Составляем электронный баланс

Mn+7 +5e ® Mn+2 2 окислитель
Перед атомами марганца в левой и правой части уравнения нужно поставить коэффициент 2. В этом действии можно не сомневаться, так как марганец в левой и правой части встречается только по одному разу.
2KMnO4 + K2SO3 + H2SO4 ® 2MnSO4 + K2SO4 + H2O
С серой возникает вопрос: к какому из атомов серы относится коэффициент 5? К тому, степень окисления которого в уравнении встречается единожды, то есть +4. Ставим коэффициент 5 перед K2SO3.
2KMnO4 + 5K2SO3 + H2SO4 ® 2MnSO4 + K2SO4 + H2O
Дальше сравниваем левую и правую часть схемы и достраиваем коэффициенты в таком порядке: калий ( в левой части 10+2=12, перед K2SO4 поставим 6)
2KMnO4 + 5K2SO3 + H2SO4 ® 2MnSO4 + 6K2SO4 + H2O
Теперь в правой части поставлены коэффициенты перед серой, число её атомов 8. В левой части уже есть коэффициент перед серой 5, не хватает еще 3.
2KMnO4 + 5K2SO3 + 3H2SO4 ® 2MnSO4 + 6K2SO4 + H2O
Сравниваем число атомов водорода. Ставим перед водой 3.
2KMnO4 + 5K2SO3 + 3H2SO4 ® 2MnSO4 + 6K2SO4 + 3H2O
Осталось сравнить число атомов кислорода в левой и правой части уравнения. 35 и 35.
Случаи, когда индекс при химическом элементе вносится в электронный баланс.
1) Если формула простого вещества записывается с индексом:
NH3 +O2 ® NO + H2O

5 ставим перед простым веществом – кислородом, 4 – перед азотом в левой и правой части уравнения, уравниваем водород, проверяем кислород.
2) Если в молекуле атомы одного элемента соединены между собой (то есть присутствует ковалентная неполярная связь): пероксиды, дисульфиды, тиосульфат, веселящий газ, органические вещества:
Cr(OH)3 + H2O2 + KOH ® K2CrO4 + H2O

3 ставим перед пероксидом водорода, 2 – перед хромом в левой и правой части уравнения, уравниваем калий, потом — водород, проверяем кислород.
2Cr(OH)3 + 3H2O2 + 4KOH = 2 K2CrO4 + 8H2O
3) Если у элемента усредненная степень окисления получается нецелым числом
(железная окалина, надпероксиды, озониды, органические вещества):
Fe3O4 + H2SO4 (конц)®Fe2(SO4)3 + SO2 + H2O

S+6 +2e ® S+4 1 окислитель
2 ставим перед железной окалиной, тогда перед сульфатом железа – 3, перед сернистым газом коэффициента не будет, тогда справа 10 атомов серы, 10 ставим перед серной кислотой, уравниваем водород (перед водой – 10), сравниваем кислород
2Fe3O4 + 10H2SO4 (конц)=3Fe2(SO4)3 + SO2 + 10 H2O
4) Если у одного элемента в левой и правой части уравнения есть одинаковый индекс:
K2Cr2O7 + K2SO3 + H2SO4 ® Cr2(SO4)3 + K2SO4 + H2O

Перед сульфитом ставим 3, перед хромом в левой и правой части коэффициент не нужен, уравниваем калий (в правой части перед сульфатом калия ставим 4), затем – серу (в левой части перед серной кислотой – 4), водород – перед водой 4, проверяем кислород.
K2Cr2O7 + 3K2SO3 + 4H2SO4 = Cr2(SO4)3 + 4K2SO4 + 4H2O
5) Если без удвоения не уравнивается, хотя индекс у элемента есть только в одной из частей уравнения.
NO2 + P2O3 + KOH → NO + K2HPO4+ H2O

Перед азотом и фосфором коэффициенты не нужны, но чтобы уравнять фосфор перед гидрофосфатом калия поставим 2, тогда перед гидроксидом калия – 4, водорода в левой и правой части уравнения становится по 4, а кислород при этом не уравнивается (в левой части 9, в правой – 10):
NO2 + P2O3 + 4KOH → NO + 2K2HPO4+ H2O
Удвоим фосфор в электронном балансе:
 |  |
Тогда перед азотом в левой и правой части уравнения ставим 2, чтобы уравнять фосфор перед гидрофосфатом калия поставим 2, тогда перед гидроксидом калия – 4, водорода в левой и правой части уравнения становится по 4, а кислород при этом уравнивается (в левой и правой части по 11):
2NO2 + P2O3 + 4KOH = 2NO + 2K2HPO4+ H2O
Расстановка коэффициентов методом электронного баланса, если в уравнении более 2 элементов меняют степени окисления.
As2S3 + HNO3 ® H3AsO4 + SO2 + NO2 + H2O
В этом уравнении 2 восстановителя (мышьяк и сера) в составе одного вещества, поэтому в электронном балансе обязательно учитываются индексы из формулы исходного вещества, отданные восстановителями электроны суммируются:

3S–2 – 18e ® 3S+4 22 e 1 восстановители
N+5 +1e ® N+4 22 окислитель
Перед азотом в левой и правой части уравнения ставим 22, перед мышьяковой кислотой – 2, перед сернистым газом – 3, уравниваем водород и проверяем правильность расстановки коэффициентов по кислороду.
As2S3 + 22HNO3 = 2H3AsO4 + 3SO2 + 22NO2 + 8H2O
Можно использовать и такую запись поведения восстановителя:
Слева записано электронейтральное вещество, справа считаем сумму зарядов.
В рассмотренном примере степени окисления серы и мышьяка очевидны. Однако, встречаются вещества нестехиометрического состава, в которых определить степень окисления элементов затруднительно. Например, цементит Fe3C.
Fe3C + HNO3 ® Fe(NO3)3 + CO2 + NO2 + H2O
Чтобы не выяснять, какие в этом веществе степени окисления у элементов, воспользуемся выше приведенным приёмом:

Коэффициент 13 ставим перед оксидом азота, перед нитратом железа – 3, перед цементитом и углекислым газом коэффициенты не нужны. Пересчитываем азот в правой части (22), ставим 22 перед формулой азотной кислоты, уравниваем водород, проводим проверку по кислороду:
Fe3C + 22HNO3 ® 3Fe(NO3)3 + CO2 + 13NO2 + 11H2O
В случаях, когда 2 восстановителя находятся в составе одного вещества, элементам можно присваивать даже нереальные степени окисления, при этом будут получаться те же коэффициенты. Например, предположим, что углерод в цементите имеет степень окисления – 4, тогда степень окисления железа +4/3. Составим баланс с этими значениями:

Можно присвоить элементам такие степени окисления, чтобы степень окисления изменялась только у одного элемента. Пусть степень окисления железа +3 в исходном веществе и продукте, тогда степень окисления углерода в цементите – 9 (такого не бывает, но в данном случае мы весьма формально используем степень окисления).
Опять восстановитель отдал 13 электронов.
ЗАДАНИЕ 2. Расставьте коэффициенты методом электронного баланса в следующих схемах реакций:
1) Na + HNO3 ® NaNO3 + N2O + H2O
2) K2FeO4 + H2SO4 ® Fe2(SO4)3 + K2SO4 + H2O + O2
3) H2O2 + KMnO4 + HNO3 ® Mn(NO3)2 + KNO3 + H2O + O2
4) Ti2(SO4)3 + KClO3 + H2O ® TiOSO4 + KCl + H2SO4
5) Mn3O4 + KClO3 + K2CO3 ® K2MnO4 + KCl + CO2
6) Na2S4O6 + KMnO4 + HNO3 ®Na2SO4 + H2SO4 + Mn(NO3)2 + KNO3 + H2O
7) Cu2S + O2 + CaCO3 ® CuO + CaSO3 + CO2
8) FeCl2 + KMnO4 + HCl ® FeCl3 + Cl2 + MnCl2 + KCl + H2O
9) CuFeS2 + HNO3 ®Cu(NO3)2 + Fe(NO3)3 + H2SO4 + NO + H2O
10)KSCN + K2Cr2O7 + H2SO4 → Cr2(SO4)3 + K2SO4 + CO2+ NO2 + SO2 + H2O
Ответы (с указанием фамилии) оформляются в файле WORD, имя файла Familija—Z-1. (Familija— фамилия участника – англ.) Работы, выполненные в WORDe, отправляются электронной почтой на адрес *****@***ru, с обязательным указанием в Теме письма слов «дистанционное обучение» с указанием номера задания ( Z1 ) и фамилии (Например: Дистанционное обучение, Z1, ).
В самом письме можно ничего не писать, а файл с заданием нужно прикрепить к этому письму.
Можно присылать отсканированные варианты решения
Контрольный срок выполнения задания №1 до 21-00 мск вр, 04.06.11.