учебно-методический материал по химии (8 класс) на тему
Химический диктант «Первоначальные химические понятия и законы» предназначен для учащихся 8 класса для проверки уровня усвоения теоретических знаний в области основ общей химии. Диктант включает все основные понятия и определения, изучаемые в первый год обучения химии и может применятся учителем как полностью после изучения курса химии в 8 классе, так и фрагментарно в течение года.
Скачать:
| Вложение | Размер |
|---|---|
| 8_klass_pervonachalnye_khimicheskie_ponyatiya.docx | 17.18 КБ |
Предварительный просмотр:
8 класс Первоначальные химические понятия
Химия – наука о веществах, составе и свойствах веществ, а также превращениях между ними.
Вещество — материя, из которой состоит физическое тело.
Химический элемент –определенный вид атомов, имеющих одинаковый размер, массу и свойства.
Атом- наименьшая частица вещества, являющаяся носителем его свойств.
Молекула – частица, образованная из двух или большего числа атомов и способная к самостоятельному существованию.
Простое вещество — вещество, состоящее из атомов одного химического элемента.
Сложное вещество — вещество, состоящее из атомов разных химических элементов.
Относительная атомная масса (Ar) — величина, которая показывает, во сколько раз масса атома химического элемента больше атомной единицы массы (1/12 массы атома углерода).
Относительная молекулярная масса(Mr) – величина, которая показывает, во сколько раз масса молекулы больше атомной единицы массы (1/12 массы атома углерода).
Ион — это положительно или отрицательно заряженная частица, образованная из атома химического элемента в результате отдачи или присоединения электронов. Положительно заряженный ион- катион , отрицательно заряженный ион – анион.
Химическая связь — такое взаимодействие между атомами, которое связывает их в молекулы, ионы, кристаллы.
- Ионная связь — связь, возникающая между ионами. (за счет перехода электронов от атома металла к атому неметалла):NaCl, CaBr 2 , K 2 O и др.
- Ковалентная неполярная связь — связь, возникающая между атомами одного и того же химического элемента – неметалла (О 2 , N 2 , Cl 2, Br 2 , O 3 и т.п.)
- Ковалентная полярная связь — связь, возникающая между атомами разных неметаллов (СО 2 , H 2 O, NH 3 ).
- Металлическая связь — связь, возникающая между атомами и ионами металлов за счет обобществленных электронов (Сu, Al, Na, K и др.).
Электроотрицательность — способность атома химического элемента притягивать к себе общие электронные пары от атомов других химических элементов.
Степень окисления – условный заряд атомов химического элемента в соединении, вычисленный на основе предположения, что соединения состоят только из ионов.
— простые (металлы и неметаллы)
— сложные (оксиды, основания, кислоты, соли).
- Оксиды — сложные вещества, состоящие из двух химических элементов, один из которых кислород со степенью окисления -2. ( Э х О у -2 )
- Основания — сложные вещества, состоящие из катионов металла и гидроксид-ионов ОН. (Me +x (OH) x )
- Кислоты — сложные вещества, состоящие из катионов водорода Н + и анионов кислотных остатков.
- Соли — сложные вещества, состоящие из катионов металла и анионов кислотных остатков.
Моль — такое количество вещества, в котором содержится 6∙10 23 частиц этого вещества (атомов, молекул или ионов)
Молярная масса(M)- масса 1 моль вещества, численно равна относительной молекулярной массе, но в отличие от нее имеет единицы измерения. [M]=[г/моль].
Молярный объем (Vm)- объем газа количеством вещества 1 моль, измеренный при нормальных условиях ( t= 0 o C или 273К, р=101,3 кПа, 1 атм или 760мм рт. ст.). Vm= 22,4 л/моль
Химическая реакция — явление, в результате которого из одних веществ образуются другие вещества, при этом изменяется состав и свойства веществ.
- Реакции разложения — реакции, в результате которых из одного сложного вещества образуются нескольно простых или сложных веществ( АВ= А+В)
- Реакции соединения — реакции, в результате которых из нескольких простых или сложных веществ образуется одно сложное. (А+В=АВ).
- Реакции замещения – реакции, в результате которых атомы простого вещества замещают один или несколько атомов в сложного вещества ( А +ВС= А С +В)
- Реакции обмена — реакции, в результате которых атомы сложных веществ обмениваются своими составными частями ( А В+ C D= A D + C B)
Физические явления — явления, при которых могут изменяться размеры, форма тел и агрегатное состояние веществ, при этом состав их остается постоянным.
Химическое уравнение – условная запись химической реакции с помощью химических формул и математических знаков.
Закон сохранения массы веществ (1748г М.В. Ломоносов, 1789г А.Лавуазье): масса веществ , вступивших в химическую реакцию, равна массе образовавшихся веществ.
Закон постоянства состава (1808г Ж. Пруст)- вещества молекулярного строения имеют постоянный количественный и качественный состав, не зависящий от способа их получения.
Периодический закон (1861 г Д.И.Менделеев ) –свойства химических элементов и их соединений находятся в периодической зависимости от зарядов ядер их атомов.
Химический диктант для учащихся 8 класса
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
«Актуальность создания школьных служб примирения/медиации в образовательных организациях»
Свидетельство и скидка на обучение каждому участнику
Химический диктант 8 класс 1 вариант
1. Что означает запись: 3Н 2 , 2 Fe , CuO , 5С, H 2 SO 4 , 2 KNO 3
2. Напишите формулы : метана, углекислого газа, оксида меди, сульфида железа, соляной кислоты, хлорида натрия, нитрата серебра ___________________________________________________________________________________________________________________________________________________
3. Рассчитайте молекулярную массу веществ: сульфида цинка, серной кислоты, поваренной соли ___________________________________________________________________________________________________________________________________________________
4. Составьте формулы соединений с кислородом азота ( II ), фосфора ( III ), меди ( I ), хрома ( VI ), калия, магния ___________________________________________________________________________________________________________________________________________________
5. Закончите предложение : химическая формула — это ________________________________________________;
Химический диктант 8 класс 2 вариант
2. Напишите формулы : воды, угарного газа, оксида цинка, сульфида алюминия, серной кислоты, хлорида калия, нитрата натрия ___________________________________________________________________________________________________________________________________________________
3. Рассчитайте молекулярную массу в еществ: сульфида железа( II ), азотной кислоты, углекислого газа ___________________________________________________________________________________________________________________________________________________
4. Составьте формулы соединений с кислородом бора ( III ), фосфора ( V ), меди ( II ), хрома ( II ), натрия, кальция ___________________________________________________________________________________________________________________________________________________
5. Закончите предложение : химическая реакция — это _________________________________________________;
Химический диктант для 8 класса
Химический диктант для 8 класса
Поставьте плюсики, если утверждение верно
- Основания – это сложные вещества, состоящие из атомов металла и гидроксильных групп.
- Кислоты – это сложные вещества, состоящие из двух элементов одним из которых является кислород.
- Соль – это сложное вещество, состоящее из атомов металла и кислотного остатка.
- Оксид – это сложное вещество, состоящее из двух элементов, один из которых водород.
- K3PO4 – растворимая кислота;
- P2O5 – кислотный оксид;
- AgCl – нерастворимая соль;
- HNO3 – азотистая кислота;
- Mg – неметалл;
- H2CO3 – кислота образует соли карбонаты;
- Гидроксид железа (lll) — Fe(OH)2
- Щелочь – нерастворимое основание;
- Na2SO 4 – сульфит натрия;
- Li3PO4 – фосфат лития;
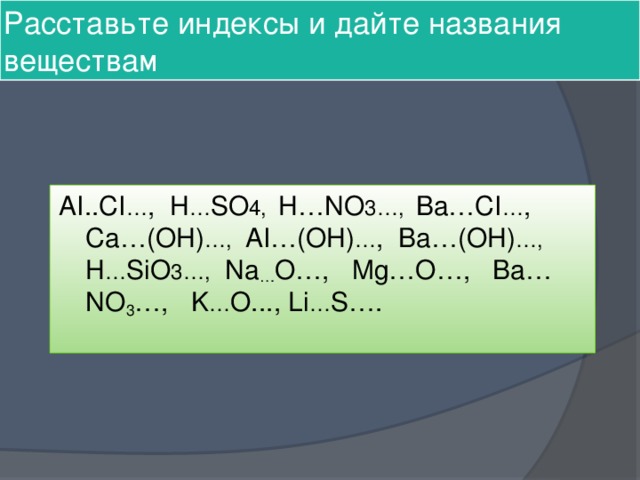
Расставьте индексы и дайте названия веществам
AI.CI…, H…SO4, H…NO3…, Ba…CI…, Ca…(OH)…, AI…(OH)…, Ba…(OH)…, H…SiO3…, Na…O…, Mg…O…, Ba…NO3…, K…O., Li…S….
Допишите название или формулу
- Серная кислота — …;
- Силикат натрия — …;
- H2SO3 — ;
- BaCI2 — …;
- Оксид цинка — …;
(I вариант) основные оксиды
(ii вариант) кислотные оксиды
CO2, P2O5, CaO
MgO, BaO, K2O
Подпишите растворимо или нерастворимо основание
Просмотр содержимого презентации
«Химический диктант для 8 класса »
Химический диктант для 8 класса
Классы неорганических соединений
Поставьте плюсики, если утверждение верно
- Основания – это сложные вещества, состоящие из атомов металла и гидроксильных групп.
- Кислоты – это сложные вещества, состоящие из двух элементов одним из которых является кислород.
- Соль – это сложное вещество, состоящее из атомов металла и кислотного остатка.
- Оксид – это сложное вещество, состоящее из двух элементов, один из которых водород.
- K 3 PO 4 – растворимая кислота;
- P 2 O 5 – кислотный оксид;
- AgCl – нерастворимая соль;
- HNO 3 – азотистая кислота;
- Mg – неметалл;
- H 2 CO 3 – кислота образует соли карбонаты;
- Гидроксид железа (lll) — Fe(OH) 2
- Щелочь – нерастворимое основание;
- Na 2 SO 4 – сульфит натрия;
- Li 3 PO 4 – фосфат лития;
Расставьте индексы и дайте названия веществам
AI..CI … , H … SO 4, H…NO 3…, Ba…CI … , Ca…(OH) …, AI…(OH) … , Ba…(OH) …, H … SiO 3…, Na … O…, Mg…O…, Ba…NO 3 …, K … O. Li … S….
Допишите название или формулу
- Серная кислота — …;
- Силикат натрия — …;
- H 2 SO 3 — ;
- BaCI 2 — …;
- Оксид цинка — …;
Выберите (I вариант) основные оксиды (ii вариант) кислотные оксиды и назовите их
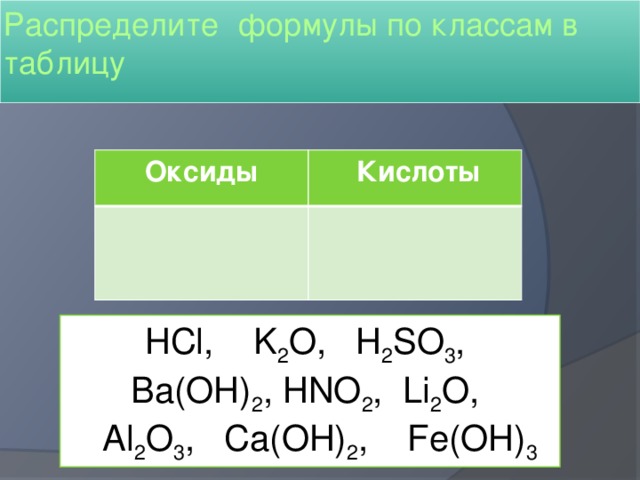
Распределите формулы по классам в таблицу
HCl, K 2 O, H 2 SO 3 ,
Ba(OH) 2 , HNO 2 , Li 2 O,
Al 2 O 3 , Са(OH) 2 , Fe(OH) 3
Распределите формулы кислот
HNO 3 , H 2 SO 3 ,
H 2 SO 4 , H 3 PO 4
Подпишите растворимо или нерастворимо основание