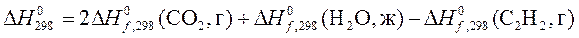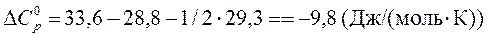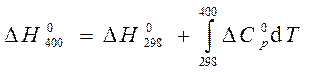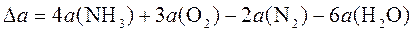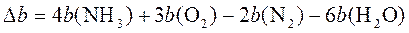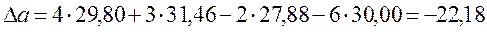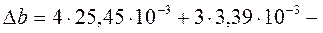ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ. ПРОЦЕССЫ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ И ПРИ ПОСТОЯННОМ
ОБЪЕМЕ
Пример 1. Рассчитайте разницу между тепловыми эффектами при постоянном давлении и постоянном объеме (Qp — Qv ) реакции
С2 H4 0(г) + H2 (г) =C2 Н5 0Н(Ж) , протекающей при 298 К. Чему равна эта разница, если температуру повысить до 400 К и спирт перевести в газообразное состояние?
Решение. 1-й закон термодинамики можно выразить уравнением
где ΔU — изменение внутренней энергии системы (U2-U1) при переходе системы из состояния «1» в состояние “2″; Q — теплота; Aмех — работа механическая, равная рΔV, где р — давление, а ΔV- изменение объема (V2-V1).
Тепловой эффект процесса, протекающего при р=const
Qp= ΔH = ΔU+pΔ , (1.1.2)
ΔH — изменение энтальпии.
Тепловой эффект процесса, протекающего при р = const
где R — газовая постоянная = 8,3144 Дж/моль *К; Δn=n2-n1 ;
n1 и n2 — количество молей реагентов и продуктов реакции газообразных веществ; T — температура, К.
Отсюда: 1) при 298 К Qр — Qv = ΔnRT = (0-2) 8,3144-298 = -4955,38 Дж;
2) при 400 К и газообразном С2Н5ОН Qp – Qv = (1-2) 8,3144-400 = -3325,76 Дж.
Ответ при 298 К Qp-Qv = -4955,38 Дж;
Пример 2. Определить стандартную энтальпию образования
ацетилена по энергиям связей отдельных его атомов:
Решение. Стандартная энтальпия (теплота) образованиям Δ H о обр — тепло, поглощенное или выделенное в процессе синтеза 1 моля соединения из простых веществ при условии, что все компоненты системы находятся в стандартных состояниях.
Верхний индекс Δ H о здесь и в последующих случаях Δ G о, Δ S о, Δ F о обозначает, что реагирующие вещества находятся в своих стандартных состояниях. Стандартное состояние для газов — это состояние идеального газа при давлении 1 атм (101330 Па) и определенной температуре. Для жидкости — это состояние чистой жидкости, а для твердых веществ — это кристаллическое состояние при тех же условиях. Строго говоря, температура должна быть точно указана в виде индекса.
Например, Δ H о 273 , однако, если не оговорено, то стандартное состояние относится к 298 К. Образование молекулы ацетилена Н – С ≡С- Н сопровождается образованием двух связей Н — С (358,2 кДж/моль) и одной связи С ≡ С (536 кДж/моль); разрушением связи H – H (430 кДж/моль) и переходом 2C(rp) → 2-С(г) (525 кДж/моль).
Образование связи сопровождается выделением энергии, разрушение — поглощением.
1.Вычислить разность между Qp и Qv при 298 К для реакции полного сгорания бензола С6Н6, нафталина С10 Н8 и этилена C2H4 с образованием диоксида углерода и воды в жидком состоянии.
2. Найти разность между Qp и Qv при 298 К для следующих реакций:
3. Тепловой эффект реакции 1/2 N2(r)+3/2 H2(г) ⇄NH3(г) при постоянном давлении, при температуре 298 К Qp = Δ H= = -46,26 кДж/моль.
Определить Qv для этой реакции при этой же температуре.
4. Тепловой эффект изобарного процесса, протекающего по реакции
2Fe(кр)+3/2 О2(г)=Fe2O3 (кр) , при 291 К равен -82З,З кДж/моль. Определить тепловой эффект для изохорного процесса, протекающего по этой реакции при той же температуре.
6. Энергия диссоциации H2 , Cl2 и стандартная энтальпия образования HCl соответственно составляют 436,243 и -92 кДж/моль. Вычислить энергию связи H-Cl .
7. Рассчитайте тепловой эффект сгорания метилацетата по энергиям связей при 298 К. Реакция сгорания метилацетата протекает по уравнению
Структурная формула метилацетата
8. Рассчитать стандартную энтальпию образования этилена
получаемого по уравнению
2C(гр) + 2H2(г)— C2H4(г) ; ΔH
по величинам энергии связей. Сравнить полученный результат с табличным (см. табл. 1).
9. Вычислить стандартную энтальпию образования H — бутана
H H H H
по энергиям связей.
Уравнение образования бутана
10. Вычислить стандартную энтальпию образования метанола по величинам энергий связи
Сравнить полученную величину с табличным значением (см. табл. З).
11. Рассчитайте тепловой эффект (ΔH° ) дегидратации этилового спирта по уравнению реакции
H — C— C — OH(ж) → C = C + H — O — H ; ΔH°
Энергии соответствующих связей взять в табл. 1, теплоты испарения спирта
и воды — в табл. 2.
12. Рассчитать тепловой эффект ( ΔH° ) сгорания этилацетата
по энергиям разрыва связей при 298 К. (Энергию связей см. в табл. 1, теплоту испарения этилацетата и H2 O — в табл. 2).
1.2. ЗАКОН ГЕССА. РАСЧЕТ ТЕПЛОПРОИЗВОДИТЕЛЬНОСТИ ТОПЛИВА. ЗАВИСИМОСТЬ ТЕПЛОВОГО ЭФФЕКТА РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ. УРАВНЕНИЕ КИРХГОФА
Пример 1. Определить при 298 К тепловой эффект (ΔH°) реакции
Решение. Если ΔH реакции > О — реакция эндотермическая, идет с поглощением тепла; если ΔH реакции о обр продуктов реакции и реагентов с учетом их стехиометрических коэффициентов νj, νi) :
Из табл. 3 выпишем значения стандартных энтальпий образования:
Тепловой эффект реакции находим по (1.2.1):
= -3439,0+1672+3*395,7 = -580,8 кДж
Пример 2. Определить тепловой эффект ΔΗ° реакции этерификации щавелевой кислоты метиловым спиртом, протекающей по уравнению
если стандартные энтальпии сгорания (см. табл. 5)
ΔH o cгop (СН3ОН) = -727,59 кДж/моль;
Решение. По следствию из закона Гесса имеем: тепловой эффект реакции равен разности между суммой энтальпий сгорания реагентов и суммой энтальпий сгорания конечных продуктов с учетом их стехиометрических коэффициентов:
Энтальпия сгорания Н20 (а также CO2 ) равны нулю.
Ответ. ΔH o = -26,79 кДж.
Пример 3. Определить стандартную энтальпию образования (Δ H о 298 обр) этилена, если тепловой эффект реакции горения этилена равен — 1412,99 кДж/моль, а стандартные энтальпии образования (Δ H о 298 обр) CО2 и H2O(ж) равны соответственно — 394,07 и — 286,26 кДж/моль.
Решение. Горение этилена происходит по реакции
ΔΗ = -1412,99 кДж/моль
По следствию из закона Гесса (1.2.1):
Δ H о =2Δ H о 298 Н2О + 2Δ H о 298 СО2 — Δ H о 298 С2Н4 — Δ H о 298 О2
Стандартные энтальпии образования простых веществ равны нулю, отсюда Δ H о 298 О2= 0. Тогда
Пример 4. Рассчитать теплотворную способность метана. Реакция горения метана протекает по уравнению
ΔH o cгop метана равна -891,63 кДж/моль.
Решение. Теплотворной способностью топлива называется количество тепла, выделяющееся при сгорании одного килограмма топлива (топливо состоит из горючего и окислителя).
По формуле (1.2.2) имеем
Поэтому ΔΗ 0 = ΔH o cгop CH4 = -891,632 кДж/моль. Это количество тепла выделяется при сгорании 80 г топлива (вес 1-го моля метана и 2-х молей кислорода). Следовательно, теплотворная способность метана
Ответ. т.С. метана равна 1114,54 кДж/кг.
Пример 5. Определить тепловой эффект реакции
Решение. Зависимость теплового эффекта реакции от температуры выражается уравнением Кирхгофа (если в данном процессе отсутствуют фазовые превращения)
ΔΗΤ = ΔΗ 0 Т0 + 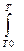
где ΔС°р -разность сумм молярных изобарных теплоемкостей продуктов реакций и реагентов с учетом их стехиометрических коэффициентов. Приняв, что ΔС°р не зависит от температуры в данном температурном интервале(T0 до T), уравнение (1.2.3) запишем в виде
Для решения этого уравнения необходимо знать тепловой эффект реакции при какой-либо температуре Т0. Удобно воспользоваться тепловым эффектом, вычисленным по закону Гесса- при Т0=298 К. Стандартные энтальпии образования компонентов берем из табл. 3. По формуле (1.2.1)
Далее находим ΔС°рпо табличным значениям Ср (табл.4):
= 16,31·10 — 3 кДж/моль*К, отсюда по формуле (1.2.4)
δΗ°500 = -676,4+16,31·10 — 3 (500-298) = -676,4 + 3,29 = -673,11 кДж.
13. Вычислить тепловой эффект реакции дегидрирования этана
Расчет произвести по стандартным энтальпиям сгорания компонентов табл. 5 и по стандартным энтальпиям образования табл. 3. Ответы сравнить.
14. Опpедeлить теплоту cгopания фocфopиcтогo водорода
Cтандapтныe энтальпии образования компонентов взять в табл. 3.
15. Опpедeлить тепловой эффект peaкции:
16. При cοединении 2,1 г железа c ceρой выдeлилocь
3,77 кДж. Pаccчитать cтандаpтнyю энтальпию oбpазoвания сульфида железа.
17. Найти кoличecтво теплоты, выделяющейся при взрыве
8,4 л гpeмучeгo газа, взятого при ноpмaльныx ycлoвияx.
18. Определить cтандаρтнyю энтальпию (Δ H о 298 ) обpазoвания
РH3 , иcxoдя из ypавнения
19. Cpавнить Δ H о 298 peакций воccтановления оксида железа (III) различными вoccтановителями при 298 K:
20. Bычиcлить Δ H о 298 обpaзования MgCO3(кр) при 298 K, пользуясь cледyющими данными:
2 . Bычиcлить Δ H298 pеaкций :
Cтандаpтные энтальпии обpазοвания Li + (водн), Na + (водн) и OH — (водн) принять cooтвeтcтвeннo paвными — 278,5: -239 и 228,9 кДж/моль.
22. Bычиcлить, какое кoличеcтвo тепла выделяeтcя при протекающих в opганизмe pеакциях пpевpaщения глюкозы:
Какая из этих реакций πocтавляeт оpганизмy больше энергии?
23. Cтандаpтная теплота oбpазoвания жидкого бензола при
298 K paвнa 82,9 кДж/моль. Haпишитe ypaвнение peaкции, к
котopой отноcитcя этот тепловой эффект.
24. Сколько тепла выдeлитcя при вoccтанoвлeнии 8г окиси
меди водородом c oбpазoванием жидкой воды?
25. Реакция oбpазoвания xлopиcтoгo водоpодa из xлоpа и
водорода выpажаeтcя ypавнeниeм:
Cкoлькo тепла выдeлитcя при coeдинeнии 1 литра xлopа c
водородом?
26. Oпpeдeлить тeплотвоpнyю cпоcобноcть этилена. Реакция
гоpeния этилена выpажаeтcя уравнением:
27. Определить теплотвоpнyю cпocoбнocть этана. Реакция
горения этана:
28. Рассчитать тeплoтвopнyю cпоcобноcть ацетилена. Реакция горения ацетилена:
29. Οпpeдeлить тепловой эффект реакции:
30. Οпpеделить тепловой эффект реакции:
31. Οпpeдeлить тепловой эффект peакции:
32. Οпpeдeлить тепловой эффект реакции:
ЗЗ. Οпредeлить тепловой эффект реакции oбpазoвания хлориcтoгo водopoда из xлopа и вoдopoдa при 800 K.
34. Реакция получения водяного газа H2+CO идет по уравнению
Вычислите тепловой эффект ΔH o реакции. Найдите, сколько поглощается тепла при образовании 1000 л водяного газа (н.у.).
35. Исходя из ΔH o 298 образования H2O(г) (-241,8 кДж/моль)
и следующих данных:
вычислить Δ H о 298 реакции
36. Найти массу метана, при полном сгорании которой с образованием жидкой воды выделяется теплота, достаточная для нагревания 100 г воды от 293 K до 303 K. Мольную теплоемкость воды принять равной 75,3 Дж/моль*К.
37. Рассчитайте тепловой эффект ΔHo реакции
2Cl2 + 2H2O=4HCl + O2 ,
протекающей при 798 K, считая, что теплоемкости вcex веществ — участников реакции — в интервале 298 — 798K остаются постоянными.
38. Укажите, как изменится (увеличится, уменьшится или останется неизменным тепловой эффект реакции СО +2Н2= СН3ОН(г) при изменении температуры от 298 K до 1ООО K при
P=const.
1.3. ВТОРОЙ 3AKОH ТЕРМОДИНАМИКИ. ЭНТРОПИЯ.
ЭНЕРГИИ ГИББСА И ГЕЛЬМГОЛЬЦА. КРИТЕРИЙ
САМОПРОИ3ВОЛЬНОГО ПРОТЕКАНИЯ ПРОЦЕССА
Пример 1. Один моль кислорода расширяется до десятикратного увеличения объема и одновременно охлаждается от 400К до 300К. Чему равно изменение энтропии, если для заданного
температурного интервала мольная изобарная теплоемкость кислорода C = 29,2 Дж/моль*К (Ср считаем в данном интервале температур постоянной).
Решение. Общее изменение энтропии ΔS будет складываться из изменения энтропии газа ΔS1 при его расширении и изменения энтропии газа ΔS2 при изменении температуры:
ΔS1= R ln 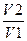
где R — газовая постоянная; V1 и V2 — соответственно конечный и начальный объемы газа. .Находим по формуле (1.3.1)
ΔS1= 8,31*ln10=19,1 Дж/моль*K.
ΔS2 =Cp*ln 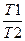
где С — мольная изобарная теплоемкость О2; Т2 и Т1 — конечная и начальная температуры.
Отсюда
ΔS2 = 29,2·1n 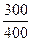
Ответ. ΔS = 11,05 Дж/моль*К.
Пример 2. При охлаждении 12 л кислорода от 473 до 233 K одновременно повышается давление от 10 5 до 6·10 6 . Рассчитать изменение энтропии, если мольная изобарная теплоемкость кислорода Ср = 29,2 Дж/моль*К (газ считать идеальным).
Решение. Рассчитаем число молей кислорода из уравнения состояния идеального газа
pV= nRT ; n= 
Общее изменение энтропии ΔS будет складываться из изменения энтропии ΔS1 при увеличении давления и изменения энтропии ΔS2 при охлаждении газа
ΔS1 =R ln 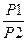
где Ρ1 и Ρ2 — исходное и конечное давления; R — газовая постоянная.
ΔS2 находим по формуле (1.3.2).
Отсюда
ΔS = R ln 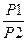
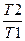
Так как у нас участвует 0,3052 молей кислорода, то
ΔS =0,3052(8,31*ln(10 5 /(6*10 6 )) + 29,2*ln(233/437))=-16,77 Дж/моль*К.
(энтропия уменьшается при охлаждении газа).
Ответ. ΔS = —16,77 Дж/моль*К.
Пример 3. Определить изменение энтропии ΔS при нагревании 30 г ледяной уксусной кислоты (СН3 СООН) от температуры плавления до 333 K. Τпл уксусной кислоты 289,6 K. Теплота
плавления ΔΗпл= 194 Дж/г, удельная теплоемкость уксусной кислоты равна 2,19 Дж/г*К.
Решение. Общее изменение энтропии Δ S Равно сумме изменения энтропии при плавлении уксусной кислоты Δ S1 и при нагревании жидкой уксусной кислоты от Τпл до заданной температуры (333 К) Δ S2
1 моль СН3СООН= 60 г.
По формуле (1.3.4) находим Δ S1=194*30/289,6*60=20,1 Дж/К
Δ S2 рассчитываем по формуле (1.3.2):
Δ S = Δ S1 + Δ S2= 20,1+9,2=29,3 Дж/К.
Ответ: Δ S = 29,3 Дж/К.
Пример 4. Определить изменение энтропии ΔS о и энергии Гиббса ΔG о при стандартных условиях для системы
Fe3О4 + CO = 3FeO + CO2
и решить вопрос о возможности самопроизвольного протекания ее при указанных условиях.
Решение. Значения ΔS о и ΔG о Для реакции определяем по следствию из закона Гесса (2.2.1). Стандартные энтропии S°298 и энергии Гиббса ΔG о 298 компонентов берем из табл.3.
Следовательно,
продукты реагенты
продукты реагенты
ΔG о = ∑ νj ΔG о 298 — ∑νi ΔG о 298. (1.3.6)
Если ΔG 0 процесс не идет. В данном случае ΔG > 0, следовательно, процесс самопроизвольно не пойдет.
Ответ. ΔS° = 39,11 Дж; ΔG о = 14,51 кДж, реакция самопроизвольно не пойдет.
Пример 5. Вычислить стандартное значение изменения свободной энергии ΔG о реакции: C2H2+5/2 О2 = 2 CО2 + Н2О (ж); ΔG о ,
По табличным данным -S о 298 и ΔΗ о 298 для компонентов (табл. 3).
Решение. Определяем тепловой эффект и изменение энтропии реакции по закону Гесса (формулы (1.2.1) и (1.3.5)).
ΔS°= S о 298 H2O + 2S о 298 CO2 — S о 298 C2H2 – 5/2S о 298 O2 =
= 70+2213,6-200,8-2,5*205= -216,2 Дж/моль*К;
ΔS°= -0,2162 кДж/моль*К.
Изменение изобарно-изотермического потенциала находим по формуле
Дата добавления: 2016-03-27 ; просмотров: 11148 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Зависимость теплового эффекта реакции: H2 + ½ O2 = H2O от температуры выражается уравнением: DH= -237,65*103-13,01Т+ 2,88*10-3Т2 – 1,71*105/Т






Чтобы получить решение , напишите мне в WhatsApp , оплатите, и я Вам вышлю файлы.
Кстати, если эта работа не по вашей теме или не по вашим данным , не расстраивайтесь, напишите мне в WhatsApp и закажите у меня новую работу , я смогу выполнить её в срок 1-3 дня!
Описание и исходные данные задания, 50% решения + фотография:
Зависимость теплового эффекта реакции: H2 + ½ O2 = H2O от температуры выражается уравнением:
D H = -237,65*10 3 -13,01Т+ 2,88*10 -3 Т2 – 1,71*10 5 /Т
Рассчитать изменение теплоемкости ΔСр и ΔСv для этой реакции при 800К
Решение:
| Если вам нужно решить химию, тогда нажмите ➔ помощь по химии. |
| Похожие готовые решения: |
- Вычислить тепловой эффект реакции при стандартных условиях Fe2O3 + 3CO = 2Fe + 3CO2 + ΔH Если теплоты образования Fe2O3 = -821.3 кДж/моль
- Определить изменение изобарно-изотермического потенциала при стандартных условиях для реакции: 2Hl + Ca = CaCl2 + H2 Если DGo для Hl = -94.9
- Рассчитать теплоту образования сульфата цинка из простых веществ при Т=298 на основании следующих данных: ZnS = Zn + S DH1= 200.5 кДж/моль
- Стандартная энтальпия образования Al2O3(тв) при 298К равна -1675 кДж/моль. Рассчитать стандартную энтальпию образования Al2O3(тв) при 800К
Присылайте задания в любое время дня и ночи в ➔
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Все авторские права на размещённые материалы сохранены за правообладателями этих материалов. Любое коммерческое и/или иное использование кроме предварительного ознакомления материалов сайта natalibrilenova.ru запрещено. Публикация и распространение размещённых материалов не преследует за собой коммерческой и/или любой другой выгоды.
Сайт предназначен для облегчения образовательного путешествия студентам очникам и заочникам по вопросам обучения . Наталья Брильёнова не предлагает и не оказывает товары и услуги.
Примеры решения типовых задач.
1. Рассчитать, пользуясь таблицей термодинамических свойства простых веществ и соединений (Приложение 9), тепловой эффект химической реакции
при р = 1 атм, Т = 298 К. Все реагенты и продукты – газы.
2.Рассчитать, пользуясь таблицей термодинамических величин, стандартное изменение энтальпии 
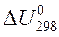
3.При сгорании 1 моль С2Н2 в кислороде
выделилось 1299,60 кДж теплоты. Рассчитать, пользуясь таблицей термодинамических данных, теплоту образования ацетилена 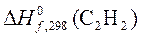

4.При стандартных условиях теплота полного сгорания белого фосфора 760,1 кДж/моль, а теплота полного сгорания черного фосфора 722,1 кДж/моль. Найти теплоту превращения черного фосфора в белый.
По закону Гесса:
5.Теплоемкости Н2, О2 и Н2О (все вещества – газы) равны 28,8; 29,3; 33,6 Дж/(моль×К) соответственно в диапазоне температур от 25°С до 100°С. При температуре 25°С известно изменение энтальпии в реакции
Н2 + 1 /2О2 = Н2О, 
Рассчитать тепловой эффект этой реакции при температуре 100°С.
Так как теплоемкости приняты постоянными, то
6.Рассчитать, пользуясь таблицей термодинамических данных, тепловой эффект реакции
при Т = 400 К (все вещества – газы).
Для расчета используем уравнение Кирхгофа (56)
Так как для всех веществ вид уравнения для теплоемкости 
и после интегрирования
При Т = 400 К тепловой эффект равен
Задачи для самостоятельного решения
1. Найти изменение теплоемкости 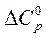
при 75°С, если средние мольные изобарные теплоемкости ацетилена и бензола при этой температуре соответственно равны 10,43 и 32,0 ккал/(моль×К).
2. Определить DU реакции СаСО3 = СаО + СО2 при 900°С, если DН при этой же температуре равно 42,560 ккал/моль.
(Ответ: 168,3 кДж/моль)
3. В стандартных условиях теплота сгорания Н2 в О2 равна 286,2 кДж/моль, а теплота сгорания Н2 в О3 равна 333,9 кДж/моль. Найти теплоту образования озона из кислорода.
(Ответ: 15,9 кДж/моль)
4. Даны уравнения химических реакций:
б) СаО(тв) + Н2О(ж) = Са 2+ (aq.) + 2ОН – (aq.),DН2 = – 19,5 ккал;
в) Са(тв) + 2Н2О(ж) = Са 2+ (aq.) + 2ОН – (aq.) + Н2(г),
Рассчитать тепловой эффект реакции
5. Рассчитайте, пользуясь справочными данными, сколько энергии надо затратить для разложения 9 г Н2О на простые вещества в стандартных условиях?
6. Рассчитайте, пользуясь справочными данными, на сколько увеличится энтальпия человека, потребившего продукт, содержащий 80 г углеводов, 25 г белков, 32 г жиров и какое количество теплоты выделится при сжигании таких же количеств указанных питательных веществ в калориметре?
(Ответ: 728,1 ккал; 768,1 ккал)
7. Рассчитайте, пользуясь справочными данными, стандартное значение энтальпии реакции окисления сероводорода в избытке кислорода и в недостатке кислорода при температуре 25°С.
(Ответ: –562,13 кДж/моль; –265,23 кДж/моль)
8. Рассчитать, пользуясь справочными данными, тепловой эффект реакции образования HCl(г)
9. Для реакции
зависимость теплового эффекта (Дж) от температуры выражается уравнением
DH = – 684710 + 36,77 T – 38,56×10 –3 T 2 + 8,21×10 –6 T 3 +
+ 2,88×10 5 / T
Рассчитать изменение теплоемкости 
Второе начало термодинамики. Энтропия
Основные уравнения
Второе начало термодинамики(С.Карно, 1824 г.) устанавливает критерий направленности термодинамических процессов Известно много формулировок второго закона термодинамики, которые эквивалентны друг другу.
Ø Р.Клаузиус (1850 г.): Теплота не может самопроизвольно переходить от более холодного тела к более горячему
или другая формулировка:
Ø В.Оствальд (1888 г.): Осуществление вечного двигателя второго рода невозможно
Аналитическое выражение второго начала термодинамики (неравенство Клаузиуса):
 , , | (60) |
где S – энтропия (введена Р.Клаузиусом); знак «=» относится к обратимым процессам, а знак «>» – к необратимым.
Для изолированных систем уравнение второго начала термодинамики упрощается:
 , , | (61) |
то есть энтропия изолированной системы в необратимых условиях может только возрастать, а в состоянии термодинамического равновесия она постоянна (достигает максимума).
В расчетах используют стандартную энтропию 
Расчет энтропии1 моль вещества при произвольной температуре и постоянном давлении, если в процессе нагревания не происходит изменения агрегатного состояния, производят по уравнению:
 , , | (62) |
а изменение энтропии в процессе нагревания 1 моль вещества от температуры T1 до температуры T2 без изменения агрегатного состояния при постоянном давлении по уравнению:
 . . | (63) |
Если теплоемкость не зависит от температуры, то уравнения (62) и (63) упрощаются:
 , , | (64) |
 . . | (65) |
Энтропию и изменение энтропии веществ при постоянном объеме рассчитывают по уравнениям, которые аналогичны уравнениям (62) – (65):
 , , | (66) |
 , , | (67) |
 , , | (68) |
 . . | (69) |
Изменение энтропии при фазовом переходе(плавление, кристаллизация, испарение, конденсация, возгонка) вычисляется по уравнению:
 . . | (70) |
Изменение энтропии в процессе изменения объемаn моль идеального газа от V1 до V2 (Т – const) равно:
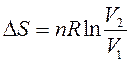 | (71) |
или, учитывая, что 
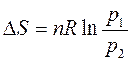 . . | (72) |
Изменение энтропии в химической реакциирассчитывают по формуле:
 , , | (73) |
где