Тепловой эффект E процесса – это сумма количества теплоты, которую отдала система Q ‘ в этом процессе, и теплового эквивалента работы A
, элемент которой равняется:
= δ A — p d V ( 1 ) , где δ A считается элементарной полной работой системы, p d V – работой расширения.
Тогда получим, что:
Разрешается записать в виде E = — Q с Q , обозначающей количество теплоты, подведенное к системе. Согласно первому началу термодинамики:
E = — ∆ U — ∫ 1 2 p d V ( 3 ) , где ∆ U = U 2 — U 1 является изменением внутренней энергии системы, p – давлением, V – объемом.
Тепловой эффект применяется в термохимии. Тепловым эффектом химической реакции считается количество тепла, выделяемое в ходе данной реакции. При выделении теплоты реакция получила название экзотермической, при поглощении – эндотермической. Считается, что уравнение экзотермической реакции характеризуется E > 0 , а эндотермической –
Допустим, имеется химическая реакция, протекающая при V = c o n s t . Это говорит о тепловом эффекте реакции E V , который необходимо рассчитывать по формуле:
E V = U 1 — U 2 ( 4 ) .
Если прохождение этой реакции обусловлено наличием постоянного давления, то выражение ( 3 ) с использованием тепловой функции запишется:
H = U + p V ( 5 ) , E = H 1 — H 2 + ∫ 1 2 V d p ( 6 ) , то случай говорит о наличии теплового эффекта реакции с p = c o n s t :
E p = H 1 — H 2 ( 7 ) .
По уравнениям ( 4 ) , ( 5 ) видно прохождение теплового эффекта при изохорном и изобарном процессах в не зависимости от ее хода реакции (промежуточных стадий). Он определяется начальным и конечным состоянием системы. Данная формулировка получила название закона Гесса – первого закона термохимии. При твердых или жидких начальных и конечных продуктах реакции значения E p и E V практически аналогичны. Это происходит по причине неизменности системы. Реакции, имеющие газообразные составляющие, в виду существенной переменности объема тепловые эффекты E p и E V значительно отличаются, а тепловой эффект рассматривается при постоянном давлении. Наличие заданной температуры теплового эффекта E p почти не зависит от внешнего давления, которое является постоянным для данного процесса. Тепловой эффект, который определяется при t = 25 ° C и p = 760 м м р т . с т . называют стандартным.
Из закона Гесса вытекают следствия, упрощающие расчет химических реакций, в системах с p = c o n s t или V = c o n s t :
- Тепловой эффект реакции разложения химического соединения численно равен и противоположен по знаку тепловому эффекту реакции синтеза этого соединения из продуктов разложения.
- Разность тепловых эффектов двух реакций, приводящих из разных состояний к одинаковым конечным состояниям, равняется тепловому эффекту реакции перехода из одного начального состояния в другое.
- Разность тепловых эффектов двух реакций, приводящих из одного исходного состояния к разным конечным состояниям, равна тепловому эффекту реакции перехода из одного конечного состояния в другое.
Закон Гесса позволяет использовать термохимические уравнения в качестве алгебраических. Зависимость количества теплоты, которая выделяется в реакции E от теплового эффекта реакции E o , и количества вещества n b одного из участников реакции( вещества b в качестве исходного вещества или продукта реакции), выражается при помощи уравнения:
E = n b v b E 0 ( 8 ) , где v b — является количеством вещества b , задаваемое коэффициентом перед формулой вещества b в химическом уравнении.
Уравнение Кирхгофа
Большинство термохимических данных в справочниках приведено при температуре 298 К . Чтобы рассчитать тепловые эффекты, обладающие другими температурами, применяют уравнения Кирхгофа. Они записываются для изохорного E V и изобарного E p тепловых эффектов. Дифференциальная форма приобретает вид:
∂ E V ∂ T V = ∂ U 1 ∂ T V — ∂ U 2 ∂ T V = C V 1 — C V 2 = — ∆ C v ( 9 ) , ∂ E p ∂ T p = ∂ H 1 ∂ T p — ∂ H 2 ∂ T p = C p 1 — C p 2 = — ∆ C p ( 10 ) .
В ( 10 ) , ( 9 ) имеется C V , C p , являющиеся теплоемкостями веществ при соответствующих процессах.
Уравнение Кирхгофа для энтальпии изображается в интегральной форме вида:
H T 2 = H T 1 + ∫ T 1 T 2 ∆ C p T d T ( 11 ) , где ∆ C p = ∑ i v j C p B j — ∑ v i C p A i i считается разностью изобарных теплоемкостей продуктов реакции и исходных веществ. Зачастую выражение ( 11 ) применяют в химии.
Примеры задач на вычислыние теплового эффекта
Записать выражение для расчета изменения стандартной энтальпии реакции.
Для решения задания необходимо взять за основу закон Гесса.
Именно он способствует оперированию термохимическими уравнениями как алгебраическими. Получаем, что запись принимает вид:
∆ H = ∑ j v j H B j — ∑ i v i H A i ( 1 . 1 ) , с B j , являющейся продуктами реакции, A i – исходными веществами. В задании требуют записать формулу для расчета стандартной энтальпии. Отметим, что все энтальпии, записанные уравнениями ( 1 . 1 ) , выбираются при температуре T = 298 К . Реже это фиксируется в самой формуле.
Даны химические уравнения. Произвести вычисление теплового эффекта реакции E образования 1 моль F e 2 O 3 при стандартных условиях из F e и O 2 .
1 . 2 F e + O 2 = 2 F e O , H 298 К , 1 = — 529 , 6 к Д ж ; 2 . 4 F e O + O 2 = 2 F e 2 O 3 , H ( 298 К , 2 ) = — 585 , 2 к Д ж .
По условию видно, что следует рассчитать тепловой эффект образования 1 моль оксида железа F e 2 O 3 реакции вида:
3 . 2 F e + 1 , 5 O 2 = F e 2 O 3 ( 2 . 1 ) .
Из двух данных реакций, следует сформировать реакцию ( 2 . 1 ) . Далее нужно разделить коэффициенты в ( 2 ) на 2 и произвести сложение с ( 1 ) . Отсюда:
2 F e + O 2 + 2 F e O + 0 , 5 O 2 = 2 F e O + F e 2 O 3 ( 2 . 2 ) .
Проведем преобразование (сокращение):
2 F e + 1 , 5 O 2 = F e 2 O 3 .
Было получено уравнение ( 2 . 1 ) :
Выше перечисленная последовательность действий с уравнениями привела к необходимому ( 2 . 1 ) . При проведении аналогичной схемы действий с тепловыми эффектами, будет результат эффекта реакции ( 2 . 1 ) . Протекание всех процессов обусловлено стандартными условиями, то есть при T = 298 К . Следовательно формула примет вид:
E 3 = H ( 1 ) + 0 , 5 H ( 2 ) ( 2 . 3 ) , где находящиеся в скобках цифры обозначают номер химической реакции. Рассчитаем и получим:
E 3 = — 529 , 6 + 0 , 5 · — 585 , 2 = — 822 , 2 ( к Д ж ) .
Ответ: тепловой эффект реакции равняется — 822 , 2 к Д ж .
Влияние температуры на тепловой эффект реакции. Уравнения Кирхгофа
Температура может оказывать существенное влияние на тепловой эффект химической реакции. Иногда значительное изменение температуры может изменять дажезнак теплового эффекта (переход от экзотермической реакции к эндотермической или от эндотермической к экзотермической).
Уравнение, характеризующее влияние температуры на тепловой эффект химической реакции, можно вывести следующим образом.
Пусть энтальпии исходных веществ и продуктов реакции в соответствии с реакцией (2 — 1) равны
исходных веществ продуктов реакции
Суммарная энтальпия исходных веществ выражается так:
а суммарная энтальпия продуктов реакции равна
Переход из исходного состояния в конечное, т.е. протекание реакции, приводит к изменению энтальпии
DH = H2 — H1 = Snj`HAj` — SniHAi , (2 — 6)
представляющему собой тепловой эффект реакции.
Дифференцируя равенство (2 — 6) по температуре при постоянном давлении, получим
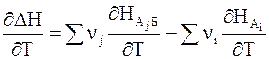
Напомним, что производная энтальпии вещества k по температуре является теплоемкостью при постоянном давлении
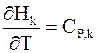
Поэтому равенство (2 — 7) приобретает следующий вид:

Уравнение ( 2 — 8), отражающее зависимость теплового эффекта от температуры, называется уравнением Кирхгофа в дифференциальной форме.
Еще один тип уравнения Кирхгофа в дифференциальной форме относится к реакциям, проводимым при постоянном объеме:
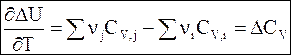
Интегрирование дифференциальных уравнений Кирхгофа в температурных пределах от Т1 до Т2 дает
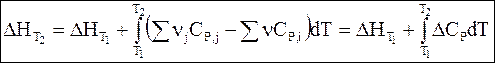
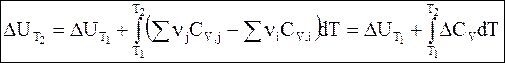
Обращаем внимание на то, что разности, заключенные в скобки, в уравнениях (2 — 10) и (2 — 11) затем обозначены символами DCP и DCV.
Уравнения (2 — 10) и (2 — 11) называются уравнениями Кирхгофа в интегральной форме. В них входят теплоты реакции при температуре Т1 ( 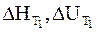
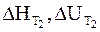
Уравнения Кирхгофа позволяют рассчитывать тепловые эффекты реакций в широком диапазоне температур, используя только справочные данные. В частности, теплоту реакции при определенной температуре можно рассчитать на основе первого или второго следствия из закона Гесса, а затем по известным из справочной литературы значениям теплоемкости тепловой эффект рассчитывается для другой температуры.
В справочниках зависимость теплоемкости веществ от температуры, как правило, приводится в виде степенных рядов следующих типов:
Диапазон температур, для которого температурная зависимость теплоемкости выполняется, четко оговаривается. Проведение вычислений при температурах, выходящих за пределы (особенно верхние) диапазона, недопустимо.
Уравнения Кирхгофа позволяют решать и некоторые качественные задачи. Например, зная, что теплоемкость пара всегда меньше теплоемкости жидкости, можно утверждать, что с повышением температуры теплота (изменение энтальпии) испарения жидкости уменьшается.
Дата добавления: 2015-07-24 ; просмотров: 2679 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Зависимость теплового эффекта химической реакции от температуры. Закон Кирхгофа
Зависимость теплового эффекта химической реакции от температуры. Закон Кирхгофа.
Тепловой эффект химической реакции или изменение энтальпии системы вследствие протекания химической реакции. 3
Стандартная энтальпия образования(ΔHfO). 4
Стандартная энтальпия сгорания(ΔHгоро). 4
Уравнение Кирхгофа. 4
Тепловой эффект химической реакции или изменение энтальпии системы вследствие протекания химической реакции.
Чтобы тепловой эффект являлся величиной, зависящей только от характера протекающей химической реакции, необходимо соблюдение следующих условий:
· Реакция должна протекать либо при постоянном объёме Qv(изохорный процесс), либо при постоянном давлении Qp(изобарный процесс).
· В системе не совершается никакой работы, кроме возможной (при изобарном процессе) работы расширения.
Если реакцию проводят в стандартных условиях при Т = 298 К и Р = 101.3 кПа, тепловой эффект называют стандартным тепловым эффектом реакции или стандартной энтальпией реакции ΔHrO.
Для правильного понимания понятия необходимо знать следующие понятия.
Теплоёмкость тела (обозначается с) — физическая величина, определяющая отношение бесконечно малого количества теплоты ΔQ, полученного телом, к соответствующему приращению его температуры ΔT. Единица измерения теплоёмкости в системе СИ — Дж/К.
Если же говорить про теплоёмкость произвольной системы, то ее уместно формулировать в терминах термодинамически — теплоёмкость есть отношение малого приращения количества теплоты Q к малому изменению температуры T:
Удельная теплоемкость вещества определяется как количество тепловой энергии, необходимой для повышения температуры одного килограмма вещества на один градус по Цельсию.
Формула расчёта удельной теплоёмкости [Дж/(кг• К)]:
Молярная теплоёмкость — это теплоёмкость одного моля вещества(количество теплоты, необходимое для нагревания тела массой 1 кг на 1 К) Часто употребляется обозначение C. Однако буквой C часто обозначается и простая теплоёмкость.
Связь с удельной теплоёмкостью:
где с — удельная теплоёмкость, М — молярная масса [Дж/(К•моль)].
Средняя молярная теплоемкость — количество теплоты, необходимое для нагревания 1 моль вещества на ΔТ.
Для расчета энтальпий и энтропии вещества используют интегралы от теплоемкости:
Стандартная энтальпия образования(ΔHfO).
Стандартная теплота образования – это тепловой эффект реакции образования одного моля вещества из простых веществ, его составляющих, находящихся в устойчивых стандартных состояниях. Обозначается ΔHfO.
Термохимические эффекты можно включать в химические реакции. Химические уравнения в которых указано количество выделившейся или поглощенной теплоты, называются термохимическими уравнениями. Реакции, сопровождающиеcя выделением тепла в окружащию среду имеют отрицательный тепловой эффект и называются экзотермическими. Реакции, сопровождающиеся поглощением тепла имеют положительный тепловой эффект и называются эндотермическими. Тепловой эффект обычно относится к одному молю прореагировавшего исходного вещества, стехиометрический коэффициент которого максимален.
Стандартная энтальпия сгорания(ΔHгоро).
Тепловой эффект реакции сгорания одного моля вещества в кислороде до образования оксидов в высшей степени окисления. Теплота сгорания негорючих веществ принимается равной нулю.
Уравнение Кирхгофа — соотношение, устанавливающее зависимость теплового эффекта химической реакции от температуры.
«Равенство, выражающее температурную зависимость теплового эффекта химических реакций через разность теплоемкостей конечных продуктов и исходных веществ. В частности, для реакций, происходящих при постоянном объеме, уравнение Кирхгофа связывает температурную зависимость изменения внутренней энергии ΔU при реакции с разностью изохорных теплоёмкостей cv в форме
Теплоемкость при постоянном давлении (Р):
Изменение энтальпии равно изменению теплоты:
Теплоемкость при постоянном объеме (V):
Cv1 и Cv2 — суммы теплоёмкостей исходных веществ и продуктов реакции с учётом их стехиометрических коэффициентов в уравнении реакции. Интегрируя это уравнение, можно определить изменение внутренней энергии ΔUT при интересующей температуре Т, если известны ΔUT1 при какой-нибудь другой температуре T1 и теплоёмкости исходных веществ и продуктов реакции в рассматриваемом температурном интервале. Уравнение было выведено в 1858.»
1. , , «Физическая химия», Москва, Высшая школа, 1990.
2. «Физическая химия», Москва, Мир, 1980.
3. Киреев физической химии. 1975 год, с 264-272.







