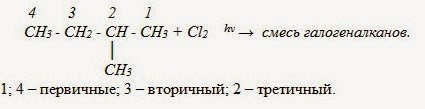Химия | 5 — 9 классы
Заполните таблицу химические свойства и применение алканов.
Все ответы в прикреплённых изображениях.

- Помогите пожалуйста?
- Заполните таблицу в которой отражены химические свойства углерода допишите уравнения реакции?
- Химические свойства Алканов Алкенов и т?
- Химические свойства алканов?
- Химические свойства алканов?
- Химические свойства : алканов, алкенов, алкинов, алкодиенов, аренов ввиде формул?
- Перечислите химические свойства воды?
- Химические свойства алканов?
- Перечислите области применения кислорода ?
- Как строение алканов повлияло на их химические свойства?
- Методическая разработка урока «Химические свойства и применений алканов» план-конспект урока по химии (10 класс) на тему
- Скачать:
- Предварительный просмотр:
- Заполните таблицу химические свойства и применение алканов уравнение реакции
- Химические свойства алканов
- Строение алканов
- Химические свойства
- Применение
- Что мы узнали?
Помогите пожалуйста?
Заполните таблицу «Химические свойства металлов», записав уравнения возможных реакций.
Заполните таблицу в которой отражены химические свойства углерода допишите уравнения реакции?
Заполните таблицу в которой отражены химические свойства углерода допишите уравнения реакции.
Химические свойства Алканов Алкенов и т?
Химические свойства Алканов Алкенов и т.
Химические свойства алканов?
Химические свойства алканов.
Химические свойства алканов?
Химические свойства алканов.
Химические свойства : алканов, алкенов, алкинов, алкодиенов, аренов ввиде формул?
Химические свойства : алканов, алкенов, алкинов, алкодиенов, аренов ввиде формул.
Перечислите химические свойства воды?
Перечислите химические свойства воды.
Какие из этих свойств находят практическое применение.
Химические свойства алканов?
Химические свойства алканов.
Перечислите области применения кислорода ?
Перечислите области применения кислорода .
На каких химический или физический свойствах основано это применение.
Как строение алканов повлияло на их химические свойства?
Как строение алканов повлияло на их химические свойства?
Вы находитесь на странице вопроса Заполните таблицу химические свойства и применение алканов? из категории Химия. Уровень сложности вопроса рассчитан на учащихся 5 — 9 классов. На странице можно узнать правильный ответ, сверить его со своим вариантом и обсудить возможные версии с другими пользователями сайта посредством обратной связи. Если ответ вызывает сомнения или покажется вам неполным, для проверки найдите ответы на аналогичные вопросы по теме в этой же категории, или создайте новый вопрос, используя ключевые слова: введите вопрос в поисковую строку, нажав кнопку в верхней части страницы.
D = 8, 83 M = 28, 98 г / моль молярная масса воздуха M(S) = 32 г / моль M(Sₓ) = xM(S) M(Sₓ) = DM xM(S) = DM 32x = 8, 83 * 28, 98 x = 8 S₈ молекула состоит из восьми атомов.
Так як шукаючи масу кальцію треба множити його молярну масу на кількість речовини, можна зробити висновок, що збільшення маси кальцію у сполуках буде дорівнювати збільшенню його кількості речовини Тому послідовність буде така В) n(Ca) = n(CaSO4) = 0.
Ответ а Алкан : а, д Циклоалкан : бжз Алкен : бв Алкин : г.
Ответ на фотографии.
2K + H2 = 2КН S + O2 = SO2 4Al + 3O2 = 2Al2O3 2Ca + O2 = 2CaO.
А)2Н2 + О2 = 2Н2О г)2Р + 3О2 = Р2О5.
Молекулы которые имеют большую разность.
Однородные : — воздух — морская вода — молоко — раствор сахара в воде — туман — дым — смесь уксуса и воды Неоднородные : — свежевыжатый апельсиновый сок — ил в реке.
Белый пудель. Он же белый. Соответствует названию. Наверное.
Методическая разработка урока «Химические свойства и применений алканов»
план-конспект урока по химии (10 класс) на тему
Методическая разработка урока «Химические свойства алканов и их применение»
Скачать:
| Вложение | Размер |
|---|---|
| khimicheskie_svoystva_alkanov.docx | 116.56 КБ |
Предварительный просмотр:
Методическая разработка урока:
«Химические свойства и применение алканов»
Цель урока: изучение важнейших химических свойств и применения алканов.
Образовательные задачи урока:
- рассмотреть основные химические свойства – реакции замещения, горения, разложения, дегидрирования и их практическое применение в жизни человека
- выявить взаимосвязь между строением алканов, их химическими свойствами и важнейшими областями применения
Развивающие задачи урока:
- развивать умения обучающихся составлять уравнения химических реакций, находить зависимость в ряду: строение – свойства – применение;
- развивать умение анализировать, сравнивать, обобщать, классифицировать, строить умозаключения, делать выводы;
- развивать навыки самостоятельной работы;
- привить любовь к предмету, желание познать новое.
Воспитательные задачи урока:
- воспитывать культуру умственного труда;
- воспитывать информационную культуру;
- воспитывать потребность добиваться успехов в приобретении знаний;
Индивидуальная, фронтальная работа
Комбинированный урок с применением ИКТ
Компьютер, проектор, презентация «Химические свойства алканов и важнейшие области их применения», таблицы: «Генетический ряд алканов», видеоопыты: « «Горение метана», «Горение жидких углеводородов», карточки для самостоятельной работы у доски и на местах, проверочные тесты, мел, доска
Используемые учебники и учебные пособия :
- О.С. Габриелян. Химия. 10 класс. Базовый уровень. Дрофа. Москва. 2013.
- О.С. Габриелян. Химия. Методическое пособие. 10 класс. Базовый уровень. Дрофа. Москва. 2008
Используемая методическая литература:
- О.С. Габриелян, А.В. Яшукова. Химия. Методическое пособие 10 класс. Базовый уровень
- О.С. Габриелян, И.Г. Остоумов. Настольная книга учителя химии. 10 класс
«Горение жидких углеводородов»
I этап. Организационный момент.
II этап. Актуализация знаний обучающихся
III этап. Изучение нового материала.
IV этап. Физкультминутка
V этап. Закрепление полученных знаний и способов деятельности
VI этап. Подведение итогов урока.
VII этап. Домашнее задание.
VIII этап. Рефлексия.
I. Организационный момент
Учитель приветствует обучающихся, проверяет готовность класса к уроку, определяет отсутствующих учеников.
Приветствуют учителя, дежурный сообщает о готовности класса к уроку и называет отсутствующих
II.Актуализация знаний обучающихся
Учитель приглашает трех учеников к доске для самостоятельного выполнения индивидуальных заданий по карточкам:
1 ученик – работа по карточке: Назовите предложенные вещества.
2 ученик – работа по карточке: Составьте структурные формулы: а) 2,2-диметилбутана,
3 ученик – решает задачу: Установите формулу алкана, если его молекулярная масса равна 58. Составьте структурные формулы одного изомера и одного гомолога для данного вещества, назовите их.
В это время учитель проводит фронтальную беседу с остальными обучающимися в классе:
- Какие вещества называются алканами?
- Почему их называют “предельными” или “насыщенными” углеводородами?
- Назовите общую формулу для класса алканов?
- Какой тип химической связи присутствует в молекулах алканов?
- Расскажите об основных способах получения алканов?
Учитель вместе с обучающимися класса проверяет задания, выполненные самостоятельно у доски тремя учениками.
Трое учеников самостоятельно решают полученные задания у доски.
В ходе беседы обучающиеся класса отвечают на поставленные вопросы учителя.
Ученики вместе с учителем проверяю правильность выполненных заданий
III. Изучение нового материала
Учитель рассказывает: Как мы с вами знаем, алканы при комнатной температуре химически малоактивны и даже с сильными окислителями тяжело реагируют. Поэтому их еще называют парафинами – от греческого «парум афинис» – что означает не терпящие сродства. Однако при специальных условиях алканы могут вступать в различные реакции. Сегодня мы приступаем к изучению химических свойств алканов и важнейших областей их применения человеком. Запишите тему урока.
Учитель записывает на доске тему урока «Химические свойства и применение алканов»
Демонстрация слайда № 1 (Эпиграф к теме урока «Границ научному познанию и предсказанию предвидеть невозможно» Д.И. Менделеев)
Определяет цель и задачи урока
Демонстрация слайда № 2-3(Цель и задачи урока)
В течение урока в ходе объяснения учителя ученики заполняют таблицу «Химические свойства алканов и важнейшие области их применения», которую учитель чертит на доске:
Учитель объясняет: Наиболее характерными для алканов являются реакции замещения, в ходе которых атом водорода замещается на атом галогена или какую-либо другую группу. Эти реакции протекают только при ярком освещении, сильном нагревании. Механизм цепных реакций достаточно сложен, объяснение ему было дано русским учёным Н.Н. Семёновым, за что он в 1956 г. был удостоен Нобелевской премии.
Демонстрация слайда № 4 (слайд о Н.Н. Семенове)
Учитель записывает на доске уравнения реакций замещения:
СН 4 + Cl 2 CH 3 Cl + HCl
Демонстрация слайда № 5:
СН 3 Cl (хлорметан или хлористый метил )– газ, легко сжижается и при последующем испарении поглощает большое количество теплоты. Применяется в холодильных установках.
СН 3 Cl + Cl 2 CH 2 Cl 2 + HCl
Демонстрация слайда № 6:
СН 2 Cl 2 (хлористый метилен) – применяется как растворитель, для склеивания пластиков
СН 2 Cl 2 + Cl 2 CHCl 3 + HCl
Демонстрация слайда № 7:
СН Cl 3 – хлороформ , бесцветная летучая жидкость с эфирным запахом и сладким вкусом используется:
при производстве фреонового хладагента; в качестве растворителя в фармакологической промышленности; для производства красителей и пестицидов
СНCl 3 + Cl 2 CCl 4 + HCl
Демонстрация слайда № 8:
СCl 4 (четрыххлористый углерод) — применяется как растворитель (жиров, смол, каучука);для получения фреонов, в медицине. Являлся стандартным наполнителем переносных огнетушителей для советской бронетехники
Учитель записывает уравнения реакции на доске:
СН 4 + HO-NO 2 = CH 3 -NO 2 + H 2 O
Учитель объясняет: Несмотря на то, что в обычных условиях алканы не взаимодействуют с концентрированной азотной кислотой, при нагревании их до 140°С с разбавленной (10%-ной) азотной кислотой под давлением осуществляется реакция нитрования – замещение атома водорода нитрогруппой (реакция М.И.Коновалова).
Демонстрация слайда №9 : Эта реакция была проведена в 19 веке и про учёного говорили, что он сумел оживить « химических мертвецов. Эта реакция применяется для получения нитро соединений, растворителей, используемыми человеком в промышленности.
Учитель объясняет второе важнейшее химическое свойство алканов:
Горение — при поджигании на воздухе алканы горят, превращаясь в двуокись углерода и воду и выделяя большое количество тепла.
Учитель показывает видеоопыт : «Горение метана»
Учитель записывает уравнение реакции на доске:
CH 4 + 2O 2 –– пламя > CO 2 + 2H 2 O
Учитель показывает видеоопыт: «Горение жидких углеводородов»
Учитель записывает уравнение химической реакции на доске:
2C 6 H 14 + 19O 2 –– пламя > 12CO 2 + 14H 2 O
Учитель демонстрирует горение пропанобутановой смеси на примере газовой зажигалки и дает задание учащимся записать уравнения горения: 1 вариант — горение пропана; 2 вариант – горение бутана.
Учитель проверяет правильность составленных уравнений реакций, вызывая к доске 2-х человек.
Демонстрация слайда № 9: ( Горение алканов – это экзотерическая реакция, которая имеет очень большое значение при использовании алканов в качестве топлива)
Учитель объясняет, показывая практическое значение реакции горения алканов – это экзотермическая реакция, имеющая большое значение при использовании алканов в качестве топлива.
Ученики слушают учителя.
Обучающиеся записывают тему урока и эпиграф к уроку в тетрадь.
Ученики чертят таблицу в тетрадь, заполняют шапку таблицы.
Ученики начинают заполнять таблицу в ходе объяснения учителя, записывая первое химическое свойство алканов реакции замещения
Ученики записывают в таблицу уравнения реакции галогенирования, смотрят слайды и отмечают области применения хлорметана, дихлорметана,
Заполните таблицу химические свойства и применение алканов уравнение реакции
II. Химические свойства алканов
1. Реакции замещения
а) Галогенирование
При действии света — hν или нагревании (стадийно – замещение атомов водорода на галоген носит последовательный цепной характер. Большой вклад в разработку цепных реакций внёс физик, академик, лауреат Нобелевской премии Н. Н. Семёнов )
В реакции образуются вещества галогеналканы RГ или С n H 2n+1 Г
(Г — это галогены F, Cl, Br, I)
CH 4 + Cl 2 hν → CH 3 Cl + HCl (1 стадия)
CH 3 Cl + Cl 2 hν → CH 2 Cl 2 + HCl (2 стадия)
Скорость реакции замещения водорода на атом галогена у галогеналканов выше, чем у соответствующего алкана, это связано с взаимным влиянием атомов в молекуле:
Электронная плотность связи С – Cl смещена к более электроотрицательному хлору, в результате на нём скапливается частичный отрицательный заряд, а на атоме углерода – частичный положительный заряд.
На атом углерода в метильной группе ( — СН3) создаётся дефицит электронной плотности, поэтому он компенсирует свой заряд за счёт соседних атомов водорода, в результате связь С – Н становится менее прочной и атомы водорода легче замещаются на атомы хлора. При увеличении углеводородного радикала наиболее подвижными остаются атомы водорода у атома углерода ближайщего к заместителю:
Со фтором реакция идёт со взрывом.
С хлором и бромом требуется инициатор.
Иодирование происходит обратимо, поэтому требуется окислитель для удаления HI из рекции.
Внимание!
В реакциях замещения алканов легче всего замещаются атомы водорода у третичных атомов углерода, затем у вторичных и, в последнюю очередь, у первичных. Для хлорирования эта закономерность не соблюдается при T>400˚C.
б) Нитрование (реакция М.И. Коновалова , он провёл её впервые в 1888 г)
2. Реакции отщепления (дегидрирование)
б) При нагревании до 1500 С происходит образование ацетилена и водорода:
3. Реакции перегруппировки (изомеризация)
4. Реакции горения (горят светлым не коптящим пламенем)
Помните! Смесь метана с воздухом и кислородом взрывоопасна
5. Реакции разложения
а) Крекинг при температуре 700-1000°С разрываются (-С-С-) связи:
б) Пиролиз при температуре 1000°С разрываются все связи,
продукты – С и Н2:
в) Конверсия метана с образованием синтез – газа (СО + Н2)
III. Получение алканов
1. Получение в лаборатории
1. Гидролиз карбида алюминия (получение метана):
2. Реакция Вюрца (взаимодействие натрия с галогенпроизводными алканов):
(R- это радикал; Г- это галоген)
3. Термическое декарбоксилирование солей карбоновых кислот в присутствии щелочей:
(ацетат натрия+ едкий натр=(метан+карбонат натрия)
этилат натрия этан
4. Каталитическое гидрирование алкенов и алкинов:
5. Электролиз растворов солей карбоновых кислот — реакция КОЛЬБЕ
Пример. Электролиз водного раствора ацетата натрия
Катод (-): H2O , Na + — Процесс восстановления: 2H 2 O + 2ē → H 2 ↑ + 2OH —
Анод (+): H 2 O, CH3COO — (анионы органических кислот активнее воды) – Процесс окисления:
2H2O + 2CH3COONa эл . ток = H2 + 2NaHCO3 + C2H6
2. Получение в промышленности
1. Из природного и попутного нефтяного газа
Важнейшим источником алканов в природе является природный газ, минеральное углеводородное сырье — нефть и сопутствующие ей нефтяные газы. Природный газ на 95 процентов состоит из метана. Такой же состав имеет болотный газ, образующийся в результате переработки бактериями (гниения) углеводов.
Метан называют ещё и болотным; рудничным газом.
Попутные нефтяные газы состоят в основном из этана, пропана, бутана и частично пентана. Их отделяют от нефти на специальных установках по подготовке нефти. При отсутствии газоконденсатных станций попутные нефтяные газы сжигают в факелах, что является крайне неразумной и разорительной практикой в нефтедобыче. Одновременно с газами нефть очищается от воды, грязи и песка, после чего поступает в трубу для транспортировки. Из нефти при ее разгонке (перегонке, дистилляции) отбирая последовательно все более и более высококипящие фракции получают:
бензины — т. кип. от 40 до 180 С, (содержит углеводороды С5-С10), состоит более, чем из 100 индивидуальных соединений, нормальных и разветвленных алканов, циклоалканов, алкенов и ароматических углеводородов;
легкий газойль (дизельное топливо) 230-305 С (С13-С17);
тяжелый газойль и легкий дистиллят смазочного масла 305-405 С (С18-С25);
смазочные масла 405-515 С (С26-С38).
Остаток после перегонки нефти называется асфальтом или битумом.
2. Синтезом из водяного газа:
3. Синтезом из простых веществ:
IV. Применение
1. Предельные углеводороды находят широкое применение в самых разнообразных сферах жизни и деятельности человека.
2. Использование в качестве топлива – в котельных установках, бензин, дизельное топливо, авиационное топливо, баллоны с пропан-бутановой смесью для бытовых плит.
3. Вазелин используется в медицине, парфюмерии, косметике, высшие алканы входят в состав смазочных масел, соединения алканов применяются в качестве хладагентов в домашних холодильниках.
4. Смесь изомерных пентанов и гексанов называется петролейным эфиром и применяется в качестве растворителя. Циклогексан также широко применяется в качестве растворителя и для синтеза полимеров.
5. Метан используется для производства шин и краски.
6. Значение алканов в современном мире огромно. В нефтехимической промышленности предельные улеводороды являются базой для получения разнообразных органических соединений, важным сырьем в процессах получения полупродуктов для производства пластмасс, каучуков, синтетических волокон, моющих средств и многих других веществ. Велико значение в медицине, парфюмерии и косметике.
Химические свойства алканов

Средняя оценка: 4.1
Всего получено оценок: 750.
Средняя оценка: 4.1
Всего получено оценок: 750.
Алканы – соединения гомологического ряда метана. Это насыщенные нециклические углеводороды. Химические свойства алканов зависят от строения молекулы и физического состояния веществ.
Строение алканов
Молекула алкана состоит из атомов углерода и водорода, которые образуют метиленовые (-CH2-) и метильные (-CH3) группы. Углерод может создавать четыре ковалентные неполярные связи с соседними атомами. Именно наличие прочных σ-связей -С-С- и -С-Н обуславливает инертность гомологического ряда алканов.

Соединения реагируют на свету или при нагревании. Реакции протекают по цепному (свободно-радикальному) механизму. Таким образом, связи способны расщепляться только под действием свободных радикалов. В результате замещения водорода образуются галогеналканы, соли, циклоалканы.
Алканы относятся к предельным или насыщенным углеродам. Это значит, что молекулы содержат максимальное количество атомов водорода. Из-за отсутствия свободных связей реакции присоединения для алканов не характерны.
Химические свойства
Общие свойства алканов приведены в таблице.
Типы химических реакций
Описание
Уравнение
Реагируют с F2, Cl2, Br2. Реакция с йодом не идёт. Галогены замещают атом водорода. Реакция с фтором сопровождается взрывом. Хлорирование и бромирование происходит при температуре 300-400°C. В результате образуются галогеналканы
Нитрование (реакция Коновалова)
Взаимодействие с разбавленной азотной кислотой при температуре 140°C. Атом водорода замещается нитрогруппой NO2. В результате образуются нитроалканы
Сопровождается окислением с образованием алкансульфонилхлоридов
Образование алкансульфоновых кислот в избытке кислорода. Атом водорода замещается группой SO3H
Происходит в присутствии катализатора при высоких температурах. В результате разрыва связей С-С образуются алканы и алкены
В избытке кислорода происходит полное окисление до углекислого газа. При недостатке кислорода происходит неполное окисление с образованием угарного газа, сажи
Происходит частичное окисление алканов при небольшой температуре и в присутствии катализаторов. Могут образовываться кетоны, альдегиды, спирты, карбоновые кислоты
Отщепление водорода в результате разрыва связей С-Н в присутствии катализатора (платины, оксида алюминия, оксида хрома) при температуре 400-600°С. Образуются алкены
Реакция дегидрирования с образованием циклоалканов
Образование изомеров под действием температуры и катализаторов
Чтобы понимать, как проходит реакция и какие радикалы замещаются, рекомендуется записывать структурные формулы.
Применение
Алканы широко применяются в промышленной химии, косметологии, строительстве. Из соединений изготавливают:
- топливо (бензин, керосин);
- асфальт;
- смазочные масла;
- вазелин;
- парафин;
- мыло;
- лаки;
- краски;
- эмали;
- спирты;
- синтетические ткани;
- каучук;
- адьдегиды;
- пластмассы;
- моющие средства;
- кислоты;
- пропелленты;
- косметические средства.

Что мы узнали?
Узнали о химических свойствах и применении алканов. Из-за прочных ковалентных связей между атомами углерода, а также между атомами углерода и водорода, алканы проявляют инертность. Возможны реакции замещения и разложения в присутствии катализатора при высоких температурах. Алканы – предельные углеводороды, поэтому реакции присоединения невозможны. Алканы используются для производства материалов, моющих средств, органических соединений.