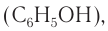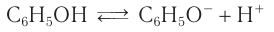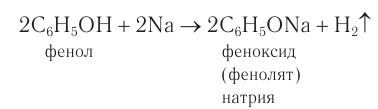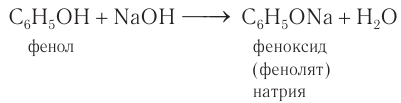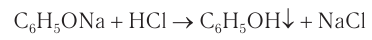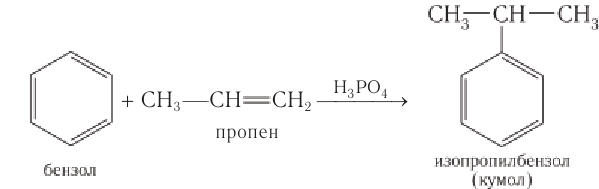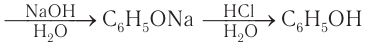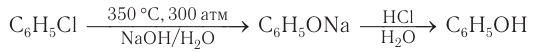Гидроксисоединения – это органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Гидроксисоединения делят на спирты и фенолы.
| Спирты – это гидроксисоединения, в которых группа ОН соединена с алифатическим углеводородным радикалом R-OH. Если гидроксогруппа ОН соединена с бензольным кольцом, то вещество относится к фенолам. |
Общая формула предельных нециклических спиртов: CnH2n+2Om, где m ≤ n.
- Классификация фенолов
- По числу гидроксильных групп:
- Строение фенолов
- Химические свойства фенолов
- 1.1. Взаимодействие с раствором щелочей
- 1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
- 2. Реакции фенола по бензольному кольцу
- 2.1. Галогенирование
- 2.2. Нитрование
- 3. Поликонденсация фенола с формальдегидом
- 4. Взаимодействие с хлоридом железа (III)
- 5. Гидрирование (восстановление) фенола
- Получение фенолов
- 1. Взаимодействие хлорбензола с щелочами
- 2. Кумольный способ
- 3. Замещение сульфогруппы в бензол-сульфокислоте
- Фенолы в химии — свойства, формула, получение, номенклатура и определение с примерами
- Строение фенола
- Физические свойства фенола
- Химические свойства фенола
- Получение и применение фенола
- Фенолы
Классификация фенолов
По числу гидроксильных групп:
- фенолы с одной группой ОН — содержат одну группу -ОН. Общая формула CnH2n-7OH или CnH2n-6O.
- фенолы с двумя группами ОН — содержат две группы ОН. Общая формула CnH2n-8(OH)2 или CnH2n-6O2.
| Соединения, в которых группа ОН отделена от бензольного кольца углеродными атомами – это не фенолы, а ароматические спирты: |
Строение фенолов
В фенолах одна из неподеленных электронных пар кислорода участвует в сопряжении с π–системой бензольного кольца, это является главной причиной отличия свойств фенола от спиртов.
Химические свойства фенолов
| Сходство и отличие фенола и спиртов. |
Сходство: как фенол, так и спирты реагируют с щелочными металлами с выделением водорода.
Отличия:
- фенол не реагирует с галогеноводородами: ОН- группа очень прочно связана с бензольным кольцом, её нельзя заместить;
- фенол не вступает в реакцию этерификации, эфиры фенола получают косвенным путем;
- фенол не вступает в реакции дегидратации.
- фенол обладает более сильными кислотными свойствами и вступает в реакцию со щелочами.
1. Кислотные свойства фенолов
| Фенолы являются более сильными кислотами, чем спирты и вода, т. к. за счет участия неподеленной электронной пары кислорода в сопряжении с π-электронной системой бензольного кольца полярность связи О–Н увеличивается. |
Раствор фенола в воде называют «карболовой кислотой», он является слабым электролитом.
1.1. Взаимодействие с раствором щелочей
В отличие от спиртов, фенолы реагируют с гидроксидами щелочных и щелочноземельных металлов, образуя соли – феноляты.
| Например, фенол реагирует с гидроксидом натрия с образованием фенолята натрия |
Так как фенол – более слабая кислота, чем соляная и даже угольная, его можно получить из фенолята, вытесняя соляной или угольной кислотой:
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Фенолы взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются феноляты. При взаимодействии с металлами фенолы ведут себя, как кислоты.
| Например, фенол взаимодействует с натрием с образованием фенолята натрия и водорода . |
2. Реакции фенола по бензольному кольцу
| Наличие ОН-группы в бензольном кольце (ориентант первого рода) приводит к тому, что фенол гораздо легче бензола вступает в реакции замещения в ароматическом кольце. |
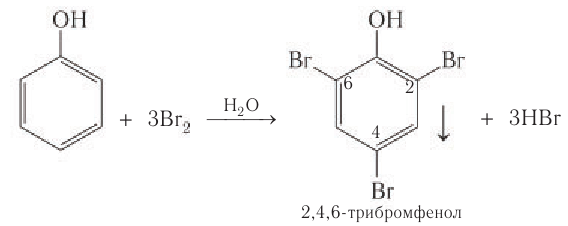
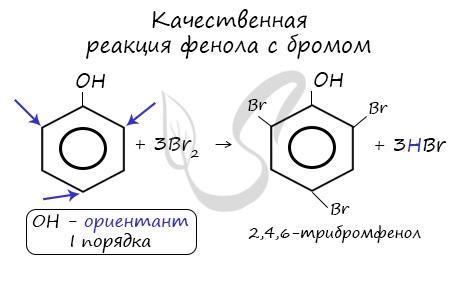
2.1. Галогенирование
| Фенол легко при комнатной температуре (без всякого катализатора) взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол). |
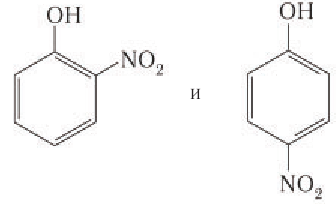
2.2. Нитрование
Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов.
| Например, при нитровании фенола избытком концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота): |
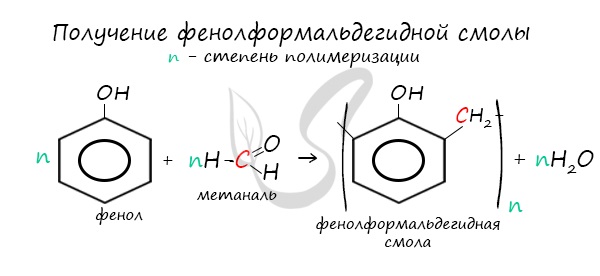
3. Поликонденсация фенола с формальдегидом
С формальдегидом фенол образует фенолоформальдегидные смолы.
4. Взаимодействие с хлоридом железа (III)
При взаимодействии фенола с хлоридом железа (III) образуются комплексные соединения железа, которые окрашивают раствор в сине-фиолетовый цвет. Это качественная реакция на фенол.
5. Гидрирование (восстановление) фенола
Присоединение водорода к ароматическому кольцу.
Продукт реакции – циклогексанол, вторичный циклический спирт.
Получение фенолов
1. Взаимодействие хлорбензола с щелочами
При взаимодействии обработке хлорбензола избытком щелочи при высокой температуре и давлении образуется водный раствор фенолята натрия.
При пропускании углекислого газа (или другой более сильной кислоты) через раствор фенолята образуется фенол.
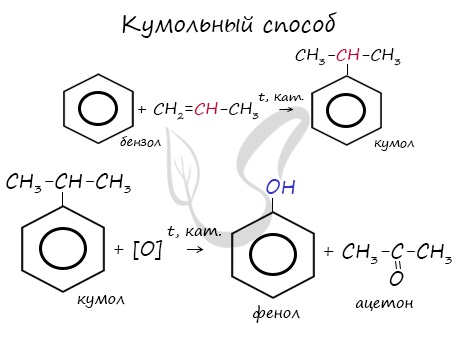
2. Кумольный способ
Фенол в промышленности получают из каталитическим окислением кумола.
Первый этап процесса – получение кумола алкилированием бензола пропеном в присутствии фосфорной кислоты:
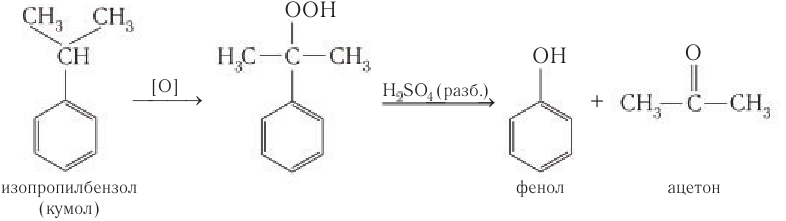
Второй этап – окисление кумола кислородом. Процесс протекает через образование гидропероксида изопропилбензола:
Суммарное уравнение реакции:
3. Замещение сульфогруппы в бензол-сульфокислоте
Бензол-сульфокислота реагирует с гидроксидом натрия с образованием фенолята натрия:
Получается фенолят натрия, из которого затем выделяют фенол:
Фенолы в химии — свойства, формула, получение, номенклатура и определение с примерами
Содержание:
Фенолы:
К гидроксилпроизводным органическим соединениям, кроме спиртов, относятся фенолы.
Фенолами называют производные ароматических углеводородов, в молекулах которых один или несколько атомов водорода, непосредственно связанных с бензольным кольцом, замещены на гидроксильные группы.
Число гидроксильных групп в молекуле определяет атомность фенолов. Они могут содержать до шести гидроксильных групп в молекуле. По числу гидроксильных групп фенолы, как и спирты, классифицируют как одно- и многоатомные фенолы.
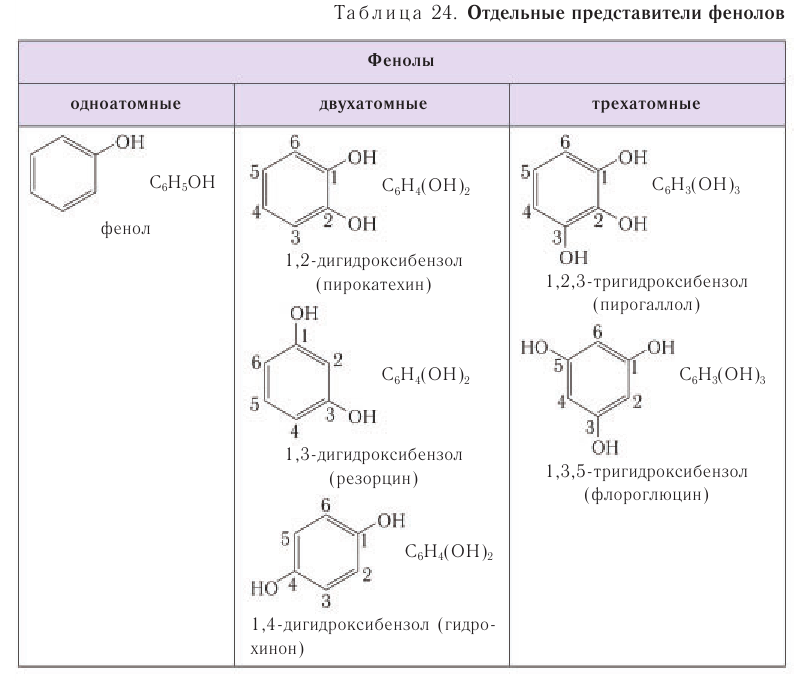
В таблице 24 для ознакомления приведены формулы и названия некоторых фенолов различной атомности.
В данном курсе органической химии вы познакомитесь со строением и свойствами одного представителя класса — фенолом
Строение фенола
Фенол 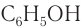
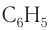
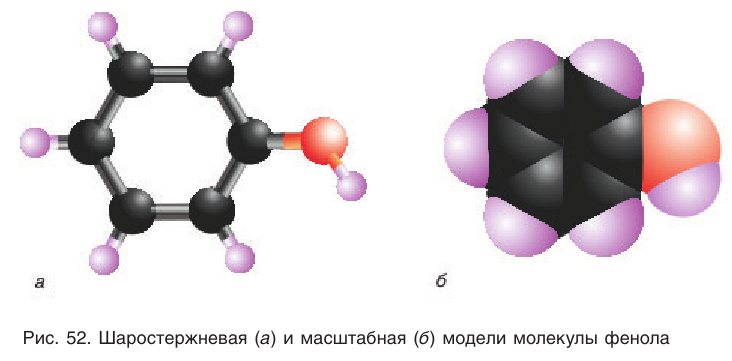
Шаростержневая и масштабная модели молекулы фенола приведены на рисунке 52.
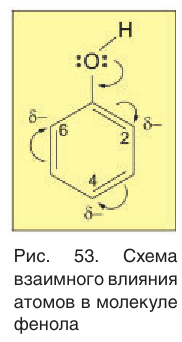
Рассмотрим электронное строение молекулы фенола. Одна из неподеленных электронных пар атома кислорода вступает в сопряжение с 
Сопряжение неподеленной электронной пары атома кислорода с 
Физические свойства фенола
Фенол — бесцветное кристаллическое вещество с резким характерным запахом. Кристаллическое состояние фенола обусловлено наличием прочных водородных связей между его молекулами. При обычной температуре фенол незначительно растворяется в воде, но хорошо раетворяетея в горячей воде. Фенол очень ядовит, при попадании на кожу вызывает cильнейшие ожоги, поэтому работать е ним в школьном химичееком кабинете запрещено.
Химические свойства фенола
Химические свойства фенола обусловлены наличием в молекуле функциональной группы —ОН и бензольного кольца, которые взаимно влияют друг на друга. В молекуле фенола бензольное кольцо влияет на гидроксильную группу, что проявляется в повышенной кислотности фенола по сравнению с насыщенными одноатомными спиртами. Влияние гидроксильной группы на бензольное кольцо обусловливает более легкое замещение в нем атомов водорода на какой-либо заместитель у атомов углерода в положениях 2, 4, 6.
Рассмотрим последовательно химические реакции, протекающие с участием гидроксильной группы и бензольного кольца.
1) Диссоциация в водных растворах. Молекулы фенола диссоциируют в водных растворах по кислотному типу:
Фенол является слабой кислотой (иногда его называют карболовой кислотой), что отличает его от спиртов, которые практически не диссоциируют в водных растворах.
2) Взаимодействие со щелочными металлами. Наличие в молекуле фенола гидроксильной группы, непосредственно связанной с бензольным кольцом, обусловливает определенное сходство по химическим свойствам с одноатомными спиртами. Если в расплавленный фенол поместить кусочек металлического натрия, то происходит реакция замещения атома водорода в гидроксильной группе. При этом образуется соединение, которое по номенклатуре ИЮПАК называют феноксид. Используется и другое название — фенолят, допускаемое номенклатурой ИЮПАК. В реакции со щелочными металлами фенол проявляет кислотные свойства:
3) Взаимодействие со щелочами. Кислотные свойства у фенола, как вам известно, выражены сильнее, чем у одноатомных насыщенных спиртов. Поэтому, в отличие от них, фенол реагирует не только со щелочными металлами, но и с водными растворами щелочей с образованием феноксидов (фенолятов):
Кислотные свойства у фенола выражены слабее, чем у неорганических кислот, даже таких слабых, как угольная. Поэтому добавление к водному раствору фенолята натрия соли угольной кислоты (кислотные свойства фенола примерно в три тысячи раз слабее, чем угольной кислоты) приводит к образованию фенола. Образуется фенол и при добавлении к водному раствору фенолята сильных минеральных кислот:
4) Галогенирование. Реакции галогенирования, в частности бромирования, протекают с замещением атомов водорода в бензольном кольце. В отличие от бензола для бромирования фенола не требуется катализатор, так как влияние гидроксильной группы значительно облегчает протекание реакций замещения в бензольном кольце. При действии на фенол раствора брома в воде образуется белый осадок 2,4,6-трибромфенола (рис 54).
Эта реакция часто используется для качественного обнаружения фенола.
Фенол дает характерное фиолетовое окрашивание с водным раствором хлорида железа(III) вследствие образования комплексной соли железа. Эту реакцию также используют для обнаружения фенола и относят к цветной качественной реакции.
5) Нитрование. Фенол так же, как и бензол, взаимодействует е азотной кислотой, но нитрование фенола протекает легче, чем нитрование бензола. Реакция фенола с разбавленной азотной кислотой идет при комнатной температуре, и в результате образуется смесь изомеров нитрофенола:
2, 4, 5 — Тринитрофенол (пикриновую кислоту) 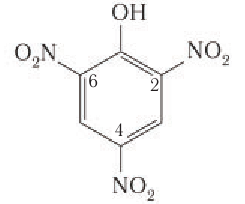
получают из фенола под действием сначала концентрированных серной, а затем азотной кислот. Наличие в молекуле пикриновой кислоты трех заместителей — 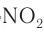
Фенолами называют производные ароматических углеводородов, в молекулах которых один или несколько атомов водорода, непосредственно связанных с бензольным кольцом, замещены на гидроксильные группы.
Фенол 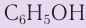
Для фенола характерны реакции гидроксильной группы (со щелочными металлами, щелочами) и бензольного кольца (галогенирование, нитрование).
Получение и применение фенола
Получение: Одним из основных промышленных методов получения фенола является кумольный метод. Он был разработан в 40-е гг. XX в. в Советском Союзе Р. Ю. Удрисом, Б. Д. Кружаловым, П. С. Сергеевым, М. С. Немцовым и до наших дней не утратил своей эффективности. Для получения фенола используются экономически выгодные исходные вещества — бензол и пропей.
Упрощенно синтез фенола можно представить так. Сначала в реакции бензола с пропеном синтезируют изопропилбензол (кумол):
Затем кумол окисляют, продукт окисления кумола разлагают разбавленной серной кислотой и получают при этом фенол и ацетон 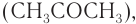
Схема получения из кумола фенола приведена для ознакомления и не требует запоминания.
Ранее фенол выделяли только из каменноугольной смолы, образующейся как побочный продукт коксохимического производства. Каменноугольную смолу обрабатывали щелочами, а, как вам известно, водные растворы щелочей взаимодействуют с фенолом с образованием фенолятов. Затем феноляты обрабатывали минеральными кислотами и получали фенол. Схематически процесс экстрагирования фенола из каменноугольной смолы можно представить так:
каменноугольная смола
Фенол можно получить, используя в качестве исходного вещества бензол. При хлорировании бензола сначала получают хлорбензол, затем хлорбензол под действием водного раствора гидроксида натрия дает фенолят натрия, который в реакции с минеральными кислотами превращается в фенол:
Этот способ получения фенола в настоящее время практически не используется как технически устаревший и экономически нецелесообразный. Однако знакомство с ним представляет интерес как пример генетической связи между углеводородами, галогенпроизводными и гидроксилпроизводными (фенолами).
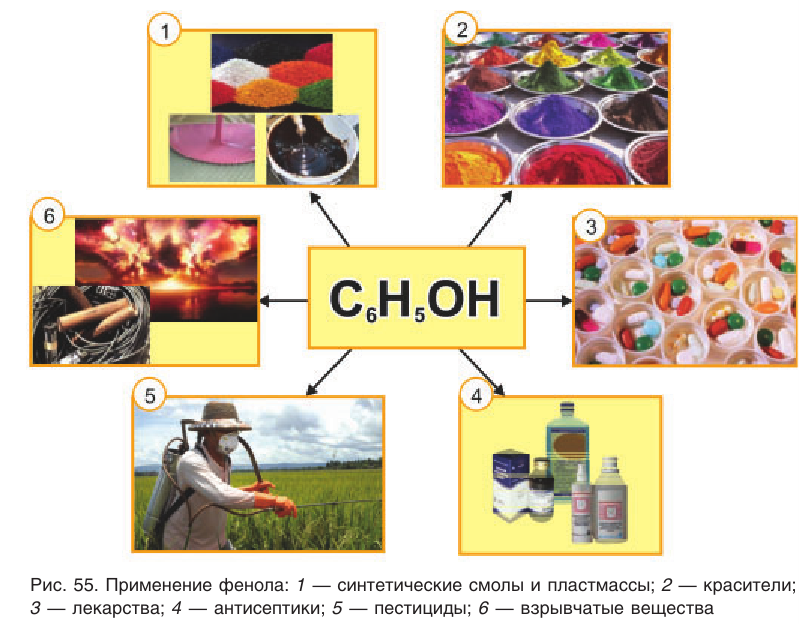
Применение: Фенол и продукты, получаемые на его основе, находят широкое применение (рис. 55). Практически половина производимого фенола расходуется на синтез фенолформальдегидных смол. Полимеры на основе этих смол применяются для изготовления лаков и красок, пластмассовых изделий, устойчивых к действию кислот и щелочей, нагреванию. Из пластмасс на основе фенолформальдегидных смол изготовляют важные детали электро- и радиоприборов, аппаратуры, используемой для работы при высокой температуре и в агрессивных средах. Клеи, полученные на основе фенолформальдегидных смол, надежно соединяют детали, изготовленные из самых различных веществ, сохраняя высокую прочность соединения.
Фенол служит исходным веществом для получения многих лекарственных препаратов, например аспирина, красителей, пестицидов, антисептиков. Он используется в генной инженерии и молекулярной биологии в качестве средства для очистки и выделения молекул ДНК.
Тринитрофенол (пикриновая кислота) находит применение в производстве взрывчатых веществ.
Гидрохинон применяется в фотографии в качестве проявителя, так как он очень легко окисляется.
Пирокатехин используется для получения адреналина — гормона, вырабатываемого надпочечниками.
Резорцин применяется наружно как антисептик при кожных заболеваниях в виде водных и спиртовых растворов; в производстве красителей, стабилизаторов и пластификаторов полимеров.
Фенол и его производные — ядовитые вещества, очень опасные для человека, животных и растительных организмов. Вдыхание паров фенола может привести к ожогам дыхательных путей и последующему отеку легких. При попадании фенола на кожу образуются химические ожоги. Фенол не теряет летучих свойств даже в составе пластмасс, вот поэтому во многих странах мира запрещено производство предметов быта и детских игрушек с использованием фенопластов, представляющих опасность для здоровья людей.
В составе отходов производства могут содержаться чрезвычайно ядовитые вещества, например диоксин:
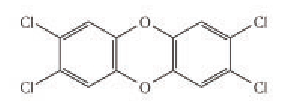
Чтобы предотвратить их попадание в окружающую среду, применяются различные физические и химические методы очистки.
Фенол в основном получают в процессе органического синтеза кумольным методом.
Фенол и его производные применяются в качестве исходных веществ для производства синтетических смол и пластмасс, синтеза красителей, лекарств и многих других ценных продуктов.
| Рекомендую подробно изучить предметы: |
|
| Ещё лекции с примерами решения и объяснением: |
- Альдегиды в химии
- Карбоновые кислоты в химии
- Сложные эфиры в химии
- Жиры в химии
- Насыщенные углеводороды
- Ненасыщенные углеводороды
- Ароматические углеводороды
- Спирты в химии
При копировании любых материалов с сайта evkova.org обязательна активная ссылка на сайт www.evkova.org
Сайт создан коллективом преподавателей на некоммерческой основе для дополнительного образования молодежи
Сайт пишется, поддерживается и управляется коллективом преподавателей
Telegram и логотип telegram являются товарными знаками корпорации Telegram FZ-LLC.
Cайт носит информационный характер и ни при каких условиях не является публичной офертой, которая определяется положениями статьи 437 Гражданского кодекса РФ. Анна Евкова не оказывает никаких услуг.
Фенолы
Фенолы — кислородсодержащие ароматические соединения, в молекулах которых содержится одна или несколько гидроксильных групп (OH), присоединенных к бензольному кольцу.
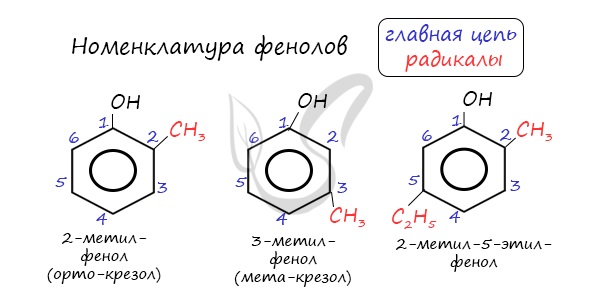
Номенклатура фенолов
Нумерацию атомов углерода в молекуле фенола начинают в такой последовательности, чтобы заместители получили наименьшие номера (идут кратчайшим путем). В основе названия принято сохранять тривиальное название «фенол».
Напомню, что гидроксильная группа является ориентантом I порядка (орто-, пара-ориентант). Поэтому реакции галогенирования, нитрования протекают в орто- и пара-положениях.
Получение фенолов
- Гидролиз галогенбензолов
При гидролизе галогенбензолов происходит обмен: гидроксогруппа встает на место атома галогена.
Этим способом получают 95% всего производимого фенола. В ходе этой реакции кумол (изопропилбензол) подвергают окислению, в результате получается фенол и ацетон.
Химические свойства фенолов
- Кислотные свойства
Щелочные металлы (Li, Na, K) способны вытеснять водород из фенолов с образованием солей — фенолятов. В отличие от алифатических одноатомных спиртов, фенолы способны вступать в реакцию с щелочами (KOH, LiOH, NaOH)
Реакция фенола с бромной водой является качественной: в ходе нее выпадает белая взвесь — осадок трибромфенола.
Реакция между фенолом и азотной кислотой происходит по типу замещения. В бензольном кольце появляется новый радикал — нитрогруппа. Важно учитывать, что OH группа фенола является ориентантом I порядка: замещение идет в орто-, пара-положении.
При гидрировании разрываются двойные связи бензольного кольца, образуется циклогексанол.
В промышленности получила широкое распространение реакция поликонденсации фенола с формальдегидом, приводящая к образованию смолообразных полимеров (фенолформальдегидные смолы) и воды.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.