- Ваш ответ
- решение вопроса
- Похожие вопросы
- ГДЗ (ответы) Химия 9 класс Попель П.П., Крикля Л.С., 2017 ПРАКТИЧЕСКАЯ РАБОТА №3 Свойства уксусной (этановой) кислоты
- Практическая работа № 19-20 «Растворимость различных карбоновых кислот в воде. Взаимодействие уксусной кислоты с металлами»
- Просмотр содержимого документа «Практическая работа № 19-20 «Растворимость различных карбоновых кислот в воде. Взаимодействие уксусной кислоты с металлами»»
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,401
- гуманитарные 33,632
- юридические 17,905
- школьный раздел 607,977
- разное 16,854
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
ГДЗ (ответы) Химия 9 класс Попель П.П., Крикля Л.С., 2017 ПРАКТИЧЕСКАЯ РАБОТА №3 Свойства уксусной (этановой) кислоты
Действие уксусной кислоты на индикатор
кислоты на полоску
Уксусная кислота имеет
Наличие ионов Гидрогена,
которые образуются при
диссоциации ее молекул,
является причиной изменения
Уравнение электролитической диссоциации уксусной кислоты:
ОПЫТ 2
Реакция уксусной кислоты с металлом
В пробирку с гранулой
цинка наливаем 2 мл
На поверхности гранулы
Составляем уравнения реакций в молекулярной и ионно-молекулярной формах .
ОПЫТ 3
Реакция уксусной кислоты с оснвным (амфотерным) оксидом
В пробирку с порошком
купрум (II) оксида
Составляем уравнения реакций в молекулярной и ионно-молекулярной формах .
2CH 3 COOH + СuO -> 2CH 3 COO — + Cu 2+ + H 2 O
ОПЫТ 4
Реакция уксусной кислоты со щелочью
| Действия | Наблюдение | Выводы | |||
| Действия | Наблюдения | Выводы |
| Действия | Наблюдения | Выводы |

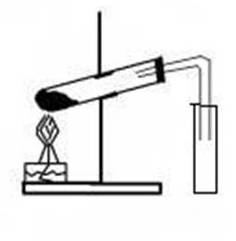 месь в пробирке осторожно нагревайте до тех пор, пока в приёмнике – пробирке не собёрётся 1 -2 мл жидкости. Прекратите нагревание, закройте спиртовку.
месь в пробирке осторожно нагревайте до тех пор, пока в приёмнике – пробирке не собёрётся 1 -2 мл жидкости. Прекратите нагревание, закройте спиртовку.