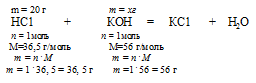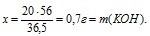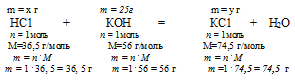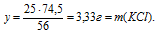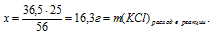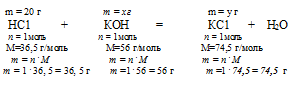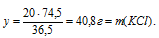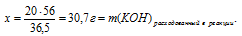Задачи на выход продукта химической реакции. Как решать задачи на выход продукта реакции. Что такое выход продукта химической реакции. Теоретическое и практическое количество продукта химической реакции.
При решении задач на расчеты по уравнениям химических реакций мы принимаем, что в ходе реакции образуется точно рассчитанное количество продукта, исходя из мольного соотношения реагентов и продуктов. Количество продукта реакции, которое должно получится из реагентов согласно стехиометрическим расчетам — это теоретическое количество (масса, объем) или теоретический выход продукта реакции nтеор.
Однако на практике это соотношение не выполняется, и в большинстве случаев образуется меньшее количество продукта реакции, чем было рассчитано — практическое количество (масса, объем) или практический выход продукта реакции nпр.
Практический и теоретический выход не совпадают в силу разных причин — неэффективные соударения реагирующих частиц, побочные процессы, потери в ходе проведения реакции и т.д.
Обратите внимание! Понятия теоретического или практического количества реагента не существует. Ведь мы всегда берем определенное количество реагентов. А вот вступать в реакцию не полностью реагенты могут.
Массовая (мольная, объемная) доля выхода продукта реакции η или ω — это соотношение массы (количества вещества, объема) продукта, которая практически получена в ходе реакции, mпр., к массе (количеству, объему) продукта, которая рассчитана теоретически, mтеор.:
Массовую (мольную, объемную) долю выхода продукта реакции можно выражать в долях, а можно в процентах:
Рассмотрим несколько задач на определение и использование выхода продукта реакции.
1. Какое количество вещества аммиака получится при действии избытка раствора гидроксида натрия на 500 г сульфата аммония, если выход в данной реакции 70%?
Решение.
Количество вещества сульфата аммония:
Теоретическое количество аммиака:
Зная мольную долю выхода продукта реакции, определим практический выход аммиака:
Ответ: nпр.(NH3) = 5,3 моль
2. При хлорировании метана объемом 112 л (н. у.) получен дихлорметан массой 255 г. Определите долю выхода дихлорметана.
Решение.
Количество вещества метана:
Теоретическое количество дихлорметана:
Масса дихлорметана, которая приведена в условии задачи — это практический выход дихлорметана.
Доля выхода дихлорметана:
η = mпр./mтеор. = 255/425 = 0,6 или 60%
Ответ: выход продукта реакции 60%
3. Определите массу оксида меди (II), которая потребуется для получения 500 г нитрата меди, если доля выхода в реакции взаимодействия оксида меди с HNO3 составляет 92%?
4. Определите объем (н.у., л) аммиака, который получится при действии избытка раствора гидроксида натрия на 48 г карбоната аммония, если выход в реакции составляет 70%?
5. Определите массу соли, г, которая образуется при растворении в избытке азотной кислоты 80 г оксида меди (II), если выход в реакции составляет 80%?
6. При термическом разложении 1700 г нитрата натрия было получено 174,4 л кислорода (н.у.). Определите массовую долю выхода в этой реакции.
7. Рассчитайте массу оксида магния, которая образуется при разложении гидроксида магния массой 50 г, если реакция разложений прошла с выходом 95,5%.
8. Какая масса бензола (кг) может получиться из 369,6 м 3 (н.у.) ацетилена, если доля выхода бензола составила 65% от теоретически возможного?
9. Определите массу спирта, полученного при гидратации 40 л пропилена (н.у.), если доля выхода продукта реакции составляет 65% от теоретически возможного.
10. Определите долю выхода в реакции каталитического окисления аммиака кислородом, если при окислении 10 моль аммиака образуется 200 л оксида азота (II) при н.у.?
11. Пары брома объемом 20 л смешали с избытком водорода, в результате из смеси выделили 32 л бромоводорода. Определите долю выхода, %, если объемы газов измерялись при одинаковых условиях.
12. Оксид кальция массой 0,64 кг нагрели до 1200° С с достаточной массой оксида кремния (IV). Масса образовавшегося силиката кальция оказалась равной 1,024 кг. Определите выход (%) реакции соединения.
13. Из 36 г метанола было получено 24 г диметилового эфира. Рассчитайте выход реакции дегидратации
14. Углекислый газ объемом 6 л (н.у.) пропустили над раскалённым углем, продукт реакции пропустили через избыток известковой воды, после чего собрали 7,2 л (н.у.) газа. Определите степень превращения углекислого газа, %.
15. Определите массу, г нитрата аммония, которая содержалась в растворе, если при действии на этот раствор избытка гидроксида кальция выделилось 6 г аммиака. Реакция прошла с выходом 88,2 %.
16. При термическом разложении не загрязненного примесями карбоната кальция образовалось 20 г оксида кальция. Известно, что реакция прошла с выходом 85%. Вычислите массу карбоната кальция, взятого для проведения реакции разложений и объем (н.у.) образовавшегося углекислого газа.
17. Какой объем пропана (н.у.) потребуется для получения 42 г пропена, если доля выхода продуктов реакции составляет 60% от теоретически возможного?
18. При бромировании пентена-2 массой 8,4 г получен 2,3-дибромпентан массой 24,3 г. Определите долю выхода продукта реакции.
19. Из 69 г этанола получен бутадиен-1,3 массой 36,85 г. Определите массовую долю выхода продукта реакции.
20. При бромировании 5,4 г дивинила избытком брома образуется 28,2 г 1,2,3,4-тетрабромбутана. Определите выход продукта реакции.
21. Определите, какая масса 2-метилбутана необходима для получения 46,24 г изопрена, если доля выхода продукта реакции составляет 85%?
22. Определ ите объем метана, который потребуется для получения 63 л ацетилена (н.у.), если доля выхода продуктов реакции составляет 70% от теоретически возможного.
23. Определите, какую массу уксусного альдегида можно получить по реакции Кучерова из 11,2 л ацетилена (н. у.), если доля выхода продуктов реакции составляет 80% от теоретически возможного?
24. При действии избытка воды на 48 г технического карбида кальция, содержащего 10% примесей, образовался ацетилен объемом 10,08 л (н.у.). Определите долю выхода продукта реакции.
25. Определите массу технического карбида алюминия, содержащего 7% примесей, необходимого для получения 56 л метана (н.у.), если доля выхода продуктов реакции составляет 70% от теоретически возможного.
26. Из 179,2 л бутана (н.у.) с объемной долей примесей 25% двухстадийным синтезом получен бутанол-2 массой 159,84 г. Доли выхода продуктов на первой и второй стадиях одинаковы. Определите доли выхода продуктов реакций.
27. Циклогексан массой 16 г сожгли в избытке кислорода и полученный углекислый газ пропустили через избыток раствора гидроксида кальция, в результате чего выпал осадок массой 90 г. Определите массовую долю негорючих примесей в циклогексане, если доля выхода продуктов горения составляет 90% от теоретически возможного.
28. При нитровании 46,8 г бензола получен нитробензол массой 66,42 г. Определите выход продуктов реакции.
Химия, Биология, подготовка к ГИА и ЕГЭ
Задачи такого типа (точнее, это может быть даже не самой задачей, а частью задачи) есть в части С ГИА, они входят в часть С ЕГЭ, теперь они появились и в части B.
Классический пример задачи на избыток и недостаток.
Этапы решения задачи:
1. Записываем уравнение реакции и уравниваем его:
2. Находим количество моль тех веществ, массы которых нам даны в условии:
n(Cu) = mAr =3.2 г 63.5 гмоль = 0,05 моль
m(Hg(NO3)2) = mMr = 20 324 = 0,06 моль
3. Сравниваем количество моль веществ и определяем недостаток:
0,05 моль 0,06 моль
по уравнению реакции меди и нитрат ртути реагируют 1:1, значит, их количество моль тоже должно быть одинаковым
0,05 моль ПО НЕДОСТАТКУ
Почему по недостатку? Это аналогично вопросу — «сколько целых яблок можно сложить из 5 половинок? «
4. Вычисляем массу продукта по количеству моль, соответствующему недостатку:
0,05 моль ——> 0,05 моль
m(Hg)= n*Ar = 0,05 моль * 200 гмоль = 10 г
______________________________________________________________________________________
Пример задачи на избыток и недостаток,
где вещества в другом соотношении:
те же самые этапы решения:
1. Записываем уравнение реакции и уравниваем его:
2. Находим количество моль тех веществ, массы которых нам даны в условии:
n(N2 ) = mMr = 1428=0.5 моль
3. Сравниваем количество моль веществ и определяем недостаток:
0.5 моль 0.5 моль
в этом уравнении все не так очевидно, как в предыдущем, поэтому нужно просто прикинуть:
- если считать по азоту (0.5 моль), то по соотношению коэффициентов (2:5) кислорода должно быть в 2.5 раза больше, т.е. (0.5*2.5) 1,25 моль, а у нас только 0.5, значит, O2 в недостатке;
- если бы количество моль азота оказалось бы меньше, значит, считали бы по азоту
4. Вычисляем массу продукта по количеству моль, соответствующему недостатку:
m(N2O5) = n*Mr = 2* 0.55 моль * 108 гмоль = 21 г
______________________________________________________________________________________
Есть задачи, очень похожие на задачи избыток-недостаток,
1. Записываем уравнение реакции и уравниваем его:
здесь у нас возможно 2 варианта — образование средней и кислой соли:
2. Находим количество моль тех веществ, массы которых нам даны в условии:
n(CO2 ) = V22.4 лмоль = 24.9 22.4 = 1,11 моль
n(NaOH)= mMr = 44.440 = 1,11 моль
т.к. количество моль веществ одинаково, то делаем вывод, что реакция протекает по схеме образования кислой соли:
4. Вычисляем массу продукта по количеству моль:
m ( NaHCO3) = n*Mr = 1,11 * 84 = 93,24 г
_____________________________________________________________________________________ _
Задачи на избыток и недостаток не трудные, зачастую они являются частью более сложных задач, поэтому все, что нужно сделать, это натренироваться — порешать как можно больше таких примеров, внимательно уравнивая и работая с коэффициентами.
Задачи на определение избытка-недостатка в реакциях нейтрализации
В основе всех задач на избыток-недостаток лежит химическая реакция. В ней одно из взаимодействующих веществ взято в избытке по отношению к другому веществу 1 . Рассмотрим примеры решения таких задач.
Задача 1.
Определите массу гидроксида калия, который необходим для полной нейтрализации раствора, содержащего 20 г НС1.
Дано: масса хлороводорода: m(НСГ) = 20 г.
Найти: массу гидроксида калия: m(КОН) = ?
Решение:
Это простейшая задача, которая решается по уравнению реакции в одно действие.
Составляем пропорцию:
20 г НС1 реагируют без остатка с x: г КОН (по условию)
36,5 г НС1 реагируют без остатка с 56 г КОН (по уравнению)
Ответ: 30,7 г КОН потребуется для полной нейтрализации раствора, содержащего 20 г НС1.
Задача 2.
Представим себе ситуацию, когда мы вместо 30,7 г КОН добавили недостаточное его количество, например, 25г. Тогда часть НС1 прореагирует с КОН, а часть останется. В этом случае КОН будет в недостатке, а НС1 — в избытке. Посмотрим, какие вещества и в каких количествах будут находиться в растворе после реакции, если к раствору, содержащему 20 г НС1 добавить недостаточное для полной нейтрализации количество КОН, например, 25 г.
Дано: масса хлороводорода: m(НС1) = 20 г;
масса гидроксида калия: m(КОН) = 25 г.
Найти: Массы всех веществ в растворе после реакции.
Решение:
Так как КОН взят в недостатке, он израсходуется весь в химической реакции. Количество НС1, по отношению к количеству КОН, находится в избытке, следовательно, часть хлороводорода останется после реакции. Кроме того, в процессе химической реакции образуется соль КСl, которая тоже будет содержаться в растворе. Образующаяся вода разбавит имеющийся раствор.
Итак, качественный состав раствора после реакции мы установили:
1) избыточная хлороводородная кислота (НС1);
2) образующаяся соль КС1;
3) вода в виде растворителя.
Определим массы НС1 и КС1 в конечном растворе. Массу КС1 легко определить путем расчета по химической реакции.
Массу оставшейся НС1 можно найти по разности:
m(HCl)оставшейся после р-ции = m(HCl)исх. – m(HCl)израсходованной в р-ци
Массу израсходованной НС1 также необходимо найти по уравнению реакции.
В задачах на избыток-недостаток расчет по уравнению реакции всегда ведут по веществу, взятому в недостатке. Вещество, взятое в недостатке, всегда в реакции расходуется полностью. А вещество, взятое в избытке, расходуется лишь частично, и какая часть его участвует в химической реакции нам неизвестно. Поэтому вести расчет по веществу, взятому в избытке, невозможно.
В данном случае в недостатке у нас КОН. По нему и ведем расчет образовавшейся соли КС1 и расходовавшейся НС1:
Найдем массу образовавшейся соли КС1. Для этого составим пропорцию:
25 г КОН дают у г КС1 (по условию)
56 г КОН дают 74,5 г КС1 (по уравнению)
Находим массу НС1, которая расходовалась в реакции. Для этого составим пропорцию:
х г НС1 расходуется на 25 г КОН (по условию)
36,5 г НС1 расходуется на 56 г КОН (по уравнению)
Теперь мы можем определить массу НС1, которая осталась неизрасходованной:
m(НС1)осталось послс р-ции = m(НС1)исх. – m(НС1)расх. в р-ции = 20 – 16,3 = 3,7 г.
Итак, в результате добавления 25 г КОН к раствору, содержащему 20 г НС1, образовалось 33,3 г КС1 и осталось 3,7 г неизрасходованной НС1. Таким образом, в итоге получился раствор двух веществ (КС1 и НС1) в воде.
Ответ: m(KCl) = 33,3 г; m(HCl) = 3,7г.
Задача 3.
Теперь рассмотрим обратную ситуацию, когда к раствору НС1 мы добавили больше КОН, чем это необходимо для полной нейтрализации. В этом случае КОН будет в избытке, а НС1 — в недостатке. Посмотрим, какие вещества и в каких количествах будут находиться в растворе после реакции, если к раствору, содержащему 20 г НС1 добавить избыточное количество КОН, например, 40 г.
Дано:
масса хлороводорода: m(НС1) = 20 г;
масса гидроксида калия: m(КОН) = 40 г.
Найти: Массы всех веществ в растворе после реакции.
Решение:
КОН взят в избытке, следовательно, НС1 находится в недостатке. НС1 в реакции израсходуется весь, а КОН частично израсходуется и частично останется. В результате реакции образуется соль КС1. Образующаяся вода разбавит имеющийся раствор. Следовательно, качественный состав раствора после реакции будет следующим:
1. Избыточный гидроксид калия (КОН);
2. Образующаяся соль КС1;
3. Вода в виде растворителя.
Массу образовавшейся соли КС1 можно определить путем расчета по химической реакции, а массу оставшегося КОН по разности:
m(КОН)оставшийся после р-ии = m(КОН)исх – m(КОН)расход в р-ии
Массу расходовавшегося КОН можно определить по уравнению реакции.
Напомним, что в задачах на избыток-недостаток расчет по уравнению реакции всегда ведут по веществу, взятому в недостатке. В данном случае по НС1:
Находим массу образовавшейся соли. Для этого составим пропорцию:
20г НС1 даютуг x г КСl (по условию)
36,5г НС1 дают 74,5 г КС1 (по уравнению)
Находим массу расходовавшегося КОН. Для этого составим пропорцию:
20 г НС1 расходуется на х г КОН (по условию)
36,5 г НС1 расходуется на 56 г КОН (по уравнению)
Теперь мы можем определить массу КОН, который остался неизрасходованным:
m(КОН)остат. = m(КОН)исх. — m(КОН)расх.в р-ии = 40 — 30,7 = 9,3г.
Итак, в результате добавления 40 г КОН к раствору, содержащему 20 г НС1, образовалось 40,8 г КС1 и осталось 9,3 г неизрасходованного КОН. Таким образом, получился раствор двух веществ (КС1 и КОН) в воде.
Комментарии:
1 В условиях задач на определение избытка-недосатка не указывается, какое вещество в избытке, а какое в недостатке. Более того, в условии нет прямого указания на то, что это задача на избыток-недостаток. Поэтому, в первую очередь, перед нами стоит два вопроса:
1. Как отличить задачу на избыток-недостаток от всех остальных задач?
2. Как определить, какое вещество взято в избытке?