Оксид магния MgO — бинарное неорганическое вещество . Белый, тугоплавкий, термически устойчивый, не реагирует с водой. Проявляет основные свойства.
Относительная молекулярная масса Mr = 40,3; относительная плотность для тв. и ж. состояния d = 3,62; tпл ≈ 2825º C; tкип = 3600º C.
- Способ получения
- Химические свойства
- Взаимодействие оксида магния и серной кислоты к какой реакции относится?
- Взаимодействие раствора серной кислоты с магнием относится к реакциям?
- Сколько грамм соли образуется при взаимодействии 4 грамм оксида магния с серной кислотой?
- Помогите с реакциями?
- Составьте уравнение реакции взаимодействия серы с кислородом серы с литием раствор серной кислоты с магнием раствор серной кислоты с оксидом кальция серной кислоты с раствором гидрооксда бария?
- Тип реакции взаимодействия оксида магния с соляной кислотой?
- Водород образуется при взаимодействии : а) соляной кислоты с оксидом меди (II) б) раствора серной кислоты с медью в) раствора серной кислоты с магнием г) соляной кислоты с серебром Напишите уравнение ?
- Коэффициент перед формулой кислоты в реакции взаимодействия оксида алюминия с раствором серной кислоты?
- Серная кислота + оксид магния?
- Какие продукты образуються в реакциях магния и оксиды магния с серной кислотой?
- С какими из перечисленных веществ взаимодействует углекислый газ : серная кислота, водород, вода, известковая вода, оксид магния, кислород, магний?
- Серная кислота
Способ получения
1. Оксид магния получается при разложении карбоната магния при температуре 350 — 650º C. В результате разложения образуется оксид магния и углекислый газ:
2. В результате разложения нитрата магния при температуре выше 300º С образуется оксид магния, оксид азота (IV) и кислород:
3. Гидроксид магния разлагается при 350-480º С с образованием оксида магния и воды:
4. Оксид магния можно получить путем разложения сульфата магния при температуре выше 1200º C, образуется оксид магния, кислород и оксид серы (IV):
5. Оксид магния можно получить сжиганием магния в в кислороде при 600 — 650º С:
2Mg + O2 = 2MgO
Химические свойства
1. Оксид магния реагирует с простыми веществами :
1.1. В результате реакции между оксидом магния и кальцием при температуре выше 400º С образуется магний и оксид кальция:
MgO + Ca = CaO + Mg
1.2. Оксид магния реагирует с углеродом при температуре выше 2000º С и образует магний и угарный газ:
MgO + C = Mg + CO
2. Оксид магния взаимодействует со сложными веществами:
2.1. Оксид магния взаимодействует с кислотами . При этом образуются соль и вода.
2.1.1. О ксид магния с разбавленной соляной кислотой образует хлорид магния и воду:
MgO + 2HCl = MgCl2 + H2O
2.3. Оксид магния взаимодействует с водой при 100 — 125º С, образуя гидроксид магния:
Взаимодействие оксида магния и серной кислоты к какой реакции относится?
Химия | 5 — 9 классы
Взаимодействие оксида магния и серной кислоты к какой реакции относится?
MgO + H2SO4 = MgSO4 + H2O реакция обмена.
Взаимодействие раствора серной кислоты с магнием относится к реакциям?
Взаимодействие раствора серной кислоты с магнием относится к реакциям.
Сколько грамм соли образуется при взаимодействии 4 грамм оксида магния с серной кислотой?
Сколько грамм соли образуется при взаимодействии 4 грамм оксида магния с серной кислотой.
Помогите с реакциями?
Помогите с реакциями!
Магний + соляная кислота Магний + серная кислота Оксид меди 3 + серная кислота Азотная кислота + оксид углерода Сульфат натрия + соляная кислота Гидрооксид бория + фосфорная кислота.
Составьте уравнение реакции взаимодействия серы с кислородом серы с литием раствор серной кислоты с магнием раствор серной кислоты с оксидом кальция серной кислоты с раствором гидрооксда бария?
Составьте уравнение реакции взаимодействия серы с кислородом серы с литием раствор серной кислоты с магнием раствор серной кислоты с оксидом кальция серной кислоты с раствором гидрооксда бария.
Тип реакции взаимодействия оксида магния с соляной кислотой?
Тип реакции взаимодействия оксида магния с соляной кислотой.
Водород образуется при взаимодействии : а) соляной кислоты с оксидом меди (II) б) раствора серной кислоты с медью в) раствора серной кислоты с магнием г) соляной кислоты с серебром Напишите уравнение ?
Водород образуется при взаимодействии : а) соляной кислоты с оксидом меди (II) б) раствора серной кислоты с медью в) раствора серной кислоты с магнием г) соляной кислоты с серебром Напишите уравнение реакции.
Коэффициент перед формулой кислоты в реакции взаимодействия оксида алюминия с раствором серной кислоты?
Коэффициент перед формулой кислоты в реакции взаимодействия оксида алюминия с раствором серной кислоты.
Серная кислота + оксид магния?
Серная кислота + оксид магния.
Какие продукты образуються в реакциях магния и оксиды магния с серной кислотой?
Какие продукты образуються в реакциях магния и оксиды магния с серной кислотой?
К какому типу относиться эти ракции?
С какими из перечисленных веществ взаимодействует углекислый газ : серная кислота, водород, вода, известковая вода, оксид магния, кислород, магний?
С какими из перечисленных веществ взаимодействует углекислый газ : серная кислота, водород, вода, известковая вода, оксид магния, кислород, магний.
Напишите уравнения возможных реакций.
Если вам необходимо получить ответ на вопрос Взаимодействие оксида магния и серной кислоты к какой реакции относится?, относящийся к уровню подготовки учащихся 5 — 9 классов, вы открыли нужную страницу. В категории Химия вы также найдете ответы на похожие вопросы по интересующей теме, с помощью автоматического «умного» поиска. Если после ознакомления со всеми вариантами ответа у вас остались сомнения, или полученная информация не полностью освещает тематику, создайте свой вопрос с помощью кнопки, которая находится вверху страницы, или обсудите вопрос с посетителями этой страницы.
AgCl молярная масса = 108 + 35, 5 = 143, 5г / моль в 143, 5г хлорида содержится 35, 5 г хлора в 0, 5413 г — хг х = 0, 5413 * 35, 5 / 143, 5 = 0, 1339 г.
Ba(OH)2 + CuCL2 — — >BaCL + Cu(OH)2↓ 2OH — + Cu²⁺ — — >Cu(OH)2 Mg(NO3)2 + CaCL2≠ Na2CO3 + H2SO4 — — >Na2SO4 + H2O + CO2 CO⁻²₃ + 2H⁺ — — >H2O + CO2.
Дано : m(C) = 250 r + H2 Найти : V(CH4) — ? M(C) = 12 г / моль n = m / M n = 250 г / 12 г / моль = 20, 833 моль Vm = 22, 4 л / моль С + 2Н2 = СН4 Из УХР следует, что n(CH4) = n(C) n(CH4) = 20, 833 моль V = n * Vm V(CH4) = 20, 833 моль * 22, 4 л / мо..
Дано m(C) = 250 g H2 — — — — — — — — — — — — — — — V(CH4) — ? 250 X C + 2H2 — — >CH4 M(C) = 12 g / mol , Vm = 22. 4L / mol 12 22. 4 X = 250 * 22. 4 / 12 X = 466. 67 L ответ 466. 67 л.
1. 5NaI + NaIO3 + 3H2SO4 = 3I2 + 3Na2SO4 + 3H2O 2. 3KNO2 + KCLO3 = KCL + 3KNO3 4. 3C + 4HNO3 = 3CO2 + 4NO + 2H2O.
SiO₂ + 2Mg = Si + 2MgO 2Ca (изб. ) + Si = Ca₂Si Ca₂Si + 4HCl = CaCl₂ + SiH₄↑ SiH₄ + 2O₂ = SiO₂ + 2H₂O SiO₂ + 2Mg = Si + 2MgO.
Дано : m(Fe2O3) = 16 г Найти : V(H2) — ? M(Fe2O3) = 160 г / моль n(Fe2O3) = m / M = 16 г / 160 г / моль = 0, 1 моль Fe2O3 + 3H2 = 2Fe + 3H2O Из УХР следует, что n(H2) = 3n(Fe2O3) n(H2) = 3 * 0. 1 моль = 0, 3 моль V(H2) = n * Vm = 0, 3 моль * 22, 4 ..
Решение на листочке — — — — — — — -.
Хл 0, 5моль Н2 + CI2 = 2HCI Х = 22, 4 * 0, 5 22, 4л 1моль — — — — — — — — — — — = 11, 2 л.
Серная кислота
Серная кислота — сильная двухосновная кислота, при н.у. маслянистая жидкость без цвета и запаха.
Обладает выраженным дегидратационным (водоотнимающим) действием. При попадании на кожу или слизистые оболочки приводит к тяжелым ожогам.
Замечу, что существует олеум — раствор SO3 в безводной серной кислоте, дымящее жидкое или твердое вещество. Олеум применяется при изготовлении красителей, органическом синтезе и в производстве серной кислот.
Получение
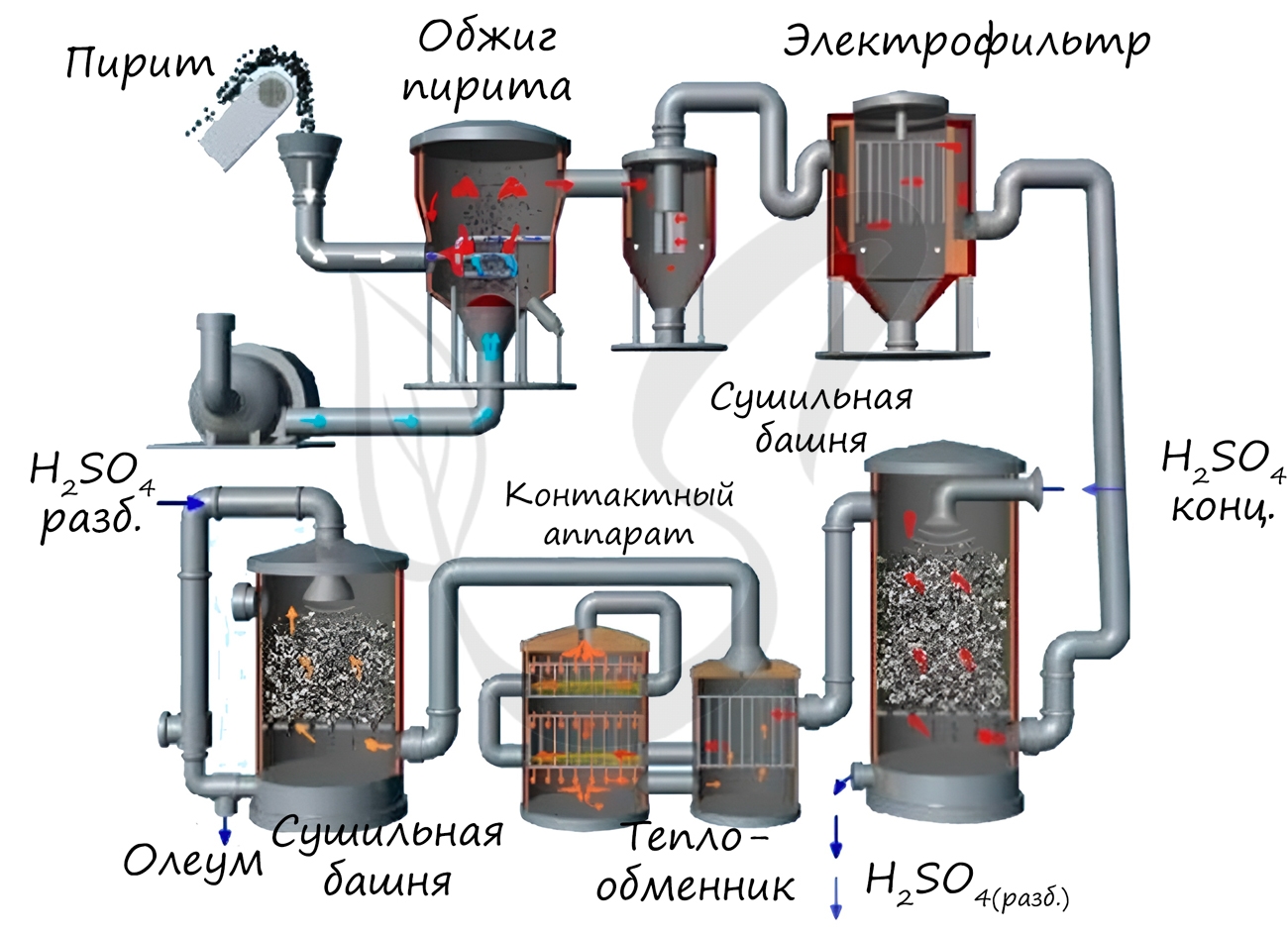
Известны несколько способов получения серной кислоты. Применяется промышленный (контактный) способ, основанный на сжигании пирита, окислении образовавшегося SO2 до SO3 и последующим взаимодействием с водой.
Нитрозный способ получения основан на взаимодействии сернистого газа с диоксидом азота IV в присутствии воды. Он состоит из нескольких этапов:
В окислительной башне смешивают оксиды азота (II) и (IV) с воздухом:
Смесь газов подается в башни, орошаемые 75-ной% серной кислотой, здесь смесь оксидов азота поглощается с образованием нитрозилсерной кислоты:
В ходе гидролиза нитрозилсерной кислоты получают азотистую кислоту и серную:
В упрощенном виде нитрозный способ можно записать так:
Химические свойства
- Кислотные свойства
В водном растворе диссоциирует ступенчато.
Сильная кислота. Реагирует с основными оксидами, основаниями, образуя соли — сульфаты.
KOH + H2SO4 = KHSO4 + H2O (гидросульфат калия, соотношение 1:1 — кислая соль)
2KOH + H2SO4 = K2SO4 + 2H2O (сульфат калия, соотношение 2:1 — средняя соль)
С солями реакция идет, если в результате выпадает осадок, образуется газ или слабый электролит (вода). Серная кислота, как и многие другие кислоты, способна растворять осадки.
Серная кислота окисляет неметаллы — серу и углерод — соответственно до угольной кислоты (нестойкой) и сернистого газа.
Реакции с металлами
Реакции разбавленной серной кислоты с металлами не составляют никаких трудностей: она реагирует как самая обычная кислота, например HCl. Все металлы, стоящие до водорода, вытесняют из серной кислоты водород, а стоящие после — не реагируют с ней.
Подчеркну, что реакции разбавленной серной кислоты с железом и хромом не сопровождаются переходом этих элементов в максимальную степень окисления. Они окисляются до +2.
Cu + H2SO4(разб.) ⇸ (реакция не идет, медь не может вытеснить водород из кислоты)
Концентрированная серная кислота ведет себя совершенно по-иному. Водород никогда не выделяется, вместо него с активными металлами выделяется H2S, с металлами средней активности — S, с малоактивными металлами — SO2.
Холодная концентрированная серная кислота пассивирует Al, Cr, Fe, Ni, Be, Co. При нагревании или амальгамировании данных металлов реакция идет.
Обратите особое внимание, что при реакции железа, хрома с концентрированной серной кислотой достигается степень окисления +3. В подобных реакциях с разбавленной серной кислотой (написаны выше) достигается степень окисления +2.
Иногда в тексте задания даны подсказки. Например, если написано, что выделился газ с неприятным запахом тухлых яиц — речь идет об H2S, если же написано, что выделилось простое вещество — речь о сере (S).
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.