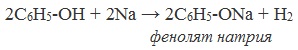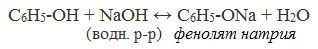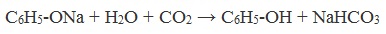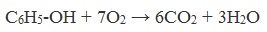Гидроксисоединения – это органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Гидроксисоединения делят на спирты и фенолы.
| Спирты – это гидроксисоединения, в которых группа ОН соединена с алифатическим углеводородным радикалом R-OH. Если гидроксогруппа ОН соединена с бензольным кольцом, то вещество относится к фенолам. |
Общая формула предельных нециклических спиртов: CnH2n+2Om, где m ≤ n.
- Классификация фенолов
- По числу гидроксильных групп:
- Строение фенолов
- Химические свойства фенолов
- 1.1. Взаимодействие с раствором щелочей
- 1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
- 2. Реакции фенола по бензольному кольцу
- 2.1. Галогенирование
- 2.2. Нитрование
- 3. Поликонденсация фенола с формальдегидом
- 4. Взаимодействие с хлоридом железа (III)
- 5. Гидрирование (восстановление) фенола
- Получение фенолов
- 1. Взаимодействие хлорбензола с щелочами
- 2. Кумольный способ
- 3. Замещение сульфогруппы в бензол-сульфокислоте
- Взаимодействие фенола с калием уравнение реакции
- I. Реакции с участием гидроксильной группы
- II . Реакции, с участием бензольного кольца
- III. Реакция окисления
- IV. Качественная реакция! — обнаружение фенола
- Напишите уравнение реакций : 1) дегидратация бутанола — 1 2) фенол + калий 3) фенол + гидроксид калия 4) фенол + бром 5) фенол + азотная кислота?
- Напишите уравнение реакции бромбензол фенол пикриновая кислота?
- Фенол не реагирует с 1?
- Вычислите массу фенолята калия, полученного при взаимодействии фенола с 1, 12г гидроксида калия?
- Как распознать этиловый спирт от фенола ?
- Напишите уравнения реакции доказывающие что фенол слабая кислота?
- Какую массу фенолята калия можно получить при взаимодействие 188 г фенола с гидроксидом калия?
- Напишите уравнение реакций : 1) дегидратация бутанола — 1 2) фенол + калий 3) фенол + гидроксид калия 4) фенол + бром 5) фенол + азотная кислота?
- Хлорбензол + азотная кислота Фенол + водород Уравнение?
- Фенол образует белый осадок при взаимодействии с А) бромной водой Б) азотной кислотой В) гидроксидом калия Г) аммиаком?
- Составить уравнения фенола с натрием, гидроксидом натрия, с бромной водой, азотной кислотой?
Классификация фенолов
По числу гидроксильных групп:
- фенолы с одной группой ОН — содержат одну группу -ОН. Общая формула CnH2n-7OH или CnH2n-6O.
- фенолы с двумя группами ОН — содержат две группы ОН. Общая формула CnH2n-8(OH)2 или CnH2n-6O2.
| Соединения, в которых группа ОН отделена от бензольного кольца углеродными атомами – это не фенолы, а ароматические спирты: |
Строение фенолов
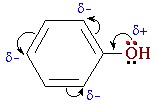
В фенолах одна из неподеленных электронных пар кислорода участвует в сопряжении с π–системой бензольного кольца, это является главной причиной отличия свойств фенола от спиртов.
Химические свойства фенолов
| Сходство и отличие фенола и спиртов. |
Сходство: как фенол, так и спирты реагируют с щелочными металлами с выделением водорода.
Отличия:
- фенол не реагирует с галогеноводородами: ОН- группа очень прочно связана с бензольным кольцом, её нельзя заместить;
- фенол не вступает в реакцию этерификации, эфиры фенола получают косвенным путем;
- фенол не вступает в реакции дегидратации.
- фенол обладает более сильными кислотными свойствами и вступает в реакцию со щелочами.
1. Кислотные свойства фенолов
| Фенолы являются более сильными кислотами, чем спирты и вода, т. к. за счет участия неподеленной электронной пары кислорода в сопряжении с π-электронной системой бензольного кольца полярность связи О–Н увеличивается. |
Раствор фенола в воде называют «карболовой кислотой», он является слабым электролитом.
1.1. Взаимодействие с раствором щелочей
В отличие от спиртов, фенолы реагируют с гидроксидами щелочных и щелочноземельных металлов, образуя соли – феноляты.
| Например, фенол реагирует с гидроксидом натрия с образованием фенолята натрия |
Так как фенол – более слабая кислота, чем соляная и даже угольная, его можно получить из фенолята, вытесняя соляной или угольной кислотой:
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Фенолы взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются феноляты. При взаимодействии с металлами фенолы ведут себя, как кислоты.
| Например, фенол взаимодействует с натрием с образованием фенолята натрия и водорода . |
2. Реакции фенола по бензольному кольцу
| Наличие ОН-группы в бензольном кольце (ориентант первого рода) приводит к тому, что фенол гораздо легче бензола вступает в реакции замещения в ароматическом кольце. |
2.1. Галогенирование
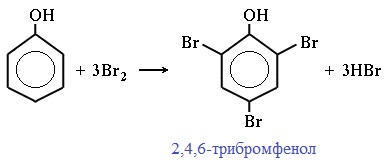
| Фенол легко при комнатной температуре (без всякого катализатора) взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол). |
2.2. Нитрование
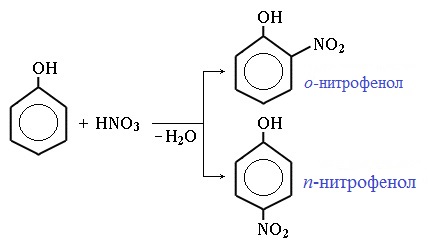
Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов.
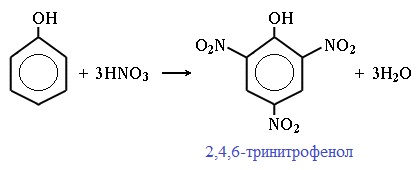
| Например, при нитровании фенола избытком концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота): |
3. Поликонденсация фенола с формальдегидом
С формальдегидом фенол образует фенолоформальдегидные смолы.
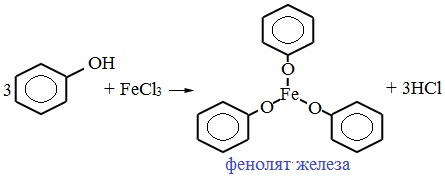
4. Взаимодействие с хлоридом железа (III)
При взаимодействии фенола с хлоридом железа (III) образуются комплексные соединения железа, которые окрашивают раствор в сине-фиолетовый цвет. Это качественная реакция на фенол.
5. Гидрирование (восстановление) фенола
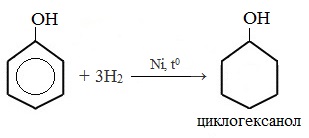
Присоединение водорода к ароматическому кольцу.
Продукт реакции – циклогексанол, вторичный циклический спирт.
Получение фенолов
1. Взаимодействие хлорбензола с щелочами
При взаимодействии обработке хлорбензола избытком щелочи при высокой температуре и давлении образуется водный раствор фенолята натрия.
При пропускании углекислого газа (или другой более сильной кислоты) через раствор фенолята образуется фенол.
2. Кумольный способ
Фенол в промышленности получают из каталитическим окислением кумола.
Первый этап процесса – получение кумола алкилированием бензола пропеном в присутствии фосфорной кислоты:
Второй этап – окисление кумола кислородом. Процесс протекает через образование гидропероксида изопропилбензола:
Суммарное уравнение реакции:
3. Замещение сульфогруппы в бензол-сульфокислоте
Бензол-сульфокислота реагирует с гидроксидом натрия с образованием фенолята натрия:
Получается фенолят натрия, из которого затем выделяют фенол:
Взаимодействие фенола с калием уравнение реакции
Химические свойства фенолов определяются наличием в молекуле гидроксильной группы и бензольного кольца.
I. Реакции с участием гидроксильной группы
Фенолы являются более сильными кислотами, чем спирты и вода, т.к. за счет участия неподеленной электронной пары кислорода в сопряжении с π-электронной системой бензольного кольца полярность связи О–Н увеличивается.
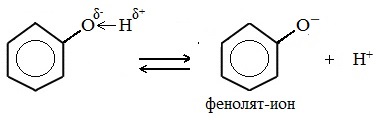
Фенолы в водных растворах диссоциируются по кислотному типу: на фенолят-ионы и ионы водорода:
Фенол диссоциирует обратимо, это слабая кислота. Однако его силы кислотных свойств достаточно, чтобы изменять окраску индикатора, имеющего в нейтральной среде фиолетовый цвет. В растворе фенола лакмус краснеет.
1) Взаимодействие с активными металлами с образованием фенолятов (сходство со спиртами)
Видеоопыт «Взаимодействие фенола с металлическим натрием»
2) Взаимодействие со щелочами с образованием фенолятов (отличие от спиртов)
Видеоопыт «Взаимодействие фенола с раствором щелочи»
Образующиеся в результате реакций феноляты легко разлагаются при действии кислот. Даже такая слабая кислота, как угольная, вытесняет фенол из фенолятов. Следовательно, !Феноляты – соли слабой карболовой кислоты, разлагаются угольной кислотой:
По кислотным свойствам фенол превосходит этанол в 10 6 раз. При этом во столько же раз уступает уксусной кислоте. В отличие от карбоновых кислот, фенол не может вытеснить угольную кислоту из её солей
C6H5-OH + NaHCO3 = реакция не идёт – прекрасно растворяясь в водных растворах щелочей, он фактически не растворяется в водном растворе гидрокарбоната натрия.
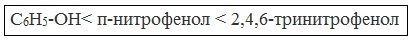
Кислотные свойства фенола усиливаются под влиянием связанных с бензольным кольцом электроноакцепторных групп (NO2 — , Br — )
2,4,6-тринитрофенол или пикриновая кислота сильнее угольной.
3) Образование сложных и простых эфиров
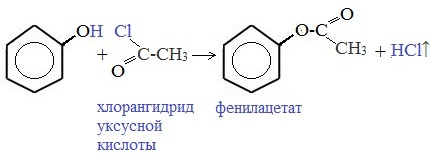
Как и спирты, фенолы могут образовывать простые и сложные эфиры. Фенолы не образуют сложные эфиры в реакциях с кислотами. Сложные эфиры образуются при взаимодействии фенола с ангидридами или хлорангидридами карбоновых кислот:
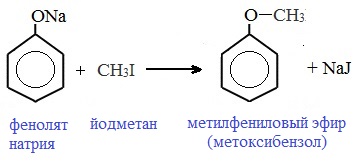
Простые эфиры образуются при взаимодействии фенолятов с алкилгалогенидами:
II . Реакции, с участием бензольного кольца
Взаимное влияние атомов в молекуле фенола проявляется не только в особенностях поведения гидроксигруппы, но и в большей реакционной способности бензольного ядра. Гидроксильная группа повышает электронную плотность в бензольном кольце, особенно, в орто- и пара- положениях (+ М -эффект ОН-группы):
Поэтому фенол значительно активнее бензола вступает в реакции электрофильного замещения в ароматическом кольце.
Реакции замещения
1) Нитрование
Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара- нитрофенолов:
При использовании концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота):
У нее кислотные свойства выражены сильнее, чем у фенола, т.к. нитрогруппы оттягивают электронную плотность от бензольного кольца и делают связь О-Н еще более полярной.
Пикриновая кислоты является взрывчатым веществом, в чистом виде представляет собой желтые кристаллы.
2) Галогенирование
Фенол легко при комнатной температуре взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола ( качественная реакция на фенол! ):
Образуется белый осадок трибромфенола.
Видеоопыт «Взаимодействие фенола с бромной водой»
3) Сульфирование
Соотношение о- и п-изомеров определяется температурой реакции: при комнатной температуре в основном образуется о-фенолсульфокислота, при t=1000С – пара-изомер: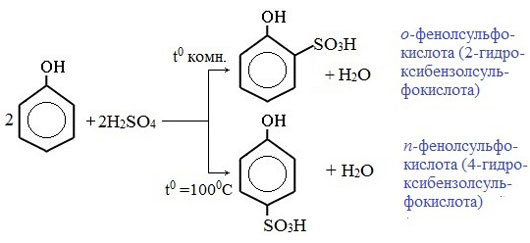
1) Гидрирование фенола
Эта реакция идет с разрушением ароматического кольца. Продукт реакции циклический одноатомный спирт — циклогексиловый спирт (циклогексанол).
2) Конденсация с альдегидами
При нагревании фенола с формальдегидом в присутствии кислотных или основных катализаторов происходит реакция поликонденсации и образуется фенолформальдегидная смола.
Данная реакция имеет большое практическое значение и используется при получении фенолформальдегидных смол.
III. Реакция окисления
Фенолы легко окисляются даже под действием кислорода воздуха. При стоянии на воздухе фенол постепенно окрашивается в розовато-красный цвет.
1) Горение (полное окисление)
Фенолы, как и большинство органических веществ, сгорают до углекислого газа и воды.
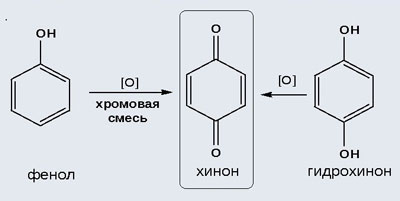
2) Окисление хромовой смесью
При энергичном окислении фенола хромовой смесью основным продуктом окисления является хинон. Двухатомные фенолы окисляются еще легче. При окислении гидрохинона также образуется хинон:
IV. Качественная реакция! — обнаружение фенола
Для обнаружения фенолов используется качественная реакция с хлоридом железа (III). Одноатомные фенолы дают устойчивое сине-фиолетовое окрашивание, что связано с образованием комплексных соединений железа.
Видеоопыт «Качественная реакция на фенол»
Образование фиолетового окрашивания при добавлении раствора FeCl3 служит качественной реакцией на фенол:
Для фенолов реакции по связям С-О не характерны, поскольку атом кислорода прочно связан с атомом углерода бензольного кольца за счет участия своей неподеленной электронной пары в системе сопряжения.
Напишите уравнение реакций : 1) дегидратация бутанола — 1 2) фенол + калий 3) фенол + гидроксид калия 4) фенол + бром 5) фенол + азотная кислота?
Химия | 10 — 11 классы
Напишите уравнение реакций : 1) дегидратация бутанола — 1 2) фенол + калий 3) фенол + гидроксид калия 4) фенол + бром 5) фенол + азотная кислота.
1) дегидратация бутанола — 1
CH3 — CH2 — CH2 — CH2 — OH = CH2 = CH — CH2 — CH2 — CH3 + H2O
2C6H5OH + 2K = 2C6H5OK + H2
3) фенол + гидроксид калия
C6H5OH + KOH = C6H5OK + H2O
C6H5OH + 3Br2 = C6H2Br3(OH) + 3HBr
5) фенол + азотная кислота
C6H5OH + 3HNO3 = C6H2(NO2)3OH + 3H2O.
Напишите уравнение реакции бромбензол фенол пикриновая кислота?
Напишите уравнение реакции бромбензол фенол пикриновая кислота.
Фенол не реагирует с 1?
Фенол не реагирует с 1.
Гидроксидом калия 3.
Вычислите массу фенолята калия, полученного при взаимодействии фенола с 1, 12г гидроксида калия?
Вычислите массу фенолята калия, полученного при взаимодействии фенола с 1, 12г гидроксида калия.
Как распознать этиловый спирт от фенола ?
Как распознать этиловый спирт от фенола ?
Ответ подтвердите уравнениями реакции.
Задача : какая масса фенолята калия образуется при взаимодействии 14, 1 г.
Фенола со 120 г.
10% — ного раствора гидроксида калия?
Напишите уравнения реакции доказывающие что фенол слабая кислота?
Напишите уравнения реакции доказывающие что фенол слабая кислота.
Какую массу фенолята калия можно получить при взаимодействие 188 г фенола с гидроксидом калия?
Какую массу фенолята калия можно получить при взаимодействие 188 г фенола с гидроксидом калия?
Напишите уравнение реакций : 1) дегидратация бутанола — 1 2) фенол + калий 3) фенол + гидроксид калия 4) фенол + бром 5) фенол + азотная кислота?
Напишите уравнение реакций : 1) дегидратация бутанола — 1 2) фенол + калий 3) фенол + гидроксид калия 4) фенол + бром 5) фенол + азотная кислота.
Хлорбензол + азотная кислота Фенол + водород Уравнение?
Хлорбензол + азотная кислота Фенол + водород Уравнение.
Фенол образует белый осадок при взаимодействии с А) бромной водой Б) азотной кислотой В) гидроксидом калия Г) аммиаком?
Фенол образует белый осадок при взаимодействии с А) бромной водой Б) азотной кислотой В) гидроксидом калия Г) аммиаком.
Составить уравнения фенола с натрием, гидроксидом натрия, с бромной водой, азотной кислотой?
Составить уравнения фенола с натрием, гидроксидом натрия, с бромной водой, азотной кислотой.
Получение фенола в промышленности ( реакция гидролиза хлорбензола).
Вы открыли страницу вопроса Напишите уравнение реакций : 1) дегидратация бутанола — 1 2) фенол + калий 3) фенол + гидроксид калия 4) фенол + бром 5) фенол + азотная кислота?. Он относится к категории Химия. Уровень сложности вопроса – для учащихся 10 — 11 классов. Удобный и простой интерфейс сайта поможет найти максимально исчерпывающие ответы по интересующей теме. Чтобы получить наиболее развернутый ответ, можно просмотреть другие, похожие вопросы в категории Химия, воспользовавшись поисковой системой, или ознакомиться с ответами других пользователей. Для расширения границ поиска создайте новый вопрос, используя ключевые слова. Введите его в строку, нажав кнопку вверху.
Дано m(SO3) = 8 g Na2O — — — — — — — — — — — — — — — m(Na2SO4) — ? 8 X SO3 + Na2O — — >Na2SO4 M(SO3) = 80 g / mol M(Na2SO4) = 142 g / mol 80 142 8 / 80 = x / 142 X = 14. 2 g ответ 14. 2 г.
8 г Х г SO3 + Na2O — > Na2SO4 n = 1 моль n = 1 моль М = 80 г / моль М = 142 г / моль m = 80 г m = 142 г 8 г SO3 — Х г Na2SO4 80 г SO3 — 142 г Na2SO4 m(Na2SO4) = 8 * 142 / 80 = 14, 2 г.
Zn — >K2ZnO2 — >ZnSO4 — >K2[Zn(OH)4] — >Zn(NO3)2 — >ZnO 1)4Zn + KNO3 + 7KOH = NH3 + 4K2ZnO2 + 2H2O 2)K2ZnO2 + 2H2SO4 = K2SO4 + ZnSO4 + 2H2O 3)ZnSO4 + 4KOH = K2[Zn(OH)4] + K2SO4 4)K2[Zn(OH)4] + 4HNO3 = 2KNO3 + Zn(NO3)2 + 4H2O 5)2Zn(NO3)2 = 2ZnO + 4NO2..
Ca + H2O = Ca(OH)2 + H2n(Ca) = 6 г / моль : 40 г = 0, 15 мольV(Ca) = 0, 15моль * 22, 4 л / моль = 3, 36л3, 36л — 100%3 л — х%х = 89%.
Дано : Жк₁ = 11 мг — экв / л Жк₂ = 3 мг — экв / л Vв = 100 м³ Найти : m(Ca(OH)₂) Решение. Переведем единицы заданияв более удобные мг — экв / л = г — экв / м³ Снизить карбонатную жесткость с 11 г — экв / м³до 3г — экв / м³ — значит убрать из каждого..
Масса О2 = 0, 888. Если реак. 2Fe + O2 = 2FeO.
1 — Ответ 6NaOH + Al2O3 + 3H2O = 2Na3[Al(OH)6] NaOH + HCl = H2O + NaCl.
2) CH3 — CH2 — CH(CH3) — CH(CH2 — CH3) — CH2 — CH2 — CH3 3) CH3 — CH2 — CH2 — Cl + 2Na + Cl — CH2 — CH2 — CH3 — > CH3 — CH2 — CH2 — CH2 — CH2 — CH3 + 2NaCl.
Ca — 2e = Ca( + 2) коэффициент 4 Восстановитель, окисление 2N( + 5) + 8e = 2 N ( + 1) коэффициент 1 Окислитель, восстановление 4Ca + 10HNO3 = 4Ca(NO3)2 + N2O + 5H2O Если помог, нажми кнопку Спасибо)).