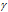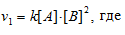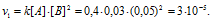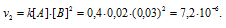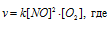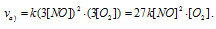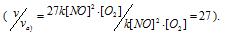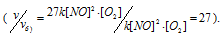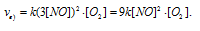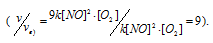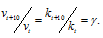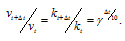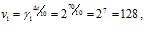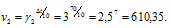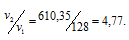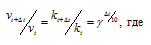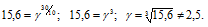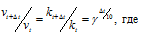Вопрос по химии:
Вычислить скорость химической реакции, протекающей по уравнению 2А(газ) +
B(газ) -> 2AB(газ), если исходная концентрация в-ва А — 0,05
моль(л), В — 0,03 моль(л), а константа скорости реакции 1л/моль * с.
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок — бесплатно!
- Как написать хороший ответ?
- Вычислить скорость химической реакции, протекающей по уравнению 2А(газ) + B(газ) — > ; 2AB(газ), если исходная концентрация в — ва А — 0, 05 моль(л), В — 0, 03 моль(л), а константа скорости реакции ?
- Реакция протекает по уравнению 2A + B = 2C?
- Химическая реакция протекает в растворе согласно уравнению А + В = С?
- Некоторая реакция, отображаемая равнением 2А + Х + А2Х, протекает в растворе?
- Для реакции А + 2В = С + 2D константа скорости К = 10⁻⁶л² / моль²∙с, концентрации веществ А и В равны соответственно 0, 6 моль / л, 1 моль / л?
- Для реакции 2so2 + o2 < ; = > ; 2so3 начальные концентрации исходных веществ были равны 1, 6 моль / л — so2 и 1, 2 моль / л — o2?
- Помогите 30 баллов Вычислите скорость химической реакции А + Б = АБ, если через 10 с после начала реакции концентрация вещества А составляла 0, 025 моль / л, а через 20 с — 0, 015 моль / л?
- ПРОШУ, СРОЧНО НУЖНА ВАША ПОМОЩЬ?
- Вычислите среднюю скорость реакции , если начальная концентрация исходного вещества была равно 10 моль / л а через 4 мин стаала 2 моль / л?
- Через 25 с после начала реакции концентрация одного из исходных веществ составила 0, 5 моль / л, а через 50 с стала 0, 1 моль / л?
- 2. Рассчитать скорость химической реакции синтеза аммиака при 623 К, если концентрация [H2] = 1, 2 моль / л, а [N2]?
- Расчеты изменения скорости реакции
Ответы и объяснения 1
V=k*[a]^n*[b]^n где n стехиометрический коэффициент при веществе
V=1*0,05^2*0,03=0,00075
Спасибо за задачу.
Знаете ответ? Поделитесь им!
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете правильный ответ;
- Писать подробно, чтобы ответ был исчерпывающий и не побуждал на дополнительные вопросы к нему;
- Писать без грамматических, орфографических и пунктуационных ошибок.
Этого делать не стоит:
- Копировать ответы со сторонних ресурсов. Хорошо ценятся уникальные и личные объяснения;
- Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не знаю» и так далее;
- Использовать мат — это неуважительно по отношению к пользователям;
- Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
Вычислить скорость химической реакции, протекающей по уравнению 2А(газ) + B(газ) — > ; 2AB(газ), если исходная концентрация в — ва А — 0, 05 моль(л), В — 0, 03 моль(л), а константа скорости реакции ?
Химия | 10 — 11 классы
Вычислить скорость химической реакции, протекающей по уравнению 2А(газ) + B(газ) — > ; 2AB(газ), если исходная концентрация в — ва А — 0, 05 моль(л), В — 0, 03 моль(л), а константа скорости реакции 1л / моль * с.
V = k * [a] ^ n * [b] ^ n где n стехиометрический коэффициент при веществе
V = 1 * 0, 05 ^ 2 * 0, 03 = 0, 00075
Спасибо за задачу.
Реакция протекает по уравнению 2A + B = 2C?
Реакция протекает по уравнению 2A + B = 2C.
В начале реакции концентрации реагирующих веществ одинаковы и равны 1 моль / л, через 1 мин концентрация вещества B стала 0, 6 моль / л.
Какой стала концентрация A и C?
Какова скорость этой реакции по веществу B?
Химическая реакция протекает в растворе согласно уравнению А + В = С?
Химическая реакция протекает в растворе согласно уравнению А + В = С.
Исходные концентрации веществ : А – 2, 7 моль / л, В – 2, 5 моль / л.
Определите концентрацию вещества С через 30 мин и среднюю скорость реакции за этот промежуток времени, если концентрация вещества В снизилась до 2, 2 моль / л.
Некоторая реакция, отображаемая равнением 2А + Х + А2Х, протекает в растворе?
Некоторая реакция, отображаемая равнением 2А + Х + А2Х, протекает в растворе.
Исходная концентрация А была = 2 моль / л.
Через 5 минут концентрация вещества А составляла 0, 4 моль / л.
Вычислите среднюю скорость реакции за указанный промежуток времени.
Во сколько раз изменится концентрация вещества Х за то же время?
Для реакции А + 2В = С + 2D константа скорости К = 10⁻⁶л² / моль²∙с, концентрации веществ А и В равны соответственно 0, 6 моль / л, 1 моль / л?
Для реакции А + 2В = С + 2D константа скорости К = 10⁻⁶л² / моль²∙с, концентрации веществ А и В равны соответственно 0, 6 моль / л, 1 моль / л.
Вычислите скорость этой реакции.
Для реакции 2so2 + o2 < ; = > ; 2so3 начальные концентрации исходных веществ были равны 1, 6 моль / л — so2 и 1, 2 моль / л — o2?
Для реакции 2so2 + o2 < ; = > ; 2so3 начальные концентрации исходных веществ были равны 1, 6 моль / л — so2 и 1, 2 моль / л — o2.
Вычислите константу равновесия этой реакции если равновесная концентрация SO3 равна 0, 6 моль / л.
Помогите 30 баллов Вычислите скорость химической реакции А + Б = АБ, если через 10 с после начала реакции концентрация вещества А составляла 0, 025 моль / л, а через 20 с — 0, 015 моль / л?
Помогите 30 баллов Вычислите скорость химической реакции А + Б = АБ, если через 10 с после начала реакции концентрация вещества А составляла 0, 025 моль / л, а через 20 с — 0, 015 моль / л.
ПРОШУ, СРОЧНО НУЖНА ВАША ПОМОЩЬ?
ПРОШУ, СРОЧНО НУЖНА ВАША ПОМОЩЬ!
Определите среднюю скорость химической реакции, если за 20 сек протекания химической реакции концентрация исходного вещества уменьшилась с 0.
12 моль / л до 0.
Вычислите среднюю скорость реакции , если начальная концентрация исходного вещества была равно 10 моль / л а через 4 мин стаала 2 моль / л?
Вычислите среднюю скорость реакции , если начальная концентрация исходного вещества была равно 10 моль / л а через 4 мин стаала 2 моль / л.
Через 25 с после начала реакции концентрация одного из исходных веществ составила 0, 5 моль / л, а через 50 с стала 0, 1 моль / л?
Через 25 с после начала реакции концентрация одного из исходных веществ составила 0, 5 моль / л, а через 50 с стала 0, 1 моль / л.
Вычислите среднюю скорость реакции.
2. Рассчитать скорость химической реакции синтеза аммиака при 623 К, если концентрация [H2] = 1, 2 моль / л, а [N2]?
2. Рассчитать скорость химической реакции синтеза аммиака при 623 К, если концентрация [H2] = 1, 2 моль / л, а [N2].
Константа скорости реакции при этой температуре k = 12000.
На этой странице находится ответ на вопрос Вычислить скорость химической реакции, протекающей по уравнению 2А(газ) + B(газ) — > ; 2AB(газ), если исходная концентрация в — ва А — 0, 05 моль(л), В — 0, 03 моль(л), а константа скорости реакции ?, из категории Химия, соответствующий программе для 10 — 11 классов. Чтобы посмотреть другие ответы воспользуйтесь «умным поиском»: с помощью ключевых слов подберите похожие вопросы и ответы в категории Химия. Ответ, полностью соответствующий критериям вашего поиска, можно найти с помощью простого интерфейса: нажмите кнопку вверху страницы и сформулируйте вопрос иначе. Обратите внимание на варианты ответов других пользователей, которые можно не только просмотреть, но и прокомментировать.
M(H2SO4) = 200 г * 0, 3 = 60 г m(H2O) = 200 мл * 1 г / мл = 200 г m»(p. H2SO4) = 200 г + 200 г = 400 г ω»(H2SO4) = 60 г / 400 г = 0, 15 або 15% Відповідь : 15%.
Решение в прикрепленном файле.
Ме2О = 17% имеет кислород 83% имеет неизвестный металл 17% — — — — — 16г / моль 100% — — х г / моль 100 * 16 = 1600 / 17 = 94г / моль m(Me2) = 94 — 16 = 78 г / моль 78 / 2 = 39( К ) Ответ : К2О.
Н3С — С = С — СН3 2 — метилбутен — 2 СН3 1) Н2С = С — СН2 — СН3 изомерия СН3. Положения кратной всязи.
Si + 2NaOH + H2O = Na2SiO3 + 2H2 По реакции 1 моль (28 г) кремния дает 44, 8 л водорода. Чтобы выделилось 5, 6 л надо х г кремния. Составляем пропорцию : 28 — 44, 8 х — 5, 6 х = 28 * 5, 6 / 44, 8 = 3, 5 г Т. К. примеси составляют 8% нужно взять 3.
W(BaCl2)в кристаллогидрате BaCl2 * 2H2O = 208 / 244 = 0, 85 m(BaCl2) = 20 * 0, 85 = 17г m(H2O) = 180мл * 1г / мл = 180г m(р — ра) = 20 + 180 = 200г W(Ba Cl2) в р — ре = 17 / 200 = 0, 085(8, 5%).
1)2Cu + O2 = 2CuO (Реакция соединения) 2)CaCO3 = CaO + CO2 ( реакция разложения) 3)Fe + 2HCI = FECI2 + H2 (реакция замещения).
Расчеты изменения скорости реакции
Задача 331.
Реакция между веществами А и В выражается уравнением: А + 2В → С. Начальные концентрации составляют: [А]0 = 0,03 моль/л, [В]0 = 0,05 моль/л. Константа скорости реакции равна 0,4. Найти начальную скорость реакции и скорость реакции по истечении некоторого времени, когда концентрация вещества А уменьшится на 0,01 моль/л.
Решение:
До изменения концентрации скорость реакции можно выразить уравнением:
v — скорость реакции, k — константа скорости реакции, [А] и [В] – концентрации исходных веществ.
Для нахождения скорости реакции по истечении некоторого времени учтём, что на образование 1 моля вещества С затрачивается 1 моль вещества А и 2 моля вещества В, поэтому при уменьшении концентрации вещества А на 0,01 моль/л, концентрация вещества В уменьшится соответственно на 0,02 моль/л (2 . 0.01 = 0,02). Тогда оставшиеся концентрации веществ будут равны [A]ост. = 0.03 – 0,01 = 0,02 моль/л, [B]ост. = 0,05 – 0,02 = 0,03моль/л. Тогда скорость реакции по истечении некоторого времени будет составлять:
Ответ: v1 = 3 . 10 -5 ; v2 = 7,2 . 10 -6 .
Задача 332.
Как изменится скорость реакции 2NO (г.) + O2 (г.) → 2NO2 (г.), если: а) увеличить давление в системе в 3 раза; б) уменьшить объем системы в 3 раза; в) повысить концентрацию в 3 раза?
Решение:
До изменения объёма, давления и концентрации скорость реакции можно выразить уравнением:
а) Вследствие увеличения давления в системе в 3 раза, соответственно концентрация каждого из реагирующих веществ возрастёт в 3 раза. Следовательно, теперь скорость реакции будет равна:
Тогда, сравнивая выражения v и vа) , находим, что скорость реакции возрастает в 27 раз
б) при уменьшении объёма в 3 раза в системе концентрация каждого из реагирующих веществ возрастёт в 3 раза. Следовательно, теперь скорость реакции будет равна:
Тогда, сравнивая выражения v и vб), находим, что скорость реакции возрастает в 27 раз
в) При увеличении концентрации NO в 3 раза скорость реакции будет равна:
Cравнивая выражения v и vв), находим, что скорость реакции возрастает в 9 раз
Ответ: а) возрастёт в 27 раз; б) возрастёт в 27 раз; в) возрастёт в 9 раз.
Задача 333.
Две реакции протекают при 25 °С с одинаковой скоростью. Температурный коэффициент скорости первой реакции равен 2,0, а второй 2,5. Найти отношение скоростей этих реакций при 95°С.
Решение:
Зависимость скорости реакции (или константы скорости реакции) от температуры может быть выражена уравнением:
Здесь vt и kt — скорость и константа скорости реакции при температуре t °С; v(t + 10) и k(t + 10) те же величины при температуре (t + 10 °С); 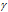
Поскольку 
Скорость второй реакции равна:
Найдём отношение этих скоростей:
Ответ:
Задача 334.
Чему равен температурный коэффициент скорости реакции, если при увеличении температуры на 30 градусов скорость реакции возрастает в 15,6 раза?
Решение:
Согласно правилу Вант Гоффа зависимость скорости реакции от температуры выражается уравнением:
vt и kt — скорость и константа скорости реакции при температуре t °С; v(t + 10) и k(t + 10) те же величины при температуре (t + 10 °С); 

Ответ: 2,5.
Задача 335.
Температурный коэффициент скорости некоторой реакции равен 2,3. Во сколько раз увеличится скорость этой реакции, если повысить температуру на 25 градусов?
Решение:
Согласно правилу Вант Гоффа зависимость скорости реакции от температуры выражается уравнением:
vt и kt — скорость и константа скорости реакции при температуре t °С; v(t + 10) и k(t + 10) те же величины при температуре (t + 10 °С);