— это реакции, протекающие с изменением степеней окисления элементов. В ходе таких реакций происходит отдача (отрыв) электронов от одного элемента и присоединение их к другому.
Важно запомнить следующие термины: окислитель, восстановитель, окисление, восстановление
Процесс отдачи электронов атомом называется окислением, при этом степень окисления этого элемента повышается (он — восстановитель)
Процесс присоединения электронов атомом называется восстановлением, при этом степень окисления этого элемента снижается (он — окислитель)
Восстановитель — это элемент, степень окисления которого повышается, т.е. он отдает электроны
Окислитель — это элемент, степень окисления которого снижается за счет присоединения электронов
Помним, что электрон заряжен отрицательно. Поэтому, когда атом отдает электроны, отрицательных частиц в нем становится меньше, чем положительных протонов, и его степень окисления повышается (он — восстановитель). И наоборот, если атом присоединяет к себе электроны, отрицательных частиц становится больше, чем положительных, соответственно, степень окисления снижается.
Восстановителями могут быть элементы в низших степенях окисления:
— простые вещества металлы,
— соединения неметаллов в низших степенях окисления (HCl, HBr, HI, H 2 S и их соли, NH 3 , PH 3, соли аммония )
Окислителями могут быть элементы в высших степенях окисления:
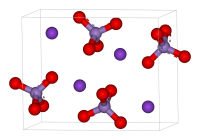
— KMnO4, K2CrO4, K2Cr2O7,
— H2SO4 (конц), HNO3 в любой концентрации, ее соли (KNO3, NaNO3), CO2
— простые вещества F2, О3
И окислителями и восстановителями могут быть элементы с промежуточной степенью окисления:
— простые вещества неметаллы H2, Cl2, Br2, I2, S, P, N2, C
— соединения металлов в промежуточной степени окисления (FeSO2, FeCl2, Cr2(SO4)3, MnO2, K2MnO4)
— H2O2, HClO3 и ее соли
Важно : нередко в реакциях один и тот же элемент может одновременно повысить и понизить степень окисления. Такие реакции называют реакциями диспрапорционирования
В ОВР часто в реакцию вступает третье вещество, которое не является ни окислителем, ни восстановителем. Такие вещества создают среду раствора. Она может быть кислой (за счет H2SO4), нейтральной (H2O), щелочной (KOH или NaOH). Среда раствора определяет по какому пути пойдет реакция
- Соединения марганца
- Соли марганца (II)
- Оксид марганца (IV) MnO2
- Перманганат калия KMnO4
- Соединения хрома
- Соединения хрома (III)
- Хроматы и бихроматы
- Acetyl
- Перманганат калия ГОСТ 20490-75
- Содержание
- Физические свойства
- Термодинамические свойства
- Химические свойства
- Применение
- Медицинское применение
- Фармакологическое действие
- Показания
- Противопоказания
- Способ применения и дозы
- Предосторожности
- Другие сферы применения
- Получение
- Ограничение на покупку
Соединения марганца
Марганец имеет несколько степеней окисления, наиболее характерными являются +2, +4, +6, +7.
В зависимости от с.о. соединения Mn будут проявлять различную окислительно-восстановительную способность:
Mn в с.о. 0 — это простое вещество, металл, степень окисления которого может только повышаться, значит Mn(0) — только восстановитель.
Mn в с.о. +6 — манганаты калия и натрия (K2MnO4, Na2MnO4) — так же являются как окислителями, так и восстановителями, их растворы имеют зеленоватый оттенок
Соли марганца (II)
Mn в с.о. +2 — обычно представляются в виде солей (хлоридов, сульфатов) и имеют бледно-розовый оттенок раствора. Преимущественно является восстановителем, но в некоторых реакциях может выступать как окислитель, например, при электролизе или реакциях замещения
Оксид марганца (IV) MnO2
Mn в с.о. +4 — только MnО 2 — амфотерный оксид, может быть как окислителем, так и восстановителем в зависимости от условий реакции (при наличии более сильного окислителя, он — восстановитель, при более сильном восстановителе, проявляется как окислитель)
MnO 2 + KBr + H 2 SO 4 = MnSO 4 + Br 2 + K 2 SO 4 + H2O ( MnO 2 — окислитель)
КBr не может быть окислителем, т.к. Br находится в низшей с.о. (-1)
MnO 2 + NaClO3 + NaOH = Na2MnO4 + NaCl + H2O ( MnO 2 — восстановитель)
Хлорат натрия NaClO3 — сильный окислитель, а значит MnO2 — будет восстановителем
Перманганат калия KMnO4
Mn в с.о. +7 — перманганаты калия и натрия (KMnO4, NaMnO4) — только окислители, т.к. марганец находится в высшей степени окисления, а значит повышать ее и быть восстановителем уже не может. Растворы перманганатов имеют ярко малиновый окрас
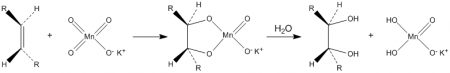
KMnO4 — сильный окислитель, реагирует как с неорганическими веществами, так и с органическими (спиртами, альдегидами, непредельными углеводородами).
В зависимости от среды, в реакциях будут образовываться различные продукты восстановления Mn:
— в кислой среде образуются соли Mn (+2), например MnCl2, MnSO4
— в нейтральной среде выпадает осадок MnO2 бурого цвета
— в щелочной среде образуется манганат K2MnO4? где Mn (+6)
FeSO4 + KMnO4 + H2SO4 = Fe2(SO4) + MnSO4 + K2SO4 + H2O
KMnO4 + KNO2 + H2O = KNO3 + MnO2 + KOH
Cr2(SO4)3 + KMnO4 + KOH = K2CrO4 + K2MnO4 + K2SO4 + H2O
Соединения хрома
Хром имеет несколько степеней окисления, наиболее характерны из которых +3 и +6.
Соединения Cr (+2) не стабильны, легко окисляются до +3, являясь сильнейшими восстановителями
Соединения хрома (III)
Cr в с.о. +3 представляются в виде солей (сульфата, нитрата или хлорида) и гидроксида. Т.к. хром в этих соединениях находится в промежуточной степени окисления, то он может выступать в роли и окислителя и восстановителя, хотя ОВР, где Cr (+3) — окислитель в практике ЕГЭ редки.
Цвета растворимых солей располагаются в лилово-зеленой гамме в зависимости от формулы и температуры. Гидроксид хрома (III) имеет грязно-зеленый оттенок.
При взаимодействии Cr (+3) с сильными окислителями, он окисляется до Cr (+6), т.е. до хромата или бихромата (зависит от кислотности среды):
— в кислой среде образуется оранжевый бихромат (К2Cr2О7)
— в щелочной среде — желтый хромат (К2CrО4)
Хроматы и бихроматы
Cr в с.о. +6 представлен двумя группами веществ — хроматами и бихроматами (или дихроматами, разницы нет). Они являются сильными окислителями, восстанавливаясь до Cr (+3).
Ядовиты. Редко вступают в реакции ионного обмена. Так, хроматы могут реагировать с солями бария и серебра образуя желтый осадок хромата бария и кроваво-красный осадок хромата серебра.
К2 Cr2О7 — бихромат калия — вещество оранжевого цвета, стабильно в нейтральной и кислой среде.
K2 CrO4 — хромат калия — вещество желтого цвета, стабильно в нейтральной и щелочной среде.
При добавлении щелочи к раствору бихромата, он окрашивается в желтый цвет — бихромат превращается в хромат. И наоборот, при добавлении кислоты в желтый раствор хромата, окраска изменятся на оранжевый.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Перманганат калия ГОСТ 20490-75
Перманганат калия (лат. Kalii permanganas , распространённое название в быту — марганцовка) — марганцовокислый калий, калиевая соль марганцовой кислоты. Химическая формула — KMnO4. Представляет собой тёмно-фиолетовые, почти чёрные кристаллы, при растворении в воде образующие ярко окрашенный раствор цвета фуксии. Содержание
Физические свойстваВнешний вид: тёмно-фиолетовые кристаллы с металлическим блеском. Показатель преломления составляет 1,59 (при 20 °C). Растворяется в воде (см. таблицу), жидком аммиаке, ацетоне (2:100), метаноле, пиридине.
Химические свойства
Является сильным окислителем. В зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде — до соединений марганца(II), в нейтральной — до соединений марганца(IV), в сильно щелочной — до соединений марганца(VI). Примеры реакций приведены ниже (на примере взаимодействия с сульфитом калия):
2KMnO4 + 5K2SO3 + 3H2SO4 → 6K2SO4 + 2MnSO4 + 3H2O
2KMnO4 + 3K2SO3 + H2O → 3K2SO4 + 2MnO2 + 2KOH
2KMnO4 + K2SO3 + 2KOH → K2SO4 + 2K2MnO4 + H2O При соприкосновении с концентрированной серной кислотой перманганат калия взрывается, однако при аккуратном соединении с холодной кислотой реагирует с образованием неустойчивого оксида марганца(VII): при этом в качестве промежуточного продукта может образовываться интересное соединение — оксосульфат марганца MnO3HSO4. По реакции с фторидом иода(V) можно получить аналогичный оксофторид: При нагревании разлагается с выделением кислорода (этим способом пользуются в лаборатории для получения чистого кислорода). Схему реакции упрощённо можно представить уравнением: На самом деле реакция идёт намного сложнее, например, при не очень сильном нагревании её можно примерно описать уравнением: Реагирует с солями двухвалентного марганца, например: Эта реакция в принципе обратна дисмутации (диспропорционирование) K2MnO4 на MnO2 и KMnO4. Окисляет органические вещества. В частности, разбавленные растворы перманганата калия в щелочной и нейтральной среде окисляют алкены до диолов (реакция Вагнера): Водные растворы перманганата калия термодинамически нестабильны, но кинетически довольно устойчивы. Их сохранность резко повышается при хранении в темноте. При смеси с пероксидом водорода протекает следующая реакция: ПрименениеПрименение этой соли чаще всего основано на высокой окисляющей способности перманганат-иона, обеспечивающей антисептическое действие. Медицинское применение
Разбавленные растворы (около 0,1 %) перманганата калия нашли широчайшее применение в медицине как антисептическое средство, для полоскания горла, промывания ран, обработки ожогов. В качестве рвотного средства для приёма внутрь при отравлениях морфином, аконитином и некоторыми другими алкалоидами используют разбавленный (0,02—0,1 %) раствор перманганата калия. Фармакологическое действиеАнтисептическое средство. При соприкосновении с органическими веществами выделяет атомарный кислород. Образующийся при восстановлении препарата оксид образует с белками комплексные соединения — альбуминаты (за счёт этого калия перманганат в малых концентрациях оказывает вяжущее, а в концентрированных растворах — раздражающее, прижигающее и дубящее действие). Обладает также дезодорирующим эффектом. Эффективен при лечении ожогов и язв. Способность калия перманганата обезвреживать некоторые яды лежит в основе использования его растворов для промывания желудка при отравлениях неизвестным ядом и пищевых токсикоинфекциях. При попадании внутрь всасывается, оказывая действие (приводит к развитию метгемоглобинемии). ПоказанияСмазывание язвенных и ожоговых поверхностей — инфицированные раны, язвы и ожоги кожи. Полоскание полости рта и ротоглотки — при инфекционно-воспалительных заболеваниях слизистой оболочки полости рта и ротоглотки (в том числе при ангинах). Для промывания и спринцеваний при гинекологических и урологических заболеваниях — кольпиты и уретриты. Для промываний — желудка при отравлениях, вызванных приёмом внутрь алкалоидов (морфин, аконитин, никотин), синильной кислотой, фосфором, хинином; кожи — при попадании на неё анилина; глаз — при поражении их ядовитыми насекомыми. ПротивопоказанияПри передозировке: резкая боль в полости рта, по ходу пищевода, в животе, рвота, диарея; слизистая оболочка полости рта и глотки — отёчная, тёмно-коричневого, фиолетового цвета, возможен отёк гортани, развитие механической асфиксии, ожогового шока, двигательного возбуждения, судорог, явлений паркинсонизма, геморрагического колита, нефропатии, гепатопатии. При пониженной кислотности желудочного сока возможно развитие метгемоглобинемии с выраженным цианозом и одышкой. Смертельная доза для детей — около 3 г , для взрослых — 0,3—0,5 г/кг . Лечение: метиленовый синий ( 50 мл 1 % раствора), аскорбиновая кислота (внутривенно — 30 мл 5 % раствора), цианокобаламин — до 1 мг , пиридоксин (внутримышечно — 3 мл 5 % раствора). Способ применения и дозыНаружно, в водных растворах для промывания ран ( 0,1—0,5 % ), для полоскания рта и горла ( 0,01—0,1 % ), для смазывания язвенных и ожоговых поверхностей ( 2—5 % ), для спринцевания ( 0,02—0,1 % ) в гинекологической и урологической практике, а также промывания желудка при отравлениях. ПредосторожностиАктивно взаимодействует при нагреве и даже при комнатной температуре с большинством восстановителей, например, органическими веществами (сахарозой, танинами, глицерином и многими другими), легкоокисляющимися веществами, поэтому при смешивании происходит саморазогревание, что иногда вызывает самовоспламенение смеси (с концентрированным раствором глицерина, или безводным — всегда) и может привести к взрыву. Очень опасно растирание сухого перманганата калия с органическими веществами и порошками активных металлов и неметаллов (кальцием, алюминием, магнием, фосфором, серой и др.) — весьма вероятен взрыв. Другие сферы применения
ПолучениеХимическое или электрохимическое окисление соединений марганца, диспропорционирование манганата калия. Например: Последняя реакция происходит при электролизе концентрированного раствора манганата калия и эндотермична, она является основным промышленным способом получения перманганата калия. Ограничение на покупкуВходит в IV список прекурсоров ПККН в России (допускается исключение некоторых мер контроля). 14 июня 2013 года на Украине был признан прекурсором и внесён в список наркотических веществ. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||