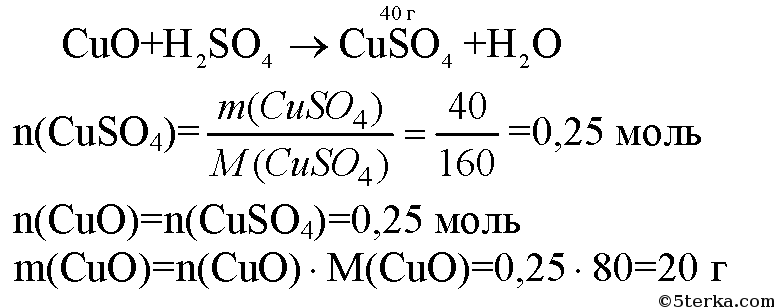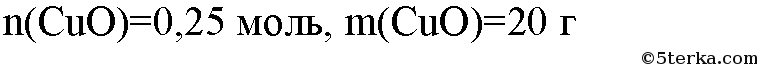Контрольная работа 3 по химии в 8 классе «Изменения, происходящие с веществами» с ответами (2 варианта). УМК Габриелян О.С. (Дрофа). Поурочное планирование по химии для 8 класса (Ястребова О.Н). Урок 44. Контрольная работа по теме «Изменения, происходящие с веществами». Цитаты из пособия использованы в учебных целях. Химия 8 Габриелян Контрольная работа № 3.
- Контрольная работа № 3 «Изменения, происходящие с веществами»
- 1. Организационный момент
- 2. Выполнение контрольной работы
- Контрольная работа по химии. Вариант 1
- Контрольная работа по химии. Вариант 2
- 3. Рефлексия учебной деятельности
- Ответы на контрольную работу. Вариант 1
- Ответы на контрольную работу. Вариант 2
- Please wait.
- We are checking your browser. gomolog.ru
- Why do I have to complete a CAPTCHA?
- What can I do to prevent this in the future?
- Тема III. Работа 2. Свойства кислот. Соли. Вариант 4
- Вопросы:
- Решения и ответы:
- Верны ли следующие высказывания? А. В уравнении реакции: Х + H2SO4 = CuSO4 + H2Oвеществом Х является вещество с формулой CuO.
- Ваш ответ
- решение вопроса
- Похожие вопросы
Контрольная работа № 3
«Изменения, происходящие с веществами»
Цели урока : проверка знаний и умений учащихся, степени усвоения ими учебного материала.
Тип урока : урок развивающего контроля.
Оборудование : карточки с заданиями, справочные таблицы.
ХОД УРОКА
1. Организационный момент
Мотивация к учебной деятельности. Учитель сообщает тему урока, формулирует цели урока.
2. Выполнение контрольной работы
Контрольная работа по химии. Вариант 1
Базовый уровень
A1. Физическое явление — это
1) скисание молока; 2) горение керосина;
3) плавление железа; 4) подгорание пищи.
А2. Укажите на признак реакции, протекающей при гниении белка.
1) растворение осадка; 2) выделение энергии;
3) появление запаха; 4) образование осадка.
А3. Укажите уравнение эндотермической реакции.
1) 2SO2 + O2 = 2SO3 + Q; 2) СаСO3 → СаО + СO2 – Q;
3) 2НСl + Zn = ZnCl2 + H2 + Q; 4) N2 + H2 → NН3 + Q.
A4. Какая из реакций является реакцией замещения?
А5. Составьте уравнение реакции по схеме: Аl + O2 = Аl2O3, и определите сумму всех коэффициентов.
1) 4; 2) 6; 3) 9; 4) 1.
А6. Укажите фактор, влияющий на скорость химической реакции.
1) вода; 2) воздух; 3) температура; 4) свет.
А7. Найдите объем водорода, который полностью прореагирует в реакции H2 + Сl2 = 2НСl с 0,5 моль хлора (н. у.).
1) 5,6 л; 2) 11,2л; 3) 22,4 л; 4) 44,8 л.
А8. Укажите схему, являющуюся уравнением химической реакции.
1) СаСO3 → СаО+ СO2, 2) Са + O2 → СаО;
3) Mg + НСl → MgCl2 + H2; 4) СО + O2 → СO2.
А9. По левой части уравнения ZnO + 2НСl = … восстановите его правую часть.
A10. Атомы простого вещества замещают атомы одного из элементов в сложном веществе в реакции:
1) соединения; 2) обмена; 3) разложения; 4) замещения.
Повышенный уровень
В1. По схеме запишите уравнение и укажите тип реакции: гидроксид натрия + хлорид меди (II) = гидроксид меди (II) + хлорид натрия.
В2. По уравнению реакции Fe(OH)2 = FeO + H2O определите массу оксида железа (II), образовавшегося при разложении 75 г исходного вещества.
В3. Расставьте коэффициенты в схемах, укажите типы химических реакций:
1) МnO2 + H2 → Мn + H2O; 2) Аl + Cl2 → AlCl3.
В4. Запишите план разделения смеси речного песка и поваренной соли.
В5. Восстановите символы в уравнениях реакций, укажите типы реакций:
Контрольная работа по химии. Вариант 2
Базовый уровень
A1. Химическое явление – это:
1) дробление камня; 2) испарение керосина;
3) плавление железа; 4) подгорание пищи.
А2. Укажите признак реакции, протекающей при горении парафина.
1) растворение осадка; 2) выделение энергии;
3) появление запаха; 4) образование осадка.
А3. Укажите уравнение экзотермической реакции.
1) 2SO3 = 2SO2 + O2↑ – Q; 2) 2HgO = 2Hg + O2↑ – Q;
3) Zn + 2HCI = ZnCl2 + H2 + Q; 4) CaCO3 → CaO + CO2 – Q.
A4. Укажите уравнение реакции обмена.
А5. Определите сумму всех коэффициентов в уравнении Р + O2 = Р2O5.
1) 7; 2) 9; 3) 11; 4) 1.
А6. Какие факторы влияют на скорость химической реакции?
1) вода; 2) воздух; 3) свет; 4) катализатор.
А7. Найдите объем хлора, который полностью прореагирует в реакции H2 + Сl2 = 2НСl с 0,5 моль водорода (н. у.).
1) 5,6 л; 2) 11,2л; 3) 22,4 л; 4) 33,6 л.
А8. Укажите схему, являющуюся уравнением химической реакции.
1) Р + О2 = Р2O5; 2) Са + S → CaS;
3) Mg + НСl → MgCl2 + H2; 4) СО + O2 → СO2.
А9. По левой части уравнения СаО + 2НCl = … восстановите его правую часть.
A10. Реакция, в результате которой из одного сложного вещества образуется два или несколько веществ, называется реакцией
1) замещения; 2) обмена; 3) разложения; 4) соединения.
Повышенный уровень
В1. По схеме запишите уравнение и укажите тип реакции: натрий + вода = гидроксид натрия + водород.
В2. По уравнению реакции Cu(OH)2 = СuО + H2O определите массу оксида меди (II), образовавшегося при разложении 98 г исходного вещества.
В3. Расставьте коэффициенты в схемах, укажите типы химических реакций:
1) СuО + H2 → Сu + H2O; 2) Cr + Cl2 → СrСl3.
В4. Запишите план разделения смеси древесных, железных опилок и поваренной соли.
В5. Восстановите символы в уравнениях реакций, укажите типы реакций:
1) … + H2SO4 → CuSO4 + H2O; 2) 2Аl + … → 2АlСl3.
3. Рефлексия учебной деятельности
В конце урока учитель раздает на каждую парту краткую запись с ответами на контрольную работу.
Ответы на контрольную работу. Вариант 1
Базовый уровень
A1. 3) плавление железа.
А2. 3) появление запаха.
А3. 2) СаСO3 → СаО + СO2 – Q.
A4. 2) СuО + H2 = Сu + H2O.
А5. 3) 9.
А6. 3) температура.
А7. 2) 11,2 л.
А8. 1) СаСO3 → СаО+ СO2.
A10. 4) замещения.
Повышенный уровень
В1. 2NaOH + CuCl2 = Сu(ОН)2 + 2NaCl. Реакция обмена.
В2. Решение.
n(FeO) = n(Fe(OH)2) = m(Fe(OH)2) : M(Fe(OH)2) = 75 г : 90 г/моль = 0,833 моль;
m(FeO) = n(FeO) • M(FeO) = 0,833 моль • 72 г/моль = 60 г.
Ответ: m(FeO) = 60 г.
В3.
1) МnO2 + 2H2 → Мn + 2H2O реакция замещения;
2) 2Аl + 3Cl2 → 2AlCl3 реакция соединения.
В4. Смесь можно разделить растворением соли в воде, фильтрованием песка и выпариванием соли.
В5.
1) Zn + H2SO4 = ZnSO4 + H2 реакция замещения;
2) 4Al + 3O2 = 2Аl2O3 реакция соединения.
Ответы на контрольную работу. Вариант 2
Базовый уровень
A1. 4) подгорание пищи.
А2. 2) выделение энергии.
А3. 3) Zn + 2HCI = ZnCl2 + H2+ Q.
А5. 3) 11.
А6. 4) катализатор.
А7. 2) 11,2 л.
А8. 2) Са + S → CaS.
A10. 3) разложения.
Повышенный уровень
В1. 2Na + 2H2O = 2NaOH + H2. Реакция замещения.
В2. Решение.
n(СuО) = n(Сu(ОН)2)= m(Сu(ОН)2) : М(Сu(ОН)2) = 98 г : 98 г/моль = 1 моль;
m(CuO) = n(СиО) • M(CuO) = 1 моль х 80 г/моль = 80 г.
Ответ: m(СuО) = 80 г.
В3.
1) СuО + H2 → Сu + H2O реакция замещения;
2) 2Cr + 3Cl2 → 2СrСl3 реакция соединения.
В4. Смесь можно разделить, отделив железные стружки магнитом, затем растворением соли и древесных опилок в воде, отстаиванием и фильтрованием опилок и последующим выпариванием соли.
В5. Восстановите символы в уравнениях реакций, укажите типы реакций:
1) СuО + H2SO4 → CuSO4 + H2O реакция замещения;
2) 2Аl + Сl2 → 2АlСl3 реакция соединения.
Вы смотрели: Химия 8 Габриелян Контрольная работа № 3 по химии в 8 классе с ответами (2 варианта). УМК Габриелян О.С. (Дрофа). Поурочное планирование по химии для 8 класса (Ястребова О.Н). Урок 44. Контрольная работа по теме «Изменения, происходящие с веществами» + ОТВЕТЫ.
Вернуться к Списку уроков Тематического планирования по химии в 8 классе.
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 708acfbfcc2afa1c • Your IP : 178.45.22.152 • Performance & security by Cloudflare
Тема III. Работа 2. Свойства кислот. Соли. Вариант 4
Вопросы:
1. Допишите уравнения реакций получения солей: а) Mg + H2SO4 = б) Fe2O3 + HCl = в) BaO + HNO3 =
Расставьте коэффициенты и назовите образующиеся соли.
2. Перечислите общие химические свойства кислот.
3. При взаимодействии оксида меди(II) с серной кислотой образовалось 40 г сульфата меди(II). Рассчитайте массу и количество вещества оксида меди(II), вступившего в реакцию.
Решения и ответы:
2. Кислоты реагируют с металлами, основными оксидами, основаниями, солями.

задача №4
к главе «Тема III. Водород. Кислоты. Соли. Работа 2. Свойства кислот. Соли».
Верны ли следующие высказывания? А. В уравнении реакции: Х + H2SO4 = CuSO4 + H2Oвеществом Х является вещество с формулой CuO.
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,429
- гуманитарные 33,634
- юридические 17,906
- школьный раздел 608,227
- разное 16,858
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.