| Гидрид алюминия | |
|---|---|
 | |
| Систематическое наименование | Гидрид алюминия |
| Традиционные названия | Гидрид алюминия, гидрид алюминия III, алан |
| Хим. формула | (AlH3)n |
| Рац. формула | AlH3 |
| Состояние | твёрдое |
| Молярная масса | 30,005 г/моль |
| Плотность | 1,45 |
| Температура | |
| • разложения | 105 |
| Энтальпия | |
| • образования | − 12 кДж/моль |
| Рег. номер CAS | 7784-21-6 |
| PubChem | 14488 |
| Рег. номер EINECS | 232-053-2 |
| SMILES | |
| ChEBI | 30136 |
| ChemSpider | 13833 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Гидрид алюминия — AlH3, неорганическое бинарное соединение алюминия с водородом. В нормальных условиях — бесцветное или белое твёрдое вещество, имеющее полимерную структуру: (AlH3)n.
Впервые был получен в 1942 году действием тлеющего электрического разряда на смесь триметилалюминия и водорода.
Используется как компонент ракетного топлива, мощный восстановитель в органическом синтезе и в качестве катализатора для реакций полимеризации.
- Содержание
- Молекулярная структура
- Физические свойства
- Химические свойства
- Получение
- Применение
- Реакции алюминия с водородом и другими веществами
- Взаимодействие алюминия с другими веществами
- Взаимодействие с неметаллами
- Взаимодействие алюминия с водородом
- Алюминий и его водородная пористость
- Гидрид алюминия (AlH3): строение, свойства, применение
- Содержание:
- Состав
- Координации
- Изолированная молекула
- Полиморфы
- Свойства
- Внешность
- Молярная масса
- Температура плавления
- Растворимость воды
- Растворимость
- Разложение
- Образование аддукта
- Получение
- Приложения
- Восстановитель
- Резервуар с водородом
- Ссылки
Содержание
- 1 Молекулярная структура
- 2 Физические свойства
- 3 Химические свойства
- 4 Получение
- 5 Применение
Молекулярная структура
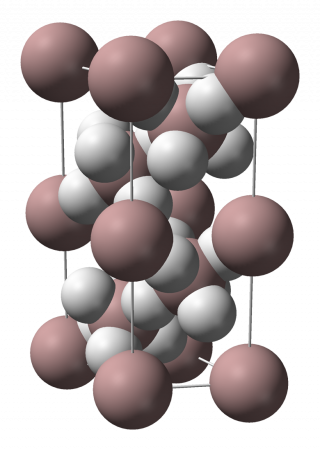
В обычных условиях гидрид алюминия имеет полимерную молекулярную структуру (AlH3)n, при этом его кристаллическая форма существует в семи полиморфных модификациях: α-(AlH3)n, α 1 -(AlH3)n, β-(AlH3)n, δ-(AlH3)n, ε-(AlH3)n, γ-(AlH3)n, ζ-(AlH3)n.
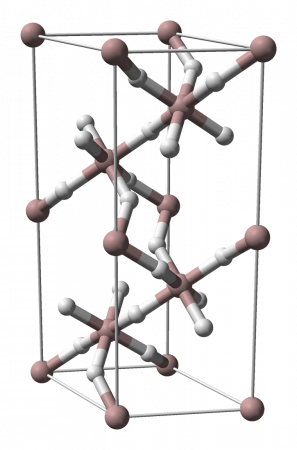
Самой устойчивой является модификация α-(AlH3)n, имеющая гексагональную сингонию (пространственная группа R3c, а = 4,449 Å, b = 4,449 Å, c = 11,804 Å). Длина связи Al—H составляет 1,72 Å, длина связи Al—Al: 3,24 Å. Структура α-(AlH3)n представляет собой совокупность октаэдров АlН6, объединенных шестью трехцентровыми двухэлектронными связями Аl—Н—Аl в кристаллический каркас.
Модификация γ-(AlH3)n существует в ромбической сингонии, пространственная группа Pnnm (а = 5,3806 Å, b = 7,3555 Å, c = 5,77509 Å). Ячейка кристаллической решётки гидрида состоит из двух октаэдров AlH6, длина связи Al—Al составляет 2,606 Å. Особенностью структуры является наличие разветвлённой двойной мостиковой связи Al—2H—Al (длина связи Al—H: 1,68—1,70 Å) в дополнение к обычной связи Al—H—Al (длина связи Al—H: 1,77—1,78 Å). Из-за наличия больших полостей в кристаллической структуре γ-(AlH3)n, данная модификация имеет плотность примерно на 11 % меньше, чем α-(AlH3)n.
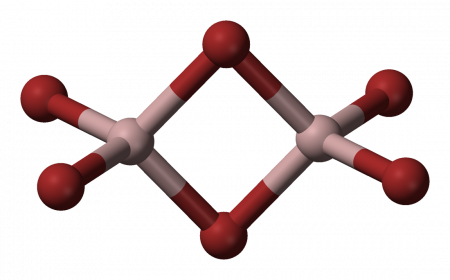
При взаимодействии распылённых лазером атомов алюминия с водородом при сверхнизких температурах (3,5 K) с последующим ультрафиолетовым излучением и нормализацией при 6,5 K, в продуктах фотолиза можно обнаружить структуры димера Al2H6, аналогичные структуре диборана B2H6. Димер (см. структуру на рисунке) очень неустойчив в конденсированном состоянии, поэтому его существование обнаружилось лишь спустя примерно пятьдесят лет после открытия гидрида алюминия.
В 2007 году группа учёных из США воздействовала на алюминий плазменным потоком атомов водорода и обнаружила, что в результате образуются различные анионные полиядерные гидриды алюминия, среди которых особый интерес вызвал анион Al4H6 − , чей нейтральный гибрид Al4H6 по расчётам должен отличаться заметной стабильностью. Структурно соединение должно представлять искажённый тетраэдр с вершинами — атомами алюминия, в котором атомы водорода образуют четыре терминальные связи Al–H и две мостиковые связи Al–H–Al. Большой энергетический порог между высшими занятыми и низшими свободными молекулярными орбиталями в сочетании с исключительно высоким значением теплоты сгорания позволяют предположить, что этот гидрид алюминия может представлять собой перспективный материал для ракетного топлива.
Физические свойства
Гидрид алюминия представляет собой твёрдое белое или бесцветное вещество. Плотность 1,45 (по другим данным 1,47) г/см³. Растворим в тетрагидрофуране (5 г в 100 г растворителя при 19,5 °C).
- стандартная энтальпия образования, ΔH o 298: −12 кДж/моль (по другим данным: −11,43±0,84 кДж/моль);
- стандартная энтропия, S o 298: 30 Дж/(моль·K) (по другим данным: 30,06±0,42 Дж/(моль·K));
- стандартная энергия Гиббса, ΔG o 298: 46 кДж/моль (по другим данным: 46,52±0,96 кДж/моль).
Большое содержание водорода в гидриде алюминия обуславливает ряд его свойств, связанных с проблемой высокотемпературной сверхпроводимости: в области давлений
60 ГПа и температуре
1000 K он обладает полупроводниковым механизмом проводимости, а в области высоких давлений и температур (до 90 ГПа и 2000 K) его проводимость сопоставима с металлической электропроводностью водорода.
Химические свойства
- Соединение нестабильно: при нагревании выше 100 °C разлагается:
2 AlH3 → to 2 Al + 3 H2
- Бурно взаимодействует с водой:
AlH3 + 3 H2O → Al(OH)3 + 3 H2 ↑
- С диэтиловым эфиром образует высокореакционный, но относительно стабильный комплекс переменного состава, который часто используется для синтетических целей:
AlH3 + n(C2H5)2O → AlH3 ⋅ n(C2H5)2O Аналогичный комплекс образуется с другими низшими алифатическими эфирами, а также с триметиламином: AlH3 • N(CH3)3. Последний взаимодействует с водой со взрывом. Для стабилизации гидрида алюминия также можно использовать комплексы с другими аминами, например с N-метилпирролидином (NMP): AlH3 • NMP и AlH3 • (NMP)2.
- Гидрид алюминия — очень сильный восстановитель. Он способен восстановить углекислый газ до метана:
4 AlH3 + 3 CO2 → to 3 CH4 + 2 Al2O3 Известны многочисленные реакции восстановления органических соединений с использованием гидрида алюминия.
- Взаимодействует с гидридом лития, образуя алюмогидрид:
AlH3 + LiH → (C2H5)2O LiAlH4 Медленно вступает в реакцию с дибораном, образуя борогидрид алюминия (точнее тетрагидридоборат алюминия): 2 AlH3 + B2H6 → 2 Al(BH4)3
Получение
Используемый сегодня принципиальный метод получения чистого гидрида алюминия из гидрида лития в среде диэтилового эфира был предложен ещё в 1947 году:
Хлорид лития выпадает в осадок до момента полимеризации AlH3 и отделяется от эфирного раствора, из которого путём дальнейшей отгонки эфира получают комплекс гидрида алюминия с диэтиловым эфиром.
Также гидрид алюминия по аналогии можно получить реакцией алюмогидрида лития с серной кислотой, хлоридом бериллия, хлоридом цинка, хлороводородом и алкилгалогенидами:
2 LiAlH4 + H2SO4 → 2 AlH3 + Li2SO4 + 2 H2 LiAlH4 + HCl → AlH3 + LiCl + H2 2 LiAlH4 + BeCl2 → 2 AlH3 + 2 LiCl + BeH2 2 LiAlH4 + ZnCl2 → 2 AlH3 + 2 LiCl + ZnH2 LiAlH4 + R−CH2−Cl → AlH3 + LiCl + R−CH3
Вместо алюмогидрида лития можно использовать алюмогидрид натрия:
Для получения чистого гидрида (без примесей растворителя) эфирный комплекс подвергают нагреванию в вакууме с добавлением бензола или в присутствии небольших количеств LiAlH4 или смеси LiAlH4+LiBH4. При этом сперва получаются β-AlH3 и γ-AlH3 модификации, которые затем переходят в более стабильный α-AlH3.
Другим способом получения несольватированного эфиром гидрида алюминия, является электролиз алюмогидрида натрия в среде тетрагидрофурана.
Среди прочих методов отметим синтез с использованием гидрида магния:
Долгое время считалось, что гидрид алюминия невозможно получить прямым взаимодействием элементов, поэтому для его синтеза использовали приведённые выше косвенные методы. Однако, в 1992 году группа российских учёных осуществила прямой синтез гидрида из водорода и алюминия, используя высокое давление (выше 2 ГПа) и температуру (более 800 K). Вследствие очень жёстких условий протекания реакции, в настоящий момент метод имеет лишь теоретическое значение.
Применение
Гидрид алюминия находит широкое применение в органическом синтезе в качестве сильнейшего восстанавливающего агента.
В связи с тем, что гидрид алюминия представляет собой соединение с высоким содержанием водорода (10,1 %), он используется в производстве ракетных топлив и некоторых взрывчатых веществ, а также для систем хранения и генерации в автономных энергетических водородных установках.
Реакции алюминия с водородом и другими веществами
Химические свойства самого распространенного металла
Алюминий — активный металл. Он устойчив на воздухе, при нормальной температуре быстро окисляется, покрываясь плотной пленкой оксида, которая защищает металл от дальнейшего разрушения.
Взаимодействие алюминия с другими веществами
При обычных условиях не взаимодействует с водой даже в состоянии кипения. При удалении защитной оксидной пленки алюминий вступает в энергичное взаимодействие с водяным паром воздуха, превращаясь в рыхлую массу гидроксида алюминия с выделением водорода и тепла. Уравнение реакции:
2Al + 6H₂O = 2Al(OH)₃ + 3H₂
Если снять защитную оксидную пленку с алюминия, то металл вступает в активное взаимодействие с кислородом. При этом порошок алюминия сгорает, образуя оксид. Уравнение реакции:
Этот металл также активно взаимодействует со многими кислотами. При реакции с соляной кислотой наблюдается выделение водорода:
2Al + 6HCl = 2AlCl₃ + 3H₂
При обычных условиях концентрированная азотная кислота не взаимодействует с алюминием, так как будучи сильным окислителем, она делает оксидную пленку еще крепче. По этой причине азотная кислота хранится и перевозится в алюминиевой посуде.
Алюминий при обычной температуре пассивируется разбавленной азотной и концентрированной серной кислотами. В горячей серной кислоте металл растворяется:
2Al + 4H₂SO4 = Al₂(SO4)₃ + S + 4H₂O
Взаимодействие с неметаллами
Алюминий реагирует с галогенами, серой, азотом, углеродом и всеми неметаллами. Для протекания реакции необходимо нагревание, после чего взаимодействие происходит с выделением большого количества тепла.
Взаимодействие алюминия с водородом
Алюминий непосредственно с водородом не реагирует, хотя известно твердое полимерное соединение алан, в котором существуют так называемые трехцентровые связи. При температуре выше 100 градусов Цельсия алан необратимо разлагается на простые вещества. Гидрид алюминия бурно реагирует с водой.
Алюминий напрямую не реагирует с водородом: металл образует соединения путем потери электронов, которые принимаются другими элементами. Атомы водорода не принимают электроны, которые отдают металлы для образования соединений. «Принуждать» атомы водорода принять электроны с образованием твердых ионных соединений (гидридов) могут только очень реактивные металлы (калий, натрий, магний, кальций). Для прямого синтеза гидрида алюминия из водорода и алюминия требуется огромное давление (около 2 миллиардов атмосфер) и температура выше 800 К. Здесь вы сможете узнать о химических свойствах других металлов.
Следует отметить, что водород — это единственный газ, заметно растворяющийся в алюминии и его сплавах. Растворимость водорода изменяется пропорционально температуре и квадратному корню из давления. Растворимость водорода в жидком алюминии значительно выше, чем в твердом. Это свойство незначительно изменяется в зависимости от химического состава сплавов.
Алюминий и его водородная пористость
Образование в алюминии пузырей водорода непосредственно зависит от скорости охлаждения и затвердевания, а также от наличия центров зарождения для выделения водорода — захваченных внутрь расплава оксидов. Для образования пористости алюминия необходимо значительное превышение содержания растворенного водорода по сравнению с растворимостью водорода в твердом алюминии. При отсутствии центров зарождения для выделения водорода требуется относительно высокая концентрация вещества.
Расположение водорода в затвердевшем алюминии зависит от уровня его содержания в жидком алюминии и условий, при которых происходило затвердевание. Так как водородная пористость — это результат механизмов зарождения и роста, контролируемых диффузией, то такие процессы, как снижение концентрации водорода и увеличение скорости затвердевания, подавляют зарождение и рост пор. Из-за этого выполненные методом литья в разъемный кокиль отливки металла более подвержены дефектам, связанным с водородом, чем отливки, изготовленные методом литья под давлением.
Есть разные источники попадания водорода в алюминий.
Шихтовые материалы (лом, слитки, литейный возврат, оксиды, песок и смазки, применяющиеся при механической обработке). Эти загрязнители — потенциальные источники водорода, образовавшегося при химическом разложении паров воды или восстановлении органических веществ.
Плавильные инструменты. Скребки, пики, лопаты являются источником водорода. Оксиды и остатки флюсов на инструментах впитывают влагу из окружающего воздуха. Печные огнеупоры, распределительные каналы, ковши для отбора проб, известковые желоба и цементные растворы — потенциальные источники водорода.
Атмосфера печи. Если плавильная печь работает на мазуте или на природном газе, возможно неполное сгорание топлива с образованием свободного водорода.
Флюсы (гигроскопичные соли, готовые мгновенно впитывать воду). По этой причине влажный флюс неизбежно вносит в расплав водород, образовавшийся при химическом разложении воды.
Литейные формы. В процессе заполнения литейной формы жидкий алюминий течет турбулентно и захватывает воздух во внутренний объем. Если воздух не успеет выйти из формы до начала затвердевания алюминия, то водовод проникнет в металл.
Гидрид алюминия (AlH3): строение, свойства, применение
Гидрид алюминия (AlH3): строение, свойства, применение — Наука
Содержание:
В гидрид алюминия неорганическое соединение, химическая формула которого AlH3. Хотя это может показаться простым по своей природе, на самом деле это довольно сложная субстанция. Из-за кристаллического блеска, который может проявляться в твердом теле, его обычно принимают за ионный гидрид, образованный ионами Al. 3+ и H – .
Однако его свойства демонстрируют обратное: это полимерное твердое тело, наиболее точное представление которого будет иметь тип (AlH3)п, будучи п количество мономерных единиц AlH3 который будет включать цепочку или слой кристалла. Следовательно, AlH3 Это один из тех полимеров, которому удается принять кристаллическую структуру.
Гидрид алюминия не является твердым телом с большим коммерческим распространением, поэтому его изображений мало. Он специально предназначен для органического синтеза, где он служит мощным восстановителем. Кроме того, он занимает особое место в технологическом прогрессе материалов, являясь многообещающей альтернативой хранению водорода.
Это соединение, также называемое аланом, тесно связано с LiAlH.4, названиями которых являются алюмогидрид лития, аланат лития или тетрагидроалюминат лития. Хотя он имеет полимерные характеристики и термическую метастабильность, он встречается в семи полиморфных модификациях с различной кристаллической морфологией.
Состав
Координации
Независимо от рассматриваемого полиморфа или кристаллической фазы, координаты между атомами алюминия и водорода остаются постоянными. На верхнем изображении, например, как и на первом изображении, показан координационный октаэдр для атомов алюминия (коричневая сфера).
Каждый атом Al окружен шестью атомами водорода, образующими шесть связей Al-H. То, как октаэдры ориентированы в пространстве, будет иметь структурное различие между одним полиморфом и другим.
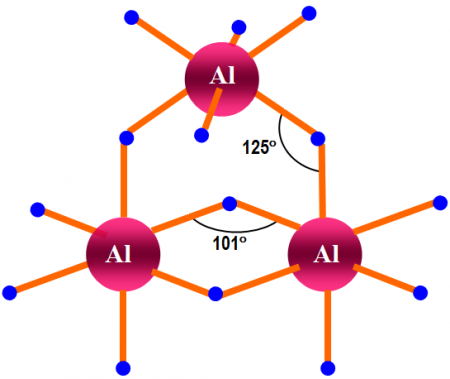
С другой стороны, каждый атом H координируется с двумя атомами Al, устанавливая связь Al-H-Al, что может быть оправдано связью типа 3c2e (3 центра — 2 электрона). Эта ссылка отвечает за соединение нескольких октаэдров AlH.6 через кристалл алана.
Изолированная молекула
АльГ3 считается полимерным из-за сетей AlH6 которые составляют кристалл. Чтобы выделить отдельную молекулу аллана, необходимо применить низкое давление в инертной атмосфере благородного газа. Таким образом, полимер разрушается и высвобождает молекулы AlH.3 геометрия тригональной плоскости (аналог BH3).
С другой стороны, можно димеризовать два AlH3 чтобы сформировать Al2ЧАС6, как и диборан, B2ЧАС6. Однако для достижения этого требуется использование твердого водорода, поэтому он не может иметь большого долгосрочного промышленного или коммерческого значения.
Полиморфы
Алано или AlH3 Он способен образовывать до семи полиморфов: α, α ’, β, γ, δ, ε и ζ, из которых α является наиболее устойчивым к изменениям температуры. Α-AlH3 он отличается кубической морфологией и гексагональной кристаллической структурой. Как правило, это продукт, в который превращаются другие полиморфы, когда они подвергаются термической дестабилизации.
Морфология γ-AlH3, с другой стороны, он отличается игольчатым типом. Вот почему AlH3 Твердое вещество может содержать смесь более двух полиморфов и представлять различные кристаллы под микроскопом.
Свойства
Внешность
Гидрид алюминия представляет собой твердое вещество от бесцветного до не совсем белого цвета с кристаллическим внешним видом и тенденцией проявлять игольчатую форму.
Молярная масса
29,99 г / моль или 30 г / моль
Температура плавления
150 ° С. Но он начинает разлагаться при 105ºC.
Растворимость воды
Высокий, потому что он реагирует с ним.
Растворимость
Нерастворим в диэтиловом эфире и в неполярных растворителях, таких как бензол и пентан. Реагирует со спиртами и другими полярными растворителями.
Разложение
АльГ3 он подвержен разложению с разной скоростью в зависимости от внешних условий, морфологии и термической стабильности его кристаллов или использования катализаторов. Когда это происходит, он выделяет водород и превращается в металлический алюминий:
Фактически, это разложение, а не проблема, представляет собой одну из причин, по которой алано считается интересным для развития новых энергетических технологий.
Образование аддукта
Когда AlH3 он не вступает в необратимую реакцию с растворителем, он образует с ним аддукт, то есть своего рода комплекс. Например, он может образовывать комплекс с триметиламином, AlH32N (CH3)3, с тетрагидрофураном, AlH3THF, или с диэтиловым эфиром, AlH3Et2О. Последний был наиболее известен, когда в 1947 году был введен синтез или производство алана.
Получение
Первые выступления AlH3 восходит к 1942 и 1947 годам, именно в этом году был представлен его синтез с использованием LiAlH.4 в среде диэтилового эфира:
Эфирный раствор AlH3 · пEt2Или он должен был впоследствии подвергнуться десольватации с целью устранения Et2Или и получить AlH3 чистый. В дополнение к этой проблеме необходимо было удалить LiCl из среды продуктов.
Таким образом, с 1950 по 1977 год были разработаны новые синтезы для получения более высоких выходов AlH.3, а также более чистые твердые вещества с лучшими термическими и морфологическими свойствами. Изменяя количество, этапы и используемые инструменты, можно получить один полиморф лучше, чем другой. Однако α-AlH3 это обычно продукт большинства.
Другие методы синтеза заключаются в использовании электрохимии. Для этого используются алюминиевый анод и платиновый катод. На аноде происходит следующая реакция:
При этом в катоде получается металлический натрий. Тогда AlH3 · пTHF также подвергается десольватации для удаления THF и, наконец, получения AlH.3.
Приложения
Восстановитель
АльГ3 он служит для восстановления определенных функциональных групп органических соединений, таких как карбоновые кислоты, кетоны, альдегиды и сложные эфиры. Фактически он добавляет водород. Например, сложный эфир можно восстановить до спирта в присутствии нитрогруппы:
Резервуар с водородом
Гидрид алюминия представляет собой альтернативу тому, чтобы служить резервуаром для водорода и, таким образом, иметь возможность переносить его в устройства, которые работают с водородными батареями. Объемы, полученные из H2 соответствуют объему более чем в два раза больше AlH3.
Принимая AlH3, и разложив его контролируемым образом, желаемое количество H2 в любой момент. Следовательно, его можно использовать в качестве ракетного топлива и во всех тех энергетических приложениях, которые стремятся использовать преимущества сжигания водорода.
Ссылки
- Шивер и Аткинс. (2008). Неорганическая химия. (Четвертый выпуск). Мак Гроу Хилл.
- Википедия. (2020). Гидрид алюминия. Получено с: en.wikipedia.org
- Национальный центр биотехнологической информации. (2020). Гидрид алюминия. База данных PubChem., CID = 14488. Получено с: pubchem.ncbi.nlm.nih.gov
- J. Graetz et al. (2011). Гидрид алюминия как материал для хранения водорода и энергии: прошлое, настоящее и будущее. Elsevier B.V.
- Сюй Бо и др. (2014). Получение и термические свойства полиморфов гидрида алюминия. doi.org/10.1016/j.vacuum.2013.05.009
Устойчивое потребление: для чего это нужно, важность, действия, примеры
6 типичных ремесел Наярит, наиболее популярных