Химические свойства фенолов определяются наличием в молекуле гидроксильной группы и бензольного кольца.
I. Реакции с участием гидроксильной группы
Фенолы являются более сильными кислотами, чем спирты и вода, т.к. за счет участия неподеленной электронной пары кислорода в сопряжении с π-электронной системой бензольного кольца полярность связи О–Н увеличивается.
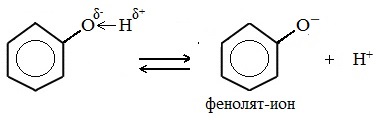
Фенолы в водных растворах диссоциируются по кислотному типу: на фенолят-ионы и ионы водорода:
Фенол диссоциирует обратимо, это слабая кислота. Однако его силы кислотных свойств достаточно, чтобы изменять окраску индикатора, имеющего в нейтральной среде фиолетовый цвет. В растворе фенола лакмус краснеет.
1) Взаимодействие с активными металлами с образованием фенолятов (сходство со спиртами)
Видеоопыт «Взаимодействие фенола с металлическим натрием»
2) Взаимодействие со щелочами с образованием фенолятов (отличие от спиртов)
Видеоопыт «Взаимодействие фенола с раствором щелочи»
Образующиеся в результате реакций феноляты легко разлагаются при действии кислот. Даже такая слабая кислота, как угольная, вытесняет фенол из фенолятов. Следовательно, !Феноляты – соли слабой карболовой кислоты, разлагаются угольной кислотой:
По кислотным свойствам фенол превосходит этанол в 10 6 раз. При этом во столько же раз уступает уксусной кислоте. В отличие от карбоновых кислот, фенол не может вытеснить угольную кислоту из её солей
C6H5-OH + NaHCO3 = реакция не идёт – прекрасно растворяясь в водных растворах щелочей, он фактически не растворяется в водном растворе гидрокарбоната натрия.
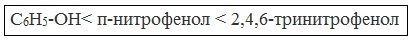
Кислотные свойства фенола усиливаются под влиянием связанных с бензольным кольцом электроноакцепторных групп (NO2 — , Br — )
2,4,6-тринитрофенол или пикриновая кислота сильнее угольной.
3) Образование сложных и простых эфиров
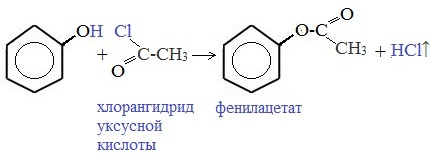
Как и спирты, фенолы могут образовывать простые и сложные эфиры. Фенолы не образуют сложные эфиры в реакциях с кислотами. Сложные эфиры образуются при взаимодействии фенола с ангидридами или хлорангидридами карбоновых кислот:
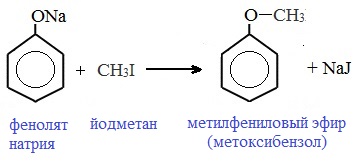
Простые эфиры образуются при взаимодействии фенолятов с алкилгалогенидами:
II . Реакции, с участием бензольного кольца
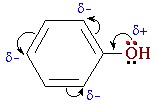
Взаимное влияние атомов в молекуле фенола проявляется не только в особенностях поведения гидроксигруппы, но и в большей реакционной способности бензольного ядра. Гидроксильная группа повышает электронную плотность в бензольном кольце, особенно, в орто- и пара- положениях (+ М -эффект ОН-группы):
Поэтому фенол значительно активнее бензола вступает в реакции электрофильного замещения в ароматическом кольце.
Реакции замещения
1) Нитрование
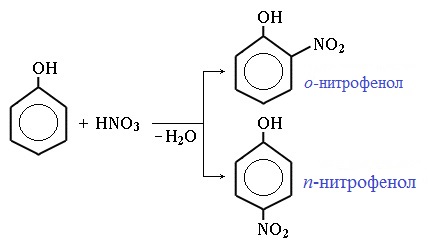
Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара- нитрофенолов:
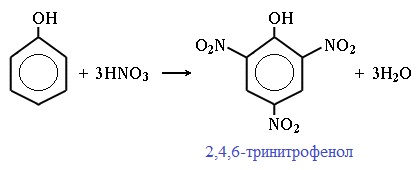
При использовании концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота):
У нее кислотные свойства выражены сильнее, чем у фенола, т.к. нитрогруппы оттягивают электронную плотность от бензольного кольца и делают связь О-Н еще более полярной.
Пикриновая кислоты является взрывчатым веществом, в чистом виде представляет собой желтые кристаллы.
2) Галогенирование
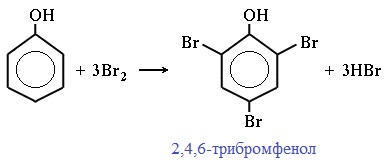
Фенол легко при комнатной температуре взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола ( качественная реакция на фенол! ):
Образуется белый осадок трибромфенола.
Видеоопыт «Взаимодействие фенола с бромной водой»
3) Сульфирование
Соотношение о- и п-изомеров определяется температурой реакции: при комнатной температуре в основном образуется о-фенолсульфокислота, при t=1000С – пара-изомер: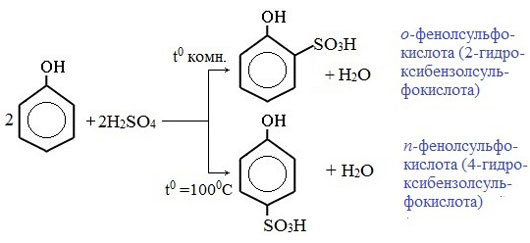
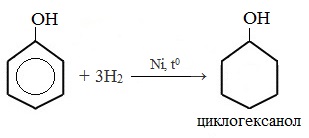
1) Гидрирование фенола
Эта реакция идет с разрушением ароматического кольца. Продукт реакции циклический одноатомный спирт — циклогексиловый спирт (циклогексанол).
2) Конденсация с альдегидами
При нагревании фенола с формальдегидом в присутствии кислотных или основных катализаторов происходит реакция поликонденсации и образуется фенолформальдегидная смола.
Данная реакция имеет большое практическое значение и используется при получении фенолформальдегидных смол.
III. Реакция окисления
Фенолы легко окисляются даже под действием кислорода воздуха. При стоянии на воздухе фенол постепенно окрашивается в розовато-красный цвет.
1) Горение (полное окисление)
Фенолы, как и большинство органических веществ, сгорают до углекислого газа и воды.
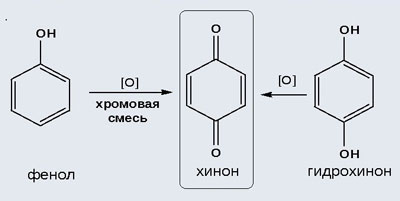
2) Окисление хромовой смесью
При энергичном окислении фенола хромовой смесью основным продуктом окисления является хинон. Двухатомные фенолы окисляются еще легче. При окислении гидрохинона также образуется хинон:
IV. Качественная реакция! — обнаружение фенола
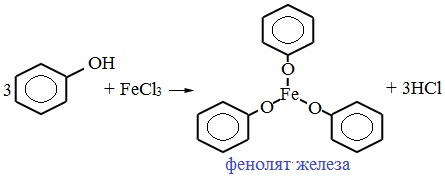
Для обнаружения фенолов используется качественная реакция с хлоридом железа (III). Одноатомные фенолы дают устойчивое сине-фиолетовое окрашивание, что связано с образованием комплексных соединений железа.
Видеоопыт «Качественная реакция на фенол»
Образование фиолетового окрашивания при добавлении раствора FeCl3 служит качественной реакцией на фенол:
Для фенолов реакции по связям С-О не характерны, поскольку атом кислорода прочно связан с атомом углерода бензольного кольца за счет участия своей неподеленной электронной пары в системе сопряжения.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Урок по химии «Химические свойства фенола» (естественно-научный профиль). 10-й классКласс: 10 Презентация к урокуФорма урока: комбинированный (2 часа). Цели:
Оборудование: мультимедийная установка, шаростержневые модели бензола, этилового спирта, презентация “Химические свойства фенола”. На ученических столах: коллекция изделий на основе фенолформадегильной смолы, FeCl3, чайная заварка. 1. Организационный момент. 2. Актуализация опорных знаний и мотивация познавательной деятельности. Учитель: Предлагает ответить на вопросы (Слайды: 1, 2) и наводит на определение темы и целей урока.
Учитель: В основе учения об органических веществах лежит теория химического строения А.М.Бутлерова. Объясните почему? (Ответ: Эта теория раскрывает взаимосвязь между строением веществ и их свойствами, показывает, что свойства веществ неслучайные). Из каких двух знакомых фрагментов состоит молекула фенола? Сформулируйте 3 положение теории А.М.Бутлерова. 3. Определение темы урока, целей и задач урока. Учитель задаёт вопрос: Как вы считаете, какой будет тема урока? (Ученики высказывают версии, формулируют с помощью учителя тему урока. Записывают тему урока в тетрадь). Слайд 3. 4. Изучение нового материала. Учитель: Свойствами каких соединений формально должен обладать фенол? (Ответ: фенол должен сочетать свойства аренов (бензола) и одноатомных спиртов). Учитель: Оказывается, это не совсем так. Именно поэтому фенолы рассматриваются отдельно от класса спиртов. Учитель: Как Вы думает, в чем причина? (Ответ: причина кроется в том, что в результате взаимного влияния гидроксильной группы и ароматического радикала химические свойства этих фрагментов изменяются, а фенол в целом приобретает некоторые особенные свойства). (Слайд: 7). 4.1. Кислотные свойства фенола. Ученики предполагают, что для фенола характерна реакция с Ме (IА). (Слайды: 8, 9).
Учитель: первым доказательством более сильных кислотных свойств фенола по сравнению со спиртами является тот факт, что в водном растворе наблюдается незначительная диссоциация фенола: C6H5OHFC6H5O – + H + . (Слайд: 10). В отличие от спиртов фенол взаимодействует с щелочами.
Реакция обратима, т.к. фенолят натрия — это соль, образованная слабой кислотой и сильным основанием. (Слайд: 11, 12). Вопрос: что происходит с солями в водном растворе? Какова реакция среды в растворе фенолята натрия? (Ответ: они гидролизуются; среда щелочная). (Слайд: 13). Учитель: первым названием фенола было карболовая кислота. Однако кислота эта значительно слабее не только сильных, но даже некоторых неорганических кислот, даже угольной:
Отличие от спиртов: (Слайд: 14).
Вопрос: Чем обусловлено различие кислотных свойств спиртов и фенола? (Ответ: различие кислотных свойств спиртов и фенола обусловлено влиянием радикала на гидроксильную группу: радикал фенил — C6H5 увеличивает подвижность атома водорода в ОН группе, а алкильные радикалы (- СН3, — C2H5) уменьшают ее, поэтому кислотные свойства у фенола выражены сильнее, чем у спиртов. (Слайд: 15). Вопрос: как можно получить сложные и простые эфиры? Ученики высказывают свои предположения. Затем идет объяснение. Учитель: в отличие от спиртов, фенолы не образуют сложных эфиров при действии на них карбоновых кислот, для этого можно использовать хлорангидриды кислот. H3CC(O)Cl+HO–C6H5 —> H3C–C(O)–O–C6H5+HCl (Слайд: 16). В качестве исходных веществ для получения простых и сложных эфиров используются также феноляты. (Слайды: 17, 18). Затем ученики составляют уравнения возможных реакций получения эфиров. (Слайд: 19). (На усмотрение учителя данное упражнение может быть выполнено учениками в качестве домашнего задания). 4.2. Реакции электрофильного замещения. Учитель: Почему реакции электрофильного замещения в бензольном кольце фенола протекают легче, чем у бензола, и в более мягких условиях? (Слайд: 20). Ответ: Влияние ОН — группы на бензольное кольцо ОН — группа — заместитель I рода. Подает электроны на бензольное кольцо, увеличивая электронную плотность в орто и пара положениях.Атомы Н в положениях 2,4,6 — более подвижны и легко замещаются. (Слайд: 21). Хлорирование (Слайд: 22). Реакция с бромной водой- качественная реакция. (Слайд: 23, 24). Аналогичные закономерности наблюдаются при нитровании фенола. Однако при действии на фенол разбавленной азотной кислотой можно получить смесь монозамещенных нитропроизводных: о-нитрофенола и п-нитрофенола. (Слайд: 25). Ученик у доски записывает реакцию взаимодействия фенола с разбавленной HNO3. Проверка — (Слайд: 26). При взаимодействии с концентрированной азотной кислотой образуется 2,4,6—тринитрофенол. Ученик у доски записывает реакцию взаимодействия фенола с концентрированной HNO3. Проверка — (Слайд: 27). Электроноакцепторные свойства нитрогрупп значительно усиливают кислотность тринитрофенола. Он является примерно в миллиард раз более сильной кислотой по сравнению с фенолом, и в 100 раз сильнее фосфорной кислоты. (Слайд: 28). Рассказ учителя. Впервые тринитрофенол получил в 1771г. английский химик П.Вульф действием азотной кислоты на природное органическое вещество индиго. Благодаря интенсивной желтой окраске вещества его стали использовать в качестве красителя для волокна и тканей. Из-за горького вкуса тринитрофенол назвали сначала пикрином (от греческого слова pykros — горький, острый), а затем — пикриновой кислотой. В 1779г. выяснилось, что это вещество способно взрываться. Но только после того, как на нескольких красильных фабриках произошли несчастные случаи в результате взрывов пикриновой кислоты, она в 1885г. была запатентована в качестве взрывчатого вещества. 4.3. Реакция поликонденсация. Одним из важнейших свойств фенола, используемых в промышленности, является его способность вступать в реакцию с формальдегидом в присутствии кислотных или основных катализаторов происходит реакция поликонденсации, в ходе которой образуется реакция поликонденсации, в ходе которой образуется высокомолекулярное соединение — фенолформальдегидная смола и выделяется низкомолекулярный продукт вода. (Слайд: 29, 30, 31, 32). Из фенолформальдегидной смолы получают пластмассы — фенопласты (бакелиты). Фенопласты — важнейшие заменители цветных и черных металлов во многих отраслях промышленности. Из них изготавливается большое количество изделий широкого потребления, электроизоляционные материалы и строительные детали. Сравнение с реакцией полимеризацией. Закрепление понятий “полимер”, “мономер”, “структурное звено”, “степень полимеризации”, “степень поликонденсации”. Работа с коллекцией изделий на основе фенолформадегильной смолы. 4.5. Взаимодействие с раствором хлорида железа (III). Качественной реакцией на фенол и его гомологи является образование окрашенных комплексов с раствором хлорида железа (III). (Слайд 33, 34). В экстрактах многих растений, особенно обладающих дубильным и вяжущим действием, содержатся вещества, называемые “танины”. В состав их молекул входит большое число фенольных остатков. Они также дают с хлорным железом интенсивное окрашивание. Ученики проводят опыт: в пробирку наливают 2-3 мл холодной чайной заварки светло-желтого цвета и добавляют 2-3 капли раствора хлорида железа (III). Жидкость приобретает чернильный цвет. В чайных листах содержится большое количество танина, придающего напитку терпкий вяжущий привкус. Ученик у доски записывает реакцию взаимодействия фенола с водородом. Проверка — (Слайд 35). Объяснение: фенолы легко окисляются даже под действием кислорода воздуха. На воздухе фенол постепенно окрашивается в розовато-красный цвет. При окислении фенола сильными окислителями основным продуктом окисления является хинон. Двухатомные фенолы окисляются легче. При окислении гидрохинона также образуется хинон. Окисление фенола и гидрохинона. (Слайд 37, 38). На усмотрение учителя данный материал может быть рассмотрен на элективных курсах при подготовке к ЕГЭ. 5. Заключительная часть. Задания для закрепления материала и развития логического мышления. (Слайд 39-41). 6. Подведение итогов урока. Рефлексия. Учитель предлагает ученикам определить результаты урока, сравнить их с целями. 7. (Слайд 42). Домашнее задание. Параграф 18 по учебнику О.С.Габриелян, И.Г.Остроумов, С.Ю.Пономарев. Химия. 10 класс (М. Дрофа, 2014); стр. 193 № 1-10. |

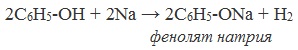
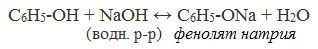
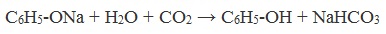

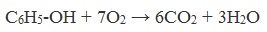


 C6H5ONa + H2O
C6H5ONa + H2O +NaHCO3.
+NaHCO3.


