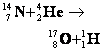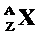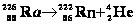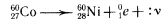Правило смещения при радиоактивном распаде в радиохимии и ядерной физике, которое также известно под названием закона Содди-Фаянса, представляет собой правило, определяющее превращение одного элемента в другой во время радиоактивного распада. Оно было изложено в 1913 году независимо двумя учеными: английским радиохимиком Фредериком Содди и американским физико-химиком с польскими корнями Казимиром Фаянсом.
- Достижения Фредерика Содди в области радиоактивности
- Работы Казимира Фаянса
- Понятие радиоактивности
- Нестабильные атомные изотопы
- Различные виды радиоактивности
- Корпускулярные виды распада
- Гамма-распад
- Правила радиоактивного смещения
- Правила смещения
- Строение атомного ядра. Типы радиоактивного распада (правило смещения).
Достижения Фредерика Содди в области радиоактивности
Содди вместе с Резерфордом стоит у истоков открытия радиоактивных атомных превращений. Так, в 1903 году Содди открыл, что радий в процессе своего распада излучает ядра гелия. Также этот ученый показал, что атомы одного и того же химического элемента могут иметь различные массы, что привело его к разработке концепции изотопов. Содди установил правила смещения химических элементов во время альфа- и бета- радиоактивных распадов, что стало важным шагом в понимании взаимосвязи между семействами радиоактивных элементов.
В 1921 году Фредерик Содди был удостоен Нобелевской премии по химии за важные открытия в области физики радиоактивных элементов и за исследования природы изотопов.
Работы Казимира Фаянса
Этот ученый провел важные исследования радиоактивности различных изотопов и разработал квантовую теорию электронной структуры молекул. В 1913 году одновременно с Фредериком Содди и независимо от него Фаянс открыл правила смещения, которые регулируют преобразование одних химических элементов в другие в процессе радиоактивных распадов. Также Фаянс открыл новый химический элемент — протактиний.
Понятие радиоактивности
Перед тем как рассмотреть законы радиоактивного распада и правила смещения, необходимо разобраться с понятием радиоактивности. В физике под этим словом понимают способность ядер некоторых химических элементов испускать излучение, обладающее следующими свойствами:
- способность проникать в человеческие ткани, оказывая разрушающее действие;
- способность ионизировать газы;
- стимуляция процесса флюоресценции;
- прохождение через различные твердые и жидкие тела.
Благодаря этим способностям обычно это излучение называют ионизирующим. Природа радиоактивного излучения может быть либо электромагнитной, например, рентгеновские лучи или гамма-излучение, либо носить корпускулярный характер, испускание ядер гелия, протонов, электронов, позитронов и других элементарных частиц.
Таким образом, радиоактивность — это феномен, наблюдаемый у нестабильных ядер атомов, которые спонтанно способны превращаться в ядра более стабильных элементов. Говоря простыми словами, нестабильный атом испускает радиоактивное излучение, чтобы стать стабильным.
Нестабильные атомные изотопы
Нестабильные изотопы, то есть атомы одного и того же химического элемента, которые обладают различной атомной массой, находятся в возбужденном состоянии. Это говорит о том, что они обладают повышенной энергией, которую стремятся отдать, чтобы перейти в равновесное состояние. Учитывая, что все энергии атома квантованы, то есть имеют дискретные значения, то и сам радиоактивный распад происходит за счет потери конкретной кинетической энергии.
Нестабильный изотоп в процессе радиоактивного распада переходит в более стабильный, но это не значит, что новое образованное ядро не будет обладать радиоактивностью, оно также может распадаться. Ярким примером этого процесса является ядро урана-238, которое за несколько столетий испытывает ряд распадов, превращаясь, в конце концов, в атом свинца. Отметим, что в зависимости от вида изотопа, он спонтанно может распадаться, как через миллионные доли секунды, так и через миллиарды лет, например, тот же уран-238 имеет период полураспада (время, за которое половина ядер распадается) равный 4,468 млрд лет, в то же время для изотопа калия-35 этот период равен 178 миллисекундам.
Различные виды радиоактивности
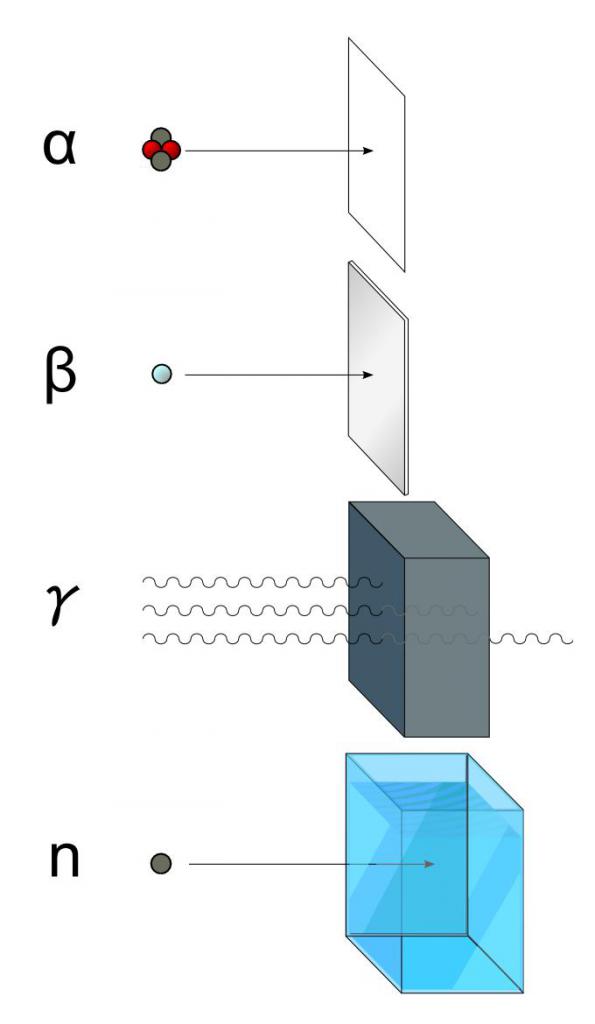
Применение того или иного правила радиоактивного смещения зависит от типа радиоактивного распада, который испытывает конкретный элемент. В общем случае выделяют следующие виды радиоактивности:
- альфа-распад;
- бета-распад;
- гамма-распад;
- распад с испусканием свободных нейтронов.
Все эти виды радиоактивного распада (за исключением испускания свободных нейтронов) установил новозеландский физик Эрнест Резерфорд еще в начале XX века.
Корпускулярные виды распада
Альфа-распад связан с испусканием ядер гелия-4, то есть речь идет о корпускулярном излучении, частицы которого состоят из двух протонов и двух нейтронов. Это означает, что масса этих частиц равна 4 в атомных единицах массы (АЕМ), а электрический заряд равен +2 в единицах элементарного электрического заряда (1 элементарный заряд в системе СИ равен 1,602*10 − 19 Кл). Испущенное ядро гелия до распада входило в состав ядра нестабильного изотопа.
Природа бета-распада заключается в испускании электронов, которые имеют массу 1/1800 АЕМ и заряд -1. Ввиду отрицательного заряда электрона, этот распад называют бета-отрицательным. В отличие от альфа-частицы электрон не существовал до распада в атомном ядре, а образовался в результате превращения в протон нейтрона. Последний остался в ядре после распада, а электрон покинул атомное ядро.
Впоследствии был обнаружен бета-положительный распад, который заключается в испускании позитрона-античастицы электрона. Радиоактивный позитрон образуется в результате обратной реакции, чем электрон, то есть протон в ядре превращается в нейтрон, теряя при этом свой положительный заряд.
В ряде радиоактивных превращений одного ядра в другое происходит испускание нейтронов различных энергий. Как и протон, нейтрон имеет массу 1 АЕМ (если быть более точным, то нейтрон на 0,137% тяжелее протона) и обладает нулевым электрическим зарядом. Таким образом, при данном типе распада ядро-родитель теряет только 1 единицу своей массы.
Гамма-распад
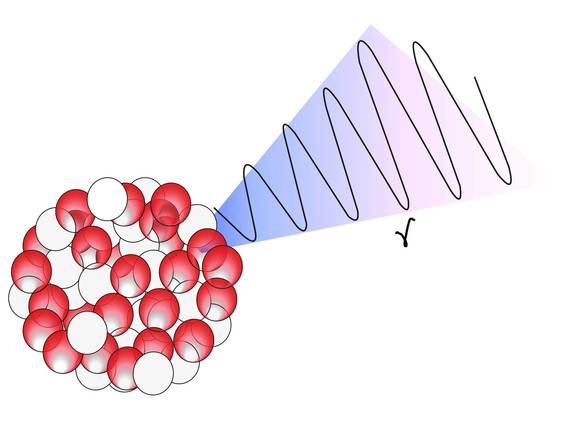
Гамма-распад в отличие от предыдущих видов распада имеет электромагнитную природу, то есть это излучение подобно рентгеновскому или видимому свету, однако, длина волны гамма-излучения намного меньше, чем у любой другой электромагнитной волны. Гамма-лучи не обладают массой покоя и зарядом. По сути, гамма-лучи — это лишняя энергия, которая существовала до распада в ядре атома, обуславливая его нестабильность. Химический элемент сохраняет свое положение в периодической таблице Д. И. Менделеева при гамма-распаде.
Правила радиоактивного смещения
Пользуясь этими правилами, можно легко определить, какой химический элемент должен получиться из данного родительского изотопа при определенном виде радиоактивного распада. Поясним эти правила смещения в физике:
- При альфа-распаде, поскольку ядро теряет 4 АЕМ массы и +2 единицы заряда, образуется химический элемент, стоящий на 2 позиции левее в периодической системе Д. И. Менделеева. Например, 92U 238 = 90Th 234 , здесь нижний индекс — заряд, верхний — масса ядра.
- В случае бета-отрицательного распада заряд материнского ядра увеличивается на 1 единицу, при этом масса остается неизменной (масса электрона, испускаемого в процессе этого распада, составляет всего 0,06% от массы протона). В данном случае правило смещения равновесия гласит, что должен образоваться изотоп химического элемента, стоящий на одну клетку правее от материнского элемента в таблице Д. И. Менделеева. Например, 82Pb 212 = 83Bi 212 .
- Правило смещения при бета-положительном распаде (излучение позитрона) гласит, что в результате этого процесса образуется химический элемент, который на 1 позицию стоит левее от материнского элемента, и имеет ту же массу ядра, что и он. Например, 7N 13 = 6C 13 .
Правила смещения
Под радиоактивным распадом,или просто распадом,понимают естественное радиоактивное превращение ядер, происходящее самопроизвольно. Атомное ядро испытывающее радиоактивный распад, называется материнским,возникающее ядро дочерним.
Теория радиоактивного распада строится на предположении о том, что радиоактивный распад является спонтанным процессом, подчиняющимся законам статистики. Поскольку отдельные радиоактивные ядра распадаются независимо друг от друга, можно считать, что число ядер dN, распавшихся в среднем за интервал времени от t до t + dt, пропорционально промежутку времени dt и числу N нераспавшихся ядер к моменту времени t:
где λ – постоянная для данного радиоактивного вещества величина, называемая постоянной радиоактивного распада;знак минус указывает, что общее число радиоактивных ядер в процессе распада уменьшается.
Разделив переменные и интегрируя, т. е.
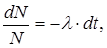
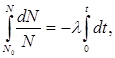

получим 
где N0 – начальное число нераспавшихся ядер (в момент времени t = 0), N – число нераспавшихся ядер в момент времени t. Формула (256.2) выражает закон радиоактивного распада,согласно которому число нераспавшихся ядер убывает со временем по экспоненте.
Интенсивность процесса радиоактивного распада характеризуют две величины: период полураспада Т½ и среднее время жизни τрадиоактивного ядра. Период полураспадаТ½ – время, за которое исходное число радиоактивных ядер в среднем уменьшается вдвое. Тогда, согласно (256.2),
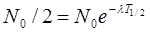

Периоды полураспада для естественно-ралиоактивиых элементов колеблются от десятимиллионных долей секунды до многих миллиардов лет.
Суммарная продолжительность жизни dN ядер равна t|dN| = = λN t dt. Проинтегрировав это выражение по всем возможным t (т. е. от 0 до ¥) и разделив на начальное число ядер N0 получим среднее время жизни t радиоактивного ядра:
(учтено (256.2)). Таким образом, среднее время жизни t радиоактивного ядра есть величина, обратная постоянной радиоактивного распада l.
Активностью Ануклида(общее название атомных ядер, отличающихся числом протонов Z, и нейтронов N) в радиоактивном источнике называется число распадов, происходящих с ядрами образца в 1 с:

Единица активности в СИ – беккерель(Бк); 1 Бк – активность нуклида, при которой за 1 с происходит один акт распада. До сих пор в ядерной физике применяется и внесистемная единица активности нуклида в радиоактивном источнике кюри(Ки): 1 Ки = 3,7×10 10 Бк.
Радиоактивный распад происходит в соответствии с так называемыми правилами смещения,позволяющими установить, какое ядро возникает в результате распада данного материнского ядра. Правила смещения;
для a-распада
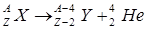
для b-распада

где 
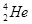
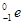
Возникающие в результате радиоактивного распада ядра могут быть, в свою очередь, радиоактивными. Это приводит к возникновению цепочки,или ряда, радиоактивных превращений,заканчивающихся стабильным элементом. Совокупность элементов, образующих такую цепочку, называется радиоактивным семейством.
Из правил смещения (256.4) и (256.5) вытекает, что массовое число при a-распаде уменьшается на 4, а при b-распаде не меняется. Поэтому для всех ядер одного и того же радиоактивного семейства остаток от деления массового числа на 4 одинаков. Таким образом, существует четыре различных радиоактивных семейства, для каждого из которых массовые числа задаются одной из следующих формул:
где п — целое положительное число. Семейства называются по наиболее долгоживущему (с наибольшим периодом полураспада) «родоначальнику»: семейства тория (от 
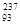



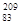

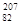
Объяснение a-распада дано квантовой механикой, согласно которой вылет a-частицы из ядра возможен благодаря туннельному эффекту – проникновению a-частицы сквозь потенциальный барьер. Всегда имеется отличная от нуля вероятность того, что частица с энергией, меньшей высоты потенциального барьера, пройдет сквозь него, т. е., действительно, из a-радиоактивного ядра a-частицы могут вылетать с энергией, меньшей высоты потенциального барьера. Этот эффект целиком обусловлен волновой природой a-частиц.
Вероятность прохождения a-частицы сквозь потенциальный барьер определяет- ся его формой и вычисляется на основе уравнения Шредингера.
Механизм происхождения электронов при b — -распадеследующий.
Электрон не вылетает из ядра и не вырывается из оболочки атома. b-Электрон рождается в результате процессов, происходящих. внутри ядра. Так как при b — -распаде число нуклонов в ядре не изменяется, а Z/ увеличивается на единицу (см. (256,5) ) , то единственной возможностью одновременного осуществления этих уcловий является превращение одного из нейтронов b — -активного ядра в протон с одновременным образованием электрона и вылетом антинейтрино:

Этот процесс сопровождается выполнением законов сохранения электрических зарядов, импульса и массовых чисел. Кроме того, данное превращение энергетически возможно, так как масса покоя нейтрона превышает массу атома водорода, т. е. протона и электрона вместе взятых. Данной разности в массах соответствует энергия. равная 0,782 МэВ. За счет этой энергии может происходить самопроизвольное превращение нейтрона в протон; энергия распределяется между электроном и антинейтрино.
Антинейтрино (античастица по отношению к нейтрино) имеет нулевой заряд, спин ħ/2 и нулевую (а скорее –4 me) массу покоя; обозначается 

Нейтрино единственная частица, не участвующая ни в сильных, ни в электромагнитных взаимодействиях; единственный вид взаимодействий, в котором может принимать участие нейтрино, — слабое взаимодействие.Поэтому прямое наблюдение нейтрино весьма затруднительно. Ионизирующая способность нейтрино столь мала, что один акт ионизации в воздухе приходится на 500 км пути. Проникающая же способность нейтрино столь огромна (пробег нейтрино с энергией 1 МэВ в свинце составляет порядка 10 18 м!), что затрудняет удержание этих частиц в приборах.
Введение нейтрино (антинейтрино) позволило не только объяснить кажущееся несохранение спина, но и разобраться с вопросом непрерывности энергетического спектра выбрасываемых электронов. Сплошной спектр b — -частиц обязан распределению энергии между электронами и антинейтрино, причем сумма энергий обеих частиц равна Етах. В одних актах распада большую энергию получает антинейтрино. в других — электрон; в граничной точке кривой (см. рис. 40), где энергия электрона равна Етах, вся энергия распада уносится электроном, а энергия антинейтрино равна нулю.
Экспериментально установлено, что γ-излучение (см. §255) не является самостоятельным видом радиоактивности, а только сопровождает α- и β-распады и также возникает при ядерных реакциях, при торможении заряженных частиц, их распаде н т. д. γ -Спектр является линейчатым γ-Спектр – это распределение числа γ-квантов по энергиям (такое же толкование β-спектра дано и § 258). Дискретность γ-спекгра имеет принципиальное значение, так как является доказательством дискретности энергетических состояний атомных ядер.
В настоящее время твердо установлено, что γ-ичлучение, испускается дочерним (а не материнским) ядром. Дочернее ядро а момент своего образования, оказываясь возбужденным, за время примерно 10 -13 — 10 –14 с, значительно меньшее времени жизни возбужденного атома (примерно 10 -8 с), переходит в основное состояние с испусканием γ-излучсния. Возвращаясь в основное состояние, возбужденное ядро может пройти через ряд промежуточных состояний, поэтому γ-излучение одного и того же радиоактивного изотопа может содержать несколько групп γ-квантов, отличающихся одна от другой своей энергией.
При γ-излучении A и Z. ядра не изменяются, поэтому оно не описывается никакими правилами смещения. γ-Излучение большинства ядер является столь коротковолновым, что его волновые свойства проявляются весьма слабо. Здесь на первый план выступают корпускулярные свойства, поэтому γ-излучение рассматривают как поток частиц — γ-квантов. При радиоактивных распадах различных ядер γ-кванты имеют энергии от 10 кэВ до 5 МэВ.
Строение атомного ядра. Типы радиоактивного распада (правило смещения).
Строение атомного ядра
В 1911 г. в результате исследований, проведенных Резерфордом по рассеянию α-частиц при прохождении через вещество, был открыт протон — ядро атома водорода, который обладает положительным электрическим зарядом, равным модулю заряда электрона.
Заряд ядра атома
Английский физик Г. Мозли в 1913 г. предсказал, что заряд ядра атома q,=Ze, где е —элементарный электрический заряд; Z — порядковый номер элемента в таблице Менделеева, определяет число электронов в атоме. Химические свойства зависят только от зарядового числа. Немецкие ученые В. Боте и Г. Беккер, изучая реакции (1930),происходящие при облучении бериллия α-частицами, обнаружили новое излучение, обладающее очень большой проникающей способностью.
В 1932 г. английский физик Дж. Чэдвик выдвинул гипотезу: бериллиевые лучи состоят из нейтральных частиц, масса которых близка к массе протона. Их назвали нейтронами.
Дальнейшие исследования показали, что нейтрон — нестабильная частица: свободный нейтрон за время 15 мин распадается на протон, электрон и нейтрино — частицу, лишенную массы покоя.
Масса нейтрона mn=1838,6 электронных масс, масса протона mp= 1836,1 электронных масс, mn > mp приблизительно на 2,5 массы электрона. После открытия нейтрона Д. Д. Иваненко и В. Гейзенберг выдвинули гипотезу о протонно-нейтронном строении ядра.
В ядре протон и нейтрон неразличимы, поэтому их называют нуклонами (ядерными частицами). Число протонов Z, число нейтронов N, массовое число—это суммарное число нуклонов в ядре А..
Z — заряд ядра,
номер элемента в таблице Менделеева
N — число нейтронов
Обозначение химических элементов (ядер) в атомной и ядерной физике.
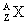
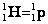
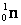
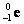
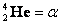
Типы радиоактивного распада
(правила смещения)
Альфа-распад
Превращение атомных ядер, сопровождаемое испусканием a—частиц, называетсяальфа-распадом. Теория создана Г.А. Гамовым в 1930-32 г. на основе квантово-механического туннельного эффекта.
Наиболее устойчивым из всех образований внутри ядра является образование двух протонов и двух нейтронов. Если при распределении энергии между частицами ядра это образование будет обладать энергией большей, чем энергия связи, то оно покинет ядро в виде a-частицы.
Если 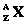
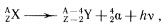
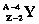
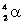
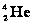
При альфа-распаде происходит смещение химического элемента на две клетки влево в таблице Менделеева.
Бета-распад Теория создана в 1930г. Энрико Ферми.
Радиоактивные ядра могут выбрасывать поток электронов, которые рождаются согласно гипотезе Ферми в результате превращения нейтронов в протоны. В соответствии с правилом смещения массовое число ядра не изменяется: 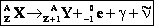
При β- распаде химический элемент перемещается на одну клетку вправо в периодической системе Менделеева и, кроме электронов, испускается антинейтрино,
Гамма-излучение возникает при ядерных превращениях и представляет собой электромагнитное излучение. Имеет высокую энергию.
Э. Резерфорд установил, что воздух сильнее всего ионизуют α-лучи, в меньшей степени— β-лучи и совсем плохо — γ-лучи. Поэтому проникающая способность оказалась самая малая у α-лучей (лист бумаги; несколько сантиметров слоя воздуха), а β-лучи проходят сквозь алюминиевую пластину толщиной в несколько миллиметров. Очень велика проникающая способность у γ-лучей (например, для алюминия — пластины толщиной десятки сантиметров).