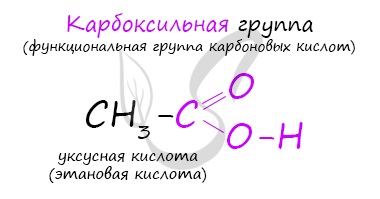
Карбоновые кислоты — класс органических соединений, молекулы которых содержат одну или несколько карбоксильных групп COOH.
Имеют разнообразное промышленное применение и большое биологическое значение. Общая формула одноосновных карбоновых кислот CnH2nO2 .
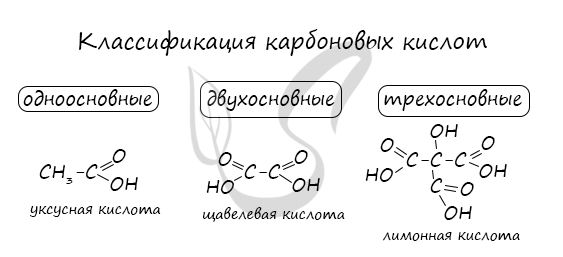
Классификация карбоновых кислот
По количеству карбоксильных групп в молекуле карбоновые кислоты подразделяются на:
- Одноосновные — 1 карбоксильная группа
- Двухосновные — 2 карбоксильных группы
- Трехосновные — 3 карбоксильных группы
Высшие карбоновые кислоты называют жирными кислотами. Более подробно мы изучим их теме, посвященной жирам, в состав которых они входят.
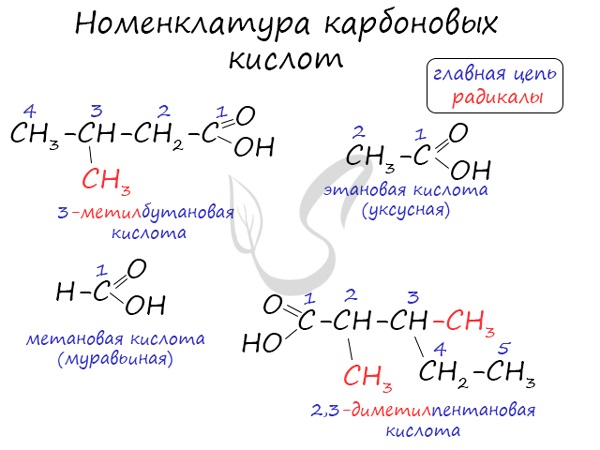
Номенклатура и изомерия карбоновых кислот
Названия карбоновых кислот формируются путем добавления суффикса «овая» к названию алкана с соответствующим числом атомов углерода и слова кислота: метановая кислота, этановая кислота, пропановая кислота, и т.д.
Многие карбоновые кислоты имеют тривиальные названия. Наиболее известные:
- Метановая — HCOOH — муравьиная кислота
- Этановая — CH3-COOH — уксусная кислота
- Пропановая — C2H5-COOH — пропионовая кислота
- Бутановая — C3H7-COOH — масляная кислота
- Пентановая — C4H9-COOH — валериановая кислота
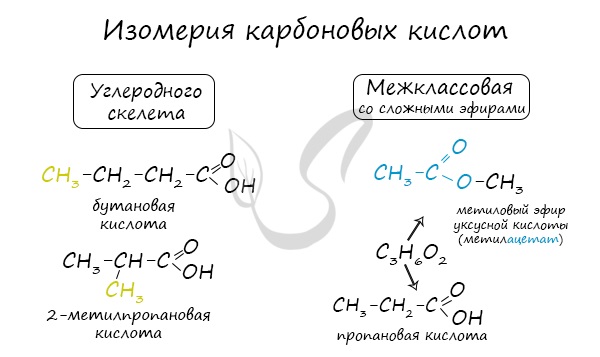
Для предельных карбоновых кислот характерна структурная изомерия: углеродного скелета, межклассовая изомерия со сложными эфирами.
Получение карбоновых кислот
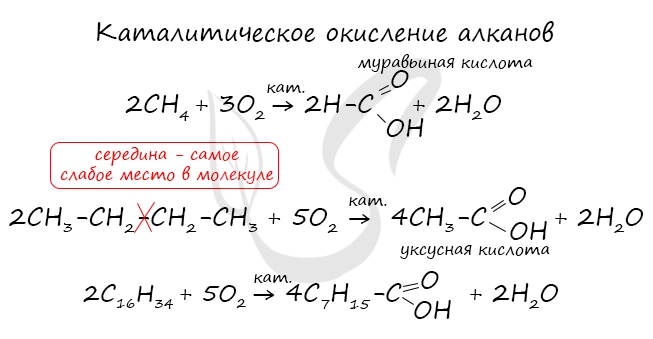
- Окисление алканов
При повышенной температуре и в присутствии катализатора становится возможным неполное окисление алканов, в результате которого образуются кислоты.
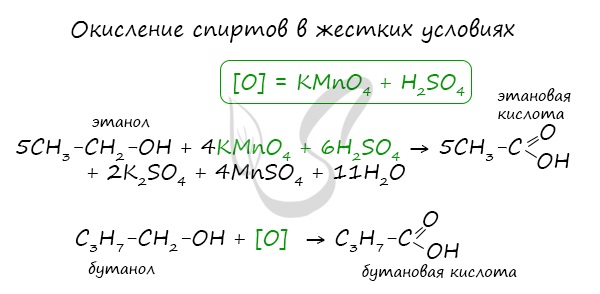
При реакции спиртов с сильными окислителями, такими как подкисленный раствор перманганата калия, спирты окисляются до соответствующих кислот.
При окислении альдегиды образуют соответствующие карбоновые кислоты. Окисление можно проводить качественной реакцией на альдегиды — реакцией серебряного зеркала.
Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли.
Окисление альдегидов также может быть успешно осуществлено другим реагентом — свежеосажденным гидроксидом меди II. В результате такой реакции образуется осадок кирпично-красного цвета оксида меди I.
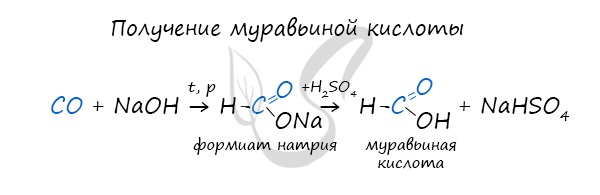
Существует специфический способ получения муравьиной кислоты, который заключается в реакции твердого гидроксида щелочного металла с угарным газом под давлением и температуре 200°С — образуется формиат (соль муравьиной кислоты).
При дальнейшей обработке формиата серной кислотой образуется муравьиная кислота.
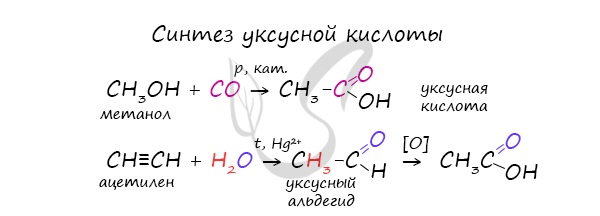
Специфичность синтеза уксусной кислоты заключается в реакции угарного газа с метанолом, в результате которой она образуется.
Также уксусную кислоту можно получить другим путем: сначала провести реакцию Кучерова, в ходе которой образуется уксусный альдегид. Окислить его до уксусной кислоты можно аммиачным раствором оксида серебра или гидроксидом меди II.
Химические свойства карбоновых кислот
Для карбоновых кислот не характерны реакции присоединения. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем спирты.
Карбоновые кислоты вступают в реакции с металлами, которые способны вытеснить водород (стоят левее водорода в ряду напряжений металлов) из кислоты. Реагируют также с основаниями, с солями более слабых кислот, например, угольной кислоты.
Галогенирование происходит по типу замещения в радикале, который соединен с карбоксильной группой. Напомню, что наиболее легко замещается водород у третичного, чуть сложнее — у вторичного, и значительно сложнее — у первичного атома углерода.
Сила карбоновых кислот тем выше, чем меньше электронной плотности сосредоточено на атоме углерода в карбоксильной группе. Поэтому самая слабая из трех кислот — уксусная, чуть сильнее — хлоруксусная, за ней — дихлоруксусная и самая сильная — трихлоруксусная.
Перераспределение электронной плотности в молекулах этих кислот для лучшего запоминания лучше увидеть наглядно. Это перераспределение обусловлено большей электроотрицательностью хлора, который притягивает электронную плотность.
Муравьиная кислота отличается от своих гомологов. За счет наличия у нее альдегидной группы, она, единственная из карбоновых кислот, способна вступать в реакцию серебряного зеркала.
В такой реакции идет ее окисление до нестойкой угольной кислоты, которая распадается на углекислый газ и воду.
При нагревании и в присутствии серной кислоты (водоотнимающего компонента) муравьиная кислота распадается на воду и угарный газ.
Сложные эфиры
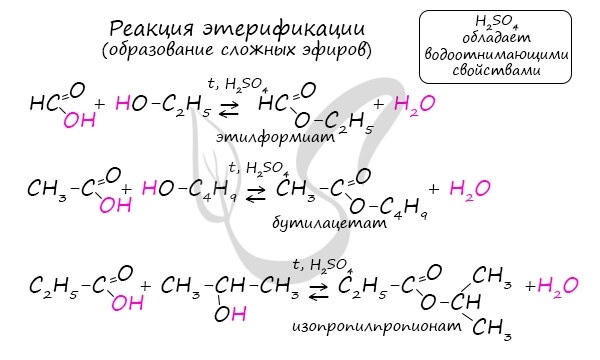
Получение сложных эфиров происходит в реакции этерификации (лат. aether — эфир), заключающейся во взаимодействии карбоновой кислоты и спирта.
Названия сложных эфиров формируются в зависимости от того, какой кислотой и каким спиртом эфир образован. Примеры:
- Метановая кислота + метанол = метиловый эфир метановой кислоты (метилформиат)
- Этановая кислота + этанол = этиловый эфир уксусной кислоты (этилацетат)
- Метановая кислота + этанол = этиловый эфир метановой кислоты (этилформиат)
- Пропановая кислота + бутанол = бутиловый эфир пропионовой кислоты (бутилпропионат)
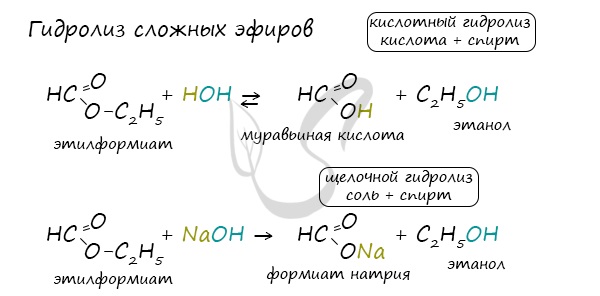
Для сложных эфиров характерной реакцией является гидролиз — их разложение. Возможен щелочной гидролиз, при котором образуется соль кислоты и спирт, и кислотный гидролиз, при котором образуются исходные спирт и кислота.
Кислотный гидролиз протекает обратимо, щелочной — необратимо. Реакция щелочного гидролиза по-другому называется реакция омыления, и напомнит о себе, когда мы дойдем до темы жиров.
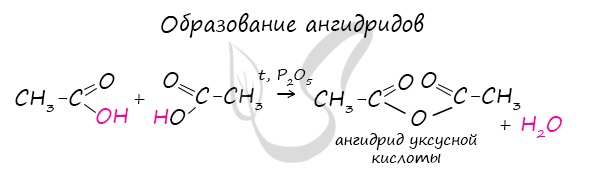
Ангидриды
Ангидриды — химические соединения, производные неорганических и органических кислот, образующиеся при их дегидратации.
Хлорангидриды карбоновых кислот образуются в реакции карбоновых кислот с хлоридом фосфора V.
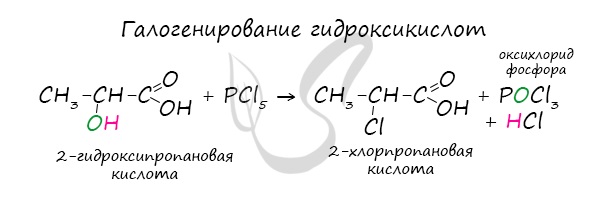
Следующая реакция не имеет отношения к ангидридам, однако (из-за их схожести) вы увидите ее здесь для наилучшего запоминания. Это реакция галогенирования гидроксикислот, в результате которой гидроксогруппа в радикале меняется на атом галогена.
Непредельные карбоновые кислоты
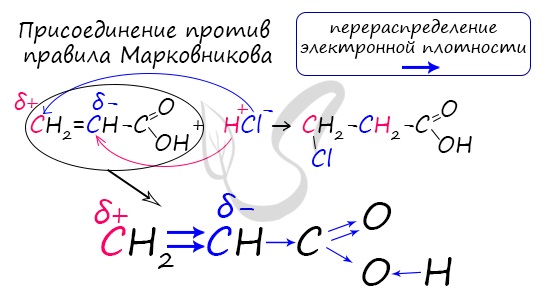
Распределение электронной плотности в молекулах творит чудеса: иногда реакции идут против правила Марковникова. Так происходит в непредельной акриловой кислоте.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
«Карбоновые кислоты» (10-11 классы)
материал для подготовки к егэ (гиа) по химии (10 класс) на тему
Материл содержит краткое теоретическое введение, примеры решения задания и задания для самостоятельного решения.
Предназначен не только для обучающихся 10 класса, но для 11 класса при подготовке к ЕГЭ. Учителям можно использовать задания для контроля знаний, распределив их дифференцированно по вариантам
Скачать:
| Вложение | Размер |
|---|---|
| Краткая теория, примеры решения и задания для самостоятельной работы | 21.54 КБ |
Предварительный просмотр:
Карбоновые кислоты – производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на карбоксильную группу
Особенности химических свойств карбоновых кислот обусловлены сильным взаимным влиянием карбонильной и гидроксильной групп.
Поэтому все химические реакции карбоновых кислот будут идти по следующим направлениям:
- замещение водорода в гидроксильной группе. Карбоновые кислоты – слабые электролиты и взаимодействуют с активными металлами, оксидами и гидроксидами металлов с образованием солей:
2CH 3 COOH + Mg → Mg(CH 3 COO) 2 + H 2 ;
уксусная кислота ацетат магния
C 2 H 5 COOH + NaOH → C 2 H 5 COONa + H 2 O.
пропионовая кислота пропионат натрия
- Замещение всей гидроксильной группы. Карбоновые кислоты реагируют со спиртами в присутствии сильных неорганических кислот, в результате образуется сложный эфир:
C 2 H 5 COOH + CH 3 OH = C 2 H 5 COOCH 3
пропионовая метиловый метиловый эфир пропионовой кислоты
кислота спирт (метилпропионат)
Примеры решения задач
Пример 1. Составить уравнения реакций, которые надо провести для осуществления следующих превращений: Метан → X → Y → уксусная кислота. Назвать вещества X и Y.
Решение . При нагревании метана получают ацетилен – вещество Х:
2СН 4 → С 2 Н 2 + 3Н 2 .
Гидратацией ацетилена в присутствии солей ртути (II) синтезируют уксусный альдегид – вещество Y:
C 2 H 2 + H 2 O → CH 3 COH.
Окислив уксусный альдегид кислородом воздуха в присутствии катализатора, получают уксусную кислоту:
2СН 3 СОН + О 2 → 2СН 3 СООН.
Пример 2. В трех пробирках без надписей находятся следующие вещества: этанол, муравьиная кислота, уксусная кислота. Какие химические реакции следует провести, чтобы различить эти вещества?
Решение . Спирт (этанол) можно отличить по действию веществ на индикаторы. Например, кислоты окрашивают синий лакмус в красный цвет, спирт – нет.
Различить муравьиную и уксусную кислоту легко, так как муравьиная кислота проявляет некоторые свойства альдегидов. Например, она вступает в реакцию «серебряного зеркала» (уксусная – нет):
НСООН + Ag 2 O → CO 2 ↑ + 2Ag + H 2 O.
Пример 3. Какой объем уксусной эссенции плотностью 1,07 г/мл надо взять для приготовления столового уксуса объмом 200 мл и плотностью 1,007 г/мл? Массовая доля уксусной кислоты в уксусной эссенции равна 80 %, в столовом уксусе – 6 %.
Решение . Определяем массу раствора уксуса, который надо приготовить:
m = V ∙ ρ; m = 200 ∙ 1,007 = 201,4 г.
Рассчитаем массу уксусной кислоты, которая содержится в уксусе:
m (CH 3 COOH) = m ∙ ω (CH 3 COOH) = 201,4 ∙ 0,06 = 12,1 г.
Вычисляем массу уксусной эссенции m ′, которая содержит уксусную кислоту массой 12,1 г: m ′ = 12,1/0,8 = 15,1 г.
Находим объем уксусной эссенции: V = 15,1/1,07 = 14,1 мл
Задачи и упражнения для самостоятельного решения
1. Составить уравнения реакций, при помощи которых можно осуществить следующие превращения:
С 2 Н 4 → С 2 Н 5 СОН → С 3 Н 7 ОН → С 3 Н 7 СООН.
2. Сколько изомерных карбоновых кислот может соответствовать формуле С 5 Н 10 О 2 ? Написать структурные формулы этих изомеров. ( Ответ : 4 изомера).
3. При окислении муравьиной кислоты получили газ, который пропустили через избыток раствора гидроксида кальция. При этом образовался осадок массой 20 г. Какая масса муравьиной кислоты взята для окисления?
4. В четырех пробирках находятся следующие вещества: пропионовая кислота, раствор формальдегида, раствор фенола в бензоле, метанол. При помощи каких химических реакций можно различить эти вещества?
5. Составить уравнения реакций, с помощью которых можно осуществить следующие превращения:
CH 4 → CH 3 Cl → CH 3 ОH → HCOH → HCOOH → CO 2 .
6. Какие массы растворов уксусной кислоты с массовой долей СН 3 СООН
90 и 10 % надо взять для получения раствора массой 200 г с массовой долей кислоты 40 %? ( Ответ : раствора с массовой долей 90 % − 75 г; 10 % − 125 г).
7. Сколько изомерных карбоновых кислот может соответствовать формуле С 6 Н 12 О 2 ? Написать структурные формулы этих изомеров.
( Ответ : 9 изомеров).
8. Назвать вещества Х и Y и составить уравнения реакций, с помощью которых можно осуществить следующие превращения:
а) метанол → Х → формиат натрия;
б) уксусный альдегид → Y → ацетат кальция.
9. Какой объем воды надо прибавить к 300 мл 70 %-го раствора уксусной кислоты (ρ = 1,07 г/мл), чтобы получить 30 %-й раствор? ( Ответ : 428 мл).
10 . Написать уравнения реакций, с помощью которых можно осуществить следующие превращения:
СаС 2 → С 2 Н 2 → СН 3 СОН → СН 3 СООН.
11. Рассчитать объем оксида углерода (II) (условия нормальные), который потребуется для получения раствора муравьиной кислоты массой 16,1 кг. Массовая доля НСООН в растворе, который требуется получить, равна 40 %.
12. Написать структурные формулы следующих кислот:
а) 3-метил-2-этилгексановая кислота;
б) 4,5-диметилоктановая кислота;
в) 2,2,3,3-тетраметилпентановая кислота.
13. Рассчитать массу бутановой кислоты, которая образуется при окислении бутанола-1 массой 40,7 г. ( Ответ : 48,4 г).
14. Какой объем 20 %-го раствора гидроксида калия плотностью 1,2 г/мл потребуется для полной нейтрализации 22,2 г пропионовой кислоты?
15. Написать уравнение реакции диссоциации бутановой кислоты и реакции получения натриевой соли этой кислоты.
16. Написать уравнения реакций, с помощью которых можно осуществить следующие превращения:
пропионовая кислота ← этилен → этанол → уксусная кислота.
17. К раствору муравьиной кислоты массой 36,8 г добавили избыток окислителя. Газ, полученный в результате окисления, пропустили через избыток баритовой воды Ba(OH) 2 , в результате чего получили осадок массой 39,4 г. Определить массовую долю кислоты в исходном растворе.
18. На нейтрализацию 3,7 г одноосновной предельной кислоты израсходовано 100 мл 0,5 М раствора КОН. Написать структурную формулу этой кислоты.
19. На нейтрализацию 30 г смеси раствора уксусной кислоты и фенола израсходовано 100 мл 2 М раствора NaOH, а при действии бромной воды на эту смесь образовалось 33,1 г осадка. Определить массовую долю (%) кислоты и фенола в растворе. ( Ответ : 20 % кислоты и 31,3 % фенола).
20. Определить массовую долю хлоруксусной кислоты, полученной при пропускании хлора в 75 %-й раствор уксусной кислоты.
Уравнения с карбоновыми кислотами с ответами
1. Относительная плотность паров предельной одноосновной карбоновой кислоты по воздуху равна 2,552. Выведите
молекулярную формулу карбоновой кислоты.
2. Относительная плотность паров предельной двухосновной карбоновой кислоты по водороду равна 59. Выведитемолекулярную формулу карбоновой кислоты.
3. Относительная плотность паров органического соединения по водороду равна 51.Массовая доля углерода в этом веществе равна 58,82%, массовая доля водорода равна 9,8%, массовая доля кислорода равна 31,38%. Выведите молекулярную
формулу органического соединения.
4. Относительная молекулярная масса органического соединения равна 284. Массовая доля углерода в этом веществе
равна 76,06%, массовая доля водорода равна 12,7%, массовая
доля кислорода равна 11,24%. Выведите молекулярную формулу органического соединения.
5. Относительная плотность паров органического соединения по водороду равна 30. При сжигании 24 г этого соединения образуется 35,2 г диоксида углерода и 14,4 г воды. Выведите молекулярную формулу органического соединения.