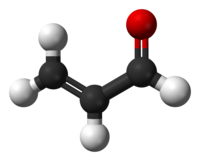
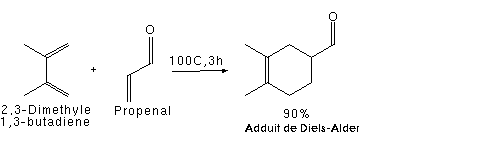
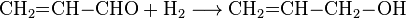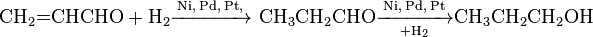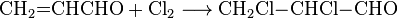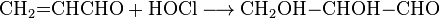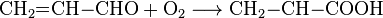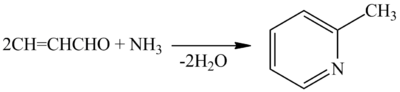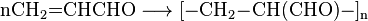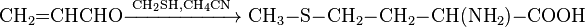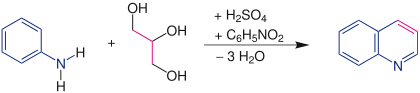Акролеин или акриловый альдегид (от лат. Acer, acris — «острый» и oleum — «масло», рус. Акролеин, англ. Acrolein, нем. Akrolein, Propenal) — С 3 Н 4 О или СН 2 = СНСН, органическое соединение с едким запахом, самый ненасыщенный альдегид, имеет очень высокую реакционную способность благодаря наличию альдегидной группы и двойной связи. Это бесцветная летучая жидкость с желтоватым оттенком, неприятным резким едким запахом пригорелых жиров, очень ядовитая, сильно раздражает слизистую оболочку глаз. В воздухе присутствует в виде паров, которые в 1,9 раза тяжелее ее и хорошо растворяются в воде. Легковоспламеняющаяся; хорошо растворяется в органических растворителях; растворимость в воде 40 г в 100 мл. Акролеин классифицируют как ядовитое вещество. При хранении он полимеризуется в твердую стекловидную массу — диакрил. Для стабилизации акролеина добавляют гидрохинон. На воздухе акролеин окисляется в пропенову кислоту.
В период между 1980 и началом 1990-х годов промышленное производство акролеина в разных странах мира составило: США — от 27 до 35 000 тонн / год, Япония (действует несколько производств) — около 20 000 тонн / год, Европейский Союз (производится во Франции и Германии) — от 60 000 тонн / год, Россия — 10 500 тонн / год (по состоянию на 1994 год).
В атмосферу акролеин поступает в виде выхлопных газов дизельных двигателей; образуется при термическом разложении жиров. Предельно допустимая концентрация акролеина — 0,2 мг / м³. Десятиминутное пребывание в атмосфере, содержащей 0,014% акролеина, для человека смертельно.
Акролеин применяют преимущественно в изготовлении фармацевтических препаратов и парфюмерии для изготовления ароматизаторов.
- Открытие
- Получение
- Синтез с формальдегид и этаналя
- Получение прямым окислением пропилена
- Окисления пропилена на медных катализаторах
- Окисления пропилена на фосфоромолибдати висмута
- Химические свойства
- Применение
- Физиологическое воздействие
- Общий характер действия
- Влияние на животных
- Воздействие на человека
- Видео по теме
- Acetyl
- Акролеин
- Открытие
- Из Википедии — свободной энциклопедии
- Реакционная способность
- Синтез
- Химические свойства
- Токсичность
- Применение
- Физиологическое воздействие
- Общий характер действия
- Влияние на животных
- Воздействие на человека
Открытие
Акролеин был открыт в 19 веке австрийским химиком Йозефом Редтенбахером при сухой перегонке жиров. В ходе своих исследований ученый также открыл и пропенову кислоту.
Получение
Синтез с формальдегид и этаналя
Метод был разработан фирмой Degussa, которая с 1942 года производила акролеин в промышленном масштабе. За ним формальдегид в виде 30% -ного водного раствора пропускается вместе с еквимолекулярною количеством этаналя при 300-320 ° C через силикагель, пропитанный 10% раствором силиката натрия. Степень превращения составляет 45-52%, а выход процесса достигает 70-80%. Альдегиды, отреагировали, отделяются перегонкой от акролеина и снова возвращаются в процесс.
Катализатором процесса является силикагель, пропитанный 10% раствором силиката натрия. Оптимальные температуры для этого катализатора 303-320 ° С. Поскольку образование акролеина протекает экзотермически, подвод тепла осуществляется в трубчатой печи.
В качестве побочных продуктов образуются метанол, 2-бутеналь и отработанный газ, которые можно без труда удалить. Для исключения полимеризации акролеина при разделении смеси нужно непрерывно подавать в перегонные колонны ингибитор. Добавление 0,1% ингибитора (гидрохинон или пирокатехин) делает акролеин устойчивым в течение года и исключает образование твердых осадков.
Получение прямым окислением пропилена
В 1936-1939 годах было установлено, что при окислении пропилена в присутствии сульфата ртути в сернокислом растворе образуется очень незначительное количество акролеина. Окисления пропилена в акролеин в промышленном масштабе проходит на катализаторах оксида меди (I) и молибдата висмута.
Окисления пропилена на медных катализаторах
В 1942 году американские ученые обнаружили, что при пропускании пропилена через оксид меди (I) и селенид серебра на асбесте при 295 ° C образовывалась значительное количество акролеина.
Это привело к разработке в 1946-1947 годах нового процесса фирмой Shell Development Co .. Пропилен вместе с воздухом и водяным паром пропускали при 370-400 ° C и небольшом давлении в присутствии 0,03 молярных% изопропилхлориду через оксид меди (I) на карбиде кремния. Максимальный выход акролеина равнялся 51%. Повышение давления кислорода увеличивает выход акролеина до 68-81%. В промышленном масштабе конверсия пропилена составляет 14% при 368 ° C и объемном соотношении пропилен: водяной пар: кислород = 4,4: 4,7: 1 в присутствии 0,4% оксида меди (I) на карбиде кремния. Выход акролеина колеблется в пределах 65-85%.
Образование акролеина происходит одновременно с полным окислением до диоксида углерода и воды, при этом катализаторы с высоким содержанием меди способствуют окислительной деструкции. Побочными продуктами реакции будут формальдегид, этаналь, диоксид углерода, органические кислоты, карбонильные соединения и полимеры.
Окисления пропилена на фосфоромолибдати висмута
В 1960 году американская фирма Sohio запустила первую промышленную установку для производства акрилонитрила по этому методу. При этом в промышленном масштабе получают и акролеин. Катализатором окисления пропилена, которое происходит при температуре 425-480 ° C, выступает фосфоромолибдат висмута на силикатной кислоте. Выход акролеина составляет около 70%.
Химические свойства
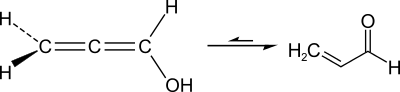
Акролеин, благодаря явлению таутомерии, находится в постоянном равновесии со своим изомер — пропадиенолом. Это равновесие может быть смещена действием кислотного или основного катализатора:
Поскольку акролеин является ненасыщенным альдегидом, то в химических реакциях он проявляет свойства как алкенов, так и альдегидов. В частности акролеин вступает в реакцию гидрогенування, с помощью которой можно получить аллиловый спирт
Кроме этого, с помощью действия катализаторов на основе никеля, палладия и платины, реакцию гидрогенування можно повести другим путем и через промежуточное образование пропаналя получить 1-пропанол:
В результате хлорирования акролеина получают α, β-дихлоропропаналь. В промышленности α, β-дихлорпропаналь действием соляной кислоты превращают в α-хлоракролеин, который является сырьем для получения α-хлоракрилатних смол:
Воздействие на акролеин хлорноватистая кислота приводит к образованию глицеральдегид:
Для акролеина характерна реакция окисления с образованием пропеновои кислоты:
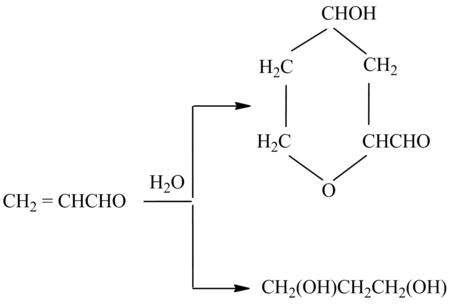
Гидролиз акролеина может проходить двумя путями. В результате образуются 1,3-пропандиол или сложная димерних состав:
Интересна взаимодействие акролеина с аммиаком, в результате которой происходит циклизация с образованием β-пиколина:
Как и любая ненасыщенная соединение, акролеин способен соединять собственные молекулы. Так в результате димеризации образуются димеры следующей строения:
а полимеризация приводит к образованию полиакролеину.
Также с акролеина можно получить незаменимую аминокислоту — метионин. Упрощенно этот процесс записывается следующим образом:
Путем реакции Скраупа ароматических аминов с акролеин, который образуется in situ из глицерина в присутствии дегидратирующего агента и окислителя, получают замещены хинолины:
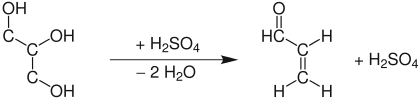
Применение
Наибольшее количество акролеина расходуется на синтез глицерина без использования хлора, где акролеин гидрогенизують к аллилового спирта, затем с помощью перекиси водорода превращают в глицерин.
Наряду с производством аллилового спирта для синтеза глицерина одной из основных областей применения акролеина является синтез метионина. При взаимодействии акролеина с метилмеркаптаном в присутствии катализаторов (пиридин, ацетат меди, пиперидин, этилат натрия) в результате ряда превращений образуется метионин.
Реакция акролеина с многофункциональными соединениями приводит к интересным конденсационных полимеров, среди которых особенно известны Полиацетали с многоосновными спиртами. При полимеризации продукта конденсации с пентаэритрита (торговая марка «ультра-лон») получают вещества с хорошей прочностью на разрыв, высокой ударной прочностью, стойкостью к истиранию. Но эти продукты обладают невысокой теплостойкостью (65-104 ° C).
В результате гидролиза продукта димеризации акролеина и его дальнейшего гидрирования образуется 1,2,6-гексантриол, который применяется как пластификатор и составная часть при производстве алкидных и полиэфирных смол.
Физиологическое воздействие
Общий характер действия
Общий характер действия акролеина выражается в сильном раздражении слизистых оболочек. Кроме этого ненасыщенный альдегид обладает некоторой общей токсичным и слабой наркотической действиями.
Влияние на животных
Острое отравление животных акролеин обычно имеет летальный исход. Так, большинство белых мышей погибает после нескольких минут пребывания в среде с концентрацией акролеина 0,02-0,3 мг / л, а 0,0075 мг / л переносится в течение нескольких часов без серьезных симптомов отравления. Ингаляция паров акролеина вызывает у белых крыс и морских свинок симптомы бронхиальной астмы. Кроме астмы также вызывает эмфизему, полнокровие и расширение капилляров легких, бронхоспазм, поражает нервную систему (прогрессирующие параличи). В результате раздражения слизистых оболочек дыхательных путей возникает значительный отек гортани, отек и деструкция слизистой и подслизистой трахеи и крупных бронхов вплоть до закрытия их просвета. Концентрации 1 и 0,75 мг / л вызывают гибель крыс. При 0,65 мг / л гибель происходит чаще осложнений — возникновение вторичной инфекции и пневмонии. У кошек при 0,25 мг / л возникает слюнотечение, слезотечение, легкий наркоз; при 0,2 мг / л — сильное раздражение легких; при 1,5 мг / л и воздействии 2,5 ч, а также при 2 мг / л и влиянии 2 часа — гибель. Вскрытие показывает, что гибель происходит вследствие ожогов слизистой оболочки верхних дыхательных путей и кровоизлияний и отеков в легких.
Хроническое отравление, возникающее при длительном воздействии акролеина на организм животного приводит к тяжелым последствиям для здоровья. При вдыхании акролеина с концентрацией 0,6 мг / л в течение 6 месяцев наблюдались точечные кровоизлияния на слизистой оболочке дыхательных путей, деструкция бронхов с частичным закрытием их просвета. Введение акролеина через рот в течение такого же срока 0,5 мг / кг вызвало нарушение функции почек, а на вскрытии обнаруживали воспалительные изменения в легких и дистрофические изменения в печени и миокарде.
Воздействие на человека
При кратковременном вдыхании небольших концентраций акролеина человеком возникает жжение в глазах, слезотечение, конъюнктивит, отек век, ощущение жжения в горле, кашель и т. Д .. При больших концентрациях возникают резкие явления раздражения, кроме того, легкое головокружение, приливы крови к головы, боли в животе, тошнота, рвота, посинение губ, акроцианоз. В тяжелых случаях — замедление пульса, гипогликемия, слюнотечение, снижение температуры конечностей, онемение кончиков пальцев, расширение зрачков, приглушенные тоны сердца и даже потеря сознания. Отмечались также состояние возбуждения, дезориентация в пространстве и времени. В легких случаях выздоровление длилось 1-2 дня, в более тяжелых случаях — 4-5 дней. Известно смертельное отравление одного из двух рабочих, которые осуществляли в течение двух часов автогенная сварки внутри котла, служивший для транспортировки рапсового масла.
Пребывание человека в среде с концентрацией акролеина 0,35 мг / л в течение 10 мин является смертельным; вдыхание воздуха с содержанием 0,002 мг / л акролеина в течение 2-3 мин вызывает раздражение глаз и носа; через 5 мин раздражение становится невыносимым; концентрация 0,0006 мг / л вызывает умеренное раздражение при вдыхании в течение 5 минут. Порог восприятия запаха 0,00007 мг / л. Пороговая концентрация по рефлекторным действием 0,00005 мг / л.
При хронических отравлениях человеческого организма акролеин может развиваться повышенная чувствительность к соединения.
Видео по теме
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. АкролеинЧто мы делаем. Каждая страница проходит через несколько сотен совершенствующих техник. Совершенно та же Википедия. Только лучше. ОткрытиеАкролеин был открыт в 19 веке австрийским химиком Йозефом Редтенбахером при сухой перегонке жиров. В ходе своих исследований ученый также открыл и пропенову кислоту. Из Википедии — свободной энциклопедии
Акролеин (лат. acris — острый, едкий + oleum — масло) (пропеналь) — H2C=CH-CHO, альдегид акриловой кислоты, простейший ненасыщенный альдегид. Бесцветная легколетучая слезоточивая жидкость с резким запахом, сильный лакриматор. Реакционная способностьАкролеин, будучи непредельным альдегидом, проявляет реакционную способность, свойственную как олефинам, так и альдегидам. Так, акролеин образует ацетали: его альдегидная группа легко окисляется до карбоксильной: и восстанавливается до гидроксильной: Карбонильная группа акролеина находится в сопряжении с двойной связью, что обуславливает его высокую реакционную способность по отношению к нуклеофилам, при этом присоединение идёт по β-атому углерода: Галогены присоединяются к акролеину по двойной связи с образованием дигалогенпроизводного, которое далее отщепляет галогеноводород с образованием α-галогенакролеина: Благодаря наличию электронакцепторной альдегидной группы, сопряженной с двойной связью, акролеин является диенофилом и реагирует с диенами с образованием продуктов циклоприсоединения (реакция Дильса-Альдера): СинтезВ лаборатории акролеин получается дегидратацией глицерина в присутствии гидросульфата калия. В промышленности акролеин получают каталитическим окислением пропилена над оксидными висмут-молибденовыми катализаторами или оксидом меди. Ранее в промышленности был распространён процесс парофазной кротоновой конденсации ацетальдегида с формальдегидом (устаревший метод): Химические свойстваАкролеин, благодаря явлению таутомерии, находится в постоянном равновесии со своим изомер — пропадиенолом. Это равновесие может быть смещена действием кислотного или основного катализатора: Поскольку акролеин является ненасыщенным альдегидом, то в химических реакциях он проявляет свойства как алкенов, так и альдегидов. В частности акролеин вступает в реакцию гидрогенування, с помощью которой можно получить аллиловый спирт Кроме этого, с помощью действия катализаторов на основе никеля, палладия и платины, реакцию гидрогенування можно повести другим путем и через промежуточное образование пропаналя получить 1-пропанол: В результате хлорирования акролеина получают α, β-дихлоропропаналь. В промышленности α, β-дихлорпропаналь действием соляной кислоты превращают в α-хлоракролеин, который является сырьем для получения α-хлоракрилатних смол: Воздействие на акролеин хлорноватистая кислота приводит к образованию глицеральдегид: Для акролеина характерна реакция окисления с образованием пропеновои кислоты: Гидролиз акролеина может проходить двумя путями. В результате образуются 1,3-пропандиол или сложная димерних состав: Интересна взаимодействие акролеина с аммиаком, в результате которой происходит циклизация с образованием β-пиколина: Как и любая ненасыщенная соединение, акролеин способен соединять собственные молекулы. Так в результате димеризации образуются димеры следующей строения: а полимеризация приводит к образованию полиакролеину. Также с акролеина можно получить незаменимую аминокислоту — метионин. Упрощенно этот процесс записывается следующим образом: Путем реакции Скраупа ароматических аминов с акролеин, который образуется in situ из глицерина в присутствии дегидратирующего агента и окислителя, получают замещены хинолины: ТоксичностьВследствие своей высокой реакционной способности акролеин является токсичным, сильно раздражающим слизистые оболочки глаз и дыхательных путей соединением, сильный лакриматор. Максимально разовая Предельно допустимая концентрация в воздухе 0,03 мг/м³; Среднесуточная Предельно допустимая концентрация в воздухе 0,01 мг/м³(Список ПДК ГН 2.1.6 1338-03). Вызывает мутагенез у бактерий и дрожжей, проявляет мутагенные свойства на культурах клеток млекопитающих. Относится к I классу опасности (чрезвычайно опасные вещества). Акролеин является одним из продуктов термического разложения глицерина и жиров-глицеридов, чем объясняются раздражающие слизистые оболочки свойства дыма горелого жира. ПрименениеНаибольшее количество акролеина расходуется на синтез глицерина без использования хлора, где акролеин гидрогенизують к аллилового спирта, затем с помощью перекиси водорода превращают в глицерин. Наряду с производством аллилового спирта для синтеза глицерина одной из основных областей применения акролеина является синтез метионина. При взаимодействии акролеина с метилмеркаптаном в присутствии катализаторов (пиридин, ацетат меди, пиперидин, этилат натрия) в результате ряда превращений образуется метионин. Реакция акролеина с многофункциональными соединениями приводит к интересным конденсационных полимеров, среди которых особенно известны Полиацетали с многоосновными спиртами. При полимеризации продукта конденсации с пентаэритрита (торговая марка «ультра-лон») получают вещества с хорошей прочностью на разрыв, высокой ударной прочностью, стойкостью к истиранию. Но эти продукты обладают невысокой теплостойкостью (65-104 ° C). В результате гидролиза продукта димеризации акролеина и его дальнейшего гидрирования образуется 1,2,6-гексантриол, который применяется как пластификатор и составная часть при производстве алкидных и полиэфирных смол. Физиологическое воздействиеОбщий характер действияОбщий характер действия акролеина выражается в сильном раздражении слизистых оболочек. Кроме этого ненасыщенный альдегид обладает некоторой общей токсичным и слабой наркотической действиями. Влияние на животныхОстрое отравление животных акролеин обычно имеет летальный исход. Так, большинство белых мышей погибает после нескольких минут пребывания в среде с концентрацией акролеина 0,02-0,3 мг / л, а 0,0075 мг / л переносится в течение нескольких часов без серьезных симптомов отравления. Ингаляция паров акролеина вызывает у белых крыс и морских свинок симптомы бронхиальной астмы. Кроме астмы также вызывает эмфизему, полнокровие и расширение капилляров легких, бронхоспазм, поражает нервную систему (прогрессирующие параличи). В результате раздражения слизистых оболочек дыхательных путей возникает значительный отек гортани, отек и деструкция слизистой и подслизистой трахеи и крупных бронхов вплоть до закрытия их просвета. Концентрации 1 и 0,75 мг / л вызывают гибель крыс. При 0,65 мг / л гибель происходит чаще осложнений — возникновение вторичной инфекции и пневмонии. У кошек при 0,25 мг / л возникает слюнотечение, слезотечение, легкий наркоз; при 0,2 мг / л — сильное раздражение легких; при 1,5 мг / л и воздействии 2,5 ч, а также при 2 мг / л и влиянии 2 часа — гибель. Вскрытие показывает, что гибель происходит вследствие ожогов слизистой оболочки верхних дыхательных путей и кровоизлияний и отеков в легких. Хроническое отравление, возникающее при длительном воздействии акролеина на организм животного приводит к тяжелым последствиям для здоровья. При вдыхании акролеина с концентрацией 0,6 мг / л в течение 6 месяцев наблюдались точечные кровоизлияния на слизистой оболочке дыхательных путей, деструкция бронхов с частичным закрытием их просвета. Введение акролеина через рот в течение такого же срока 0,5 мг / кг вызвало нарушение функции почек, а на вскрытии обнаруживали воспалительные изменения в легких и дистрофические изменения в печени и миокарде. Воздействие на человекаПри кратковременном вдыхании небольших концентраций акролеина человеком возникает жжение в глазах, слезотечение, конъюнктивит, отек век, ощущение жжения в горле, кашель и т. Д .. При больших концентрациях возникают резкие явления раздражения, кроме того, легкое головокружение, приливы крови к головы, боли в животе, тошнота, рвота, посинение губ, акроцианоз. В тяжелых случаях — замедление пульса, гипогликемия, слюнотечение, снижение температуры конечностей, онемение кончиков пальцев, расширение зрачков, приглушенные тоны сердца и даже потеря сознания. Отмечались также состояние возбуждения, дезориентация в пространстве и времени. В легких случаях выздоровление длилось 1-2 дня, в более тяжелых случаях — 4-5 дней. Известно смертельное отравление одного из двух рабочих, которые осуществляли в течение двух часов автогенная сварки внутри котла, служивший для транспортировки рапсового масла. Пребывание человека в среде с концентрацией акролеина 0,35 мг / л в течение 10 мин является смертельным; вдыхание воздуха с содержанием 0,002 мг / л акролеина в течение 2-3 мин вызывает раздражение глаз и носа; через 5 мин раздражение становится невыносимым; концентрация 0,0006 мг / л вызывает умеренное раздражение при вдыхании в течение 5 минут. Порог восприятия запаха 0,00007 мг / л. Пороговая концентрация по рефлекторным действием 0,00005 мг / л. При хронических отравлениях человеческого организма акролеин может развиваться повышенная чувствительность к соединения. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||