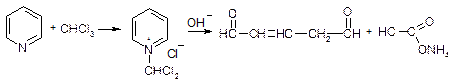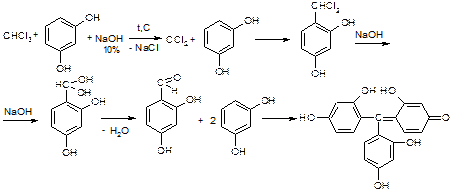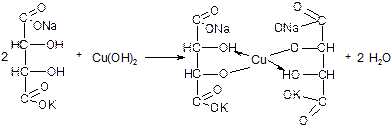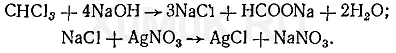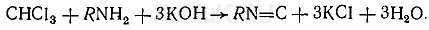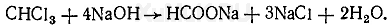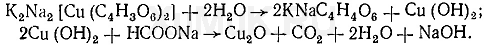1. Реакция Фудживара (предварительные испытания на хлорированные углеводороды)
К 2-3 мл исследуемого дистиллята (или мочи) прибавляют 2 мл свежеперегнанного пиридина и 2 мл 10% раствора натра едкого. Смесь нагревают на водяной бане в течение 2-3 мин. При наличии хлорированных углеводородов появляется красная окраска глутаконового альдегида.
2. Реакция отщепления органически связанного хлора
К 1 мл дистиллята прибавляют 1 мл 10% спиртового раствора натра едкого и осторожно нагревают в течение 5 мин. После охлаждения раствор подкисляют 10% раствором кислоты азотной до рН = 2 (по универсальному индикатору), а затем прибавляют 5-10 капель 10% раствора серебра нитрата. Появляется белый осадок или муть (опалесценция) серебра хлорида, растворимого в 25% растворе аммония гидроксида.
СНСl3 + 4NaOH → 3NaCI + НCOH + 2Н2О
3. Реакция с раствором резорцина в щелочной среде
К 1 мл дистиллята прибавляют I мл 1% свежеприготовленного раствора резорцина в 10% растворе натра едкого. Нагревают на кипящей водяной бане в течение 5-10 мин. Появляется розовое или малиновое окрашивание.
Примечание.Приготовление 1% раствора резорцина в растворе натра едкого. 0,01 г резорцина растворяют в 1 мл 10% раствора натра едкого.
4. Реакция с реактивом Фелинга
К 1 мл дистиллята прибавляют 1 мл 10% раствора натра едкого и 5 капель реактива Фелинга. Нагревают на кипящей водяной бане в течение 5-10 мин. При наличии хлороформа и хлоралгидрата появляется осадок гидрата меди (I) гидроксид желтого цвета, переходящий в осадок мели оксида (I) красного цвета.
Примечание.Приготовление реактива Фелинга. К 1 мл реактива Фелинга № 1 (меди сульфат в кислоте серной разбавленной) прибавляют 1 мл реактива Фелинга № 2 (натрия и калия гидротартрат в растворе натра едкого) непосредственно перед проведением реакции.
В результате реакции отщепления органически связанного хлора образуется натрия формиат (см. выше), который обладает восстановительными свойствами и взаимодействует с реактивом Фелинга.
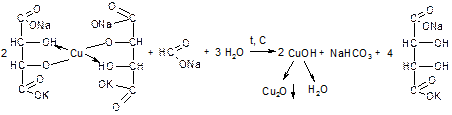
5. Реакция образования изонитрила
К 1 мл дистиллята прибавляют 10 капель 10% спиртового раствора натра едкого и одну каплю водного раствора анилина. Жидкость нагревают на водяной бане 1-2 мин. Появление неприятного запаха изонитрила указывает на наличие хлороформа в пробе.
Примечание.Реакцию выполняют под тягой.
§ 14. ХЛОРОФОРМ
Хлороформ (трихлорметан) СНCl 3 — бесцветная прозрачная летучая жидкость с характерным запахом. Смешивается с диэтиловым эфиром, этиловым спиртом и другими органическими растворителями, слабо растворяется в воде (см. табл. 1). Под влиянием света, воздуха, влаги и температуры хлороформ постепенно разлагается. При этом могут образовываться фосген, муравьиная и соляная кислоты.
Применение. Действие на организм. Хлороформ широко используется в химической промышленности и в химических лабораториях как растворитель. Раньше он применялся в медицине для наркоза. В настоящее время хлороформ в смеси с другими лекарственными препаратами используется для растирания. Пары хлороформа легко проникают в организм с вдыхаемым воздухом. Хлороформ действует на центральную нервную систе му, вызывая наркоз. Он накапливается в тканях, богатых жирами. При больших количествах хлороформа, поступившего в организм, могут появляться дистрофические изменения во внутренних органах, особенно в печени. При отравлении хлороформом смерть наступает от остановки дыхания.
Метаболизм. Хлороформ, поступивший в организм, быстро исчезает из крови. Через 15—20 мин с выдыхаемым воздухом в неизмененном виде выделяется 30—50 % хлороформа. В течение часа через легкие выделяется до 90 % хлороформа, поступившего в организм. Однако еще и через 8 ч в крови можно обнаружить незначительные количества хлороформа. Часть хлороформа подвергается биотрансформации. При этом в качестве метаболитов образуются оксид углерода (IV) и хлороводород. При химико-токсикологических исследованиях основными объектами анализа на наличие хлороформа в организме являются выдыхаемый воздух, богатые жирами ткани трупов и печень.
Хлороформ, содержащийся в дистилляте, можно обнаружить по наличию хлора в его молекуле, а также при помощи реакций Фудживара, образования изонитрила, реакций с резорцином, с реактивом Фелинга и др. Большинство этих реакций дают и некоторые другие хлорсодержащие вещества, имеющие токсикологическое значение.
Реакция отщепления хлора. При нагревании хлороформа со спиртовым раствором щелочи происходит отщепление атомов хлора, которые можно обнаружить при помощи реакции с нитратом серебра:
Перед выполнением этой реакции необходимо убедиться в том, что в исследуемом растворе (дистилляте) и в реактивах отсутствуют ионы хлора.
Выполнение реакции. В пробирку вносят 1—2 мл исследуемого раствора и 1 мл 10%-го спиртового раствора гидроксида натрия. Пробирку осторожно нагревают на пламени газовой горелки в течение 3—5 мин. После охлаждения раствора его подкисляют 10%-м раствором азотной кислоты до кислой реакции на лакмус и прибавляют 0,5 мл 1 %-го раствора нитрата серебра. Появление белого растворимого в аммиаке осадка указывает на наличие хлороформа в исследуемом растворе.
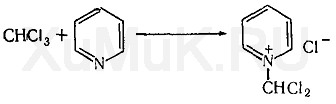
Реакция Фудживара. Хлороформ и ряд других галогенсодержащих соединений можно обнаружить при помощи реакции Фудживара, которая основана на взаимодействии этих веществ с пиридином в присутствии щелочи. При взаимодействии хлороформа с пиридином и щелочью образуется полиметиновый краситель. При этой реакции вначале образуется соль пиридиния:
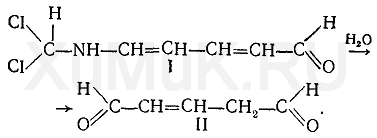
Под влиянием щелочи соль пиридиния превращается в производное глутаконового альдегида (I), при гидролизе которого образуется глутаконовый альдегид (II), имеющий окраску:
Описано два варианта реакции Фудживара. При использовании первого варианта наблюдают окраску образовавшегося глутаконового альдегида. При втором варианте этой реакции к образовавшемуся глутаконовому альдегиду прибавляют ароматический амин или другое соединение, содержащее подвижный атом водорода, а затем наблюдают окраску.
Выполнение реакции. К 2—3 мл исследуемого раствора прибавляют 2 мл свежеперегнанного пиридина и 2 мл 10 %-го раствора гидроксида натрия. Смесь нагревают на водяной бане в течение 2—3 мин. При наличии хлороформа в исследуемом растворе появляется красная окраска.
Приготовление свежеперегнанного пиридина (см. Приложение 1, реактив 27).
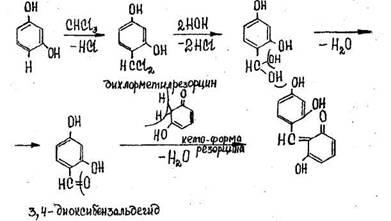
Реакция с резорцином. При нагревании хлороформа с резорцином в присутствии щелочи появляется розовая или малиново-красная окраска.
Выполнение реакции. В пробирку вносят 1 мл исследуемого раствора и 1 мл 10 %-го свежеприготовленного раствора резорцина в 10%-м растворе гидроксида натрия. После нагревания пробирки на кипящей водяной бане в течение 5—10 мин появляется розовая или малиновая окраска. Параллельно выполняют «холостой» опыт.
Реакция образования изонитрила. При нагревании хлороформа с первичными аминами и щелочью образуется изонитрил (карбиламин), имеющий неприятный запах:
Выполнение реакции. К 1 мл исследуемого раствора прибавляют 10 капель 10 %-го спиртового раствора гидроксида натрия и одну каплю водного раствора анилина. Жидкость нагревают на водяной бане 1—2 мин. Появление неприятного запаха изонитрила указывает на наличие хлороформа в пробе. Эту реакцию дают четыреххлористый углерод, хлоралгидрат и др. Дихлорэтан не дает этой реакции.
Изонитрильную реакцию выполняют под тягой. Для разложени я изонитрила в использованных для выполнения реакций пробирках их кипятят с 10 %-м раствором серной кислоты.
Реакция с реактивом Фелинга. При взаимодействии хлорофор ма со щелочью образуется соль муравьиной (формиатной) кислоты:
Реактив Фелинга, содержащий внутрикомплексное соединение K 2 Na 2 [Cu(С 4 Н 3 O 6 ) 2 ], которое образуется при взаимодействии ионов меди (II) с сегнетовой солью, при нагревании окисляет муравьиную кислоту и ее соли. В результате реакции выпадает красного цвета осадок оксида меди (I):
Выполнение реакции. В пробирку вносят 2 мл исследуемого раствора, 2 мл 10 %-го раствора гидроксида натрия и 5 капель реактива Фелинга, а затем нагревают на водяной бане. При наличии хлороформа в исследуемом растворе выпадает желтый осадок, переходящий затем в красный.
Приготовление реактива Фелинга (см. Приложение 1, реактив 42).
Предварительная проба на хлороформ и другие хлорпроиз-водные в моче. Для обнаружения хлороформа и других хлорпроизводных в моче применяют предварительную пробу, основанную на реакции Фудживара. В пробирку вносят 1 мл мочи, прибавляют 1 мл 10 %-го раствора гидроксида натрия и 1 мл свеже-перегнанного пиридина. Содержимое пробирки взбалтывают и нагревают на кипящей водяной бане в течение 2 мин. Появление розовой или красной окраски указывает на наличие в моче хлороформа или других трихлорпроизводных углеводородов. При этом необходимо производить «холостой» опыт, так как пары некоторых веществ, которые могут находиться в воздухе, тоже дают эту реакцию.
Хлороформ. Обнаружение и определение
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Хлороформ. Обнаружение и определение
Хлороформ (трихлорметан) СНСl3 представляет собой бесцветную прозрачную жидкость с резким характерным запахом, сладковатым, жгучим вкусом; т. кип. 61,1°С; образует азеотропную смесь с водой (т. кип. 56,2 °С, 97,4 % хлороформа). Используют хлороформ главным образом для производства хладона 22, как растворитель, хладагент, в синтезе лекарственных препаратов.
Ранее применялся в медицине как средство для наркоза. Хлороформ – негорюч, на свету разлагается, особенно при контакте с открытым пламенем, образуя фосген. Вызывает наркоз. Обладает гепатотропным, нефротоксическим и кардиотоксическим действием; вызывает канцерогенный и мутагенный эффекты; раздражает слизистые оболочки.
Хлороформ. Качественное обнаружение
Реакция отщепления атомов хлора
CHCl3 + 4NaOH → 3NaCl + HCOONa + 2H2O
Появляется белый осадок, растворимый в растворе аммиака. Параллельно проводят пробу в тех же условиях с 1 мл исследуемого раствора и натрия гидроксидом, но без нагревания (для исключения ионов хлора в исследуемом растворе).
Реакция не специфична, является общей для всех хлорпроизводных. Чувствительность реакции 0,2 мг.
Реакция с резорцином в щелочной среде
После нагревания пробирки на кипящей водяной бане в течение 5-10 мин. появляется розовая или малиновая окраска. Параллельно выполняется контрольный опыт («слепой» опыт), цель которого – исключить ошибки за счет продуктов окисления резорцина, окрашенных в зеленый цвет и маскирующих розовое окрашивание.
Реакция не специфична, ее дают все хлорпроизводные, кроме дихлорэтана, а также формальдегид.
Реакция образования изонитрила
Появляется резкий раздражающий запах изонитрила. Реакция не специфична, ее дают все хлорпроизводные, за исключением дихлорэтана.
Чувствительность реакции 0,01 мг.
Реакция с реактивом Фелинга.
CHCl3 + 4NaOH → HCOONa + 3NaCl + 2H2O
Выпадает желтый осадок гидрооксида меди (Cu(OH)2), переходящий в красный осадок закиси меди (Cu2O).
Реакция не специфична, ее дает хлороформ, хлоралгидрат и формальдегид. Не дают четыреххлористый углерод и дихлорэтан. Чувствительность реакции 3 мг.