Характеристика углерода. Свойства простых веществ и соединений

Физические свойства: углерод образует множество аллотропных модификаций: алмаз – одно из самых твердых веществ, графит, уголь, сажа .
Атом углерода имеет 6 электронов: 1s 2 2s 2 2p 2 . Последние два электрона располагаются на отдельных р-орбиталях и являются неспаренными. В принципе, эта пара могла бы занимать одну орбиталь, но в таком случае сильно возрастает межэлектронное отталкивание. По этой причине один из них занимает 2р х , а другой, либо 2р у , либо 2р z -орбитали.

Это явление, как известно, называют sp 3 -гибридизацией, а возникающие функции – sp 3 -гибридными . Образование четырех sp 3 -связей обеспечивает атому углерода более устойчивое состояние, чем три р—р- и одна s—s-связи. Помимо sp 3 -гибридизации у атома углерода наблюдается также sp 2 — и sp-гибридизация . В первом случае возникает взаимное наложение s- и двух р-орбиталей. Образуются три равнозначные sp 2 — гибридных орбитали, расположенные в одной плоскости под углом 120° друг к другу. Третья орбиталь р неизменна и направлена перпендикулярно плоскости sp 2 .

При sp-гибридизации происходит наложение орбиталей s и р. Между двумя образующимися равноценными гибридными орбиталями возникает угол 180°, при этом две р-орбитали у каждого из атомов остаются неизменными.
Аллотрорпия углерода. Алмаз и графит
В кристалле графита атомы углерода расположены в параллельных плоскостях, занимая в них вершины правильных шестиугольников. Каждый из атомов углерода связан с тремя соседними sp 2 -гибридными связями. Между параллельными плоскостями связь осуществляется за счет ван-дер-ваальсовых сил. Свободные р-орбитали каждого из атомов направлены перпендикулярно плоскостям ковалентных связей. Их перекрыванием объясняется дополнительная π-связь между атомами углерода. Таким образом, от валентного состояния, в котором находятся атомы углерода в веществе, зависят свойства этого вещества .
- Химические свойства углерода
- Углерод как восстановитель:
- Углерод как окислитель:
- Нахождение углерода в природе
- Неорганические соединения углерода
- Оксид углерода (II) СО
- Оксид углерода (IV) СO 2
- Угольная кислота и её соли
- Карбиды
- Цианиды
- Карбонаты
- Углерод
- Углерод. Химия углерода и его соединений
- Углерод
- Положение в периодической системе химических элементов
- Электронное строение углерода
- Физические свойства
- Качественные реакции
- Соединения углерода
- Химические свойства
- Карбиды
- Оксид углерода (II)
- Строение молекулы и физические свойства
- Способы получения
- Химические свойства
- Оксид углерода (IV)
- Строение молекулы и физические свойства
- Способы получения
- Химические свойства
- Карбонаты и гидрокарбонаты
- Гидролиз карбонатов и гидрокарбонатов
- 💡 Видео
Видео:Химические уравнения // Как Составлять Уравнения Реакций // Химия 9 классСкачать

Химические свойства углерода
Наиболее характерные степени окисления: +4, +2.
При низких температурах углерод инертен, но при нагревании его активность возрастает.
Видео:Химия. 9 класс (Урок№17 - Углерод. Аллотропные модификации углерода.Химические свойства. Адсорбция.)Скачать

Углерод как восстановитель:
— с кислородом
C 0 + O 2 – t° = CO 2 углекислый газ
при недостатке кислорода — неполное сгорание:
2C 0 + O 2 – t° = 2C +2 O угарный газ
— с водяным паром
C 0 + H 2 O – 1200° = С +2 O + H 2 водяной газ
— с оксидами металлов. Таким образом выплавляют металл из руды.
C 0 + 2CuO – t° = 2Cu + C +4 O 2
— с кислотами – окислителями:
C 0 + 2H 2 SO 4 (конц.) = С +4 O 2 + 2SO 2 + 2H 2 O
С 0 + 4HNO 3 (конц.) = С +4 O 2 + 4NO 2 + 2H 2 O
— с серой образует сероуглерод:
С + 2S 2 = СS 2 .
Видео:Составление уравнений химических реакций. 1 часть. 8 класс.Скачать

Углерод как окислитель:
— с некоторыми металлами образует карбиды
Ca + 2C 0 = CaC 2 -4
— с водородом — метан (а также огромное количество органических соединений)
— с кремнием, образует карборунд (при 2000 °C в электропечи):
Видео:Химия 9 класс (Урок№18 - Угарный газ. Углекислый газ.)Скачать

Нахождение углерода в природе
Ссвободный углерод встречается в виде алмаза и графита. В виде соединений углерод находится в составе минералов: мела, мрамора, известняка – СаСО 3 , доломита – MgCO 3 *CaCO 3 ; гидрокарбонатов – Mg(НCO 3 ) 2 и Са(НCO 3 ) 2 , СО 2 входит в состав воздуха; углерод является главной составной частью природных органических соединений – газа, нефти, каменного угля, торфа, входит в состав органических веществ, белков, жиров, углеводов, аминокислот, входящих в состав живых организмов.
Видео:Решение задач на термохимические уравнения. 8 класс.Скачать

Неорганические соединения углерода
Ни ионы С 4+ , ни С 4- ‑ ни при каких обычных химических процессах не образуются: в соединениях углерода имеются ковалентные связи различной полярности.
Оксид углерода (II) СО
Угарный газ; бесцветный, без запаха, малорастворим в воде, растворим в органических растворителях, ядовит, t°кип = -192°C; t пл. = -205°C.
Получение
1) В промышленности (в газогенераторах):
C + O 2 = CO 2
2) В лаборатории — термическим разложением муравьиной или щавелевой кислоты в присутствии H 2 SO 4 (конц.):
HCOOH = H 2 O + CO
При обычных условиях CO инертен; при нагревании – восстановитель; несолеобразующий оксид.
2) с оксидами металлов
C +2 O + CuO = Сu + C +4 O 2
3) с хлором (на свету)
CO + Cl 2 – hn = COCl 2 (фосген)
4) реагирует с расплавами щелочей (под давлением)
CO + NaOH = HCOONa (формиат натрия)
5) с переходными металлами образует карбонилы
Ni + 4CO – t° = Ni(CO) 4
Fe + 5CO – t° = Fe(CO) 5
Оксид углерода (IV) СO 2
Углекислый газ, бесцветный, без запаха, растворимость в воде — в 1V H 2 O растворяется 0,9V CO 2 (при нормальных условиях); тяжелее воздуха; t°пл.= -78,5°C (твёрдый CO 2 называется «сухой лёд»); не поддерживает горение.
- Термическим разложением солей угольной кислоты (карбонатов). Обжиг известняка:
- Действием сильных кислот на карбонаты и гидрокарбонаты:
Химические свойства СO 2
Кислотный оксид: реагирует с основными оксидами и основаниями, образуя соли угольной кислоты
При повышенной температуре может проявлять окислительные свойства
С +4 O 2 + 2Mg – t° = 2Mg +2 O + C 0
Качественная реакция
Помутнение известковой воды:
Оно исчезает при длительном пропускании CO 2 через известковую воду, т.к. нерастворимый карбонат кальция переходит в растворимый гидрокарбонат:
Угольная кислота и её соли
H 2 CO 3 — Кислота слабая, существует только в водном растворе:
Двухосновная:
H 2 CO 3 ↔ H + + HCO 3 — Кислые соли — бикарбонаты, гидрокарбонаты
HCO 3 — ↔ H + + CO 3 2- Средние соли — карбонаты
Характерны все свойства кислот.
Карбонаты и гидрокарбонаты могут превращаться друг в друга:
Карбонаты металлов (кроме щелочных металлов) при нагревании декарбоксилируются с образованием оксида:
Качественная реакция — «вскипание» при действии сильной кислоты:
Карбиды
CaO + 3 C = CaC 2 + CO
Ацетилен выделяется при реакции с водой карбидов цинка, кадмия, лантана и церия:
Be 2 C и Al 4 C 3 разлагаются водой с образованием метана:
В технике применяют карбиды титана TiC, вольфрама W 2 C (твердые сплавы), кремния SiC (карборунд – в качестве абразива и материала для нагревателей).
Цианиды
получают при нагревании соды в атмосфере аммиака и угарного газа:
Синильная кислота HCN – важный продукт химической промышленности, широко применяется в органическом синтезе. Ее мировое производство достигает 200 тыс. т в год. Электронное строение цианид-аниона аналогично оксиду углерода (II), такие частицы называют изоэлектронными:
Цианиды (0,1-0,2%-ный водный раствор) применяют при добыче золота:
2 Au + 4 KCN + H 2 O + 0,5 O 2 = 2 K[Au(CN) 2 ] + 2 KOH.
При кипячении растворов цианидов с серой или сплавлении твердых веществ образуются роданиды :
KCN + S = KSCN.
При нагревании цианидов малоактивных металлов получается дициан: Hg(CN) 2 = Hg + (CN) 2 . Растворы цианидов окисляются до цианатов :
2 KCN + O 2 = 2 KOCN.
Циановая кислота существует в двух формах:
В 1828 г. Фридрих Вёлер (1800-1882) получил из цианата аммония мочевину: NH 4 OCN = CO(NH 2 ) 2 при упаривании водного раствора.
Это событие обычно рассматривается как победа синтетической химии над «виталистической теорией».
Существует изомер циановой кислоты – гремучая кислота
H-O-N=C.
Ее соли (гремучая ртуть Hg(ONC) 2 ) используются в ударных воспламенителях.
Синтез мочевины (карбамида):
CO 2 + 2 NH 3 = CO(NH 2 ) 2 + H 2 O. При 130 0 С и 100 атм.
Мочевина является амидом угольной кислоты, существует и ее «азотный аналог» – гуанидин.
Карбонаты
Важнейшие неорганические соединения углерода – соли угольной кислоты (карбонаты). H 2 CO 3 – слабая кислота (К 1 =1,3·10 -4 ; К 2 =5·10 -11 ). Карбонатный буфер поддерживает углекислотное равновесие в атмосфере. Мировой океан обладает огромной буферной емкостью, потому что он является открытой системой. Основная буферная реакция – равновесие при диссоциации угольной кислоты:
При понижении кислотности происходит дополнительное поглощение углекислого газа из атмосферы с образованием кислоты:
CO 2 + H 2 O ↔ H 2 CO 3 .
При повышении кислотности происходит растворение карбонатных пород (раковины, меловые и известняковые отложения в океане); этим компенсируется убыль гидрокарбонатных ионов:
Твердые карбонаты переходят в растворимые гидрокарбонаты. Именно этот процесс химического растворения избыточного углекислого газа противодействует «парниковому эффекту» – глобальному потеплению из-за поглощения углекислым газом теплового излучения Земли. Примерно треть мирового производства соды (карбонат натрия Na 2 CO 3 ) используется в производстве стекла.
Видео:8 класс. Составление уравнений химических реакций.Скачать

Углерод
Углерод
Углерод — неметаллический элемент IV группы периодической таблицы Д.И. Менделеева, является важнейшей частью всех органических веществ в природе.
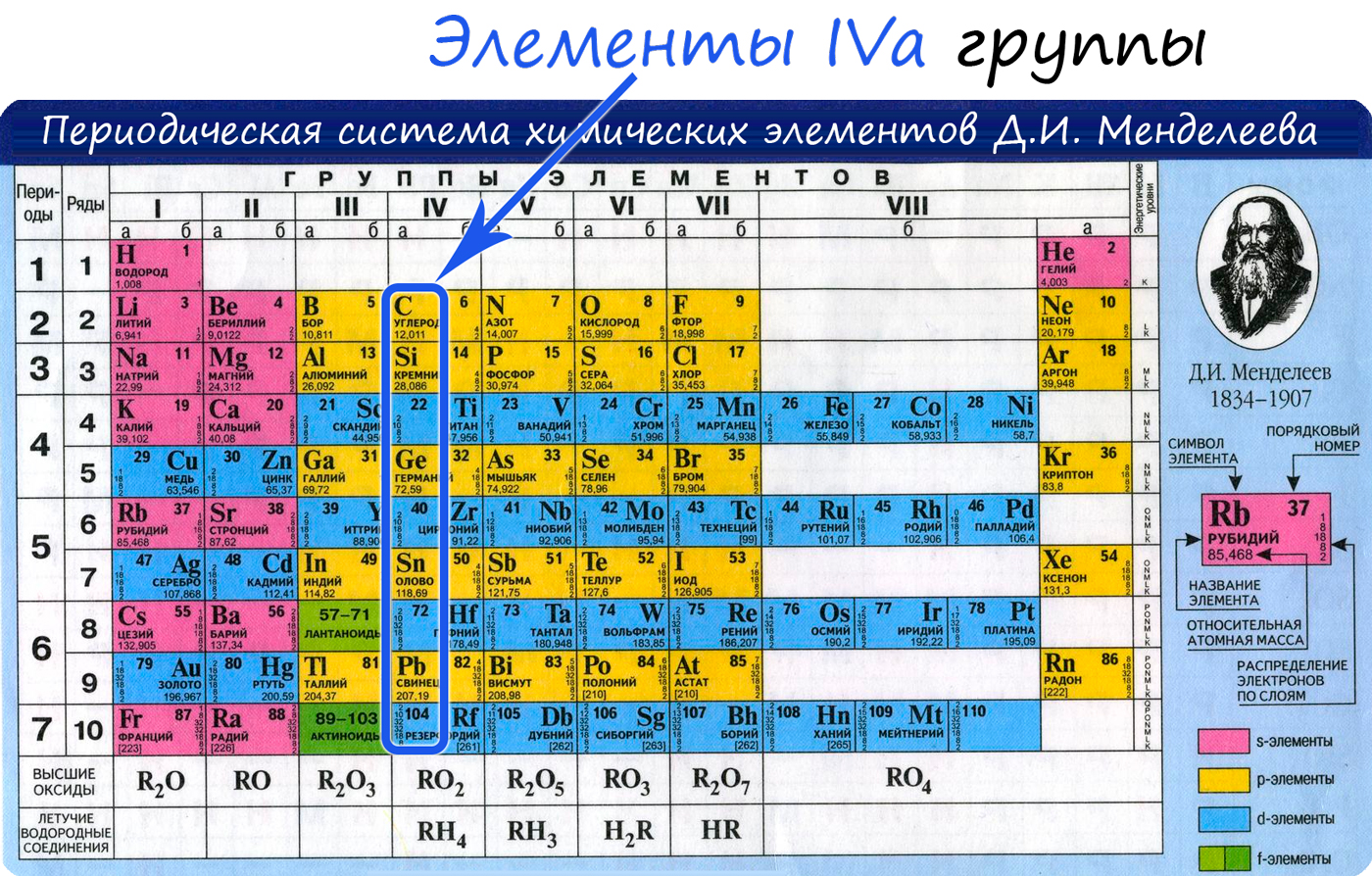
Общая характеристика элементов IVa группы
От C к Pb (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Из элементов IVа группы углерод и кремний относятся к неметаллам, германий, олово и свинец — металлы.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns 2 np 2 :
- C — 2s 2 2p 2
- Si — 3s 2 3p 2
- Ge — 4s 2 4p 2
- Sn — 5s 2 5p 2
- Pb — 6s 2 6p 2
Природные соединения
В природе углерод встречается в виде следующих соединений:
- Аллотропных модификаций — графит, алмаз, фуллерен
- MgCO3 — магнезит
- CaCO3 — кальцит (мел, мрамор)
- CaCO3*MgCO3 — доломит
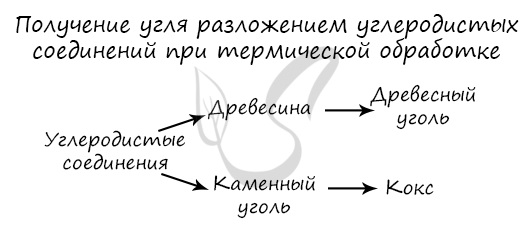
Получение
Углерод получают в ходе пиролиза углеводородов (пиролиз — нагревание без доступа кислорода). Также применяется получение углеродистых соединений: древесины и каменного угля.
Химические свойства
- Реакции с неметаллами
При нагревании углерод реагирует со многими неметаллами: водородом, кислородом, фтором.
2С + O2 → (t) 2CO (угарный газ — продукт неполного окисления углерода, образуется при недостатке кислорода)
С + O2 → (t) CO2 (углекислый газ — продукт полного окисления углерода, образуется при достаточном количестве кислорода)
Реакции с металлами
При нагревании углерод реагирует с металлами, проявляя свои окислительные свойства. Напомню, что металлы могут принимать только положительные степени окисления.
Ca + C → CaC2 (карбид кальция, СО углерода = -1)
Al + C → Al4C3 (карбид алюминий, СО углерода -4)
Очевидно, что степень окисления углерода в соединении с различными металлами может отличаться.
Углерод — хороший восстановитель. С помощью него металлургическая промышленность справляется с задачей получения чистых металлов из их оксидов:
Углерод восстанавливает не только металлы из их оксидов, но и неметаллы подобным образом:
SiO2 + C → (t) Si + CO
Может восстановить и собственный оксид:
Известная реакция взаимодействия угля с водяным паром, называемая также газификацией угля, торфа, сланца — крайне важна в промышленности:
Реакции с кислотами
В реакциях с кислотами углерод проявляет себя как восстановитель:
Оксид углерода II — СO
Оксид углерода II — продукт неполного окисления углерода. Несолеобразующий оксид. Это чрезвычайно опасное вещество часто образуется при пожарах в замкнутых помещениях, при прогревании машины в гараже.
Растворяясь в крови угарный газ (имеющий в 300 раз большее сродство к гемоглобину, чем кислород) легко выигрывает конкуренцию у кислорода и занимает его место в эритроцитах. Отравление угарным газом нередко заканчивается летальным исходом.
В промышленности угарный газ получают восстановлением оксида углерода IV или газификацией угля (t = 1000 °С).
В лаборатории угарный газ получают при разложении муравьиной кислоты в присутствии серной:
Полностью окисляется до углекислого газа в реакции с кислородом, восстанавливает оксиды металлов.
FeO + CO → Fe + CO2
Образование карбонилов — чрезвычайно токсичных веществ.
Оксид углерода IV — CO2
Продукт полного окисления углерода. Относится к кислотным оксидам, соответствует угольной кислоте H2CO3. Бесцветный газ, без запаха.
В промышленности углекислый газ получают при разложении известняка, в ходе производства алкоголя, при спиртовом брожении глюкозы.
В лабораторных условиях используют реакцию мела (мрамора) с соляной кислотой.
Углекислый газ образуется при горении органических веществ:
- Реакция с водой
В результате реакции с водой образуется нестойкая угольная кислота, которая сразу же распадается на воду и углекислый газ.
Реакции с основными оксидами и основаниями
В ходе реакций с основаниями и основными оксидами углекислый газ образует соли угольной кислоты: средние — карбонаты (при избытке основания), кислые — гидрокарбонаты (при избытке кислотного оксида).
2KOH + CO2 → K2CO3 + H2O (соотношение основание — кислотный оксид 2:1)
KOH + CO2 → KHCO3 (соотношение основание — кислотный оксид 1:1)
При нагревании способен окислять металлы до их оксидов.
Zn + CO2 → (t) ZnO + CO
Угольная кислота
Слабая двухосновная кислота, существующая только в растворах, разлагается на воду и углекислый газ.
Определить наличие карбонат-иона можно с помощью кислоты: такая реакция сопровождается «закипанием» — появлением пузырьков бесцветного газа без запаха.
Я не раз встречал описание реакций, связанных с этой кислотой, которое заслуживает нашего внимания. В задании было сказано, что при добавлении к раствору гидроксида кальция углекислого газа осадок появлялся, при дальнейшем пропускании углекислого газа — помутнение исчезало.
Это можно легко объяснить, вспомнив про способность угольной кислоты образовывать кислые соли, которые растворимы.
Чтобы сделать из средней соли (карбоната) — кислую соль (гидрокарбонат) нужно добавить угольную кислоту. Однако написать ее формулу H2CO3 — ошибка. Ее следует записать в виде воды и углекислого газа.
Li2CO3 + CO2 + H2O → LiHCO3 (средняя соль + кислота = кислая соль)
Чтобы вернуть среднюю соль, следует добавить к кислой соли щелочь.
Нагревание солей угольной кислоты
При нагревании карбонаты распадаются на соответствующий оксид металла и углекислый газ, гидрокарбонаты — на карбонат металла, углекислый газ и воду.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Видео:Уравнивание реакций горения углеводородовСкачать

Углерод. Химия углерода и его соединений
Углерод
Положение в периодической системе химических элементов
Углерод расположен в главной подгруппе IV группы (или в 14 группе в современной форме ПСХЭ) и во втором периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение углерода
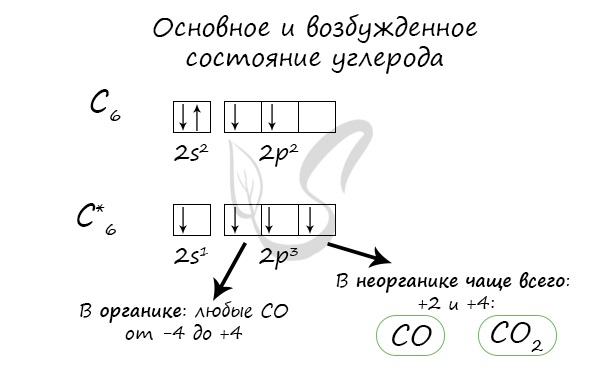
Электронная конфигурация углерода в основном состоянии :
+6С 1s 2 2s 2 2p 2 1s 

Электронная конфигурация углерода в возбужденном состоянии :
+6С * 1s 2 2s 1 2p 3 1s 

Атом углерода содержит на внешнем энергетическом уровне 2 неспаренных электрона и 1 неподеленную электронную пару в основном энергетическом состоянии и 4 неспаренных электрона в возбужденном энергетическом состоянии.
Степени окисления атома углерода — от -4 до +4. Характерные степени окисления -4, 0, +2, +4.
Физические свойства
Углерод в природе существует в виде нескольких аллотропных модификаций: алмаз, графит, карбин, фуллерен.
Алмаз — это модификация углерода с атомной кристаллической решеткой. Алмаз — самое твердое минеральное кристаллическое вещество, прозрачное, плохо проводит электрический ток и тепло. Атомы углерода в алмазе находятся в состоянии sp 3 -гибридизации.
Графит — это аллотропная модификация, в которой атомы углерода находятся в состоянии sp 2 -гибридизации. При этом атомы связаны в плоские слои, состоящие из шестиугольников, как пчелиные соты. Слои удерживаются между собой слабыми связями. Это наиболее устойчивая при нормальных условиях аллотропная модификация углерода.
Графит — мягкое вещество серо-стального цвета, с металлическим блеском. Хорошо проводит электрический ток. Жирный на ощупь.
Карбин — вещество, в составе которого атомы углерода находятся в sp-гибридизации. Состоит из цепочек и циклов, в которых атомы углерода соединены двойными и тройными связями. Карбин — мелкокристаллический порошок серого цвета.
[=C=C=C=C=C=C=]n или [–C≡C–C≡C–C≡C–]n
Фуллерен — это искусственно полученная модифицикация углерода. Молекулы фуллерена — выпуклые многогранники С60, С70 и др. Многогранники образованы пяти- и шестиугольниками, в вершинах которых расположены атомы углерода.
Фуллерены — черные вещества с металлическим блеском, обладающие свойствами полупроводников.
В природе углерод встречается как в виде простых веществ (алмаз, графит), так и в виде сложных соединений (органические вещества — нефть, природные газ, каменный уголь, карбонаты).
Качественные реакции
Качественная реакция на карбонат-ионы CO3 2- — взаимодействие солей-карбонатов с сильными кислотами . Более сильные кислоты вытесняют угольную кислоту из солей. При этом выделяется бесцветный газ, не поддерживающий горение – углекислый газ.
Например , карбонат кальция растворяется в соляной кислоте:
Видеоопыт взаимодействия карбоната кальция с соляной кислотой можно посмотреть здесь.
Качественная реакция на углекислый газ CO2 – помутнение известковой воды при пропускании через нее углекислого газа:
При дальнейшем пропускании углекислого газа осадок растворяется, т.к. карбонат кальция под действием избытка углекислого газа переходит в растворимый гидрокарбонат кальция:
Видеоопыт взаимодействия гидроксида кальция с углекислым газом (качественная реакция на углекислый газ) можно посмотреть здесь.
Углекислый газ СО2 не поддерживает горение . Угарный газ CO горит голубым пламенем.
Соединения углерода
Основные степени окисления углерода — +4, +2, 0, -1 и -4.
Наиболее типичные соединения углерода:
| Степень окисления | Типичные соединения |
| +4 | оксид углерода (IV) CO2 гидрокарбонаты MeHCO3 |
| +2 | оксид углерода (II) СО муравьиная кислота HCOOH |
| -4 | метан CH4 карбиды металлов (карбид алюминия Al4C3) бинарные соединения с неметаллами (карбид кремния SiC) |
Химические свойства
При нормальных условиях углерод существует, как правило, в виде атомных кристаллов (алмаз, графит), поэтому химическая активность углерода — невысокая.
1. Углерод проявляет свойства окислителя (с элементами, которые расположены ниже и левее в Периодической системе) и свойства восстановителя (с элементами, расположенными выше и правее). Поэтому углерод реагирует и с металлами , и с неметаллами .
1.1. Из галогенов углерод при комнатной температуре реагирует с фтором с образованием фторида углерода:
1.2. При сильном нагревании углерод реагирует с серой и кремнием с образованием бинарного соединения сероуглерода и карбида кремния соответственно:
C + 2S → CS2
C + Si → SiC
1.3. Углерод не взаимодействует с фосфором .
При взаимодействии углерода с водородом образуется метан. Реакция идет в присутствии катализатора (никель) и при нагревании:
1.4. С азотом углерод реагирует при действии электрического разряда, образуя дициан:
2С + N2 → N≡C–C≡N
1.5. В реакциях с активными металлами углерод проявляет свойства окислителя. При этом образуются карбиды:
2C + Ca → CaC2
1.6. При нагревании с избытком воздуха графит горит , образуя оксид углерода (IV):
при недостатке кислорода образуется угарный газ СО:
2C + O2 → 2CO
Алмаз горит при высоких температурах:
Горение алмаза в жидком кислороде:
Графит также горит:
Графит также горит, например, в жидком кислороде:
Графитовые стержни под напряжением:
2. Углерод взаимодействует со сложными веществами:
2.1. Раскаленный уголь взаимодействует с водяным паром с образованием угарного газа и водорода:
C 0 + H2 + O → C +2 O + H2 0
2.2. Углерод восстанавливает многие металлы из основных и амфотерных оксидов . При этом образуются металл и угарный газ. Получение металлов из оксидов с помощью углерода и его соединений называют пирометаллургией.
Например , углерод взаимодействует с оксидом цинка с образованием металлического цинка и угарного газа:
ZnO + C → Zn + CO
Также углерод восстанавливает железо из железной окалины:
4С + Fe3O4 → 3Fe + 4CO
При взаимодействии с оксидами активных металлов углерод образует карбиды.
Например , углерод взаимодействует с оксидом кальция с образованием карбида кальция и угарного газа. Таким образом, углерод диспропорционирует в данной реакции:
3С + СаО → СаС2 + СО
2.3. Концентрированная серная кислота окисляет углерод при нагревании. При этом образуются оксид серы (IV), оксид углерода (IV) и вода:
2.4. Концентрированная азотная кислотой окисляет углерод также при нагревании. При этом образуются оксид азота (IV), оксид углерода (IV) и вода:
2.5. Углерод проявляет свойства восстановителя и при сплавлении с некоторыми солями , в которых содержатся неметаллы с высокой степенью окисления.
Например , углерод восстанавливает сульфат натрия до сульфида натрия:
Карбиды
Карбиды – это соединения элементов с углеродом . Карбиды разделяют на ковалентные и ионные в зависимости от типа химической связи между атомами.
| Ковалентные карбиды | Ионные карбиды | ||
| Метаниды | Ацетилениды | Пропиниды | |
| Это соединения углерода с неметаллами Например : SiC, B4C | Это соединения с металлами, в которых с.о. углерода равна -4 Например : Al4C3, Be2C | Это соединения с металлами, в которых с.о. углерода равна -1 Например : Na2C2, CaC2 | |
| Частицы связаны ковалентными связями и образуют атомные кристаллы. Поэтому ковалентные карбиды химически стойкие. Окисляются только сильными окислителями | Метаниды разлагаются водой или кислотами с образованием метана и гидроксида или соли: Например : Al4C3 + 12H2O → 4Al(OH)3 + 3CH4 | Ацетилениды разлагаются водой или кислотами с образованием ацетилена и гидроксида или соли: Например: СаС2+ 2Н2O → Са(OH)2 + С2Н2 | |