Коэффициент сжимаемости: как рассчитать, примеры и упражнения — Наука
- Содержание:
- Как рассчитать коэффициент сжимаемости?
- Примеры
- Коэффициент сжимаемости в идеальных газах, воздухе, водороде и воде
- Идеальные газы
- Воздух
- Водород
- вода
- Решенные упражнения
- Упражнение 1
- Решение для
- Решение б
- Решение c
- Упражнение 2.
- Решение для
- Решение б
- Решение c
- Ссылки
- Уравнение состояния газов
- Коэффициент сжимаемости природного газа
- Большая Энциклопедия Нефти и Газа
- ПОИСК
- Способ оперативного определения коэффициента сжимаемости газов и их смесей
- Коэффициент сжимаемости газов и газоконденсатных смесей: экспериментальное определение и расчеты — PDF
Содержание:
В коэффициент сжимаемости Z, или коэффициент сжатия для газов, представляет собой безразмерное значение (без единиц измерения), которое вводится как поправка в уравнение состояния идеальных газов. Таким образом, математическая модель больше напоминает наблюдаемое поведение газа.
В идеальном газе уравнение состояния, связанное с переменными P (давление), V (объем) и T (температура), выглядит следующим образом: П.В. идеальный = n.R.T где n = число молей и R = постоянная идеального газа. Добавляя поправку на коэффициент сжимаемости Z, это уравнение принимает вид:
Как рассчитать коэффициент сжимаемости?
Учитывая, что молярный объем равен Vпрохладно = В / п, имеем реальный молярный объем:
Поскольку коэффициент сжимаемости Z зависит от условий газа, он выражается как функция давления и температуры:
Сравнивая первые два уравнения, можно увидеть, что если число молей n равно 1, молярный объем реального газа связан с объемом идеального газа следующим образом:
Когда давление превышает 3 атмосферы, большинство газов перестают вести себя как идеальные газы, и фактический объем значительно отличается от идеального.
Это было реализовано в его экспериментах голландского физика Йоханнеса Ван дер Ваальса (1837-1923), которые привели его к созданию модели, которая лучше подходила для практических результатов, чем уравнение идеального газа: уравнение состояния Вана. дер Ваальс.
Примеры
Согласно уравнению П.В.настоящий= Z.n.RT, для идеального газа Z = 1. Однако в реальных газах с увеличением давления увеличивается и значение Z. Это имеет смысл, потому что чем выше давление, молекулы газа имеют больше возможностей для столкновения, поэтому силы отталкивания увеличиваются, а вместе с ними и объем.
С другой стороны, при более низких давлениях молекулы движутся более свободно и силы отталкивания уменьшаются. Поэтому ожидается меньшая громкость. Что касается температуры, то при повышении Z уменьшается.
Как заметил Ван-дер-Ваальс, вблизи так называемой критической точки поведение газа сильно отличается от поведения идеального газа.
Критическая точка (Tc, Пc) любого вещества являются значениями давления и температуры, определяющими его поведение до фазового перехода:
-Tc это температура, выше которой рассматриваемый газ не сжижается.
-Пc— минимальное давление, необходимое для сжижения газа при температуре Tc
Однако у каждого газа есть своя критическая точка, определяющая температуру и пониженное давление Tр И пр следующим образом:
Замечено, что ограниченный газ с идентичным Vр Y Тр оказывает такое же давление пр. По этой причине, если Z отображается как функция пр себе Тр, каждая точка на этой кривой одинакова для любого газа. Это называется принцип соответствующих состояний.
Коэффициент сжимаемости в идеальных газах, воздухе, водороде и воде
Ниже представлена кривая сжимаемости для различных газов при различных пониженных температурах. Вот несколько примеров Z для некоторых газов и процедура определения Z с помощью кривой.
Идеальные газы
У идеальных газов Z = 1, как объяснялось в начале.
Воздух
Для воздуха Z составляет приблизительно 1 в широком диапазоне температур и давлений (см. Рисунок 1), где модель идеального газа дает очень хорошие результаты.
Водород
Z> 1 для всех давлений.
вода
Чтобы найти Z для воды, вам нужны значения критических точек. Критическая точка воды: Pc = 22,09 МПа и Tc= 374,14 ° С (647,3 К). Снова необходимо учитывать, что коэффициент сжимаемости Z зависит от температуры и давления.
Например, предположим, что вы хотите найти Z воды при 500 ºC и 12 МПа. Итак, первое, что нужно сделать, это вычислить приведенную температуру, для которой градусы Цельсия необходимо преобразовать в Кельвина: 50 ºC = 773 K:
Этими значениями поместим на график рисунка кривую, соответствующую Tр = 1,2, обозначено красной стрелкой. Затем смотрим на горизонтальную ось значение Pр ближе к 0,54, отмечен синим цветом. Теперь рисуем вертикаль, пока не перехватим кривую Tр = 1,2 и, наконец, он проецируется из этой точки на вертикальную ось, где мы читаем приблизительное значение Z = 0,89.
Решенные упражнения
Упражнение 1
Это образец газа с температурой 350 К и давлением 12 атмосфер с молярным объемом на 12% больше, чем предсказывается законом идеального газа. Рассчитать:
а) Коэффициент сжатия Z.
б) Молярный объем газа.
c) На основании предыдущих результатов укажите, какие силы преобладают в данной пробе газа.
Данные: R = 0,082 л атм / моль К
Решение для
Зная, что V настоящий на 12% больше, чем Vидеальный :
Решение б
П. Vнастоящий = Z. R. T → Vнастоящий = (1,12 x 0,082 x 350/12) л / моль = 2,14 л / моль.
Решение c
Силы отталкивания преобладают, так как объем образца увеличился.
Упражнение 2.
В объеме 4,86 л при 27 ° C содержится 10 моль этана. Найдите давление этана по формулам:
а) Модель идеального газа
б) Уравнение Ван-дер-Ваальса
c) Найдите коэффициент сжатия из предыдущих результатов.
Данные для этана
а = 5,489 дм 6 . атм. моль -2 и b = 0,06380 дм 3 . моль -1 .
Критическое давление: 49 атм. Критическая температура: 305 К
Решение для
Температура переводится в Кельвин: 27 º C = 27 + 273 K = 300 K, также помните, что 1 литр = 1 л = 1 дм 3 .
Затем предоставленные данные подставляются в уравнение идеального газа:
P.V = n.R.T → P = (10 x 0,082 x 300 / 4,86 л) атм = 50,6 атм
Решение б
Уравнение состояния Ван-дер-Ваальса:
Где a и b — коэффициенты, указанные в заявлении. При очистке P:
Решение c
Рассчитываем пониженное давление и температуру:
С этими значениями мы ищем значение Z на графике на рисунке 2, обнаруживая, что Z составляет приблизительно 0,7.
Ссылки
- Аткинс, П. 1999. Физическая химия. Издания Омега.
- Ценгель, Ю. 2012. Термодинамика. 7 ма Издание. Макгроу Хилл.
- Энгель, Т. 2007. Введение в физико-химию: термодинамика. Пирсон.
- Левин, И. 2014. Основы физико-химии. 6-е. Издание. Макгроу Хилл.
- Википедия. Фактор сжимаемости. Получено с: en.wikipedia.org.
Значение символа медицины
Морская звезда: характеристика, виды, среда обитания, дыхание
Уравнение состояния газов
Состояние газов характеризуется давлением Р, температурой 7, и объемом V. Связь между этими величинами определяется законами газового состояния.
Нефтяные и природные газы имеют значительные отклонения от законов идеальных газов вследствие взаимодействия между собой молекул, которое возникает при сжатии реальных газов. Степень отклонения сжимаемости реальных газов от идеальных характеризуется коэффициентом сжимаемости z, показывающим отношение объема реального газа к объму идеального при одних и тех же условиях.
В пласте углеводородные газы могут находиться в самых различных условиях. С увеличением давления от О до 3-4 МПа объем газов уменьшается. При этом молекулы углеводородного газа сближаются и силы притяжения между ними помогают внешним силам, сжимающим газ. Когда углеводородный газ сильно сжат, межмолекулярные расстояния оказываются настолько малыми, что отталкивающие силы начинают оказывать сопротивление дальнейшему уменьшению объема и сжимаемость газа уменьшается.
На практике состояние реальных углеводородных газов при различных температурах и давлениях можно описывать на основании уравнения Клапейрона:
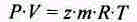 |
где Р — давление гз. Па; V’ — объем, занимаемый газом при заданном давлении, м 3 ; т — масса газа, кг; R —газовая постоянная, Дж/(кг-К); Т- температура, К; г — коэффициент сжимаемости.
Коэффициент сжимаемости определяют по графикам, построенным по экспериментальным данным.
Состояние углеводородных газожидкостных систем при изменении давления и температуры.
При движении нефти и газа в пласте, стволе скважины, системах сбора и подготовки меняются давление и температура, что обусловливает изменение фазового состояния углеводородов — переход из жидкого в газообразное состояние и наоборот. Так как нефть и газ состоят из большого числа разнообразных по своим свойствам компонентов, то при определенных условиях часть этих компонентов может находиться в жидкой фазе, а другая — в паровой (газовой) фазе. Очевидно, что закономерности движения однофазной системы в пласте и стволе скважины значительно отличаются от закономерностей многофазного движения. Условия дальнего транспорта нефти и газа и последующей переработки требуют отделения легко испаряющихся компонентов от жидкой конденсированной фракции. Поэтому выбор технологии разработки месторождения, системы внутрипромысловой подготовки нефти и газа во многом связан с изучением фазового состояния углеводородов в меняющихся термодинамических условиях.
Фазовые превращения углеводородных систем иллюстрируются диаграммами фазовых состояний, показывающими связь между давлением, температурой и удельным объемом вещества.
На рис. 2.2, а приведена диаграмма состояния чистого газа, (этана). Сплошными линиями на диаграмме показана связь между давлением и удельным объемом вещества при постоянных температурах. Линии, проходящие через область, ограниченную пунктирной кривой, имеют три характерных участка. Если рассматривать одну из линий области высоких давлений, то сначала рост давления сопровождается небольшим увеличением удельного объема вещества, которое обладает сжимаемостью и в этой области находится в жидком состоянии.
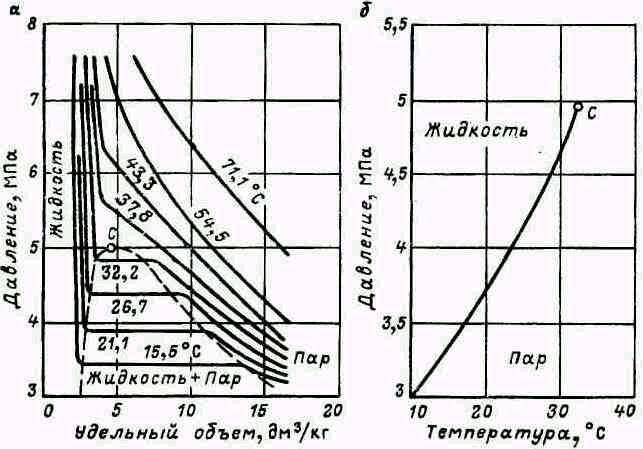 |
Рис. 2.2. Диаграмма состояния чистого газа
При некотором давлении изотерма резко изламывается и имеет вид горизонтальной линии. При постоянном давлении происходит непрерывное увеличение объема вещества. В этой области жидкость испаряется и переходит в паровую фазу. Испарение заканчивается в точке второго излома изотермы, после которого изменение объема сопровождается почти пропорциональным уменьшением давления. В этой области все вещество находится в газообразном
состоянии (в паровой фазе). Пунктирной линией, соединяющей точки излома изотерм, ограничена область перехода вещества из жидкого в паровое состояние или наоборот (в сторону уменьшения удельных объемов). Эта область соответствует условиям, при которых вещество находится одновременно в двух состояниях жидком и газообразном (область двухфазного состояния вещества). Пунктирная линия, расположенная влево от точки С, называется кривой точек парообразования. Координаты точек данной линии — давление и температура, при которых начинается кипение вещества. Вправо от точки С лежит пунктирная линия, называемая кривой точек конденсации или точек росы. Она показывает при каких давлениях и температурах начинается конденсация пара — переход вещества в жидкое состояние. Точка С, лежащая в вершине двухфазной области, называется критической точкой. При давлении и температуре, соответствующей этой точке, свойства паровой и жидкой фаз одинаковы. Кроме того, для чистого вещества критическая точка определяет наивысшие значения давления и температуры, при которых вещество может одновременно находиться в двухфазном состоянии. При рассмотрении изотермы, не пересекающей двухфазную область видно, что свойства вещества изменяются непрерывно и переход вещества из жидкого состояния в газообразное или наоборот происходит, минуя двухфазное состояние.
На рис. 2.2, б приведена диаграмма состояния этана, перестроенная в координатах давление-температура. Так как чистое вещество из одного фазового состояния в другое переходит при постоянном давлении, то кривые точек испарения и конденсации на этой диаграмме совпадают и заканчиваются критической точкой С. полученная линия разграничивает области жидкого и парообразного вещества. В двухфазном состоянии вещество может находиться только при давлениях и температурах соответствующих координатам этой линии.
Коэффициент сжимаемости природного газа
Большая Энциклопедия Нефти и Газа
Коэффициент сжимаемости природного газа определяется по температуре и давлению газа на входе в нагнетатель. График зависимости Z / ( рн, Ts, А) показан на рис. П-12. Значение газовой постоянной принимается по величине относительного удельного веса ( по воздуху) или данным химического анализа. [2]
Коэффициент сжимаемости природного газа определяется по температуре и давлению газа на входе в нагнетатель. График зависимости Z — f ( ри, Тл, А) показан на рис. П-12. Значение газовой постоянной принимается по величине относительного удельного веса ( по воздуху) или данным химического анализа. [3]
Коэффициент сжимаемости природных газов приближенно может быть определен по критическим параметрам. [4]
Коэффициенты сжимаемости природных газов в диапазоне давлений до 2 5 МПа и содержащих не более 2 % группы Cs высшие или ароматических углеводородов и не более 5 % полярных или кислых компонентов можно находить по графикам Брауна с соавторами или графикам Максвелла. [5]
Рассчитываякоэффициенты сжимаемости природных газов, обычно применяют методы, в основу которых положен принцип соответственных состояний. Согласно этому принципу значения коэффициентов сжимаемости различных УВ при одинаковых приведенных температуре ТПР и давлении рпр приблизительно равны. Это позволяет использовать для определения объема газа его зависимость от приведенных параметров. [6]
Значениякоэффициента сжимаемости природного газа указаны в табл. 3 для приведенных давления и температуры. [7]
А правильно ли мы определяемкоэффициент сжимаемости природного газа. [8]
На рис. 6 показана зависимостькоэффициента сжимаемости природного газа от приведенных параметров, а на рис. 7 и 8 та же величина, в первом случае, для паров углеводородов с молекулярным весом от 20 до 40 и, во втором случае, для паров. [10]
Все упомянутые выше методы определениякоэффициента сжимаемости природного газа применяются для расчета z газовых смесей, не содержащих пары воды. Для определения z газовых смесей с парами воды следует найти молярную долю паров воды в смеси и пересчитать ее состав. [11]
Нижеследующие три таблицы представляют некоторые результаты расчетовкоэффициента сжимаемости природного газа по методу AGA8, полученные с помощью пакета Гаэпак, в котором обе методики используются как рабочие. [12]
Метод 4 основан на применении псевдоприведенных свойств и диаграммыкоэффициента сжимаемости природных газов. [13]
И в свой кабинет и задал вопрос, который для нас был неожиданным: А правильно ли мы определяемкоэффициент сжимаемости природного газа. [14]
Сравнение рекомендованных справочных ( таблицы ГСССД 81 — 84) и расчетных данных ( по модифицированному уравнению состояния) длякоэффициентов сжимаемости природного газа, состав которого регламентирован ГОСТ 2319 — 83: 98 63 мол. [15]
ПОИСК
Минимальное значение коэффициента сжимаемости метана соответствует давлению 140—160 бар. При давлении выше 350 бар при сжатии газа начинают влиять на его объем размеры молекул и коэффициент сжимаемости становится больше единицы. [c.
Значения коэффициента сжимаемости газа, являющегося смесью различных газов, принимают в приближенных расчетах по его ОСНОВНОМ компоненту в частности, для природного и попутного газов — по метану (см. табл.
3), а в точных расчетах — в зависимости от коэффициента сжимаемости отдельных составляющих газов и их содержания в смеси. [c.8]
Вещество сравнения. Одним из методов, применяемых для нормализации или приведения уравнений, является соотнесение свойств рассматриваемого вещества со свойствами вещества сравнения, которые хорошо известны.
Так, в ходе многолетней работы Отмер [536] разработал линейную зависимость между рядом свойств и некоторым другим свойством, например давлением паров иолы при постоянной температуре. Питцер и др. [555] определили коэффициент сжимаемости как отклонение от значения коэффициента сжимаемости такой жидкости сравнения, как аргон.
Ли и Кеслер [425] соотносят свойства со свойствами двух хорошо изученных жидкостей — простой жидкости и н-октана. Авторы работы [684] в некоторых случаях применяют в качестве жидкостей сравнения метан и н-октан. [c.29]
В табл. 33 приведено содержание воды в газовой фазе системы метан — вода, полученное пересчетом данных из [Olds R. H., Sage В. H., La ey W. N., 1942 r.], при этом коэффициент сжимаемости газового раствора г) принимался рав- [c.51]
Поэтому, несмотря на доступность воспроизведения и измерения в широких пределах температуры и давления, изучение объемного поведения всей совокупности смесей практически не осуш ествимо.
Тем не менее необходимость точной интерполяции влияния состава на поведение системы требует экспериментального изучения достаточного числа различных смесей в широком диапазоне, изменения составов. На рис. 2.
3 показано влияние состава на коэффициент сжимаемости смеси метан — этан для ряда давлений при температуре 71,1° С. [c.21]
Смотреть страницы где упоминается термин Метан коэффициент сжимаемости: [c.29] [c.245] [c.28] [c.1015] Технология связанного азота Издание 2 (1974) — [ c.101 ]
Коэффициент сжимаемости
Метан коэффициенты
Сжимаемость
© 2019 chem21.info Реклама на сайте
Способ оперативного определения коэффициента сжимаемости газов и их смесей
Изобретение относится к измерительной технике и может быть использовано на замерных узлах газодобывающих и газотранспортных предприятий, при проведении исследований физических свойств газов и их смесей (в частности, топливных природных и попутных нефтяных) и в других случаях, где необходимо знание величины отступления поведения газа от идеального.
Одним из основных показателей работы газодобывающего или газотранспортного предприятия является количество добываемого или передаваемого газа в единицу времени — его объемный расход Q0.
Наиболее распространенным способом измерения объемного расхода, принятым на сегодня, является способ определения переменного перепада давления на сужающем устройстве (СУ) — сопле или диафрагме.
При этом основным расчетным соотношениям для определения величины Qo является следующее 1:
где ΔР — перепад давления на СУ, ρ — плотность газа в рабочих условиях (р.у.) (при давлении Р и температуре газа в трубопроводе 7), Q0 — объемный расход (в р.у.), А — интегральный коэффициент, учитывающий форму СУ (коэффициент расхода), поправочный множитель на расширение газа, площадь минимального проходного отверстия СУ и др.
Плотность газа в рабочих условиях р на предприятиях газовой промышленности не измеряется (из-за отсутствия надежных и сравнительно недорогих средств измерения). Как правило, поступают одним из следующих образов:
— либо в лаборатории взвешивают представительную пробу газа в особом сосуде известного объема (пикнометре) при комнатной температуре, определяют плотность, затем измеряют температуру и атмосферное давление, вносят поправку на отличие давления и температуры газа от стандартных, т.е. приводят плотность к стандартным условиям, иными словами, получают ее значение ρс при давлении Рс=1,0131·105 Па и температуре Тс=293,15K (наиболее распространенный способ);
— либо на хроматографе определяют компонентный состав (с соответствующей высокой точностью) и, уже исходя из него, вычисляют значение ρс (более редкий способ).
Для расчета состояния реальных газов и их свойств используют полуэмпирические формулы или уравнения, построенные на основе обработки реальных зависимостей, полученных из эксперимента [4].
В инженерных расчетах чаще всего пользуются обобщенным уравнением Менделеева-Клапейрона (2), в которое вводится некоторый безразмерный коэффициент Z, получивший название фактора сжимаемости; он учитывает отклонение поведения реального газа от идеального:
здесь Р — давление газа, Т — его температура, V — занимаемый газом объем, R — универсальная газовая постоянная, m — масса газа, М — его молярный вес.
Зная температуру и давление, из уравнения состояния (2) вычисляют плотность ρ газа как в рабочих, так и в стандартных условиях:
а из соотношениядалее находят ρ через ρс:
здесь Zc и Z — значения факторов сжимаемости при стандартных (Рс, Тс) и рабочих (Р, Т) условиях. При этом уравнение (1) примет вид
где коэффициент- отношение факторов сжимаемости получил название коэффициента сжимаемости.
Как видно из (5), коэффициент сжимаемости прямо входит в формулу, по которой рассчитывается расход, и его погрешность входит в погрешность определения расхода.
Наиболее точно факторы сжимаемости любых газов — чистых попутных нефтяных либо природных газов определяются экспериментально.
На специальном физическом оборудовании в лаборатории в некоторой области температур и давлений получают совокупность экспериментальных точек [Рi, Vi, Ti, или [Рi, ρi, Ti], или [Zi, ρi, Ti], где Рi, Vi, ρi, Тi, Zi — соответственно давление, удельный объем, плотность, температура и фактор сжимаемости в точке i.
Обрабатывая эти данные, получают зависимости Z(P, Т), по которым можно найти значения Z в промежуточных точках.
Техника для экспериментального определения зависимостей Z(P, Т) достаточно сложна и не может быть сегодня воспроизведена в заводской лаборатории газового предприятия или в ЦНИПРе. Кроме того, такие измерения (по существу исследования) требуют значительного труда и времени. Поэтому на практике используют графические и аналитические способы определения коэффициентов Z и K.
ГОСТ 30319.2-96 [4] рекомендует использовать один из 4-х расчетных способов определения Z и K, а именно: NX19 мод., УС GERG, УС AGA8-92DC и УС ВНИЦ СМВ.
Исходными данными для первых двух являются давление, температура, плотность в стандартных условиях ρс и молярные доли азота и углекислого газа.
Для последних двух способов исходными являются давление, температура и молярные доли всех компонентов природного газа.
Погрешность вычисления величины Z-δZ зависит от того, какой расчетный способ используется, а также от точности измерения вводимых исходных данных и термобарических параметров (рабочих условий).
Действительно, обратившись к таблице 1 ГОСТ 30319.2-96, увидим, что для способа NX19 мод.
при ρс>0,75 кг/м3 и Р>7 МПа погрешность расчета составляет 1,09%, а отклонение от экспериментальных данных — 1,65%.
Для способа GERG-91 мод.: при ρ=0,74-1,00 кг/м2 (смеси с H2S) при Р — 0,1-11 МПа погрешность расчета составляет 2,1% отклонение от экспериментальных данных 3,1%.
Для способа АGА8-92ДС: при ρ=0,74-1,00 (смеси с H2S) и Р=0,1-11 МПа погрешность расчета — 1,3%, отклонение экспериментального значения — 1,88% и т.д.
Примем далее за прототип один из способов, например, GERG-91 мод.
Таким образом, для природных газов только погрешности расчета (в отдельных областях рабочих условий) доходят до 2%. Экспериментальные данные дадут, по-видимому, расхождение с истинными еще больше.
На уровне погрешностей измерения других параметров расхода — температуры, давления, перепада давления, лежащих в диапазоне 0,1…0,5%, такие большие погрешности при установлении величины Z становятся определяющими.
Важным моментом является также то обстоятельство, что расчетная величина Z выступает как средняя за период между измерениями величин, входящими в исходные расчетные данные при подсчете, изменении компонентного состава в течение этого промежутка времени, неконтролируемая погрешность может выходить за границы погрешности расчетной величины Z.
Таким образом, недостатком существующего способа определения коэффициента сжимаемостиявляется необходимость проведения предварительного хроматографического анализа с целью получения данных о компонентном составе и высокая погрешность расчетов величины К в отдельных термобарических областях. Кроме того, полученное значение коэффициента сжимаемости относится к определенному моменту времени — времени взятия пробы для анализа tо, т.е. К=K(tо). Невозможность непрерывного слежения за величиной К=K(t) является следующим недостатком способа определения К.
Техническим результатом предлагаемого способа определения коэффициента сжимаемости К является возможность оперативно измерять этот коэффициент, т.е.
находить функцию K(t) с погрешностью не выше погрешности измерения других входящих в формулу расхода (5) физических величин (Р, ΔР, Т, ρс) в любом диапазоне термобарических параметров и, как следствие этого, понижение погрешности измерения расхода при использовании расходомеров на сужающих устройствах.
Технический результат достигается тем, что в способе оперативного определения коэффициента сжимаемости используют объемный резонатор, выполненный из металла с малым коэффициентом температурного расширения и с известной собственной частотой в вакууме ω0, заполняют газом при стандартном давлении и температуре и измеряют значение резонансной частоты ωс, затем заполняют его газом при рабочих давлениях Р и температуре Т и измеряют значение собственной частоты ωр, после чего коэффициент сжимаемости К рассчитывают по соотношению:
На фиг.1 изображена схема устройства, реализующего предложенный способ. Она включает в себя СВЧ генератор 3 см диапазона длин волн на диоде Ганна 1, два объемных резонатора, изготовленных из металла с малым температурным коэффициентом расширения — измерительный 2 и опорный 3, детектор измерительного канала 4, детектор опорного канала 5.
Электронная часть устройства состоит из блока управления 8, блока измерения частоты 9 и стабилизированного блока питания 10. Газовый тракт включает трубку подвода газа 11, редуктор 12, входной 13 и выходной 14 газовые вентили, манометр 15, термометр 16, выкидную трубку 17. Измерительный резонатор помещен в термостат 18.
Работа устройства происходит следующим образом.
В блоке 8 вырабатывается пилообразное напряжение, управляющее частотой генератора 1.
Более точно — «пила» состоит из 256 ступенек, так что номер ступеньки («код») однозначно определяет напряжение и, следовательно, частоту генератора: таким образом, осуществляется взаимнооднозначное соответствие между кодом и частотой. Код, соответствующий резонансной частоте резонатора 2, высвечивается на передней панели прибора.
Опорный канал, на основе резонатора 3 и детектора 5, служит для стабилизации начальной частоты генератора 1; электроника блока управления 8 устроена таким образом, что резонансная частота резонатора 3 всегда соответствует одному и тому же коду; в случае отклонения от заданного значения кода вырабатывается напряжение, подаваемое на диод Ганна, генератора 1, которое корректирует уход частоты.
Выходным параметром схемы регистрации является резонансная частота резонатора. В отсутствие газа (в вакууме) частота резонатора равна ωо; при заполнении резонатора газом с диэлектрической постоянной ε частота его понижается и становится равной ω.
Используем соотношение между диэлектрической проницаемостью и плотностью газа, основанное на соотношении Клаузиуса-Мосотти, которое связывает микроскопические параметры вещества газа — его поляризуемость α и молярную массу М — с макроскопическими, измеряемыми параметрами — плотностью вещества ρ и его относительной диэлектрической проницаемостью (ДП) ε 6:
где NA — число Авогадро; εо=8,854·10-12 ф/м — электрическая постоянная.
Разрешив (5) относительно ρ, получим:
Поскольку для всех газов при небольших и умеренных давлениях (P≤10 МПа) ε-1
Коэффициент сжимаемости газов и газоконденсатных смесей: экспериментальное определение и расчеты — PDF
1 120 Коэффициент сжимаемости газов и газоконденсатных смесей: экспериментальное определение и расчеты КОЭФФИЦИЕНТ СЖИМАЕМОСТИ ГАЗОВ И ГАЗОКОНДЕНСАТНЫХ СМЕСЕЙ: ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ И РАСЧЕТЫ В.И. Лапшин, А.Н. Волков, И.М.
Шафиев (ООО «Газпром ВНИИГАЗ») Коэффициент сжимаемости (Z) характеризует отличие реальных газов от идеальных. Для идеальных газов, в которых отсутствует взаимодействие между молекулами, справедлив закон Клайперона, который обобщает законы Бойля Мариотта и Гей-Люссака: (P V) / T = (P 0 V 0 ) / T 0 = R, где R универсальная газовая постоянная.
Для реальных газов произведение объема на давление (P V) при постоянной температуре не является постоянной величиной. С ростом давления это произведение вначале уменьшается до определенного предела, а затем с увеличением давления увеличивается.
При практических расчетах для оценки степени указанных отклонений в уравнение Клайперона вводится поправочный коэффициент (Z) [1, 2, 3].
Уравнение Клайперона Менделеева с учетом коэффициента сжимаемости имеет вид PV = ZNRT, где Р абсолютное давление; V объем, занимаемый газом (газоконденсатной смесью) при определенных давлении и температуре; R универсальная газовая постоянная; N число молей газа. Это уравнение можно записать в виде PV N =.
(1) ZRT Учитывая, что определение коэффициента сжимаемости проводится без изменения числа молей газа (N г = const), PV 0 0 N г =, (2) Z RT 0 0 где V 0 объем газа при Р 0 = 0,1013 МПа, м 3 ; Т 0 = 293 К; R = 24,01 МПа К Z 0 = 1. Экспериментальное определение коэффициента сжимаемости газов и газоконденсатных смесей, особенно с высоким содержанием Н 2 S и СО 2, рекомендуется проводить на установках типа Маgra-РVT, АСФ-PVT или дру- м 3 ;
2 Актуальные вопросы исследований пластовых систем месторождений углеводородов. Часть I 121 гих большеобъемных установках PVТ [2, 4, 5]. Схема соединения технологических узлов установки Маgra-РVT для изучения коэффициента сжимаемости газов и газоконденсатных смесей приведена на рис. 1.
Для более точного определения объемов газа при различных давлениях рекомендуется проведение специального комплекса тарировочных исследований, которые включают определение объемов камер PVT, а также поправок на их термическое расширение и механическую деформацию.
Проведенные авторами настоящей статьи исследования [4, 5] показали, что наиболее технологичным способом определения коэффициента сжимаемости является сжатие определенного объема газа в камере PVT за счет изменения ее объема нагнетанием ртути или введением поршня.
Определение объемов камер PVT и насосов осуществлялось методом замера объема тарировочной жидкости (ртути) после ее слива из полностью заполненных камер при нормальных условиях: Р кам = 0,1013 МПа; Т кам = 293 К; количество замеров 15. Результаты определения объемов камер PVT и насосов по 15 замерам приведены в табл. 1. Рис. 1.
Схема установки для исследования коэффициента сжимаемости газов и газоконденсатных смесей: 1, 2 ртутный насос; 3 датчик объема; 4 контейнер с газом; 5 контейнер с конденсатом; 6 камера PVT (0,7 л); 7 кран высокого давления; 8 датчик давления и температуры; 9 камера PVT (3,8 л); 10 сепаратор-термостат; 11 газовый счетчик
3 122 Коэффициент сжимаемости газов и газоконденсатных смесей: экспериментальное определение и расчеты Таблица 1 Результаты определения объемов камер PVT и насосов установки Magra-PVT Объем камер PVT и насосов, см 3 Камеры PVT Насосы 0,7 л 3,8 л ,0 3604,0 489,2 489,2 +0,3 +3,0 +0,1 +0,1 Для расчета истинного объема газа в камерах PVT использовалось следующее выражение: V г = V кам + ΔV кам (t) + ΔV кам (р) V рт (с) ΔV рт (t) + ΔV рт (р), (3) где V кам объем камеры PVT при нормальных условиях; ΔV кам (t) поправка на термическое расширение камеры PVT; ΔV кам (р) поправка на механическую деформацию камеры PVT; V рт (с) объем закачанной в камеру PVT ртути (по счетчику); ΔV pт (t) поправка на термическое расширение закачанной в камеру PVT ртути (по счетчику); ΔV рт (р) поправка на механическую деформацию ртути. Исходя из уравнения состояния для индивидуальных газов и газовых смесей, коэффициент сжимаемости рассчитывается по формуле PVT Z = 0. (4) PV 0 0T Определение коэффициента сжимаемости сухих газов начинается с заправки газа в камеру PVT, которая проводится следующим образом. В камеру PVT емкостью 0,7 л (см. рис. 1) из галонного контейнера передавливают газ в объеме, равном 50 или 100 л. Ориентировочно объем газа оценивается по давлению заправки, которое рассчитывается по формуле Р0Z тqг Р = Т з, (5) Т 0Vкам где Р 0 нормальное давление (0,1013 МПа); Т т температура термостата, К; Q г объем газа (100 л), загруженного в камеру при Т 0 ; Т 0 нормальная температура, 293 К; V кам объем камеры (0,7) с учетом поправок согласно формуле (1); Z коэффициент сжимаемости. Коэффициент сжимаемости газа при этом определяется ориентировочно расчетным или экспериментальным путем. Далее в рабочей камере создают необходимую температуру и поэтапно повышают давление до МПа. В конце каждого этапа после стабилизации давления опреде-
4 Актуальные вопросы исследований пластовых систем месторождений углеводородов. Часть I 123 ляют объем сжатого газа. Объем газа при Р 0 = 0,1013 МПа и Т 0 = 293 К замеряют, пропуская газ через термостат и газовый счетчик.
Вычисляют коэффициент сжимаемости при давлении Р по формуле Z = PVT 0 / P 0 V 0 T, (6) где V объем газа при давлении Р и температуре Т, м 3 ; V 0 объем газа при P 0 = 0,1013 МПа и Т 0 = 293 К, м 3.
Для оценки точности определения коэффициентов сжимаемости газа сепарации Карачаганакского НГКМ проведен цикл экспериментов с использованием газовой смеси одного состава.
Всего проведено 17 экспериментов, в каждом из которых определялись объем газовой смеси и давление и рассчитывался коэффициент сжимаемости (Т = Т 0 = 293 К) (табл. 2). В табл. 2 приведены результаты определения коэффициента сжимаемости газа сепарации Карачаганакского НГКМ (состав газа приведен ниже).
Таблица 2 Результаты определения коэффициента сжимаемости газа сепарации Карачаганакского НГКМ п/п Р 0, МПа V 0, л Объем смеси с поправкой, см з Давление в камере, МПа , , ,09 29,97 0, // — — // — 306,04 29,92 0, // — — // — 306,09 30,02 0, // — — // — 306,09 29,97 0, // — — // — 306,14 29,96 0, // — — // — 306,14 30,03 0, // — — // — 305,59 29,92 0, // — — // — 306,04 30,02 0, // — — // — 306,20 30,02 0, // — — // — 306,20 30,02 0, // — — // — 306,14 29,97 0, // — — // — 306,14 29,92 0, // — — // — 306,02 29,92 0, // — — // — 306,14 29,92 0, // — — // — 306,14 29,99 0, // — — // — 306,09 29,97 0, // — — // — 306,14 30,30 0,9115 Среднее — // — — // — V = 306,09 P = 29,97 Z = 0,9112 Z = PV P 0 V 0
5 124 Коэффициент сжимаемости газов и газоконденсатных смесей: экспериментальное определение и расчеты Исходя из данных, приведенных в табл. 2, определены значения давления и объема газа сепарации с учетом погрешности измерения: Р г.с = P с г. + ΔР = 29,97 ± 0,05 МПа; (7) 3 V = V + ΔV = 306,09 0,55 cм. (8) г с г ±..
с Среднее значение коэффициента сжимаемости равно PV Z = г. с 29,97 306,09 = = 0, (9) PV 0 0 0, ,87 Коэффициент сжимаемости с учетом среднеквадратичного отклонения равен Z = Z + ΔZ = 0, ,0021. (10) Относительная погрешность косвенных измерений находилась следующим образом: σz 0,0021 σ = = = 0,0023; (11) Z 0,9112 d = 0, % = 0,23 %.
Z Анализ полученных данных позволяет говорить о высокой точности определения коэффициента сжимаемости газов и газовых смесей на установке Magra-PVT, т.к. относительная погрешность составляет доли процента.
При определении коэффициента сжимаемости газоконденсатных смесей делаются следующие допущения [2, 6]: коэффициент сжимаемости определяется при давлении выше Р нк ; объем смеси при Р 0 = 0,1013 МПа и Т 0 = 293 К принимается равным сумме объемов сухого газа V 0 и газового эквивалента V г.э (V г.
э объем паров, получаемых после испарения жидких углеводородов, растворенных в газе). Определение коэффициента сжимаемости газоконденсатной смеси начинается с ее рекомбинации в камере PVT (6) (см. рис.1). Основные исследования проводят, используя газоконденсатную смесь в газообразном состоянии.
Для этого поэтапно изотермически снижают давление в камере и в конце каждого этапа определяют объем газоконденсатной смеси V см при давлении Р см. Снижение давления и определение объема исследуемой смеси проводят до достижения давления начала конденсации.
6 Актуальные вопросы исследований пластовых систем месторождений углеводородов. Часть I 125 Затем давление в камере (6) снижается до минимально возможного и она охлаждается до комнатной температуры, при этом смесь разделяется на газ и конденсат. Газ пропускается через термостат (10) при Т = 293 К и счетчик (11), в котором замеряется объем V 0.
Весь выпавший конденсат собирается в сепараторе и камере, замеряется его объем q к и определяется плотность ρ к.
Расчет коэффициента сжимаемости проводится по формуле Z = V кр Р V см ( 0 0 V Т см 0, (12) + Vк ) Т q ρ кт кк24,040 = 293 М см т, (13) где Р см, Т см, V cм давление, температура и объем смеси в камере; V 0 объем газа, замеренного счетчиком при Р 0 ; V к объем паров, получаемых после испарения выпавших жидких углеводородов (конденсата); q к количество выпавшего конденсата, см 3 ; ρ к плотность конденсата, г/см 3 ; Т т температура термостата, К; М к молярная масса конденсата, г/моль. Оценка точности разработанной методики проводилась путем сопоставления результатов определения коэффициентов сжимаемости индивидуальных газов (метана, углекислого газа, сероводорода) экспериментальным путем на установке PVT с данными, приведенными в [7, 8] (рис. 2). Рис. 2. Экспериментальные и эталонные кривые коэффициента сжимаемости для метана (а); углекислого газа (б); сероводорода (в) при температурах: 423 К (1); 383 К (2); 293 К (4): эталонные; экспериментальные
7 126 Коэффициент сжимаемости газов и газоконденсатных смесей: экспериментальное определение и расчеты Отклонение экспериментальных данных от эталонных практически во всех интервалах давлений и температур не превышает 0,2 1,3 %, что свидетельствует о достаточно высокой точности разработанной методики.
Для выявления влияния углекислого газа на сжимаемость проведены исследования смесей, состоящих из 75 % метана, 25 % углекислого газа (% мол.) и разного содержания C 5+ при различных давлениях и температурах. Результаты проведенных экспериментов показали, что растворение в метане углекислого газа (рис.
3) существенно изменяет конфигурацию кривых коэффициентов сжимаемости. Результаты, полученные в ходе экспериментальных работ, позволяют решать задачи, связанные с разработкой, добычей и транспортом газа.
Так, например, разработаны графики для определения коэффициентов сжимаемости газов сепарации Астраханского ГКМ и Карачаганакского НГКМ в интервале давлений от 0,1013 до 70.0 МПа и температур от 293 до 383 К [7, 10]. Рис. 3.
Экспериментальные зависимости коэффициента сжимаемости газовой (а) и газоконденсатных (б С 5+ = 200 г/м 3 ; в С 5+ = 800 г/м 3 ) смесей от давления и температуры: К; К Для Астраханского ГКМ графики построены по результатам исследования газа сепарации следующего состава: H 2 S 24,52; СО 2 14,68; С 1 55,43; С 2 2,63; С 3 1,09; С 4 0,56; С 5+ 0,41; N 2 0,67 % мол. (рис. 4). Этот состав газа сепарации близок к среднему составу по месторождению.
8 Актуальные вопросы исследований пластовых систем месторождений углеводородов. Часть I 127 Для Карачаганакского НГКМ графики построены по результатам исследования газа сепарации следующего состава: H 2 S 3,2; CО 2 6,72; С 1 80,61; С 2 5,20; С 3 2,11; С 4 0,79; С 5+ 0,15; N 2 1,29 % мол. (рис. 5).
Сопоставление расчетных значений коэффициентов сжимаемости различными методами с экспериментальными данными показало [2, 9], что отклонение в различных интервалах давлений и температур доходит до 27,7 %.
Наиболее близкие к экспериментальным аналитические значения коэффициентов сжимаемости для газа сепарации Астраханского ГКМ получены при использовании: метода определения коэффициентов сжимаемости по Вичерту Азизу Кей Брауну в диапазоне давлений МПа и температур К.
Рассчитанные по этому методу значения в среднем завышены на + 5,8 %; методов определения коэффициентов сжимаемости по Кей Брауну и Кей Питцеру в диапазоне давлений МПа и температур К. Отклонение расчетных коэффициентов сжимаемости от экспериментальных колеблется в пределах 0,8 5,4 %.
Из анализа расчетов коэффициентов сжимаемости с помощью уравнения состояния Пенга Робинсона [2] следует, что при давлениях до 30 МПа с наименьшей погрешностью коэффициенты сжимаемости рассчитываются с помощью вышеупомянутого уравнения. С увеличением давления погрешность расчета возрастает.
Исследование коэффициента сжимаемости газоконденсатных смесей показало, что растворение в метане жидкой фазы (конденсата) приводит к его увеличению (рис. 6). Так, при растворении 200 г/м 3 углеводородов С 5+ увеличение коэффициента сжимаемости составляет 2 5 %, при растворении порядка 800 г/м % в зависимости от температуры. Особый интерес представляют впервые экспериментально определенные коэффициенты сжимаемости реальных газоконденсатных смесей Карачаганакского НГКМ с высоким содержанием конденсата (рис. 7).
9 128 Коэффициент сжимаемости газов и газоконденсатных смесей: экспериментальное определение и расчеты Рис. 4. График для определения коэффициента сжимаемости газа сепарации Астраханского ГКМ при различных давлениях и температурах
10 Актуальные вопросы исследований пластовых систем месторождений углеводородов. Часть I 129 Рис. 5. График для определения коэффициента сжимаемости газа сепарации Карачаганакского НГКМ при различных давлениях и температурах
11 130 Коэффициент сжимаемости газов и газоконденсатных смесей: экспериментальное определение и расчеты Рис. 6.
Зависимость коэффициента сжимаемости газоконденсатной смеси от содержания конденсата при различных давлениях и температурах: 1 50 МПа; 2 60 МПа; 3 70 МПа; 4 80 МПа: а 293 К; б 343 К; в 383 К Рис. 7.
График для определения коэффициентов сжимаемости газоконденсатных смесей Карачаганакского НГКМ
12 Актуальные вопросы исследований пластовых систем месторождений углеводородов. Часть I 131 Список литературы 1. Гуревич Г.Р. Справочное пособие по расчету фазового состояния и свойств газоконденсатных смесей / Г.Р. Гуревич, А.И. Брусиловский. М.: Недра, с. 2. Гуревич Г.Р.
Коэффициенты сжимаемости природных газов с высоким содержанием сероводорода и двуокиси углеводорода / Г.Р. Гуревич, В.И. Лапшин, А.И. Брусиловский, А.П. Желтов // Изв. вузов. Сер. Нефть и газ С Ширковский А.И. Разработка и эксплуатация газовых и газоконденсатных месторождений: учебник для вузов. 2-е изд. М.: Недра, с. 4. Лапшин В.И.
Методика и результаты исследования коэффициентов сверхсжимаемости природных газов с высоким содержанием сероводорода и углекислого газа / В.И. Лапшин, А.П. Желтов, Г.Р. Гуревич // Геология нефти и газа С Лапшин В.И. Экспериментальное определение коэффициента сверхсжимаемости газовых смесей с высоким содержанием Н 2 S, CO 2 / В.И. Лапшин, Ю.Ю. Круглов, A.
П. Желтов // Экспрес. информ. Сер. Разработка и эксплуатация газовых и газоконденсатных месторождений С Лапшин В.И. Природные газы сложного состава. Результаты исследования сверхсжимаемости / В.И. Лапшин // Газовая промышленность С Динков В.А. Расчет коэффициентов сжимаемости углеводородных газов и смесей: справочное пособие / В.А. Динков, З.Т.
Галиуллин, А.П. Подкопаев. М.: Недра, С Катц Д.Л. Руководство по добыче, транспорту и переработке природного газа / Д.Л. Катц, Д. Корнелл, Р. Кобаяши и др. М.: Недра, с. 9. Лапшин В.И. Аналитическое определение коэффициента сверхсжимаемости газов Астраханского месторождения.
Совершенствование технологии строительства глубоких разведочных скважин в аномальных условиях Прикаспийской впадины / В.И. Лапшин, В.В. Томилкин, A.П. Желтов; под ред. П.С. Шмелева. Саратов, С