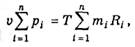Состояние каждого из атмосферных газов характеризуется значениями трех величин: температуры, давления и плотности (или удельного объема). Эти величины всегда связаны между собой некоторым уравнением, которое носит название уравнения состояния газа.
Для каждого газа существует так называемая критическая температура Ткр. Если температура газа выше критической, то ни при каком давлении газ не может быть переведен в жидкое или твердое состояние, т. е. при Т > Ткр возможно только газообразное состояние вещества. Критические температуры атмосферных газов имеют следующие значения:
Из этих данных видно, что критические температуры всех атмосферных газов, кроме углекислого газа и водяного пара, очень низкие. Температуры, которые наблюдаются в атмосфере на всех высотах, значительно выше критических температур этих газов. Хотя критическая температура углекислого газа выше, чем обычно наблюдаемые температуры воздуха, этот газ далек от состояния насыщения, поскольку его парциальное давление в условиях атмосферы мало.
По своим физическим свойствам газ тем ближе к идеальному, чем выше его температура по сравнению с критической, а также чем меньше его давление по сравнению с давлением насыщения.
При условиях, наблюдающихся в атмосфере, основные газы, входящие в состав воздуха, ведут себя практически как идеальные газы. Поэтому уравнение состояния какого-либо газа имеет вид уравнения состояния идеального газа:
где pi — парциальное давление; Т — температура; Vi — удельный объем; Ri — удельная газовая постоянная i-гo газа; п — число газов, составляющих механическую смесь.
Удельная газовая постоянная Ri ; связана с универсальной газовой постоянной R * = 8,31441 103 Дж/(кмоль • К) следующим соотношением:
где μi — относительная молекулярная масса 1-го газа.
Согласно закону Дальтона, поведение каждого газа в механической смеси не зависит от присутствия других газов, а общее давление смеси равно сумме парциальных давлений, т. е.
Пусть масса сухого воздуха равна единице, а масса i-гo газа mi Тогда
где v— удельный объем сухого воздуха.
Подставляя vi в соответствии с (1.3.4) в формулу (1.3.1) и суммируя уравнения (1.3.1), получаем:
или, согласно (1.3.3),
где Rc — удельная газовая постоянная сухого воздуха:
Уравнение (1.3.5) и представляет собой уравнение состояния сухого воздуха.
Таким образом, уравнение состояния сухого воздуха имеет тот же вид, что и уравнение состояния идеального газа. При этом удельная газовая постоянная воздуха определяется как среднее взвешенное из парциальных газовых постоянных по формуле (1.3.6).
С учетом формулы (1.3.2) и данных о составе воздуха (см. п. 1.1) получаем следующее значение удельной газовой постоянной сухого воздуха:
Относительную молекулярную массу сухого воздуха по углеродной шкале можно получить при известных Rc и R*по соотношению
Если вместо удельного объема v в уравнение (1.3.5) ввести плотность р, связанную с v соотношением р = l/v, то оно примет вид
Наряду с таким видом уравнения состояния широкое распространение, особенно при изучении верхних слоев атмосферы, получила другая форма записи его. Эта форма легко получается из уравнения (1.3.5), если левую и правую части его умножить на μс:
где V = μсv объем моля воздуха. При фиксированных р и Т объем V, согласно (1.3.9), для всех газов одинаков. Например, при Т = О °С и р = 1013,2 гПа объем Vo = 22,41 м3/кмоль.
Если теперь разделить левую и правую части (1.3.9) на число молекул воздуха в одном моле (N), то получим:
Поскольку число молекул в одном моле — число Авогадро — для всех газов одинаково (N = 6,02 • 1026 кмоль»1), то величина к представляет собой тоже универсальную постоянную, называемую постоянной Больцмана:
Следовательно, уравнение состояния воздуха, равно как и любого другого газа, можно записать также в следующем виде:
где п = N/V — число молекул воздуха в 1 м3, которое, как следует
ИЗ (1.3.12), При фиксированных р и Т одинаково для всех газов: при Т = 0 º С и р = 1013,2 гПа, п = 2,687 · 10 25 м -3 .
Из уравнений (1.3.8) и (1.3.12) следует
где m=μс / N — средняя масса одной молекулы воздуха.
Уравнения состояния атмосферного воздуха
Уравнение состояния газов применимо для теоретических расчётов и к сухому воздуху, и к водяному пару, и к влажному воздуху. Однако для влажного воздуха плотность зависит ещё и от упругости водяного пара, содержащегося в воздухе.
Уравнение состояния сухого воздуха имеет следующий вид:
где p — давление воздуха; ν — удельный объём сухого воздуха; T — абсолютная температура воздуха; Rc — удельная газовая постоянная воздуха, равная 287,05287 Дж/(кг К).
При замене удельного объёма v плотностью ρ = 1/v, уравнение состояния сухого воздуха примет вид:
Уравнение состояния влажного воздуха имеет следующий вид:
где s — массовая доля водяного пара; множитель (1 + 0,608s) можно отнести как к удельной газовой постоянной влажного воздуха, так и к температуре этого воздуха.
Уравнение состояния водяного пара с достаточной степенью точности можно записать в следующем виде:
где e — парциальное давление водяного пара; νn — удельный объём; Rn — удельная газовая постоянная водяного пара (Rn = R / Mn = 461,51 Дж / кг · К · R* = 8314,32 Дж/(кмоль∙K) — универсальная газовая постоянная).
Водяной пар отличается по своим свойствам от идеального газа (Rn не постоянна), но в пределах от 0 ºC до 40 ºC удельная газовая постоянная водяного пара близка к теоретическому значению. По этой причине уравнение состояния водяного пара может служить уравнением состояния как ненасыщенного, так и насыщенного водяного пара.
В метеорологии множитель (1 + 0,608s) обычно относят к температуре, для чего вводится понятие виртуальной температуры (Tv = T (1 + 0,608s) = T + ΔTv; ΔTv — виртуальный добавок).
С введением виртуальной температуры уравнение состояния влажного воздуха имеет вид:
где ρ = 1/ν — плотность влажного воздуха.
Из сравнения уравнений состояния сухого воздуха и влажного воздуха следует, что при одинаковой температуре и давлении плотность влажного воздуха всегда меньше плотности сухого воздуха. Физически это объясняется тем, что в состав влажного воздуха входит водяной пар, который вытесняет часть сухого воздуха.
Литература
Гидрометеорологическое Обеспечение Мореплавания — Глухов В.Г., Гордиенко А.И., Шаронов А.Ю., Шматков В.А. [2014]
Уравнение состояния газов
Основными характеристиками физического состояния газа являются его давление, температура и плотность. Все эти величины взаимозависимы. Газы сжимаемы, поэтому их плотность меняется в зависимости от давления и температуры. Связь между давлением, температурой и плотностью для идеальных газов дается уравнением состояния газов, известным из физики. Оно пишется

где 



Для каждого газа существует температура, называемая критической, выше которой любой газ можно с большой степенью точности назвать идеальным. Если температура газа выше критической, то газ ни при каком давлении не может быть переведен ни в жидкое, ни в твердое состояние.
Идеальный газ, находясь в смеси с другими газами, ведет себя независимо от них, имея собственные давление 


Рассмотрим уравнение состояния газа применительно к сухому воздуху, поскольку он как смесь газов удовлетворяет изложенным выше положениям физики. В табл. 2 приведены значения критической температуры для основных газов, входящих в состав сухого воздуха.
Критическая температура газов, входящих в состав сухой атмосферы
Для сухого воздуха, кроме входящего в него углекислого газа, все газы имеют критическую температуру более низкую, чем температуры, наблюдаемые в земной атмосфере, т.е. сухой воздух можно считать смесью идеальных газов. Углекислый газ в атмосфере имеет очень малое парциальное давление, далекое от насыщающего, т.е. в естественных условиях он также не может сконденсироваться.
Для каждого газа, входящего в атмосферу, можно записать уравнение состояния

где 


Удельная газовая постоянная связана с универсальной R= 8,31441·103 Дж/кмоль·К так:

где 

Общее давление смеси

Принимая массу сухого воздуха равной единице, а массу газа 

где: 
Используя уравнения (1), (4) и (5), запишем


где 

Относительная молекулярная масса сухого воздуха при известном 

Рассмотрим влажный воздух как смесь сухого воздуха и водяного пара. Поскольку критическая температура водяного пара равна 374ºС, он как примесь идеального газа к смеси газов, формирующих сухой воздух, рассматриваться не может. Условие, когда фактическая температура меньше критической, является необходимым, но недостаточным для перехода газа в жидкость или твердое состояние. Необходимо также, чтобы его парциальное давление достигло состояния насыщения. Последнее является только функцией температуры, свойств газа и формы поверхности, для которой она рассчитывается. Здесь будет рассмотрен водяной пар, который до момента насыщения можно считать примесью идеального газа.
Уравнение состояния водяного пара можно представить в следующем виде:

где 



где 
Как показывают экспериментальные исследования и расчеты, в диапазоне температур от 0 до 40ºС удельная постоянная водяного пара 
Для вывода уравнения состояния рассмотрим 1 кг влажного воздуха. В нем содержится q кг водяного пара и 



Сухой воздух и водяной пар равномерно распределены по объему влажного воздуха и полностью его занимают. Удельные объемы водяного пара и сухого воздуха соответственно равны


Если обозначить 



Отношение удельных газовых постоянных водяного пара и сухого воздуха

Заменив удельную газовую постоянную водяного пара удельной газовой постоянной сухого воздуха с соответствующим коэффициентом, получим уравнение состояния влажного воздуха
Множитель (1 + 0,608q) в метеорологии относят к температуре, вводя понятие виртуальной температуры
Она всегда не меньше молекулярной, так как влажность может меняться от 0 до насыщающей.
Таким образом, виртуальная температура – это температура, которую должен иметь сухой воздух, чтобы его плотность при том же давлении была равна плотности влажного воздуха.
Плотность влажного воздуха всегда меньше плотности сухого. В некоторых случаях это может служить дополнительным фактором, способствующим развитию свободной конвекции в атмосфере.
Плотность воздуха в каждом месте непрерывно меняется во времени. Кроме того, она сильно меняется с высотой, потому что с высотой меняются также атмосферное давление и температура воздуха. Давление с высотой всегда уменьшается, а вместе с ним убывает и плотность. Температура с высотой по большей части понижается, по крайней мере в нижних 10-15 кматмосферы. Но падение температуры влечет за собой повышение плотности. В результате совместного влияния изменения давления и температуры плотность с высотой, как правило, понижается, но не так сильно, как давление. В среднем для Европы она равна у земной поверхности 1250 г/м3, на высоте 5 км – 735 г/м3, 10 км – 411 г/м3, 20 км – 87 г/м3.
На высотах около 300 кмплотность воздуха имеет порядок величины 10-8 г/м3, т.е. в сто миллиардов раз меньше, чем у земной поверхности. На высоте 500 км плотность воздуха уже 10-9 г/м3,на высоте 750 км – 10-10 г/м3или еще меньше. Эти значения плотности ничтожны по сравнению с приземными. Но все же до высот более 20 тыс. кмплотность воздуха остается значительно большей, чем плотность вещества в межпланетном пространстве.
Если бы плотность воздуха не менялась с высотой, а оставалась на всех уровнях такой же, как у земной поверхности, то для высоты атмосферы получилась бы величина около 8000 м.В самом деле, приземная плотность сухого воздуха при давлении 760 мми температуре 0° равна 1293 г/м3;столб воздуха с этой плотностью должен был бы иметь высоту, очень близкую к 8000 м,чтобы производить такое же давление, какое производит столб ртути в 760 мм высотой (1033 г/см3).Указанная высота (8000 м)называется высотой однородной атмосферы. В действительности плотность воздуха с высотой убывает, и потому истинная высота атмосферы равняется многим тысячам километров.