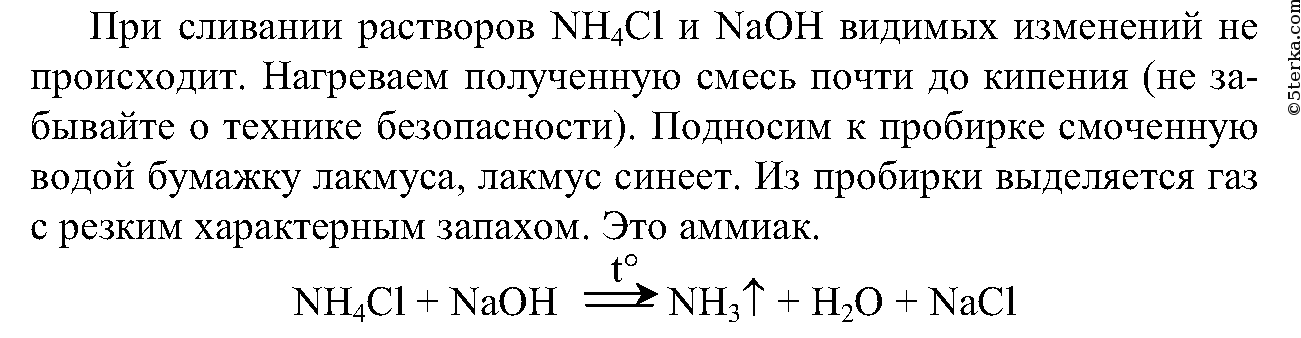
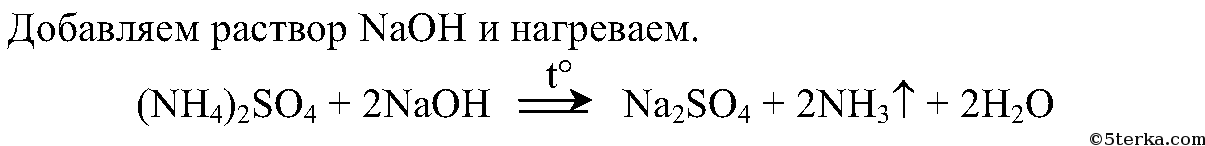- Соли аммония
- Способы получения солей аммония
- Химические свойства солей аммония
- Опыт № 6. Взаимодействие солей аммония со щелочами
- Реакция образования солей аммония
- Соли аммония — что это такое
- Химические и физические свойства
- Качественная реакция, как реагирует со щелочами
- Способы получения солей аммония, где применяются
Соли аммония
Соли аммония – это соли, состоящие из катиона аммония и аниона кислотного остатка .
Способы получения солей аммония
1. Соли аммония можно получить взаимодействием аммиака с кислотами . Реакции подробно описаны выше.
2. Соли аммония также получают в обменных реакциях между солями аммония и другими солями.
Например , хлорид аммония реагирует с нитратом серебра:
3. Средние соли аммония можно получить из кислых солей аммония . При добавлении аммиака кислая соль переходит в среднюю.
Например , гидрокарбонат аммония реагирует с аммиаком с образованием карбоната аммония:
Химические свойства солей аммония
1. Все соли аммония – сильные электролиты , почти полностью диссоциируют на ионы в водных растворах:
NH4Cl ⇄ NH4 + + Cl –
2. Соли аммония проявляют свойства обычных растворимых солей –вступают в реакции обмена с щелочами, кислотами и растворимыми солями , если в продуктах образуется газ, осадок или образуется слабый электролит.
Например , карбонат аммония реагирует с соляной кислотой. При этом выделяется углекислый газ:
Соли аммония реагируют с щелочами с образованием аммиака.
Например , хлорид аммония реагирует с гидроксидом калия:
NH4Cl + KOH → KCl + NH3 + H2O
Взаимодействие с щелочами — качественная реакция на ионы аммония. Выделяющийся аммиак можно обнаружить по характерному резкому запаху и посинению лакмусовой бумажки.
3. Соли аммония подвергаются гидролизу по катиону , т.к. гидроксид аммония — слабое основание:
4. При нагревании соли аммония разлагаются . При этом если соль не содержит анион-окислителя, то разложение проходит без изменения степени окисления атома азота. Так разлагаются хлорид, карбонат, сульфат, сульфид и фосфат аммония:
Если соль содержит анион-окислитель, то разложение сопровождается изменением степени окисления атома азота иона аммония. Так протекает разложение нитрата, нитрита и дихромата аммония:
При температуре 250 – 300°C:
При температуре выше 300°C:
Разложение бихромата аммония («вулканчик»). Оранжевые кристаллы дихромата аммония под действием горящей лучинки бурно реагируют. Дихромат аммония – особенная соль, в ее составе – окислитель и восстановитель. Поэтому «внутри» этой соли может пройти окислительно-восстановительная реакция (внутримолекулярная ОВР):
Окислитель – хром (VI) превращается в хром (III), образуется зеленый оксид хрома. Восстановитель – азот, входящий в состав иона аммония, превращается в газообразный азот. Итак, дихромат аммония превращается в зеленый оксид хрома, газообразный азот и воду. Реакция начинается от горящей лучинки, но не прекращается, если лучинку убрать, а становится еще интенсивней, так как в процессе реакции выделяется теплота, и, начавшись от лучинки, процесс лавинообразно развивается. Оксид хрома (III) – очень твердое, тугоплавкое вещество зеленого цвета, его используют как абразив. Температура плавления – почти 2300 градусов. Оксид хрома – очень устойчивое вещество, не растворяется даже в кислотах. Благодаря устойчивости и интенсивной окраске окись хрома используется при изготовлении масляных красок.
Видеоопыт разложения дихромата аммония можно посмотреть здесь.
Опыт № 6. Взаимодействие солей аммония со щелочами
Задания. 1. Изучите взаимодействие солей аммония с раствором щелочи.
2. Проведите качественную реакцию на соли аммония.
Оборудование. Штатив с пробирками, нагревательный прибор, держатель для пробирок.
Оборудование. Растворы гидроксида натрия (20% -й), хлорида бария (10% -й), хлорида аммония (20% -й), азотной кислоты (10%-й), фиолетовая лакмусовая бумажка; кристаллический сульфат аммония, вода (в стакане).
1. Налейте в пробирку 2 мл раствора хлорида аммония и столько же раствора гидроксида натрия. Что вы наблюдаете? Нагрейте эту смесь до начала кипения, соблюдая правила техники безопасности. Поднесите смоченную водой фиолетовую лакмусовую бумажку к отверстию пробирки. Почему изменился цвет индикатора? Определите по запаху выделяющийся газ. Составьте уравнение реакции.
2. Опытным путем докажите, что выданное вам вещество является сульфатом аммония. Составьте соответствующие уравнения реакций.
Сделайте вывод, для каких целей в лабораторной практике могут быть использованы реакции солей аммония со щелочами.
Выпадает белый осадок.
Ион аммония определяется аналогично предыдущему опыту.
Выделяющийся газ имеет резкий характерный запах, а также изменяет окраску лакмуса.
Вывод: реакции солей аммония со щелочами могут быть использованы в лаборатории для получения аммиака.
задача №6
к главе «Лабораторные работы и опыты».
Реакция образования солей аммония
Соли аммония — что это такое
Соли аммония являются солями, в состав которых входит катион аммония и анион кислотного остатка.
Соли аммония относятся к сложным веществам. Ион аммония образуется при взаимодействии аммиака с катионом водорода по донорно-акцепторному механизму. Соединения сформированы катионом аммония ( N H 4 ) + и кислотным остатком:
- хлорид аммония N H 4 C l ;
- сульфат аммония ( N H 4 ) 2 S O 4 ;
- нитрат аммония N H 4 N O 3 .
Свойства нелетучих солей аммония схожи со свойствами солей натрия или калия. Соединения характеризуются ионным строением и имеют вид белых кристаллов. Соли аммония обладают хорошей растворимостью в водной среде. Кристаллическая решетка с атомами хлорида аммония изображена на схеме:
Химические и физические свойства
Общие физические свойства солей аммония:
- твердые вещества;
- кристаллическая структура;
- хорошая растворимость в воде;
- отсутствие цвета.
Соли аммония являются сильными электролитами, которые диссоциируют в водных растворах:
N H 4 C l → N H 4 + + C l —
Разложение солей аммония при нагревании в случае летучей кислоты:
N H 4 C l → N H 3 + H C l
N H 4 H C O 3 → N H 3 + H 2 O + C O 2
Разложение солей аммония в условиях термического воздействия, если анион проявляет окислительные свойства:
N H 4 N O 3 → N 2 O + 2 H 2 O
( N H 4 ) 2 C r 2 O 7 → N 2 + C r 2 O 3 + 4 H 2 O
Соли аммония способны вступать в реакции обмена с кислотами:
( N H 4 ) 2 C O 3 + 2 H C l → 2 N H 4 C l + H 2 O + C O 2
Реакции обмена солей аммония с солями:
( N H 4 ) 2 S O 4 + B a C l 2 → B a S O 4 + 2 N H 4 C l
Соли аммония вступают в химические реакции гидролиза (как соль слабого основания и сильной кислоты):
N H 4 C l + H 2 O → N H 4 O H + H C l
Качественная реакция, как реагирует со щелочами
Качественную реакцию на ион аммония можно наблюдать в процессе нагрева солей аммония со щелочами, что приводит к выделению аммиака:
N H 4 C l + N a O H → N a C l + N H 3 + H 2 O
Признаком реакции является выделение газа с резким запахом.
Соли аммония обладают свойствами классических растворимых солей, то есть могут вступать в реакции обмена при образовании газа, осадка, слабого электролита с такими веществами, как:
- щелочи;
- кислоты;
- растворимые соли.
Реакция
Качественная реакция на аммиак: к отверстию сосуда, содержащего аммиак нужно поднести стеклянную палочку, смоченную в концентрированной соляной кислоте, в результате реакции появляется густой белый дым: это выделился хлорид аммония.
N H 3 + H C l = N H 4 C l
Способы получения солей аммония, где применяются
Распространенным методом синтеза солей аммония является химическое взаимодействие аммиака или гидроксида аммония и кислот.
Получают соли аммония при взаимодействии аммиака или гидроксида аммония с кислотами:
2 N H 3 + H 2 S O 4 → ( N H 4 ) 2 S O 4
Химический процесс, при котором аммиак взаимодействует с хлором, приводит к образованию нашатыря:
8 N H 3 + 3 C l 2 → N 2 + 6 N H 4 C l
Области применения солей аммония:
- Нитрат аммония называют аммиачной селитрой. Формула N H 4 N O 3 . Вещество используют в качестве азотного удобрения, как сырье в производстве взрывчатки в виде аммонитов.
- Сульфат аммония. Формула ( N H 4 ) 2 S O 4 . Соль является недорогим азотным удобрением.
- Гидрокарбонат аммония N H 4 H C O 3 и карбонат аммония ( N H 4 ) 2 C O 3 . Вещества выполняют роль разрыхлителей теста — компонентов мучных кондитерских изделий. Данные соли аммония применяют в процессе окрашивания тканых полотен. Соединения используют для производства витаминов и в медицинской отрасли.
- Хлорид аммония носит название нашатырь. Формула N H 4 C l . Данный материал используют при изготовлении гальванических компонентов, то есть сухих батарей. Вещества участвуют в процессе пайки и лужения. Хлорид аммония нашел применение в текстильной промышленности. Такие соединения являются эффективными удобрениями, активно используются в области ветеринарии и медицине.