Получение коллоидного раствора это процесс в результате которого образуются коллоидные частички которые и составляют этот раствор в растворителе.
Укрупнение этих частит приводит к слипанию вещества, в результате чего вещество переходит в осадок,примером служит коллоидное золото.
- Что такое получение коллоидных растворов
- Конденсационные методы получения коллоидных растворов
- Способы получения коллоидный растворов
- Примеры образования коллоидных растворов
- Дисперсные системы
- Как устроена мицелла
- Свойства коллоидных систем
- Как разрушить коллоидные растворы
- Что вызывает коагуляцию
- Кто открыл коллоидные растворы
- Майкл Фарадей
- Томас Грэм
- Похожие страницы:
- Leave a Comment
- Строение коллоидных частиц
- Уравнение реакции в результате которого возможно образование коллоидного раствора имеет вид
Что такое получение коллоидных растворов
Коллоидные растворы могут быть получены различными методами.
Некоторые вещества, обладающие сложным составом и большими молекулами, как, например, белок, желатина, гуммиарабик, образуют коллоидные растворы уже при длительном соприкосновении с водой.
Другие можно превратить в коллоидное состояние путем растирания с жидкостью. Грубые частицы можно также измельчать до коллоидных размеров в так называемых коллоидных мельницах.
Эти мельницы широко применяются на практике при изготовлении различных красок, наполнителей для бумаги и резины, в фармацевтической промышленности, в пищевой промышленности и т. д.
Раздробление веществ на коллоидных мельницах может быть доведено до частиц с диаметром, равным всего только 0,01
Указанные методы основаны на превращении крупных частиц в более мелкие и потому получили название дисперсионных методов.
Но можно идти и противоположным путем, создавая условия, при которых простые молекулы соединяются в более крупные агрегаты, не переходящие, однако, известного предела.
Конденсационные методы получения коллоидных растворов
В основе их лежат химические реакции, протекающие в водных растворах.
Соответственно регулируя условия реакций, во многих случаях, можно добиться, чтобы образующееся при реакции нерастворимое вещество выделялось в виде коллоидных частиц того или иного размера, и таким образом получить коллоидный раствор.
Так, например, описанный выше коллоидный раствор золота легко получить восстановлением хлорного золота формалином.
Способы получения коллоидный растворов

Нагрев раствор до кипения, вольем в него 2—3 мл очень слабого раствора формалина.
Жидкость приобретает красивый пурпурный цвет вследствие выделения коллоидных частиц золота:
Конечно, золото выделяется в этом случае сначала в виде отдельных атомов, которые, однако, сейчас же связываются в более крупные агрегаты.
Примеры образования коллоидных растворов
Приведем еще примеры образования коллоидных растворов при химических реакциях.
1. Нагреем в стакане до кипения некоторое количество де-стиллированной воды и будем прибавлять к ней по каплям раствор хлорного железа FeCl3.
Вследствие гидролиза большая часть хлорного железа превращается в гидрат окиси железа:
Одновременно получается некоторое количество основной соли FeOCl.
Хотя гидрат окиси железа нерастворим в воде, но при этих условиях он не выпадает в осадок, а остается в растворе в виде мельчайших частиц.
Получается прозрачный золь Fe(OH)3, имеющий окраску крепкого чая.
2. В раствор мышьяковистой кислоты будем пропускать некоторое время сероводород:
Получается прозрачный золотисто-желтый золь сульфида мышьяка.
3. К конденсационным методам должен быть отнесен и метод получения металлов при помощи электрической дуги.
Изучение этого явления показало, что при проскакивании искры металл непосредственно превращается в пар, состоящий из отдельных атомов; образование же коллоидных частиц металла происходит уже в результате конденсации пара.
Дисперсные системы
Дисперсные системы – гетерогенные системы, в которых одно вещество (дисперсная фаза) равномерно распределено в другом (дисперсионная среда).
Свойства вещества в раздробленном (дисперсном) состоянии значительно отличаются от свойств того же вещества, находящегося в виде твердого тела или некоторого объема жидкости.
Существует несколько различных классификаций дисперсных частиц: по размеру частиц, по агрегатному состоянию дисперсной фазы и дисперсионной среды,.
По характеру взаимодействия частиц дисперсной фазы с молекулами дисперсионной среды, по термодинамической и кинетической устойчивости.
Как устроена мицелла
Коллоидная частица представляет собой ядро из малорастворимого вещества коллоидной дисперсности, на поверхности которого адсорбируются ионы электролита раствора.
Ионы электролита обеспечивают устойчивость золя, поэтому данный электролит называют ионным стабилизатором. Значит, коллоидная частица представляет собой комплекс, состоящий из ядра, вместе с адсорбционным слоем противоионов.
Рис. 2. Структура мицеллы As2S3
Агрегат частицы или ядро представляет собой вещество кристаллического строения, состоящий из сотен или тысячи атомов, ионов или молекул, окружённый ионами. Ядро вместе с адсорбированными ионами называется гранулой.
Так гранула имеет определённый заряд. Вокруг неё собираются противоположно заряженные ионы, придающие ей в целом электронейтральность. Вся система, состоящая из гранулы и окружающих её ионов называется мицеллой и является электронейтральной.
Свойства коллоидных систем
Это свойство рассеивание света (опалесценция) (указывает на неоднородность, многофазность системы).
Опалесценция становится особенно заметной, если, как это делал Тиндаль (через коллоидный раствор пропускать пучок сходящихся лучей, поставив между источником света и кюветой с раствором линзу.
При этом растворы, прозрачные в проходящем свете, в боковом освещении проявляют все свойства мутных сред. В коллоидной жидкости, наблюдаемой сбоку, образуется яркий светящийся конус (конус Тиндаля).
Как разрушить коллоидные растворы
Процесс укрупнения коллоидных частиц, приводящий к уменьшению степени дисперсности диспергированного вещества, называется коагуляцией.
Примером может служить реакция восстановления золота из его раствора, сначала образуется коллоидный раствор золота, а затем раствор укрупняется и выпадает в осадок.
Коагуляция, или слипание частиц, приводит к осаждению (седиментации) крупных агрегатов в виде осадка.
Что вызывает коагуляцию
Снижение устойчивости коллоидных систем вызывают введением электролитов, которые изменяют структуру диффузного слоя ионов.
Причем коагулирующим действием в электролите обладают только те ионы, (коагуляторы), которые несут заряд, по закону одноименной с зарядом противоиона коллоидной частицы.
Коагулирующее действие иона коагулятора тем больше, чем больше его заряд.
Коагуляция – самопроизвольный процесс, возникающий из-за стремления системы перейти в состояние с более низкой поверхностной энергией и более низким значением изобарного потенциала.
Процесс седиментации скоагулированного вещества также протекает самопроизвольно. Коагуляция может быть обусловлена различными причинами, наиболее эффективно действие электролитов.
Минимальная концентрация электролита в растворе, вызывающая коагуляцию, называется порогом коагуляции. Коагуляция также возникает при смещении двух золей с различными знаками зарядов частиц. Это явление называется взаимной коагуляцией.
Кто открыл коллоидные растворы
Обычно считают, что основателем коллоидной химии является английский ученый Томас Грэм(1805-1869), который в 50-60-е годы позапрошлого столетия ввел в обращение основные коллоидно-химические понятия.
Однако не следует забывать, что у него имелись предшественники, и прежде всего – Яков Берцелиус, итальянский химик Франческо Сельми. В 30-е годы XIX века Берцелиус описал ряд осадков, проходящих при промывании через фильтр (кремниевая и ванадиевая кислоты, хлористое серебро, берлинская лазурь и др.).
Эти проходящие через фильтр осадки Берцелиус назвал «растворами», но в то же время он указал на их близкое сродство с эмульсиями и суспензиями, со свойствами которых он был хорошо знаком.
Франческо Сельми в 50-е годы XIX века продолжил работы в этом направлении, ища физико-химические различия между системами, образованными осадками, проходящими через фильтр (он назвал их «псевдорастворами») и обычными истинными растворами.
Майкл Фарадей
Английский ученый Майкл Фарадей в 1857 г. синтезировал коллоидные растворы золота – взвесь Au в воде размерами частиц от 1 до 10 нм. и разработал методы их стабилизации.
Эти «псевдорастворы» рассеивают свет, растворенные в них вещества выпадают в осадок при добавлении небольших количеств солей, переход вещества в раствор и осаждение из него не сопровождаются изменением температуры и объема системы, что обычно наблюдается при растворении кристаллических веществ.
Томас Грэм
Томас Грэм развил эти представления о различии между «псевдорастворами» и истинными растворами и ввел понятие «коллоид».
Грэм обнаружил, что вещества, способные к образованию студнеобразных аморфных осадков, такие как гидроокись алюминия, альбумин, желатина, диффундируют в воде с малой скоростью по сравнению с кристаллическими веществами (NaCl, сахароза).
В то же время кристаллические вещества легко проходят в растворе через пергаментные оболочки («диализируют»), а студнеобразные вещества не проходят через эти оболочки.
Принимая клей за типичный представитель студнеобразных не диффундирующих и не диализирующих веществ, Грэм дал им общее название «коллоид», т.е. клееобразный (от греческого слова колла – клей).
Кристаллические вещества и вещества, хороши диффундирующие и диализирующие он назвал «кристаллоидами».
Статья на тему Получение коллоидных растворов
Похожие страницы:
Понравилась статья поделись ей
Leave a Comment
Для отправки комментария вам необходимо авторизоваться.
Строение коллоидных частиц
Строение коллоидных частиц может быть изображено лишь схематически, т.к. они не имеет определенного состава. Рассмотрим образование золя и строение его частиц на примере иодида свинца PbI2.
Уравнение реакции имеет вид:
Образование золя возможно, если к раствору Pb(NO3)2 постепенно прибавлять раствор KI или если к раствору KI постепенно прибавлять раствор Pb(NO3)2. При этом строение коллоидных частиц будет отличаться.
1. Предположим, что золь PbI2 образуется при постепенном прибавлении раствора KI к раствору Pb(NO3)2.
Вначале образуется агрегат (PbI2)mиз ионов Pb 2+ и I — .
Далее на поверхности агрегата адсорбируются ионы, входящие в его состав и находящиеся в растворе в избытке. В нашем примере это ионы свинца.
В результате этого, агрегат (PbI2)m с адсорбированным слоем Pb 2+ приобретает положительный заряд. Адсорбированные на поверхности агрегата ионы и придающие ему заряд, называются потенциалопределяющими. А сам агрегат (PbI2)m с потенциалопределяющими ионами Pb 2+ , образуют ядро.
Далее, к ядру притягиваются противоположно заряженные ионы – противоионы, которые компенсируют заряд твердой фазы и образуют адсорбционный слой. Противоионами будут служить, ионы содержащиеся в растворе, но не входящие в состав агрегата. В данном примере – это нитрат-ионы NO 3– .
Ядро и противоионы адсорбционного слоя образуют коллоидную частицу или гранулу, знак которой определяется знаком заряда потенциалопределяющих ионов.
Те же противоионы (NO 3– ), образуют и диффузный слой. По мере удаления от ядра, их содержание постепенно снижается.
Коллоидная частица вместе с противоионами диффузного слоя называется мицеллой.
Мицела в целом электронейтральна и не имеет строго определенных размеров.
Агрегат сравнительно прочно удерживает (связывает) противоионы адсорбционного слоя, а противоионы диффузного слоя испытывают действие электростатического притяжения разноименно заряженных ионов, удерживающее их вблизи ядра, и броуновского движения, стремящегося распределить их в дисперсионной среде.
Формула мицеллы йодида свинца выглядит следующим образом:
2. Если же постепенно прибавлять раствор Pb(NO3)2 к раствору KI, то строение мицелы будет иным.
В этом случае, в избытке будут йодид-ионы, которые и будут адсорбироваться на поверхности агрегата (PbI2)m, образуя слой потенциалопределяющих ионов. В качестве противоионов адсорбционного и диффузионного слоев будут выступать ионы калия. Строение мицеллы имеет следующий вид:
[(PbI2)m, nI–, (n – x)K + ] x– xK + .
Т.к. гранула мицелы и ее диффузный слой – это заряженные частицы, то под действием электрического поля, они будут перемещаться к соответствующим электродам.
Итак, обобщая вышесказанное, приведем порядок написания формулы мицелы:
1) Ядро мицелы. Малорастворимое соединение, образуемое в результате реакции, составляет агрегат. Агрегат записывают в круглых скобках с индексом m.
2) Потенциалопределяющие ионы. Ионы, адсорбированные на поверхности агрегата и входящие в его состав, а также придающие ему заряд, находятся в растворе в избытке. Перед потенциалопределяющим ионом ставят коэффициент n.
3) Противоионы адсорбционного слоя. Ионы раствора, взятого в избытке, но не входящие в состав агрегата образуют адсорбционный слой и компенсируют заряд твердой фазы. Перед противоионом адсорбционного слоя ставят коэффициент (n-x), умноженный на численное значение заряда потенциалопределяющего иона.
Ядро и адсорбционный слой мицелы, образующие гранулу, заключают в квадратные скобки и указывают заряд гранулы — x+ или x-, умноженные на численное значение заряда потенциалопределяющего иона.
4) Противоионы диффузного слоя. Часть противоионов, находящиеся во внешней сфере мицелы, удаленной от ее ядра. Перед противоионом диффузного слоя ставят коэффициент x, умноженный на численное значение заряда потенциалопределяющего иона. Противоионы диффузного слоя записывают за квадратными скобками.
Уравнение реакции в результате которого возможно образование коллоидного раствора имеет вид
Фенол в отличие от этанола реагирует с раствором …
Для уменьшения в 32 раза скорости реакции, температурный коэффициент которой равен 2, необходимо понизить температуру на …
Уравнения реакций, в результате которых происходит образование коллоидных растворов методом химической конденсации, имеют вид …
Системами, для которых математическое выражение закона действующих масс имеет вид 
Уравнения реакций, в результате которых возможно образование коллоидных систем, имеют вид …
При электролизе водного раствора, содержащего нитраты ртути (II), меди (II), никеля (II) и калия в стандартных условиях, последовательность выделения веществ на катоде имеет вид …
Уравнения реакций, в результате которых возможно образование коллоидных растворов, имеют вид …
Для физической адсорбции характерна(о) …
Энтальпия образования 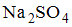
Уравнение Pосм = CRT, характеризующее зависимость осмотического давления от концентрации раствора неэлектролита и температуры, называется законом …

