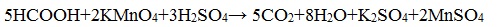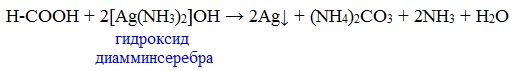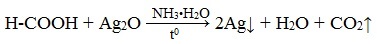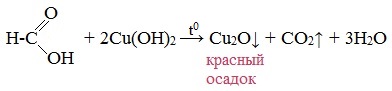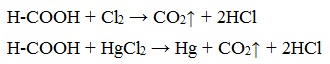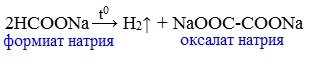Средняя оценка: 4.2
Всего получено оценок: 554.
Средняя оценка: 4.2
Всего получено оценок: 554.
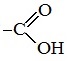
Этановая или уксусная кислота – это слабая карбоновая кислота, которая широко применяется в промышленности. Химические свойства уксусной кислоты определяет карбоксильная группа COOH.
- Физические свойства
- Получение
- Химические свойства
- Acetyl
- Уравнение реакции уксусной кислоты с водородом
- I. Реакции с разрывом связи О-Н
- Свойства солей карбоновых кислот
- II. Реакции с разрывом связи C-О
- III. Реакции с разрывом связи C-Н у ɑ-углеродного атома
- V.Реакции каталитического восстановления
- Особенности строения и свойства муравьиной кислоты
- 🔥 Видео
Видео:Взаимодействие уксусной кислоты с металламиСкачать

Физические свойства
Уксусная кислота (CH3COOH) – это концентрированный уксус, знакомый человечеству с давних времён. Его изготовляли путём брожения вина, т.е. углеводов и спиртов.
По физическим свойствам уксусная кислота – бесцветная жидкость с кислым вкусом и резким запахом. Попадание жидкости на слизистые оболочки вызывает химический ожог. Уксусная кислота обладает гигроскопичностью, т.е. способна поглощать водяные пары. Хорошо растворима в воде.
Основные физические свойства уксуса:
- температура плавления – 16,75°C;
- плотность – 1,0492 г/см 3 ;
- температура кипения – 118,1°C;
- молярная масса – 60,05 г/моль;
- теплота сгорания – 876,1 кДж/моль.
В уксусе растворяются неорганические вещества и газы, например, бескислородные кислоты – HF, HCl, HBr.
Видео:Лабораторная работа №16. Свойства уксусной кислоты. 9 класс.Скачать

Получение
Способы получения уксусной кислоты:
- из ацетальдегида путём окисления атмосферным кислородом в присутствии катализатора Mn(CH3COO)2 и высокой температуре (50-60°С) – 2CH3CHO + O2 → 2CH3COOH;
- из метанола и угарного газа в присутствии катализаторов (Rh или Ir) – CH3OH + CO → CH3COOH;
- из н-бутана путём окисления в присутствии катализатора при давлении 50 атм и температуре 200°C – 2CH3CH2CH2CH3 + 5O2 → 4CH3COOH + 2H2O.

Уравнение брожения выглядит следующим образом – СН3СН2ОН + О2 → СН3СООН + Н2О. В качестве сырья используется сок или вино, кислород и ферменты бактерий или дрожжей.
Видео:Химический видео Опыт Сода+ Уксус. Уравнение реакций. Простой опыт по ХИМИИ.Скачать

Химические свойства
Уксусная кислота проявляет слабые кислотные свойства. Основные реакции уксусной кислоты с различными веществами описаны в таблице.
Видео:Получение водорода и проверка его на чистотуСкачать

Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
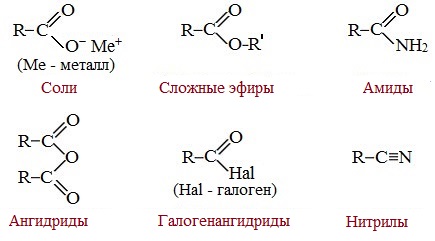
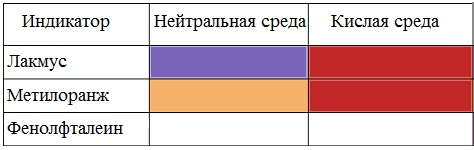
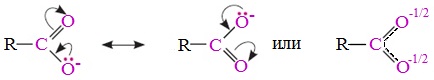
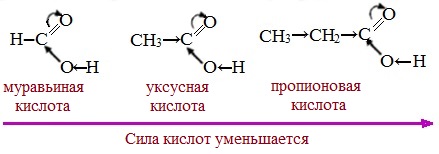
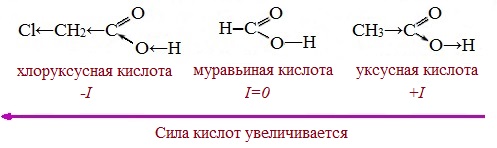
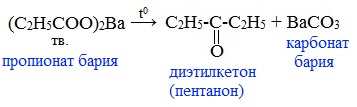
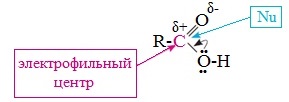
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Видео:Водород/химические свойства водорода/8 классСкачать  Уравнение реакции уксусной кислоты с водородомДля насыщенных монокарбоновых кислот характерна высокая реакционная способность. Она определяется в основном наличием в их структуре карбоксильной группы. Карбоксильная группа представляет собой сопряженную систему, в которой неподеленная пара электронов атома кислорода гидроксильной группы вступает в сопряжение с π-электронами карбонильной группы (р,π-сопряжение). Вследствие +М-эффекта со стороны группы –ОН электронная плотность в сопряженной системе смещена в сторону атома кислорода карбонильной группы Но в то же время за счет +М-эффекта со стороны группы –ОН в молекулах карбоновых кислот в некоторой степени уменьшается частичный положительный заряд (δ+) на атоме углерода карбонильной группы по сравнению с альдегидами и кетонами. Кроме того, вследствие –I-эффекта карбоксильной группы в молекуле карбоновой кислоты происходит смещение электронной плотности с углеводородного остатка, что приводит к появлению СН-кислотного центра у α-углеродного атома. Исходя из строения, в молекулах карбоновых кислот можно выделить реакционные центры, определяющие возможные реакции с их участием. 1. Кислотные свойства кабоновых кислот проявляются в реакциях с основаниями за счет ОН-кислотного центра. 2. С участием электрофильного центра (атома углерода карбоксильной группы) происходят реакции нуклеофильного замещения в карбоновых кислотах и их функциональных производных. 3. Основный центр – карбонильная группа (оксогруппа) со своей электронной парой – протонируется на стадии катализа в реакциях нуклеофильного замещения. 4. СН-кислотный центр определяет возможность замещения атома водорода в алкильном радикале и реакции конденсации. Карбоновые кислоты вступают в реакции с различными веществами и образуют разнообразные соединения, среди которых большое значение имеют функциональные производные, т.е. соединения, полученные в результате реакций по карбоксильной группе. I. Реакции с разрывом связи О-Н(кислотные свойства карбоновых кислот обусловлены подвижностью атома водорода карбоксильной группы и их способностью отщеплять его в виде протона) Предельные монокарбоновые кислоты обладают всеми свойствами обычных кислот. Карбоновые кислоты изменяют окраску индикаторов. 1. Диссоциация В водных растворах монокарбоновые кислоты ведут себя как одноосновные кислоты: они диссоциируют с образованием протона (Н + ) и кислотного остатка (карбоксилат-иона): Уравнение реакции, учитывающее участие молекулы воды: Растворы карбоновых кислот изменяют окраску индикаторов, имеют кислый вкус, проводят электрический ток. В карбоксилат-ионе оба атома кислорода равноценны, а отрицательный заряд равномерно делокализован (рассредоточен) между ними. В результате делокализации отрицательного заряда карбоксилат-ион обладает высокой устойчивостью. Сила кислоты определяется устойчивостью образующегося аниона, поэтому карбоновые кислоты превосходят по кислотным свойствам спирты и фенолы, где возможность делокализации заряда в анионе меньшая. Тем не менее, монокарбоновые кислоты являются слабыми кислотами. Наиболее сильной в гомологическом ряду насыщенных кислот является муравьиная кислота, в которой группа –СООН связана с атомом водорода. Заместители, присутствующие в молекуле карбоновой кислоты, сильно влияют на ее кислотность вследствие оказываемого ими индукционного эффекта. Алкильные радикалы, связанные с карбоксильной группой, обладают положительным индукционным эффектом (+І). Они отталкивают от себя электронную плотность, тем самым уменьшая частичный положительный заряд (δ+) на атоме углерода карбоксильной группы. Положительный индукционный эффект возрастает по мере увеличения длины углеводородного радикала, что в свою очередь ослабляет полярность связи О-Н. Алкильные группы понижают кислотность. В гомологическом ряду предельных монокарбоновых кислот кислотные свойства уменьшаются от муравьиной кислоты к высшим карбоновым кислотам. Такие заместители, как хлор или фенильный радикал, оттягивают на себя электронную плотность и, следовательно, вызывают отрицательный индукционный эффект (— I). Оттягивание электронной плотности от карбоксильного атома водорода приводит к повышению кислотности карбоновой кислоты. Карбоновые кислоты – слабые электролиты. Равновесие процесса диссоциации сильно смещено влево, об этом свидетельствует тот факт, что даже сильноразбавленные водные растворы кислот имеют резкий запах. Видеоопыт «Растворимость в воде различных карбоновых кислот» Видеоопыт «Карбоновые кислоты — слабые электролиты» 2. Образование солей Карбоновые кислоты проявляют все свойства минеральных кислот. Карбоновые кислоты при взаимодействии с активными металлами, основными оксидами, основаниями и солями слабых кислот образую соли. а) взаимодействие с активными металлами Цинк и уксусная кислота
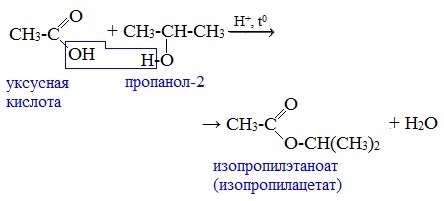
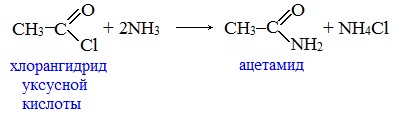
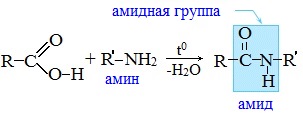
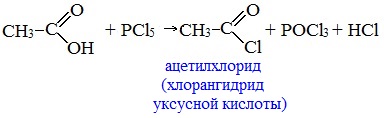
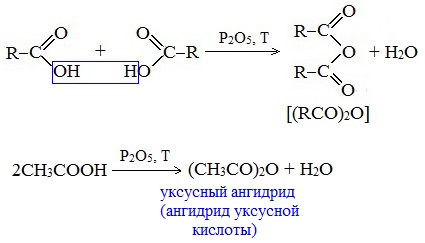
Видеоопыт «Взаимодействие уксусной кислоты с металлами» б) взаимодействие c основаниями (реакция нейтрализации) Видеоопыт «Взаимодействие уксусной кислоты с раствором щелочи» в) взаимодействие с основными и амофтерными оксидами Оксид меди(II) и уксусная кислота Видеоопыт «Взаимодействие уксусной кислоты с оксидом меди (II)» г) взаимодействие с солями более слабых кислот Видеоопыт «Взаимодействие уксусной кислоты с карбонатом натрия» д) взаимодействие с аммиаком или гидроксидом аммония Названия солей составляют из названий остатка RCOO– (карбоксилат-иона) и металла. Например, CH3COONa – ацетат натрия, (HCOO)2Ca – формиат кальция, C17H35COOK – стеарат калия и т.п. Отличие карбоновых кислот от минеральных заключается в возможности образования ряда функциональных производных. Видеоопыт «Свойства карбоновых кислот» Свойства солей карбоновых кислот1) Взаимодействие с сильными кислотами Карбоновые кислоты – слабые, поэтому сильные минеральные кислоты вытесняют их из соответствующих солей. Из неорганических кислот лишь угольная кислота слабее рассматриваемых кислот и может вытесняться ими из её солей — карбонатов и гидрокарбонатов. Качественная реакция на ацетат-ион СН3СОО — ! Запах уксусной кислоты. 2) Гидролиз по аниону Натриевыс и калиевые соли карбоновых кислот в водных растворах находятся частично в гидролизованном состояния. Этим объясняется щелочная реакция мыльного раствора. Видеоопыт «Гидролиз ацетата натрия» 3) Электролиз солей активных металлов (реакция Кольбе) Одним из применений солей карбоновых кислот является электролиз их водных растворов, в результате которого образуются насыщенные углеводороды: Электролизом раствора соли карбоновой кислоты можно получить алкан с удлиненной цепью. 4) Пиролиз солей карбоновых кислот При пиролизе (термическое разложение) кальциевых, бариевых солей карбоновых кислот образуются соответствующие карбонильные соединения. Из смешанной соли муравьиной и другой карбоновой кислоты получают альдегиды, а в остальных случаях образуются кетоны: 4) Декарбоксилирование солей щелочных металлов (реакция Дюма) В процессе сплавления солей карбоновых кислот с твердой щелочью происходит расщепление углеродной связи и образуются алканы с числом атомов углерода на один меньше, чем у исходной кислоты: II. Реакции с разрывом связи C-ОПониженная электронная плотность (δ+) на атоме углерода в карбоксильной группе обусловливает возможность реакций нуклеофильного замещения группы –ОН с образованием функциональных производных карбоновых кислот (сложных эфиров, амидов, ангидридов и галогенангидридов). 1. Взаимодействие со спиртами с образованием сложных эфиров (реакция этерификации) Карбоновые кислоты при нагревании в присутствии кислотного катализатора реагируют со спиртами, образуя сложные эфиры: Механизм этой реакции был установлен методом меченых атомов. С этой целью использовали спирт, меченный изотопом кислорода 18 О. После реакции изотоп кислорода был обнаружен в молекуле сложного эфира. 2. Взаимодействие с аммиаком с образованием амидов Амиды получают из карбоновых кислот и аммиака через стадию образования аммониевой соли, которую затем нагревают: Вместо карбоновых кислот чаще используют их галогенангидриды: Амиды образуются также при взаимодействии карбоновых кислот (их галогенангидридов или ангидридов) с органическими производными аммиака (аминами): Амиды играют важную роль в природе. Молекулы природных пептидов и белков построены из α-аминокислот с участием амидных групп — пептидных связей. 3. Взаимодействие с галогенидами фосфора или тионилхлоридом с образованием галогенангидридов карбоновых кислот Наибольшее значение имеют хлорангидриды. Хлорирующие реагенты –галогениды фосфора PCl3, PCl5, тионилхлорид SOCl2. Для получения хлорангидридов чаще используют тионилхлорид, так как в этом случае образуются газообразные побочные продукты. Галогенангидриды карбоновых кислот — весьма реакционноспособные вещества, широко применяемые в органическом синтезе. 4. Образование ангидридов кислот (межмолекулярная дегидратация) Ангидриды кислот образуются в результате межмолекулярной дегидратации кислот при их нагревании в присутствии оксида фосфора (V) в качестве водоотнимающего средства.
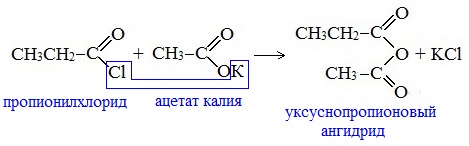
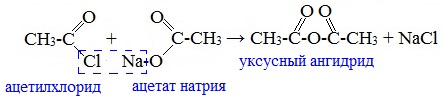
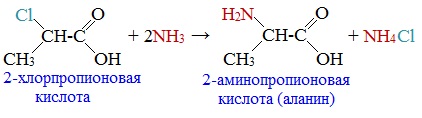
Смешанные ангидриды карбоновых кислот можно получить при взаимодействии хлорангидрида одной кислоты с безводной солью другой карбоновой кислоты: Муравьиная кислота не образует ангидрида. Дегидратация ее приводит к образованию оксида углерода (II). Наиболее широкое применение находит уксусный ангидрид. Большое количество его расходуется для синтеза ацетилцеллюлозы, которая идет на изготовление искусственного шелка. Уксусный ангидрид используется также для получения аспирина. III. Реакции с разрывом связи C-Н у ɑ-углеродного атома(реакции с участием радикала) 1. Реакции замещения (с галогенами) Атомы водорода у ɑ-углеродного атома более подвижны, чем другие атомы водорода в радикале кислоты и могут замещаться на атомы галогена с образование ɑ-галогенкарбоновых кислот. Карбоновые кислоты взаимодействуют с галогенами в присутствии красного фосфора (реакция Геля-Фольгарда-Зелинского): 2-Хлорпропионовая кислота – промежуточный продукт для получения аминокислот. Действием на 2-хлорпропионовую кислоту аммиака получают 2-аминопропионовую кислоту (аланин):
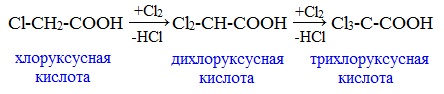
Дальнейшее хлорирование приводит к образованию дихлоруксусной и трихлоруксусной кислот:
В атмосфере кислорода карбоновые кислоты сгорают с образованием оксида углерода (IV) СО2 и Н2О: Видеоопыт «Горение уксусной кислоты на воздухе» В отличие от альдегидов, карбоновые кислоты достаточно устойчивы к действию даже такого сильного окислителя, как перманганат калия. Исключение составляет муравьиная кислота, которая проявляет восстановительные свойства благодаря наличию альдегидной группы. V. Реакции каталитического восстановленияКарбоновые кислоты с трудом восстанавливаются каталитическим гид-рированием, однако при взаимодействии с алюмогидридом лития (LiAlH4) или дибораном (В2Н6) восстановление осуществляется достаточно энергично: Особенности строения и свойства муравьиной кислоты
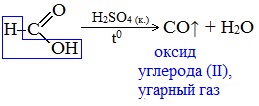
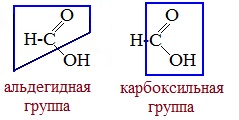
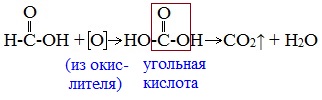
В отличие от других карбоновых кислот в молекуле муравьиной кислоты функциональная карбоксильная группа связана не с углеводородным радикалом, а с атомом водорода. Поэтому муравьиная кислота является более сильной кислотой по сравнению с другими членами своего гомологического ряда. Все предельные карбоновые кислоты устойчивы к действия концентрированной серной и азотной кислот. Но муравьиная кислота при нагревании с концентрированной серной кислотой разлагается на воду и монооксид углерода (угарный газ). 1. Разложение при нагревании При нагревании с концентрированной H2SO4 муравьиная кислота разлагается на оксид углерода (II) и воду: Данную реакцию используют в лаборатории для получения чистого оксида углерода (II). Видеоопыт «Разложение муравьиной кислоты» Молекула муравьиной кислоты, в отличие от других карбоновых кислот, наряду с карбоксильной группой содержит в своей структуре и альдегидную группу. Поэтому муравьиная кислота вступает в реакции, характерные как для кислот, так и для альдегидов. Как и альдегиды, НСООН проявляет восстановительные свойства. Проявляя свойства альдегида, муравьиная кислота легко окисляется до угольной кислоты: 2. Окисление перманганатом калия Видеоопыт «Окисление муравьиной кислоты раствором перманганата калия» Муравьиная кислота окисляется аммиачным раствором Ag2О и гидроксидом меди (II) Cu (OH)2, т.е. дает качественные реакции на альдегидную группу! 3. Реакция «серебряного зеркала» или в упрощенном виде 4. Окисление гидроксидом меди (II) 5. Окисление хлором, хлоридом ртути Муравьиная кислота окисляется и другими окислителями (Сl2, HgCl2). Формиаты щелочных металлов при сплавлении образуют соли щавелевой кислоты — оксалаты: Видеоопыт «Взаимодействие бромной воды с олеиновой кислотой» 🔥 ВидеоВодород. 8 класс.Скачать  Реакция магния с уксусной кислотойСкачать  Эта СУПЕРКИСЛОТА Растворит Все что угодно!Скачать  КИСЛОТЫ В ХИМИИ — Химические Свойства Кислот. Реакция Кислот с Основаниями, Оксидами и МеталламиСкачать  Реакции металлов с кислородом и водой. 8 класс.Скачать  Взаимодействие уксусной кислоты с металламиСкачать  Качественная Реакция На Салициловую И Уксусную КислотуСкачать  Примеры решения задач на водородный показатель pH растворов. 11 класс.Скачать  Реакция магния и уксусной кислотыСкачать  Синтез УКСУСНОЙ КИСЛОТЫ. Реакция АЦЕТАТА КАЛИЯ и СЕРНОЙ КИСЛОТЫ. Опыты по химии. Получение УКСУСА.Скачать  Взаимодействие металлического магния с уксусной кислотойСкачать  Взаимодействие металлов с кислотами. 8 класс.Скачать  Свойства и применение водорода. 8 класс.Скачать  Химия 8 класс. Водород.Скачать  Реакция уксусной кислоты с карбонатом натрияСкачать  |

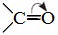 неподеленные пары электронов которого не участвуют в сопряжении. В результате смещения электронной плотности связь О-Н оказывается сильно поляризованной (по сравнению со спиртами и фенолами), что приводит к появлению в карбоксильной группе ОН-кислотного центра.
неподеленные пары электронов которого не участвуют в сопряжении. В результате смещения электронной плотности связь О-Н оказывается сильно поляризованной (по сравнению со спиртами и фенолами), что приводит к появлению в карбоксильной группе ОН-кислотного центра.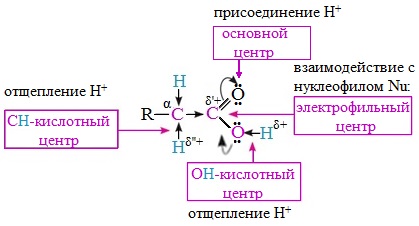
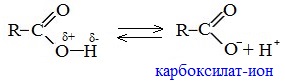
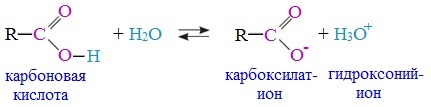
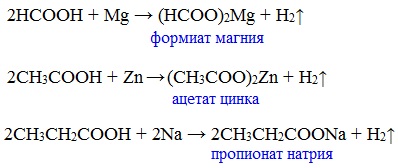

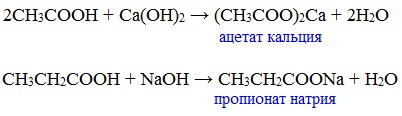
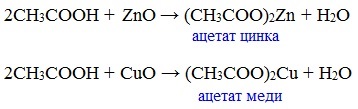

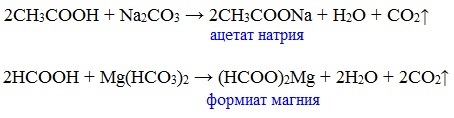

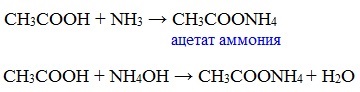
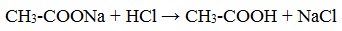
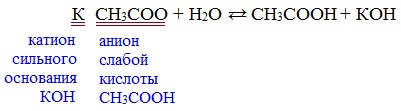
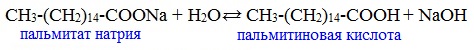

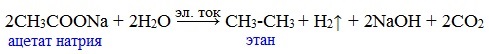
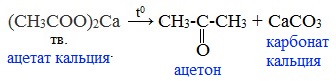
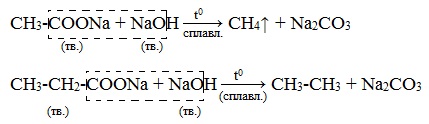
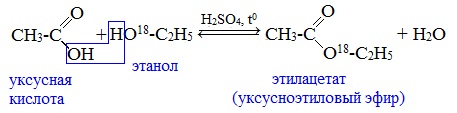
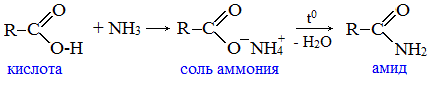

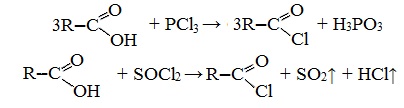

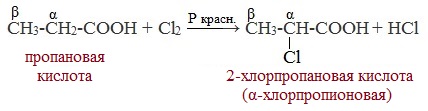
 При пропускании хлора через кипящую уксусную кислоту в присутствии красного фосфора образуется кристаллическое вещество – хлоруксусная кислота:
При пропускании хлора через кипящую уксусную кислоту в присутствии красного фосфора образуется кристаллическое вещество – хлоруксусная кислота: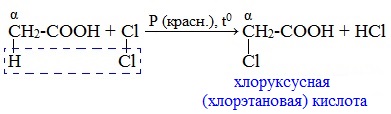
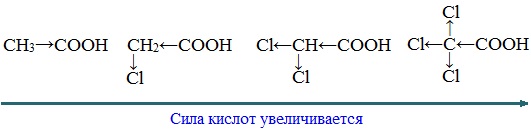
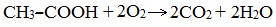
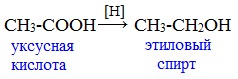
 Муравьиная (метановая) кислота НСООН по своему строению и свойствам отличается от остальных членов гомологического ряда предельных монокарбоновых кислот.
Муравьиная (метановая) кислота НСООН по своему строению и свойствам отличается от остальных членов гомологического ряда предельных монокарбоновых кислот.