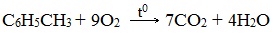Арены (ароматические углеводороды) – это непредельные (ненасыщенные) циклические углеводороды, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей.
Общая формула: CnH2n–6 при n ≥ 6.
- Химические свойства аренов
- 1. Реакции присоединения
- 1.1. Гидрирование
- 1.2. Хлорирование аренов
- 2. Реакции замещения
- 2.1. Галогенирование
- 2.2. Нитрование
- 2.3. Алкилирование ароматических углеводородов
- 2.4. Сульфирование ароматических углеводородов
- 3. Окисление аренов
- 3.1. Полное окисление – горение
- 3.2. О кисление гомологов бензола
- 4. Ориентирующее действие заместителей в бензольном кольце
- 5. Особенности свойств стирола
- Уравнение реакции толуола с этиленом
- Реакции замещения
- Реакции присоединения
- Реакции окисления
- Написать уравнение реакции взаимодействия толуола с этиленом в присутствии хлорида алюминия?
- Составьте уравнения реакций по описаниям, дайте характеристику уравнений реакций : а) натрий активно взаимодействует с хлором с образованием хлорида натрия ; б) гидроксид алюминия при нагревании разла?
- Хлороводород НЕ взаимодействует с : 1)пропином 2)этиленом 3)гидроксидом натрия 4)бензолом 5)толуолом 6)этаном?
- 3. Сокращенное ионное уравнение реакции : Al3 + + 3OH — → Al(OH)3↓ соответствует взаимодействию 1) хлорида алюминия с водой 2) алюминия с водой 3) хлорида алюминия со щелочью 4) алюминия со щелочью __?
- Написать уравнение реакции присоединения хлороводорода к этилену?
- Напишите уравнения реакций взаимодействия : алюминия с азотом?
- Составьте пожалуйста уравнение реакции хлорида магния и гидроксида алюминия?
- Тепловые эффекты образования хлоридов алюминия и меди соответственно равны 702?
- Напишите пожалуйста уравнение реакции : взаимодействие глюкозы с водородом в присутствии катализатора?
- Приведите уравнение реакции получения гидроксида алюминия из хлорида алюминия?
- Составить химическое уравнение реакции по цепочке превращений : алюминий гидроксид — алюминий оксид — алюминий сульфат — алюминий хлорид?
Химические свойства аренов
Арены – непредельные углеводороды, молекулы которых содержат три двойных связи и цикл. Но из-за эффекта сопряжения свойства аренов отличаются от свойств других непредельных углеводородов.
Для ароматических углеводородов характерны реакции:
- присоединения,
- замещения,
- окисления (для гомологов бензола).
| Из-за наличия сопряженной π-электронной системы молекулы ароматических углеводородов вступают в реакции присоединения очень тяжело, только в жестких условиях — на свету или при сильном нагревании, как правило, по радикальному механизму |
| Бензольное кольцо представляет из себя скопление π-электронов, которое притягивает электрофилы. Поэтому для ароматических углеводородов характерны реакции электрофильного замещения атома водорода у бензольного кольца. |
Ароматическая система бензола устойчива к действию окислителей. Однако гомологи бензола окисляются под действием перманганата калия и других окислителей.
1. Реакции присоединения
Бензол присоединяет хлор на свету и водород при нагревании в присутствии катализатора.
1.1. Гидрирование
Бензол присоединяет водород при нагревании и под давлением в присутствии металлических катализаторов (Ni, Pt и др.).
При гидрировании бензола образуется циклогексан:
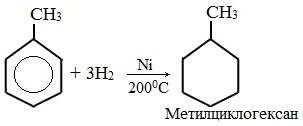
При гидрировании гомологов образуются производные циклоалканы. При нагревании толуола с водородом под давлением и в присутствии катализатора образуется метилциклогексан:
1.2. Хлорирование аренов
Присоединение хлора к бензолу протекает по радикальному механизму при высокой температуре, под действием ультрафиолетового излучения.
При хлорировании бензола на свету образуется 1,2,3,4,5,6-гексахлорциклогексан (гексахлоран).
Гексахлоран – пестицид, использовался для борьбы с вредными насекомыми. В настоящее время использование гексахлорана запрещено.
Гомологи бензола не присоединяют хлор. Если гомолог бензола реагирует с хлором или бромом на свету или при высокой температуре (300°C), то происходит замещение атомов водорода в боковом алкильном заместителе, а не в ароматическом кольце.
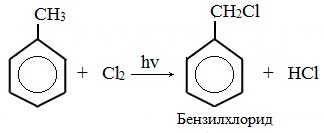
| Например, при хлорировании толуола на свету образуется бензилхлорид |
| Если у гомолога бензола боковая цепь содержит несколько атомов углерода – замещение происходит у атома, ближайшему к бензольному кольцу («альфа-положение»). |
| Например, этилбензол реагирует с хлором на свету |
2. Реакции замещения
| Реакции замещения у ароматических углеводородов протекают по ионному механизму (электрофильное замещение). При этом атом водорода замещается на другую группу (галоген, нитро, алкил и др.). |
2.1. Галогенирование
Бензол и его гомологи вступают в реакции замещения с галогенами (хлор, бром) в присутствии катализаторов (AlCl3, FeBr3).
При взаимодействии с хлором на катализаторе AlCl3 образуется хлорбензол:
Ароматические углеводороды взаимодействуют с бромом при нагревании и в присутствии катализатора – FeBr3 . Также в качестве катализатора можно использовать металлическое железо.
Бром реагирует с железом с образованием бромида железа (III), который катализирует процесс бромирования бензола:
| Гомологи бензола содержат алкильные заместители, которые обладают электронодонорным эффектом: из-за того, что электроотрицательность водорода меньше, чем углерода, электронная плотность связи С-Н смещена к углероду. На нём возникает избыток электронной плотности, который далее передается на бензольное кольцо. |
| Поэтому гомологи бензола легче вступают в реакции замещения в бензольном кольце. При этом гомологи бензола вступают в реакции замещения преимущественно в орто— и пара-положения |
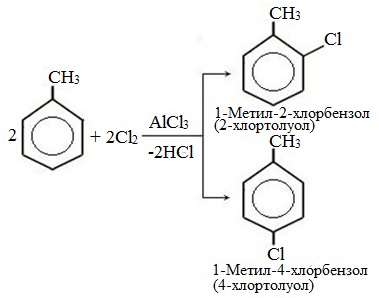
| Например, при взаимодействии толуола с хлором образуется смесь продуктов, которая преимущественно состоит из орто-хлортолуола и пара-хлортолуола |
Мета-хлортолуол образуется в незначительном количестве.
При взаимодействии гомологов бензола с галогенами на свету или при высокой температуре (300 о С) происходит замещение водорода не в бензольном кольце, а в боковом углеводородном радикале.
| Если у гомолога бензола боковая цепь содержит несколько атомов углерода – замещение происходит у атома, ближайшему к бензольному кольцу («альфа-положение»). |
Например, при хлорировании этилбензола:
2.2. Нитрование
Бензол реагирует с концентрированной азотной кислотой в присутствии концентрированной серной кислоты (нитрующая смесь).
При этом образуется нитробензол:
| Серная кислота способствует образованию электрофила NO2 + : |
Толуол реагирует с концентрированной азотной кислотой в присутствии концентрированной серной кислоты.
В продуктах реакции мы указываем либо о-нитротолуол:
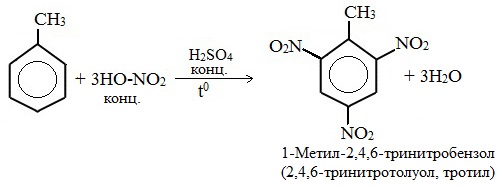
Нитрование толуола может протекать и с замещением трех атомов водорода. При этом образуется 2,4,6-тринитротолуол (тротил, тол):
2.3. Алкилирование ароматических углеводородов
- Арены взаимодействуют с галогеналканами в присутствии катализаторов (AlCl3, FeBr3 и др.) с образованием гомологов бензола.
| Например, бензол реагирует с хлорэтаном с образованием этилбензола |
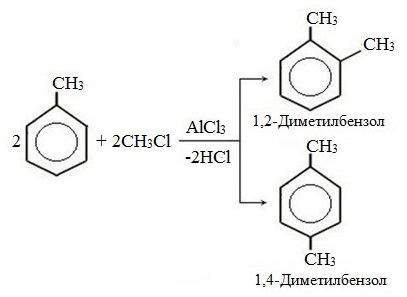
- Ароматические углеводороды взаимодействуют с алкенами в присутствии хлорида алюминия, бромида железа (III), фосфорной кислоты и др.
| Например, бензол реагирует с этиленом с образованием этилбензола |
| Например, бензол реагирует с пропиленом с образованием изопропилбензола (кумола) |
- Алкилирование спиртами протекает в присутствии концентрированной серной кислоты.
| Например, бензол реагирует с этанолом с образованием этилбензола и воды |
2.4. Сульфирование ароматических углеводородов
Бензол реагирует при нагревании с концентрированной серной кислотой или раствором SO3 в серной кислоте (олеум) с образованием бензолсульфокислоты:
3. Окисление аренов
Бензол устойчив к действию даже сильных окислителей. Но гомологи бензола окисляются под действием сильных окислителей. Бензол и его гомологи горят.
3.1. Полное окисление – горение
При горении бензола и его гомологов образуются углекислый газ и вода. Реакция горения аренов сопровождается выделением большого количества теплоты.
Уравнение сгорания аренов в общем виде:
При горении ароматических углеводородов в недостатке кислорода может образоваться угарный газ СО или сажа С.
Бензол и его гомологи горят на воздухе коптящим пламенем. Бензол и его гомологи образуют с воздухом и кислородом взрывоопасные смеси.
3.2. О кисление гомологов бензола
Гомологи бензола легко окисляются перманганатом и дихроматом калия в кислой или нейтральной среде при нагревании.
При этом происходит окисление всех связей у атома углерода, соседнего с бензольным кольцом, кроме связи этого атома углерода с бензольным кольцом.
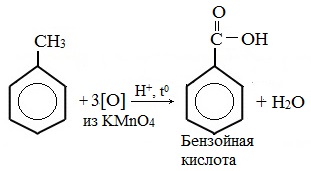
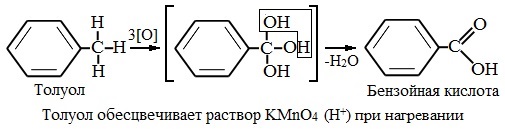
Толуол окисляется перманганатом калия в серной кислоте с образованием бензойной кислоты:
Если окисление толуола идёт в нейтральном растворе при нагревании, то образуется соль бензойной кислоты – бензоат калия:
Таким образом, толуол обесцвечивает подкисленный раствор перманганата калия при нагревании.
| При окислении других гомологов бензола всегда остаётся только один атом С в виде карбоксильной группы (одной или нескольких, если заместителей несколько), а все остальные атомы углерода радикала окисляются до углекислого газа или карбоновой кислоты. |
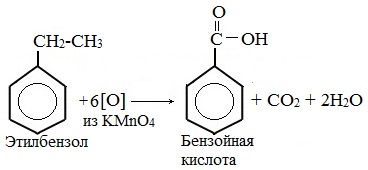
| Например, при окислении этилбензола перманганатом калия в серной кислоте образуются бензойная кислота и углекислый газ |
| Например, при окислении этилбензола перманганатом калия в нейтральной кислоте образуются соль бензойной кислоты и карбонат |
Более длинные радикалы окисляются до бензойной кислоты и карбоновой кислоты:
При окислении пропилбензола образуются бензойная и уксусная кислоты:
Изопропилбензол окисляется перманганатом калия в кислой среде до бензойной кислоты и углекислого газа:
4. Ориентирующее действие заместителей в бензольном кольце
Если в бензольном кольце имеются заместители, не только алкильные, но и содержащие другие атомы (гидроксил, аминогруппа, нитрогруппа и т.п.), то реакции замещения атомов водорода в ароматической системе протекают строго определенным образом, в соответствии с характером влияния заместителя на ароматическую π-систему.
| Заместители подразделяют на две группы в зависимости от их влияния на электронную плотность ароматической системы: электронодонорные (первого рода) и электроноакцепторные (второго рода). |
Типы заместителей в бензольном кольце
| Заместители первого рода | Заместители второго рода |
| Дальнейшее замещение происходит преимущественно в орто— и пара-положение | Дальнейшее замещение происходит преимущественно в мета-положение |
| Электронодонорные, повышают электронную плотность в бензольном кольце | Электроноакцепторные, снижают электронную плотность в сопряженной системе. |
|
|
| Например, толуол реагирует с хлором в присутствии катализатора с образованием смеси продуктов, в которой преимущественно содержатся орто-хлортолуол и пара-хлортолуол. Метильный радикал — заместитель первого рода. |
В уравнении реакции в качестве продукта записывается либо орто-толуол, либо пара-толуол.
| Например, при бромировании нитробензола в присутствии катализатора преимущественно образуется мета-хлортолуол. Нитро-группа — заместитель второго рода |

5. Особенности свойств стирола
Стирол (винилбензол, фенилэтилен) – это производное бензола, которое имеет в своем составе двойную связь в боковом заместителе.
Общая формула гомологического ряда стирола: CnH2n-8.
| Молекула стирола содержит заместитель с кратной связью у бензольного кольца, поэтому стирол проявляет все свойства, характерные для алкенов – вступает в реакции присоединения, окисления, полимеризации. |
Стирол присоединяет водород, кислород, галогены, галогеноводороды и воду в соответствии с правилом Марковникова.
| Например, при гидратации стирола образуется спирт: |
| Стирол присоединяет бром при обычных условиях, то есть обесцвечивает бромную воду |
При полимеризации стирола образуется полистирол:
Как и алкены, стирол окисляется водным раствором перманганата калия при обычных условиях. Обесцвечивание водного раствора перманганата калия — качественная реакция на стирол:
При жестком окислении стирола перманганатом калия в кислой среде (серная кислота) разрывается двойная связь и образуется бензойная кислота и углекислый газ:
При окислении стирола перманганатом калия в нейтральной среде при нагревании также разрывается двойная связь и образуется соль бензойной кислоты и карбонат:
Уравнение реакции толуола с этиленом
Все реакции толуола (метилбензола) можно подразделить на два типа: реакции, затрагивающие бензольное кольцо и реакции, затрагивающие метильную группу.
Реакции замещения
1. Реакции с участием бензольного кольца
Метилбензол вступает во все реакции замещения, в которых участвует бензол, и проявляет при этом более высокую реакционную способность, реакции протекают с большой скоростью.
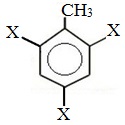
Метильный радикал, содержащийся в молекуле толуола, является ориентантом I рода, поэтому в результате реакций замещения в бензольном ядре получаются орто- и пара- производные толуола или при избытке реагента – трипроизводные общей формулы:
а) галогениерование
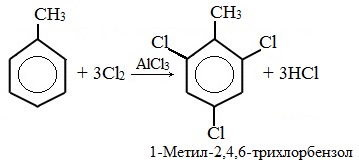
При избытке галогена можно получить ди- и три-замешенные производные в соответствии с правилами ориентации:
б) нитрование
Например, при нитровании толуола С6Н5CH3 (70°С) происходит замещение не одного, а трех атомов водорода с образованием 2,4,6-тринитротолуола:
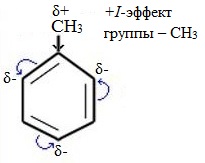
Здесь ярко проявляется взаимное влияние атомов в молекуле на реакционную способность вещества. С одной стороны, метильная группа СH3 (за счет +I-эффекта) повышает электронную плотность в бензольном кольце в положениях 2, 4 и 6 и облегчает замещение именно в этих положениях:
С другой стороны, под влиянием бензольного кольца метильная группа СH3 в толуоле становится более активной в реакциях окисления и радикального замещения по сравнению с метаном СH4.
в) сульфирование
г) алкилирование
2. Реакции с участием боковой цепи
Метильная группа в метилбензоле может вступать в реакции, характерные для алканов:
Это объясняется тем, что на лимитирующей стадии легко (при невысокой энергии активации) образуется радикал бензил ·CH2-C6H5. Он более стабилен, чем алкильные свободные радикалы (·СН3, ·СH2R), т.к. его неспаренный электрон делокализован за счет взаимодействия с π- электронной системой бензольного кольца:
Реакции присоединения
а) гидрирование
Реакции окисления
а) горение
б) неполное окисление
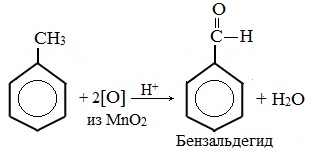
В отличие от бензола его гомологи подвергаются окислению легче предельных углеводородов. При этом окислению подвергаются лишь радикалы, связанные с бензольным кольцом, в случае толуола — метильная группа. Мягкие окислите (MnО2) окисляют ее до альдегидной группы, более сильные окислители (KMnO4) вызывают дальнейшее окисление до кислоты:
Толуол, в отличие от метана, окисляется в мягких условиях (обесцвечивает подкисленный раствор KMnO4 при нагревании).
Любой гомолог бензола с одной боковой цепью окисляется KMnO4 и другим сильным окислителем в бензойную кислоту:
Гомологи, содержащие две боковые цепи, дают двухосновные кислоты:
Написать уравнение реакции взаимодействия толуола с этиленом в присутствии хлорида алюминия?
Химия | 10 — 11 классы
Написать уравнение реакции взаимодействия толуола с этиленом в присутствии хлорида алюминия.
С6Н5 — СН3 + Н2С = СН2 = = = = СН3С6Н4СН = СН2 — H2.
Составьте уравнения реакций по описаниям, дайте характеристику уравнений реакций : а) натрий активно взаимодействует с хлором с образованием хлорида натрия ; б) гидроксид алюминия при нагревании разла?
Составьте уравнения реакций по описаниям, дайте характеристику уравнений реакций : а) натрий активно взаимодействует с хлором с образованием хлорида натрия ; б) гидроксид алюминия при нагревании разлагается с образованием оксида алюминия и воды.
Хлороводород НЕ взаимодействует с : 1)пропином 2)этиленом 3)гидроксидом натрия 4)бензолом 5)толуолом 6)этаном?
Хлороводород НЕ взаимодействует с : 1)пропином 2)этиленом 3)гидроксидом натрия 4)бензолом 5)толуолом 6)этаном.
3. Сокращенное ионное уравнение реакции : Al3 + + 3OH — → Al(OH)3↓ соответствует взаимодействию 1) хлорида алюминия с водой 2) алюминия с водой 3) хлорида алюминия со щелочью 4) алюминия со щелочью __?
3. Сокращенное ионное уравнение реакции : Al3 + + 3OH — → Al(OH)3↓ соответствует взаимодействию 1) хлорида алюминия с водой 2) алюминия с водой 3) хлорида алюминия со щелочью 4) алюминия со щелочью ___________________________________________________________________________________.
Написать уравнение реакции присоединения хлороводорода к этилену?
Написать уравнение реакции присоединения хлороводорода к этилену.
Напишите уравнения реакций взаимодействия : алюминия с азотом?
Напишите уравнения реакций взаимодействия : алюминия с азотом.
Составьте пожалуйста уравнение реакции хлорида магния и гидроксида алюминия?
Составьте пожалуйста уравнение реакции хлорида магния и гидроксида алюминия.
Тепловые эффекты образования хлоридов алюминия и меди соответственно равны 702?
Тепловые эффекты образования хлоридов алюминия и меди соответственно равны 702.
4 кДж / моль 215.
Составьте термохимическое уравнение реакции взаимодействия алюминия с раствором хлорида меди.
Напишите пожалуйста уравнение реакции : взаимодействие глюкозы с водородом в присутствии катализатора?
Напишите пожалуйста уравнение реакции : взаимодействие глюкозы с водородом в присутствии катализатора?
Приведите уравнение реакции получения гидроксида алюминия из хлорида алюминия?
Приведите уравнение реакции получения гидроксида алюминия из хлорида алюминия.
Составить химическое уравнение реакции по цепочке превращений : алюминий гидроксид — алюминий оксид — алюминий сульфат — алюминий хлорид?
Составить химическое уравнение реакции по цепочке превращений : алюминий гидроксид — алюминий оксид — алюминий сульфат — алюминий хлорид.
Вопрос Написать уравнение реакции взаимодействия толуола с этиленом в присутствии хлорида алюминия?, расположенный на этой странице сайта, относится к категории Химия и соответствует программе для 10 — 11 классов. Если ответ не удовлетворяет в полной мере, найдите с помощью автоматического поиска похожие вопросы, из этой же категории, или сформулируйте вопрос по-своему. Для этого ключевые фразы введите в строку поиска, нажав на кнопку, расположенную вверху страницы. Воспользуйтесь также подсказками посетителей, оставившими комментарии под вопросом.
Дано m(SO3) = 8 g Na2O — — — — — — — — — — — — — — — m(Na2SO4) — ? 8 X SO3 + Na2O — — >Na2SO4 M(SO3) = 80 g / mol M(Na2SO4) = 142 g / mol 80 142 8 / 80 = x / 142 X = 14. 2 g ответ 14. 2 г.
8 г Х г SO3 + Na2O — > Na2SO4 n = 1 моль n = 1 моль М = 80 г / моль М = 142 г / моль m = 80 г m = 142 г 8 г SO3 — Х г Na2SO4 80 г SO3 — 142 г Na2SO4 m(Na2SO4) = 8 * 142 / 80 = 14, 2 г.
Zn — >K2ZnO2 — >ZnSO4 — >K2[Zn(OH)4] — >Zn(NO3)2 — >ZnO 1)4Zn + KNO3 + 7KOH = NH3 + 4K2ZnO2 + 2H2O 2)K2ZnO2 + 2H2SO4 = K2SO4 + ZnSO4 + 2H2O 3)ZnSO4 + 4KOH = K2[Zn(OH)4] + K2SO4 4)K2[Zn(OH)4] + 4HNO3 = 2KNO3 + Zn(NO3)2 + 4H2O 5)2Zn(NO3)2 = 2ZnO + 4NO2..
Ca + H2O = Ca(OH)2 + H2n(Ca) = 6 г / моль : 40 г = 0, 15 мольV(Ca) = 0, 15моль * 22, 4 л / моль = 3, 36л3, 36л — 100%3 л — х%х = 89%.
Дано : Жк₁ = 11 мг — экв / л Жк₂ = 3 мг — экв / л Vв = 100 м³ Найти : m(Ca(OH)₂) Решение. Переведем единицы заданияв более удобные мг — экв / л = г — экв / м³ Снизить карбонатную жесткость с 11 г — экв / м³до 3г — экв / м³ — значит убрать из каждого..
Масса О2 = 0, 888. Если реак. 2Fe + O2 = 2FeO.
1 — Ответ 6NaOH + Al2O3 + 3H2O = 2Na3[Al(OH)6] NaOH + HCl = H2O + NaCl.
2) CH3 — CH2 — CH(CH3) — CH(CH2 — CH3) — CH2 — CH2 — CH3 3) CH3 — CH2 — CH2 — Cl + 2Na + Cl — CH2 — CH2 — CH3 — > CH3 — CH2 — CH2 — CH2 — CH2 — CH3 + 2NaCl.
Ca — 2e = Ca( + 2) коэффициент 4 Восстановитель, окисление 2N( + 5) + 8e = 2 N ( + 1) коэффициент 1 Окислитель, восстановление 4Ca + 10HNO3 = 4Ca(NO3)2 + N2O + 5H2O Если помог, нажми кнопку Спасибо)).