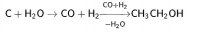Метанол CH3OH, метиловый спирт – это органическое вещество, предельный одноатомный спирт .
Общая формула предельных нециклических одноатомных спиртов: CnH2n+2O.
- Строение метанола
- Водородные связи и физические свойства метанола
- Изомерия метанола
- Химические свойства метанола
- 1.1. Взаимодействие с раствором щелочей
- 1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
- 2. Реакции замещения группы ОН
- 2.1. Взаимодействие с галогеноводородами
- 2.2. Взаимодействие с аммиаком
- 2.3. Этерификация (образование сложных эфиров)
- 2.4. Взаимодействие с кислотами-гидроксидами
- 3. Реакции замещения группы ОН
- 3.2. Межмолекулярная дегидратация
- 4. Окисление метанола
- 4.1. Окисление оксидом меди (II)
- 4.2. Окисление кислородом в присутствии катализатора
- 4.3. Жесткое окисление
- 4.4. Горение метанола
- 5. Дегидрирование спиртов
- Получение метанола
- 1. Щелочной гидролиз галогеналканов
- 2. Гидратация алкенов
- 3. Гидрирование карбонильных соединений
- 4. Промышленное получение метанола из «синтез-газа»
- Производство метанола
- Краткие сведения о метаноле
- ТЕПЛООБМЕННИКИ
- КАТАЛИТИЧЕСКИЙ НАСОС-РЕАКТОР
- Производство синтез-газа
- Диспергатор
- Эжекторный смеситель
- Общая схема установки
- Важные советы
- Реакция государства на публикацию этой информации
- Метанол ГОСТ 2222-95
- Содержание
- История
- Получение
- Применение
- Гомологизация метанола
- Биометанол
- Метанол в качестве топлива
- Свойства метанола и его реакции
- Нахождение в природе
- Токсичность
- Массовые отравления метанолом
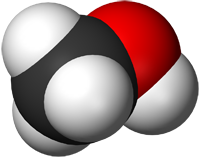
Строение метанола
В молекулах спиртов, помимо связей С–С и С–Н, присутствуют ковалентные полярные химические связи О–Н и С–О.
| Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4). |
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
| Атом кислорода в спиртах находится в состоянии sp 3 -гибридизации. |
В образовании химических связей с атомами C и H участвуют две 2sp 3 -гибридные орбитали, а еще две 2sp 3 -гибридные орбитали заняты неподеленными электронными парами атома кислорода.
Поэтому валентный угол C–О–H близок к тетраэдрическому и составляет почти 108 о .
Водородные связи и физические свойства метанола
Спирты образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Поэтому метанол – жидкость с относительно высокой температурой кипения (температура кипения метанола +64,5 о С).
Водородные связи образуются не только между молекулами метанола, но и между молекулами метанола и воды. Поэтому метанол очень хорошо растворимы в воде. Молекулы метанола в воде гидратируются:
| Чем больше углеводородный радикал, тем меньше растворимость спирта в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде. |
Метанол смешивается с водой в любых соотношениях.
Изомерия метанола
Для метанола не характерно наличие структурных изомеров – ни изомеров углеродного скелета, ни изомеров положения гидроксильной группы, ни межклассовых изомеров.
Химические свойства метанола
Метанол – органическое вещество, молекула которого содержит, помимо углеводородной цепи, одну группу ОН.
1. Кислотные свойства метанола
| Метанол – неэлектролит, в водном растворе не диссоциирует на ионы; кислотные свойства у него выражены слабее, чем у воды. |
1.1. Взаимодействие с раствором щелочей
Метанол с растворами щелочей практически не реагирует, т. к. образующиеся алкоголяты почти полностью гидролизуются водой.
Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому метанол не взаимодействуют с растворами щелочей.
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Метанол взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются алкоголяты. При взаимодействии с металлами спирты ведут себя, как кислоты.
| Например, метанол взаимодействует с калием с образованием метилата калия и водорода . |
Метилаты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
| Например, метилат калия разлагается водой: |
CH3OK + H2O → CH3-OH + KOH
2. Реакции замещения группы ОН
2.1. Взаимодействие с галогеноводородами
При взаимодействии метанола с галогеноводородами группа ОН замещается на галоген и образуется галогеналкан.
| Например, метанол реагирует с бромоводородом. |
2.2. Взаимодействие с аммиаком
Гидроксогруппу спиртов можно заместить на аминогруппу при нагревании спирта с аммиаком на катализаторе.
| Например, при взаимодействии метанола с аммиаком образуется метиламин. |
2.3. Этерификация (образование сложных эфиров)
Метанол вступает в реакции с карбоновыми кислотами, образуя сложные эфиры.
| Например, метанол реагирует с уксусной кислотой с образованием метилацетата (метилового эфира уксусной кислоты): |
2.4. Взаимодействие с кислотами-гидроксидами
Спирты взаимодействуют и с неорганическими кислотами, например, азотной или серной.
| Например, метанол взаимодействует с азотной кислотой : |
3. Реакции замещения группы ОН
В присутствии концентрированной серной кислоты от метанола отщепляется вода. Процесс дегидратации протекает по двум возможным направлениям: внутримолекулярная дегидратация и межмолекулярная дегидратация.
3.2. Межмолекулярная дегидратация
При низкой температуре (меньше 140 о С) происходит межмолекулярная дегидратация по механизму нуклеофильного замещения: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы. Продуктом реакции является простой эфир.
| Например, при дегидратации метанола при температуре до 140 о С образуется диметиловый эфир: |
4. Окисление метанола
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на каталитическое, мягкое и жесткое.
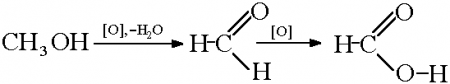
| Метанол окисляется сначала в формальдегид, затем в углекислый газ: Метанол → формальдегид → углекислый газ |
Типичные окислители — оксид меди (II), перманганат калия KMnO4, K2Cr2O7, кислород в присутствии катализатора.
Легкость окисления спиртов уменьшается в ряду:
метанол
4.1. Окисление оксидом меди (II)
Метанол можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого вещества. Метанол окисляется до метаналя.
| Например, метанол окисляется оксидом меди до муравьиного альдегида |
4.2. Окисление кислородом в присутствии катализатора
Метанол можно окислить кислородом в присутствии катализатора (медь, оксид хрома (III) и др.). Метанол окисляется до метаналя.
4.3. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) метанол окисляется до углекислого газа.
| Спирт/ Окислитель | KMnO4, кислая среда | KMnO4, H2O, t |
| Метанол СН3-ОН | CO2 | K2CO3 |
| Например, при взаимодействии метанола с перманганатом калия в серной кислоте образуется углекислый газ |
4.4. Горение метанола
При сгорании спиртов образуются углекислый газ и вода и выделяется большое количество теплоты.
| Например, уравнение сгорания метанола: |
5. Дегидрирование спиртов
При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования. При дегидрировании метанола образуется альдегид.
Получение метанола
1. Щелочной гидролиз галогеналканов
При взаимодействии галогеналканов с водным раствором щелочей образуются спирты. Атом галогена в галогеналкане замещается на гидроксогруппу.
| Например, при нагревании хлорметана с водным раствором гидроксида натрия образуется метанол |
2. Гидратация алкенов
Гидратация (присоединение воды) алкенов протекает в присутствии минеральных кислот. При присоединении воды к алкенам образуются спирты.
Однако получить метанол гидратацией алкенов нельзя.
3. Гидрирование карбонильных соединений
Присоединение водорода к альдегидам и кетонам протекает при нагревании в присутствии катализатора. При гидрировании альдегидов образуются первичные спирты, при гидрировании кетонов — вторичные спирты, а из формальдегида образуется метанол.
| Например, при гидрировании формальдегида образуется метанол |
CH2=O + H2 → CH3-OH
4. Промышленное получение метанола из «синтез-газа»
Каталитический синтез метанола из монооксида углерода и водорода при 300-400°С и давления 500 атм в присутствии смеси оксидов цинка, хрома и др.
Сырьем для синтеза метанола служит «синтез-газ» (смесь CO и H2), обогащенный водородом:
Производство метанола
Краткие сведения о метаноле

Температура кипения: +64,5°C, температура замерзания: —97,8°C, плотность: 792 г/л.
Пределы взрывоопасных концентраций в воздухе 6,7—36% по объему. Октановое число больше 110.
Температура воспламенения 467°C, теплота сгорания 24000 кДж/кг — меньше, чем у бензина (44000 кДж/кг), поэтому расход метанола (в литрах) будет выше примерно в два раза.
Как топливо применяется в гоночных машинах, например в Формуле-1.
Метиловый спирт смешивается в любых концентрациях с водой и органическими растворителями.
Традиционно метанол получали возгонкой древесины. Но более перспективен способ получения метанола — из природного газа. В дальнейшем по мере совершенствования этой технологии возможны и другие источники сырья, например биомасса (навоз).
Промышленные способы получения метилового спирта пока недостаточно эффективны для использования метанола в качества топлива, но если в ближайшие десятилетия цена на нефть будет подниматься, то ситуация может изменится в пользу спиртового топлива (особенно при использовании автомобилей на топливных ячейках).
Природный газ, как известно, почти на 100% состоит из метана — СН4. Ни в коем случае не надо его путать с баллонным газом пропан-бутаном, последний является продуктом крекинга нефти и используется напрямую в качестве автомобильного топлива.
Можно перевести любой автомобиль с бензиновым двигателем на смесь пропана и бутана, достаточно установить соответствующее оборудование. А при использовании метанола даже не потребуется никакого дополнительного оборудования.
Мы подробно опишем, как, используя метанол в качестве топлива, как можно существенно повысить мощность двигателя. Пока же только скажем, что это достигается увеличением диаметра главных жиклеров или уменьшением количества воздуха в топливной смеси.
Итак, поговорим немного о химии процесса получения метанола из природного газа.
Метан при неполном окислении превращается в окись углерода и водорода, реакция эта выглядит следующим образом:
Более простой технологически способ проходит по реакции конверсии метана с водяным паром:
В первом уравнении стоит +16,1 ккал. Это означает, что реакция идет с выделением тепла. Во втором — с поглощением. Тем не менее, мы остановимся на втором способе получения окиси углерода и водорода.
При наличии этих двух компонентов уже можно напрямую синтезировать метанол. Реакция идет по следующей формуле:
Сложность в том, что конечный продукт получается лишь при высоком давлении и температуре (Р>20 атм, Т=350°C), но при наличии катализатора этот процесс смещается вправо и при низком давлении.
Полученный метанол выводится из реакции охлаждением до конденсации, а не сконденсировавшие газы будем сжигать. При правильном сжигании остатков водорода и СО никаких вредных веществ не выделяется (отходы СО2 и Н2O — безвредны), так что никаких вытяжных устройств не требуется.
Дальше метанол заливается через трубку, обязательно с герметизацией (!), в канистру.
Как видите, химический процесс очень прост, он основывается на двух реакциях.
Сложности есть только технологические и по мерам безопасности. Мы ведь здесь имеем дело с сильно горючими и ядовитыми веществами. Нужно опасаться как взрыва, так и утечки этих газов. Поэтому необходимо строжайше соблюдать технологию и правила техники безопасности, которые мы будем описывать.
Для сборки установки нужно будет приобрести: лист нержавеющей стали (1мм), трубку из «нержавейки» бесшовную, наружным диаметром 6—8 мм, толщиной стенок не менее 1 мм и длиной около 2 метров, компрессор от любого бытового холодильника (можно со свалок, но рабочий). Ну и, само собой разумеется, нужна будет аргоновая электросварка.
Для производительности 10 л/час теплообменник может быть длиной 600 мм, а для 3 л/час должно хватить и 200 мм, h — 20 мм. Размеры частиц могут варьироваться, оптимум где-то в пределах 0,5—1 мм.
ТЕПЛООБМЕННИКИ

Для жидкостей, теплопроводность которых велика, такой теплообменник может быть приемлем. Но с газами ситуация совершенно другая.
Дело в том, что на небольших скоростях поток газа движется ламинарно и практически не обменивается теплом с окружающей средой.
Посмотрите на дымок, подымающийся от горящей сигареты. Эта стройная струйка дыма и есть ламинарный поток. Сам факт того, что дымок поднимается вверх, говорит о его высокой температуре. А то, что он остается цельным прутком примерно на высоту до 20 сантиметров подъема, свидетельствует о сохранении им тепла. То есть на этом расстоянии даже при совсем малых скоростях поток газа не успевает охладиться, обменяться теплом с воздухом.
Именно вследствие ламинарности потока газовые теплообменники всегда получаются очень громоздкими.
Внутри трубок теплообменников появляются «сквозняки», которые даже на десятках метров практически не дают теплообмена.
Это хорошо известно тем, кто когда-либо гнал самогон. Длинная, интенсивно охлаждаемая трубка, из неё вытекает конденсат, но при этом обязательно идет и пар. Значит, теплообмен недостаточно эффективен.
Проблема, однако, имеет решения и оно может быть несложным. Например, наполнить трубку медным порошком (см. рис.1).
Учитывая задачи теплообмена, материалом корпуса могут быть и железо, и медь, и алюминий, материалом набивки — медь, алюминий, — что найдется. Тогда вокруг каждой частички металла струйка газа будет образовывать завихрения.
Тем самым сразу ликвидируются сквозняки и поток становится турбулентным. Ну и одновременно увеличивается в огромной степени контакт газа с охлаждаемой поверхностью.
Набитый в трубку порошок меди постоянно принимает или отдает тепло стенкам, и поскольку теплопроводность меди примерно в 100 тысяч раз выше теплопроводности газа, то газ сравнительно быстро примет температуру стенок, если мы будем их интенсивно охлаждать.
Проточную охлаждающую воду, конечно, целесообразно пропускать навстречу потоку газа. Это дает возможность в каждый точке теплообменника иметь свою определенную температуру. Поскольку тепловой контакт у нас близок к идеальному, температура на выходе конденсируемой жидкости будет равна температуре охлаждающей жидкости.
Вот каков по идее обсуждаемый здесь теплообменник.
Приведенный эскиз есть не что иное, как дистиллятор, он же самогонный аппарат, он же теплообменник. Производительность такого дистиллятора приблизительно 10 литров в час. Его также можно применять практически в любых целях, включая установку для получения этилового спирта.
Такие теплообменники при огромной производительности в сотни раз меньше существующих.
КАТАЛИТИЧЕСКИЙ НАСОС-РЕАКТОР

Площадь контакта газа с такими шариками в тысячи раз меньше, чем если бы мы использовали частицы в 1—1000 микрон. Но тогда проходимость газа весьма затруднится.
Кроме того, мельчайшие частицы катализатора довольно скоро выйдут из строя вследствие поверхностного загрязнения.
Нами найден способ увеличить площадь контакта газа с катализатором, не затрудняя проходимости его в реакторе, и одновременно непрерывно производить очистку от так называемого «отравления» самого катализатора. Делается это следующим образом.
Порошковый катализатор смешивается с ферромагнитными частицами — железным либо ферритовым порошком, который можно получить, разбивая магниты от неисправных громкоговорителей.
Ферриты очень твёрдое вещества — это их полезное свойство пригодится в дальнейшем и позволит обойтись без добавления абразивного порошка (об этом далее).
Смесь ферромагнитного порошка с катализатором помещается в немагнитную трубку, например, из стекла, керамики, можно и в алюминиевую или медную.
Теперь смотрите, какая может быть схема.

При включении в сеть переменного тока обмотки включаются поочередно с частотою 50 Гц. При этом ферромагнитный порошок непрерывно сжимает и расширяет катализатор, обеспечивая пульсирующую проходимость газа.
Если же включать электромагниты в трехфазною сеть (см. рис.4), то в этом случае обеспечивается поступательная пульсация сжатий, и за счет этого непрерывно газ будет сжиматься в продольном направлении вперед.
Таким образом, система работает, как насос. При этом — многократно перемешивая газ, сжимая и расширяя его и тысячекратно увеличивая интенсивность процесса на катализаторе.
Попутно частички катализатора трутся друг о друга и о ферритовый абразивный порошок, что приводит к их очистке от загрязняющих пленок.
Схема работает следующим образом: с частотой 50 Гц происходит смена полярности на питании. Ток попеременно проходит по обмотке 1,3 и 2,4 (см. рис. 2). При этом в них появляется магнитное поле, которое намагничивает ферромагнитные частицы и заставляет их взаимодействовать друг с другом, вовлекая в движение частицы катализатора.
Таким образом попеременно возникает для газа проходимость сквозь мелкие частицы, сменяемая большим сопротивлением, оказываемым сдавленной массой частиц.
Работа описанного каталитического реактора эквивалентна реактору размером метров в 20—30. Увеличить производительность реактора можно, включая обмотки в трехфазную сеть. При этом система работает не как клапаны, а как активный насос, совмещая все положительные эффекты первой схемы и дополнительно принуждая газ перемещаться в направлении смещения сдвига фаз. При таком включении важно правильно выбрать фазировку.
Итак, в реакторе, приведенном здесь, работают следующие положительные факторы:
- Увеличение площади катализатора в 300—1000 раз за счет уменьшения размеров частиц.
- Происходит постоянная очистка катализатора от поверхностного загрязнения.
- Постоянные пульсации давления реагирующих газов между частицами катализатора, а во второй схеме дополнительно происходит еще и перекачки газа внутри самого реактора.
Недостаток этого реактора — повышенное сопротивление потоку газа. Это устраняется попеременным уплотнением/освобождением частиц внутри четных/нечетных катушек.
Одна важная деталь: необходимо теплоизолировать катушки от корпуса реактора.

Корпус реактора вытачивается из латунной или бронзовой болванки диаметром 50 мм. Размеры можно взять прежние — 160 мм общая длина, рабочая реакторная длина около 140 мм, внутренний диаметр 33 мм, толщина стенок приблизительно 5. 8 мм, т.е. внешний диаметр около 50 мм и того же диаметра — заглушки, их толщина по 20 мм и на каждой нарезана резьба М36х1,0 мм и длиной по 10 мм.
Всё это должно быть сделано из одного и того же материала!
К заглушкам в отверстия вставляются и привариваются переходные штуцера или просто соединительные бесшовные стальные трубки с внутренним диаметром 6. 8 мм и толщиной стенок около 2 мм.
Данную конструкцию необходимо снаружи теплоизолировать листовым асбестом и разделить по всей длине на четыре секции с помощью пяти перегородок, также вырезанных из листового асбеста.
Для фиксации перегородок их можно промазать силикатным клеем. После просушки наматывается медная проволока (d=0,15мм) в каждую секцию.
Сопротивление, измеренное омметром, для каждой секции должно быть около 1200 Ом.
Обмотки включаются по схеме рис.3 через регулятор напряжения, например, лабораторный трансформатор (ЛАТР).
Чтобы избежать перегрева обмоток, их надо охлаждать, для этого можно проложить под обмотки стеклянные трубочки диаметром 6. 8 мм, возможен принудительный обдув катушек, с контролем температуры внутри реактора.
Следует отметить, что подобная схема реактора на рис. 2 была заявлена на патент ее автором — гражданином Г.Н. Вакс. Она может работать в любых каталитических газовых процессах.
Для профессиональных химиков данная схема — это не домашняя разработка, а принципиально новый, еще не совсем изученный, но эффективный реактор.
Производство синтез-газа
Синтез-газом называется смесь H2 и СО, необходимая для производства метанола.
Вначале рассмотрим технологию синтез-газа.
Традиционные методы получения СО и H2 из метана (CH4) состоят в том, что метан смешивается с водяным паром и в нагретом состоянии поступает в реактор, где к паро-метанной смеси добавляется дозированное количество кислорода. При этом происходят следующие реакции:
Как видно, некоторые реакции эндотермические (т.е. с поглощением тепла), а некоторые экзотермические. Наша задача создать такой баланс, чтобы реакции шли с контролируемым выделением тепла.
Итак, вначале требуется дозированное смешение Н2О и СН4.
Традиционные методы ведения этого процесса сложны и громоздки. Мы будем насыщать метан водяными парами путем пропускания пузырьков этого газа через нагретую до 100 градусов Цельсия воду, а чтобы пузырьки активно разбивались, размещаем на их пути твердые ферритовые частички размером 1—2 мм.
Но в этой массе рано или поздно пузырьки находят дорогу и затем, практически не разбиваясь, проходят по образовавшемуся каналу. Чтобы этого не происходило, частички из феррита и смесительную камеру ставим в соленоид с подачей переменного тока.
В этом и заключается существенное отличие нашего диспергатора от традиционных устройств (см.рис 5).
Диспергатор
Под действием вибрации частиц феррита в пульсирующем магнитном поле пузырьки метана постоянно разбиваются, проходят сложный зигзагообразный путь и насыщаются парами воды.
К соленоиду жестких требований нет, поскольку запитывается он от ЛАТРа или от какого-либо из имеющихся в продаже регуляторов света.
Регулировка напряжения на соленоиде необходима, чтобы, изменяя магнитное поле, одновременно изменять и степень насыщения метана парами воды. О цели этих изменений будет сказано ниже.
Количество витков в катушке может быть от 500 до 1000. Диаметр провода 0,1— 0,3мм. Труба диспергатора берется из неферромагнитного металла, поэтому в переменном магнитном поле она будет разогреваться. Кроме того, и метан поступает в воду разогретым.
Но не смотря на это, воду все равно требуется предварительно нагревать до кипения, иначе не получить нужного количества водяного пара.
Ещё необходим бачок для подпитки водой, поскольку она непрерывно расходуется на образование паро-метановой смеси, для этой цели подойдет сливной бачок от стандартного унитаза, чьё сливное отверстие закрывается стальной пластиной, с приваренной сливной трубкой, конец этой трубки вставляется в диспергатор и изгибается вниз на 180° (см. рис. 5).

Готовая паро-метановая смесь разогревается до температуры 550—600 градусов в теплообменнике.
Необходимо расположить бачок таким образом, чтобы уровень воды в смесителе—диспергаторе не поднимался выше 150 мм, т.е. до половины его высоты, это связано с величиной давления в газовой сети (=150 мм водного столба!), иначе вода будет препятствовать проходу газа-метана в диспергатор.
Также воду перед подачей в бачок необходимо очистить от примесей хлора. С этим справятся стандартные средства очистки воды для бытовых целей.

Теплообменник изготавливается из нержавеющей стали, обязательно варится в среде инертного газа. Трубки из нержавеющей стали крепятся к корпусу только сваркой.
Наполнитель теплообменника изготовляется из 1—2 миллиметровых частиц керамики. Это может быть, например, дробленая фарфоровая посуда. Наполнять емкость надо достаточно плотно, с обязательным встряхиванием.
Самым сложный и ответственным узлом является конвертор-реактор (рис. 7). В нем собственно и происходит конверсия метана (превращение его в синтез-газ).
Конвертор состоит из кислород-паро-метанового смесителя и реакционных каталитических колонн. Вообще, реакция идет с выделением тепла. Однако в нашем случае, чтобы процесс начался, на подводящих трубках необходим нагрев, поскольку мы осуществляем конверсию метана по реакции:
СН4 + Н2О СО + ЗН2 — 206 кДж , с потерей тепла,
а значит нужно обязательно подводить тепло в конвертор. Для этого паро-метановый газ мы пропускаем через 
Конвертор работает следующим образом: паро-метановая смесь поступает в камеру, в которой вварены трубки из нержавеющей стали. Количество трубок может быть от 5 до 20 в зависимости от желательной производительности конвертора.
Пространство верхней камеры должно быть обязательно плотно набито крупнозернистым песком или дробленой керамикой или крошкой нержавейки, размеры частиц 0,5—1,5 мм. Это необходимо для лучшего перемешивания газов, а самое главное — для пламягашения.
При соединении воздуха с горячим метаном может произойти загорание. Поэтому в верхней камере набивка осуществляется с обязательным встряхиванием и досыпкой.
Трубки и сборная камера (на рис. 7 — нижняя), как раз и набиваются частицами, содержащими катализатор — окись никеля. Массовая доля никеля в катализаторе при пересчете на NiO, должна составлять не менее 7,5±1,5%.
Остаточное содержание метана при конверсии с водяным паром природного газа (соотношение пар:газ=2:1), при температуре 500°С — 38,5%, а при 800°С — не более 1,5%.
Массовая доля «вредной» серы в пересчете на SОз, должна быть не более 0,005%.
В качестве катализатора лучше всего использовать готовый промышленный, но в крайнем случае можно сделать его самостоятельно.
Для этого нужно на воздухе прокалить частицы никеля. Если чистого никеля нет, то можно его приготовить из никель-содержащих 10—15—20-копеечных монет СССР.
Сотрите их на грубом абразивном круге или мелкой фрезой. Попадание абразива в набивку допускается. Полученный порошок прокалите и смешайте в пропорции 1/3 объема порошка с 2/3 объема молотой керамики (0,5 мм) или чистого грубозернистого песка.
Чтобы не перегревать верхнюю камеру, промежуток между верхними частями трубок заполняются на 10 см любым высокотемпературным теплоизолятором.
Простой способ получения теплоизолятора: обычный канцелярский силикатный клей смешивают с 10—15 весовыми процентами тонкомолотого мела или талька или глины. Перемешивают тщательно.
Наливают смесь тонким слоем и сразу же прижигают огнем паяльной лампы.
Вскипевшая в клее вода образует пемзообразную белую массу. Когда она остынет, опять наливают на нее слой клея с мелом и опять обрабатывают пламенем.
И так повторяют до тех пор, пока не получат, необходимый слой теплоизолятора. В итоге покрытие получается похожим на профессиональную теплоизоляцию центрального отопления:
После окончания сборки конвертора его помещают в стальной короб, которой обязательно теплоизолируют материалом, выдерживающим температуру до 1000 градусов, например, асбестом.
Горелки инжекционного типа, могут быть любые, от 5 штук до 8. Чем их больше, тем равномернее нагрев. Возможна также система, использующая одну горелку. Пламя ее имеет несколько выходов через отверстия в трубе.
Газовые горелки есть в продаже, например, те, что используются для обработки лыж. Есть в продаже также газовые паяльные лампы, поэтому мы даем только общую схему.
Горелки должны соединяться параллельно и регулироваться стандартным газовым краном, например, от газовой плиты, но лучше взять автоматический регулятор от бытовой газовой плиты — дороговат, но надёжен и удобен — с его помощью можно задать нужную температуру внутри конвертора-реактора, повысив тем самым степень автономности установки в целом.
Эжекторный смеситель
Эжекторный смеситель подачи воздуха и метана в камеру конвертора (см.рис.8.) — это еще один из ответственных узлов.

Компрессор может быть практически от любого бытового холодильника, давление регулируется от «нуля» до необходимого, которое будет не на много выше давления в газовой магистрали (т.е. => 150 мм. вод. ст.).
Необходимость подачи воздуха (кислорода) в конвертор обусловлена тем, что по реакции [5] часть водорода должна быть поглощена с выделением СО, тем самым увеличивается количество окиси углерода до пропорции СО:Н2 = 1:2, т.е. число молей (объемов) водорода должно быть в два раза большим объемов окиси углерода.
Наличие избыточного воздуха приведёт к синтезу побочных продуктов — кислот, высших спиртов — «сивухи» и прочих вредных компонентов.
Но возникновение CO2 произойдет по реакции [1] с выделением большого количества тепла. Поэтому вначале процесса компрессор мы не включаем и винт держим вывернутым. Воздух не подаем. И по мере разогрева камеры и включении всей системы будем постепенно, включив компрессор и вворачивая винт клапана давления, увеличивать подачу воздуха и одновременно уменьшать пламя на горелках.
Контроль будем вести по количеству излишков водорода на выходе из конденсатора метанола (теплообменник 3. и 3.1) через фитиль(13, рис. 10), сокращая его.
Фитиль для дожига излишка синтез-газа представляет собой 8-миллиметровую трубку, длиной 100 мм, набитую медным проводом по всей длине, чтобы пламя не пошло вниз, в канистру с метанолом.
Мы разобрали все узлы установки получения метанола.
Как ясно из предыдущего, вся установка состоит из двух основных узлов: конвертора для создания синтез-газа (конверсия метана) и синтезатора метанола. Синтезатор (каталитический насос, см. рис. 2) достаточно хорошо описан выше. Единственно, что следует добавить — это необходимость установки теплоизолятора между трубой и катушкой. Как изготовить теплоизолятор, мы рассказывали чуть выше.
Общая схема установки

Вода (дистиллированная) добавляется в диспергатор непрерывно из бачка (1).
Вышедшая газовая смесь поступает в теплообменник (3.2), где разогревается до 500—600°C и идет в конвертор (4). На катализаторе при температуре 800°C происходит реакция [2]. Для создания этой температуры работают горелки (12).
После установления температурных режимов включается компрессор (5) и постепенно подается воздух в смеситель (11).
Повышение давления осуществляется путем вворачивания винта в клапане (8). Одновременно уменьшаем пламя на горелках (12) при помощи вентиля (14.2).
Полученный на выходе синтез-газ поступает в теплообменники (3.1; 3.2), где охлаждается до температуры 320—350°. Затем синтез-газ поступает в синтезатор метанола (6), где на катализаторе из смеси одинакового количества ZnO, CuO, CoO происходит превращение его в метанол СН3ОН.
Смесь газообразных продуктов на выхода охлаждается в теплообменнике (3.3), который описан выше (см. рис. 1) и поступает в накопительный бачок (10). В верхней его части находится трубка — фитиль (13), где дожигаются продукты, которые не прореагировали в процессах.
Метан через вентиль (14) поступает в теплообменник (3.1), разогревается до 250—300 градусов и поступает через реактор-фильтр (15) в смеситель—диспергатор (2), где насыщается парами воды.
Вода добавляется в диспергатор непрерывно из бачка(1). Вышедшая газовая смесь поступает в теплообменник (3.2), где разогревается до 500—600 градусов и идет в конвертор (4).
На NiO — катализаторе при температуре 800—900 градусов происходит реакция [2]. Рабочую температуру создают горелки (12).
Важные советы
Катализаторы можно готовить самому путем прокаливания порошковых металлов на воздухе.
Измерение температуры можно осуществлять при помощи термоиндикаторных красок, которые в настоящее время достаточно распространены. Измерение нужно проводить на входных и выходных трубках.
Если термокрасок вы не достанете, можно изготовить сплав олово — свинец — цинк. При определенных, найденных экспериментально, пропорциях смешения они будут иметь необходимую температуру плавления. Нанося полученные сплавы на трубки и следя за их плавлением, можно с некоторой погрешностью контролировать температуру.
Если вы не допустили образования газовых карманов (т.е. полностью заполнены все полости соответствующей крошкой), если устранили утечки и самое главное — своевременно зажжен и постоянно горит фитиль (11), то установка будет абсолютно безопасна.
Подбирая катализаторы можно повышать тепловой КПД, увеличить процент выхода метанола. Для достижения оптимума здесь требуются эксперименты. Они проводятся во многих институтах разных стран. В России к числу таких НИИ относится, например, ГИАП (Государственный институт азотной промышленности).
Следует иметь в виду, что получение метанола из природного газа в компактных установках — новое дело, и многие процессы еще недостаточно изучены. В то же время метанол — одно из самых экологически чистых и практически идеальных топлив. И, самое главное, получение его основано на безграничных и возобновляемых ресурсах — метане.
Реакция государства на публикацию этой информации
Приведем фрагмент интервью с редакцией журнала «Приоритет», где впервые была опубликована схема и теоритическое обоснование возможности получения метилового спирта в домашних условиях:
Дорогой спирт — это соблазн правительству залатать свою бездарную экономическую литику. Спирт дешев, и его искусственная дороговизна безумно дорого обходится всем нам. Так что, когда у власти находятся временщики, проблемы, им вверенные, остается решать изобретателям.
Мы научим людей делать чистый спирт практически из чего угодно.
— Вы всерьез хотите связать проблему власти с «бесплатным» автомобильным топливом?
Нам внушают идею о выравнивании цен на бензин под мировые цены. Но за месячную зарплату немецкий рабочий мог бы купить 3,3 тонны бензина, наш работяга — 220 литров. Это притом, что Германия бензин ввозит. Так что, вывозя в огромных количествах топливо и, обогащая на этом кучку дельцов, нас лишают не только будущего, но и настоящего.
Поэтому мы и пошли на публикацию технологии лучения метанола из природного газа.
— Но возникнут сложные проблемы. Нужно будет опять ставить газовые счетчики на каждую квартиру, контролировать их. том это просто опасно: ведь метанол — страшный яд.
Что касается счетчиков — это не наша проблема и не проблема граждан. Думаю, что в настоящее время проконтролировать лучение метанола в квартирах невозможно. Не смогли же тысячи участковых кончить с самогоноварением. А маленький чемоданчик, дключенный к плите и водопроводу и к тому же не издающий никаких запахов, искать безнадежно.
Что же до ядовитости метанола здесь вы абсолютно правы — 30 мл выпитого метанола, смертельны. Но и рюмка бензина ядовита не меньше. Но если выхлоп сгоревшего в двигателе бензина медленно губит все живое в городах, то выхлоп метанола абсолютно чист.
Кроме того, двигатель, работающий на метаноле, служит во много раз дольше и мощность его намного выше. Поэтому его широко ис льзуют в спортивных машинах. Знаю это как бывший мотогонщик. Самое главное для безопасности производства метанола на нашем оборудовании — точно следовать рекомендациям.
Метанол ГОСТ 2222-95
| Метанол | |
|---|---|
 | |
 | |
 | |
| Систематическое наименование | Метанол |
| Традиционные названия | Метиловый спирт, древесный спирт, карбинол, метилгидрат, гидроксид метила |
| Хим. формула | СН3OH |
| Состояние | жидкость |
| Молярная масса | 32,04 г/моль |
| Плотность | 0,7918 г/см³ |
| Динамическая вязкость | 5.9×10 −4 Па·с |
| Энергия ионизации | 10,84 ± 0,01 эВ |
| Т. плав. | -97 °C |
| Т. кип. | 64,7 °C |
| Т. разл. | 320-380 °C |
| Т. всп. | 6 °C |
| Т. воспл. | 13 °C |
| Т. свспл. | 440 °C |
| Пр. взрв. | 6,98-35,5 % |
| Тройная точка | 175,45 K (−97,7°C) |
| Кр. точка | 513,15 K (240 °C), 7,85 МПа |
| Энтальпия образования | -238 кДж/моль |
| Энтальпия сгорания | 726 000 Дж/моль |
| Энтальпия плавления | 3167,29 ± 0,01 Дж/моль |
| Энтальпия кипения | 37 400 Дж/моль |
| Удельная теплота испарения | 37,4 кДж/моль |
| Давление пара | 11,8 кПа (при 20 °С) |
| pKa | 15,5 |
| Дипольный момент | 1,65 Д |
| ГОСТ | ГОСТ 2222-95 ГОСТ 6995-77 |
| Рег. номер CAS | 67-56-1 |
| PubChem | 887 |
| Рег. номер EINECS | 200-659-6 |
| SMILES | |
| RTECS | PC1400000 |
| ChEBI | 17790 |
| Номер ООН | 1230 |
| ChemSpider | 864 |
| Токсичность | умеренно-токсичен для мелких животных, высокотоксичен для крупных животных и человека, поражает зрительный нерв   |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Метанол (метиловый спирт, древесный спирт, карбинол, метилгидрат, гидроксид метила) — CH3OH, простейший одноатомный спирт, бесцветная ядовитая жидкость, контаминант. Метанол — это первый представитель гомологического ряда одноатомных спиртов.
С воздухом в объёмных концентрациях 6,98—35,5 % образует взрывоопасные смеси (температура вспышки 8 °C). Метанол смешивается в любых соотношениях с водой и большинством органических растворителей.
Содержание
- 1 История
- 2 Получение
- 3 Применение
- 3.1 Гомологизация метанола
- 3.2 Биометанол
- 4 Метанол в качестве топлива
- 5 Свойства метанола и его реакции
- 6 Нахождение в природе
- 7 Токсичность
- 7.1 Массовые отравления метанолом
История
Метанол был впервые обнаружен Бойлем в 1661 году в продуктах сухой перегонки древесины. Через два столетия, в 1834 году, его выделили в чистом виде Ж. Б. Дюма и Э. М. Пелиго. Тогда же была установлена химическая формула метанола. В 1857 году Бертло получил метанол омылением метилхлорида.
Получение
Известно несколько способов получения метанола: сухая перегонка древесины и лигнина, термическое разложение солей муравьиной кислоты, синтез из метана через метилхлорид с последующим омылением, неполное окисление метана и получение из синтез-газа. Первоначально в промышленности был освоен метод получения метанола сухой перегонкой древесины, но впоследствии он потерял своё промышленное значение. Современное производство метанола из монооксида углерода и водорода впервые было осуществлено в Германии компанией BASF в 1923 году. Процесс проводился под давлением 10—35 МПа на цинк-хромовом катализаторе (ZnO/Cr2O3) при температуре 320—450 °C. Впоследствии распространение получил синтез метанола на медьсодержащих катализаторах, промотированных цинком, хромом и др., при 200—300 °C и давлении 5-10 МПа, разработанный в Англии.
Современный промышленный метод получения — синтез из оксида углерода(II) и водорода на медь-цинковом оксидном катализаторе при следующих условиях:
- температура — 250 °C,
- давление — 7 МПа (= 69,08 атм = 70 Бар = 71,38 кгс/см²)
Схема механизма каталитического получения метанола сложна и суммарно может быть представлена в виде реакции:
До промышленного освоения каталитического способа получения метанол получали при сухой перегонке дерева (отсюда его название «древесный спирт»). В настоящее время этот способ неактуален.
Молекулярная формула — CH4O или CH3—OH
Производство метанола (в тыс. тонн):
| год | США | Германия | Мир | Цена продажи($/т) |
|---|---|---|---|---|
| 1928 | 24 | 18 | 140 | 84,7 |
| 1936 | 97 | 93 | 305 | 88,9 |
| 1950 | 360 | 120 | 349 | 83,1 |
| 1960 | 892 | 297 | 3930 | 99,7 |
| 1970 | 2238 | нет данных | 5000 | 89,7 |
| 1980 | 3176 | 870 | 15000 | 236,1 |
| 2004 | 3700 | 2000 | 32000 | 270 |
Применение
В органической химии метанол используется в качестве растворителя.
Метанол используется в газовой промышленности для борьбы с образованием гидратов (из-за низкой температуры замерзания и хорошей растворимости). В органическом синтезе метанол применяют для выпуска формальдегида, формалина, уксусной кислоты и ряда эфиров (например, МТБЭ и ДМЭ), изопрена и др.
Наибольшее его количество идёт на производство формальдегида, который используется для производства карбамидоформальдегидных и фенолформальдегидных смол. Значительные количества CH3OH используют в лакокрасочной промышленности для изготовления растворителей при производстве лаков. Кроме того, его применяют (ограниченно из-за гигроскопичности и отслаивания) как добавку к жидкому топливу для двигателей внутреннего сгорания.
Благодаря высокому октановому числу, позволяещему увеличить степень сжатия до 16, увеличивая тем самым удельную мощность двигателя; метанол используется для заправки гоночных мотоциклов и автомобилей. Метанол горит в воздушной среде, и при его окислении образуется двуокись углерода и вода:
Для получения биодизеля растительное масло переэтерифицируется метанолом при температуре 60 °C и нормальном давлении приблизительно так: 1 т масла + 200 кг метанола + гидроксид калия или натрия.
Во многих странах метанол применяется в качестве денатурирующей добавки к этанолу при производстве парфюмерии. В России использование метанола в потребительских товарах запрещено. В России запрещено использование метилового спирта в средствах по уходу за автотранспортом, а также продажа населению указанных средств, содержащих метанол.
Используется в топливных элементах. Работа топливных элементов основана на реакции окисления метанола на катализаторе в диоксид углерода. Вода выделяется на катоде. Протоны (H + ) проходят через протонообменную мембрану к катоду где они реагируют с кислородом и образуют воду. Электроны проходят через внешнюю цепь от анода к катоду снабжая энергией внешнюю нагрузку.
Общая для топливного элемента:
Получение муравьиной кислоты окислением метанола:
Получение диметилового эфира дегидратацией метанола при 300—400 °C и 2-3 МПа в присутствии гетерогенных катализаторов — алюмосиликатов — степень превращения метанола в диметиловый эфир — 60 % или цеолитов — селективность процесса близка к 100 %. Диметиловый эфир (C2H6O) — экологически чистое топливо без содержания серы, содержание оксидов азота в выхлопных газах на 90 % меньше, чем у бензина. Цетановое число диметилового дизеля более 55, при том что у классического нефтяного 38-53.
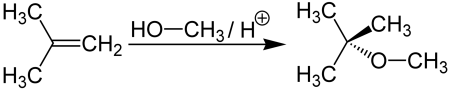
Метил-трет-бутиловый эфир получается при взаимодействии метанола с изобутиленом в присутствии кислых катализаторов (например, ионообменных смол):
Метил-трет-бутиловый эфир (C5H12O) применяется в качестве добавки к моторным топливам, повышающей октановое число бензинов (антидетонатор). Максимальное законодательное содержание МТБЭ в бензинах Европейского союза — 15 %, в Польше — 5 %. В России в среднем составе бензинов содержание МТБЭ составляет до 12 % для АИ92 и до 15 % для АИ95, АИ98.
Отдельным направлением является использование метанола для переэтерификации жиров в производстве биодизеля.
Гомологизация метанола
Гомологизация, то есть превращение органического соединения в свой гомолог путём внедрения одной или нескольких метиленовых групп, для спиртов была впервые осуществлена в 1940 году — на основе метанола каталитическим путём под воздействием высокого давления был синтезирован этанол:
Реакция гомологизации по своему механизму близка реакции гидроформилирования алкенов и в настоящее время с помощью модифицированных катализаторов кобальта и рутения и добавления йодид-ионов в качестве промоторов удаётся добиться 90 % выхода по этанолу.
Исходный метанол также получают из окиси углерода (катализаторы на основе оксидов меди и цинка, давление 5—10 МПа, температура 250 °C), так что общая схема выглядит следующим образом:
Побочными продуктами реакции в случае синтеза этанола будут ацетальдегид, этилен и диэтиловый эфир.
В 1940 году впервые была осуществлена катализируемая оксидом кобальта при давлении 600 атм реакция метанола с синтез-газом с образованием в качестве основного продукта этанола… Впоследствии эта реакция, названная гомологизацией, вызвала огромный интерес у химиков. Её привлекательность связана с возможностью получения этилена из угольного сырья Применение в качестве катализаторов карбонила кобальта Со2(СО)8 позволило понизить давление до 250 атм, при этом степень превращения метанола составила 70 %, а основной продукт — этанол образовывался с селективностью 40 %. В дальнейшем были предложены более селективные катализаторы на основе соединений кобальта и рутения с добавками фосфиновых лигандов и было установлено, что реакцию можно ускорить с помощью введения промоторов — иодид-ионов. В настоящее время удалось достичь селективности по этанолу 90 %. Хотя механизм гомологизации до конца не установлен, можно считать, что он близок к механизму карбонилирования метанола.
Биометанол
Промышленное культивирование и биотехнологическая конверсия морского фитопланктона рассматривается как одно из наиболее перспективных направлений в области получения биотоплива.
В начале 80-х рядом европейских стран совместно разрабатывался проект, ориентированный на создание промышленных систем с использованием прибрежных пустынных районов. Осуществлению этого проекта помешало общемировое снижение цен на нефть.
Первичное производство биомассы осуществляется путём культивирования фитопланктона в искусственных водоёмах, создаваемых на морском побережье.
Вторичные процессы представляют собой метановое брожение биомассы и последующее гидроксилирование метана с получением метанола.
Основными доводами в пользу использования микроскопических водорослей являются следующие:
- высокая продуктивность фитопланктона (до 100 т/га в год);
- в производстве не используются ни плодородные почвы, ни пресная вода;
- процесс не конкурирует с сельскохозяйственным производством;
- энергоотдача процесса достигает 14 (чего?) на стадии получения метана и 7 (чего?) на стадии получения метанола;
С точки зрения получения энергии данная биосистема имеет существенные экономические преимущества по сравнению с другими способами преобразования солнечной энергии.
Метанол в качестве топлива
При применении метанола в качестве топлива следует отметить, что объёмная и массовая энергоёмкость (теплота сгорания) метанола (удельная теплота сгорания = 22,7 МДж/кг) на 40—50 % меньше, чем бензина, однако при этом теплопроизводительность спиртовоздушных и бензиновых топливовоздушных смесей при их сгорании в двигателе различается незначительно по той причине, что высокое значение теплоты испарения метанола способствует улучшению наполнения цилиндров двигателя и снижению его теплонапряженности, что приводит к повышению полноты сгорания спиртовоздушной смеси. В результате этого мощность двигателя повышается на 7—9 %, а крутящий момент на 10—15 %. Двигатели гоночных автомобилей, работающих на метаноле с более высоким октановым числом, чем бензин, имеют степень сжатия, превышающую 15:1, в то время как в обычном ДВС с искровым зажиганием степень сжатия для неэтилированного бензина как правило, не превышает 11,5:1. Метанол может использоваться как в классических двигателях внутреннего сгорания, так и в специальных топливных элементах для получения электричества.
Отдельно следует отметить увеличение индикаторного КПД при работе классического ДВС на метаноле по сравнению с его работой на бензине. Такой прирост вызван снижением тепловых потерь и может достигать единиц процентов.
| Топливо | Плотность энергии | Смесь воздуха с топливом | Удельная энергия смеси воздуха | Удельная теплота испарения | Октановое число (RON) | Октановое число (MON) |
|---|---|---|---|---|---|---|
| Бензин | 32 МДж/л | 14,6 | 2,9 МДж/кг воздух | 0,36 МДж/кг | 91—99 | 81—89 |
| Бутанол-1 | 29,2 МДж/л | 11,1 | 3,2 МДж/кг воздух | 0,43 МДж/кг | 96 | 78 |
| Этанол | 19,6 МДж/л | 9,0 | 3,0 МДж/кг воздух | 0,92 МДж/кг | 132 | 89 |
| Метанол | 16 МДж/л | 6,4 | 3,1 МДж/кг воздух | 1,2 МДж/кг | 156 | 92 |
- Метанол травит алюминий. Проблемным является использование алюминиевых карбюраторов и инжекторных систем подачи топлива в ДВС. Это относится в основном к метанолу-сырцу, содержащему значительные количества примесей муравьиной кислоты и формальдегида. Технически чистый метанол, содержащий воду, начинает реагировать с алюминием при температуре выше 50 °C, а с обычной углеродистой сталью не реагирует вовсе.
- Гидрофильность. Метанол втягивает воду, что является причиной расслоения топливных смесей бензин-метанол.
- Метанол, как и этанол, повышает пропускную способность пластмассовых испарений для некоторых пластмасс (например, плотного полиэтилена). Эта особенность метанола повышает риск увеличения эмиссии летучих органических веществ, что может привести к уменьшению концентрации озона и усилению солнечной радиации.
- Уменьшенная летучесть при холодной погоде: моторы, работающие на чистом метаноле, могут иметь проблемы с запуском при температуре ниже +10 °C и отличаться повышенным расходом топлива до достижения рабочей температуры. Данная проблема однако, легко решается добавлением в метанол 10—25 % бензина.
Низкий уровень примесей метанола может быть использован в топливе существующих транспортных средств с использованием надлежащих ингибиторов коррозии. Т. н. европейская директива качества топлива (European Fuel Quality Directive) позволяет использовать до 3 % метанола с равным количеством присадок в бензине, продаваемом в Европе. Сегодня в Китае используется более 1000 млн галлонов метанола в год в качестве транспортного топлива в смесях низкого уровня, используемых в существующих транспортных средств, а также высокоуровневые смеси в транспортных средствах, предназначенных для использования метанола в качестве топлива.
Помимо применения метанола в качестве альтернативы бензина существует технология применения метанола для создания на его базе угольной суспензии, которая в США имеет коммерческое наименование «метакол» (methacoal). Такое топливо предлагается как альтернатива мазута, широко используемого для отопления зданий (Топочный мазут). Такая суспензия в отличие от водоуглеродного топлива не требует специальных котлов и имеет более высокую энергоемкость. С экологической точки зрения такое топливо имеет меньший «углеродный след», чем традиционные варианты синтетического топлива получаемого из угля с использованием процессов, где часть угля сжигается во время производства жидкого топлива.
Свойства метанола и его реакции
Метанол — бесцветная жидкость с алкогольным запахом (запах этилового спирта). Температура кипения +64,7 °C.
Удельный вес при 0°/0° = 0,8142 (Копп); при 15°/15° = 0,79726; при 25°/25° = 0,78941 (Perkin); при 64,8°/4° = 0,7476 (Шифф); при 0°/4° = 0,81015; при 15,56°/4° = 0,79589 (Dittmar и Fawsitt). Капиллярная постоянная при температуре кипения a ² =5,107 (Шифф); Критическая температура 241,9° (Шмидт). Упругость пара при 15° = 72,4 мм; при 29,3° = 153,4 мм; при 43° = 292,4 мм; при 53° = 470,3 мм; при 65,4° = 756,6 мм (Д. Коновалов). Теплота горения равна 170,6, теплота образования 61,4 (Штоман, Клебер и Лангбейн).
Метанол смешивается во всех отношениях с водой, этиловым спиртом и эфиром; при смешении с водой происходит сжатие и разогревание. Горит синеватым пламенем. Подобно этиловому спирту — сильный растворитель, вследствие чего во многих случаях может заменять этиловый спирт. Безводный метанол, растворяя небольшое количество медного купороса, приобретает голубовато-зеленое окрашивание, поэтому безводным медным купоросом нельзя пользоваться для открытия следов воды в метаноле; но он не растворяет CuSO4∙7H2O (Клепль).
Метанол (в отличие от этанола) с водой не образует азеотропной смеси, в результате чего смеси вода-метанол могут быть разделены ректификационной перегонкой. Температура кипения водных растворов метанола:
| Молярная доля метанола % | Т кип. °C, 760 мм. рт. ст. |
|---|---|
| 0 | 100 |
| 5 | 92,8 |
| 10 | 88,3 |
| 15 | 84,8 |
| 20 | 82 |
| 25 | 80,1 |
| 30 | 78,2 |
| 35 | 76,8 |
| 40 | 75,6 |
| 45 | 74,5 |
| 50 | 73,5 |
| 55 | 72,4 |
| 60 | 71,6 |
| 65 | 70,7 |
| 70 | 69,8 |
| 75 | 68,9 |
| 80 | 68 |
| 85 | 67,1 |
| 90 | 66,3 |
| 95 | 65,4 |
| 100 | 64,6 |
Метанол дает со многими солями соединения, подобные кристаллогидратам (сольваты), например: CuSO4 ∙ 2CH3OH; LiCl ∙ 3CH3OH; MgCl2 ∙ 6CH3OH; CaCl2 ∙ 4CH3OH представляет собой шестисторонние кристаллы, разлагаемые водой, но не разрушаемые нагреванием до 100° (Kane). Соединение BaO ∙ 2CH3OH ∙ 2H2O получается в виде блестящих призм при растворении BaO в водном метаноле и испарении на холоде полученной жидкости при комнатной температуре (Форкранд).
С едкими щелочами метанол образует соединения 5NaOH ∙ 6CH3OH; 3KOH ∙ 5CH3OH (Геттиг). При действии металлических калия и натрия легко даёт алкоголяты, присоединяющие к себе кристаллизационный метанол и иногда воду.
При пропускании паров метанола через докрасна накалённую трубку получается C2H2 и другие продукты (Бертло). При пропускании паров метанола над накалённым цинком получается окись углерода, водород и небольшие количества болотного газа (Jahn). Медленное окисление паров метанола при помощи раскаленной платиновой или медной проволоки представляет лучшее средство для получения больших количеств формальдегида: 2CH3OH+O2=2HCHO+2H2O. При действии хлористого цинка и высокой температуры метанол даёт воду и алканы, а также небольшие количества гексаметилбензола (Лебедь и Грин). Метанол, нагретый с нашатырём в запаянной трубке до 300°, даёт моно-, ди- и триметиламины (Бертло).
При пропускании паров метанола над KOH при высокой температуре выделяется водород и образуются последовательно формиат, ацетат и, наконец, карбонат калия.
Концентрированная серная кислота даёт метилсерную кислоту CH3HSO4, которая при дальнейшем нагревании с метанолом даёт метиловый эфир. При перегонке метанола с избытком серной кислоты в отгон переходит диметилсерная кислота (CH3)2SO4. При действии серного ангидрида SO3 получается CH(OH)(SO3H)2 и CH2(SO3H)2 (см. Метилен).
Метанол при действии соляной кислоты, пятихлористого фосфора и хлористой серы даёт хлористый метил CH3Cl. Действием HBr и H2SO4 получают бромистый метил. Подкисленный 5%-й серной кислотой и подвергнутый электролизу, метанол даёт CO2, СО, муравьинометиловый эфир, метилсерную кислоту и метилаль CH2(OCH3)2 (Ренар). При нагревании метанола с хлористо-водородными солями ароматических оснований (анилином, ксилидином, пиперидином) легко происходит замещение водорода в бензольном ядре метилом (Гофман, Ладенбург); реакция имеет большое техническое значение при приготовлении метилрозанилина и других искусственных пигментов.
Нахождение в природе
В свободном состоянии метиловый спирт встречается в природе лишь изредка и в очень небольших количествах (например в эфирных маслах), но производные его распространены довольно широко. Так, например, многие растительные масла содержат сложные эфиры метилового спирта: масла гаултерии — метиловый эфир салициловой кислоты C6H4(OH)COOCH3, масло жасмина — метиловый эфир антраниловой кислоты C6H4(NH2)COOCH3. Простые эфиры метилового спирта чрезвычайно часто встречаются среди природных веществ, например природных красителей, алкалоидов и т. п.
В промышленности метиловый спирт раньше получали исключительно путём сухой перегонки дерева. В жидких погонах, так называемом «древесном уксусе», наряду с уксусной кислотой (10 %), ацетоном (до 0,5 %), ацетальдегидом, аллиловым спиртом, метилацетатом, аммиаком и аминами содержится также 1,5—3 % метилового спирта. Для отделения уксусной кислоты продукты сухой перегонки пропускают через горячий раствор известкового молока, задерживающий её в виде уксуснокислого кальция. Значительно труднее отделить метиловый спирт от ацетона, так как температуры кипения их очень близки (ацетон, т.кип. 56,5°; метиловый спирт, т.кип. 64,7°). Все же путём тщательной ректификации на соответствующих колоннах в технике удается почти полностью отделить метиловый спирт от сопутствующего ему ацетона. Неочищенный метиловый спирт называется также «древесным спиртом».
Токсичность
Метанол — опаснейший яд, приём внутрь порядка 10 мл метанола может приводить к тяжёлому отравлению (одно из последствий — слепота), попадание в организм более 80-150 миллилитров метанола (1-2 миллилитра чистого метанола на килограмм тела) обычно смертельно. LD50 для животных — от единиц до десятка г/кг. Токсический эффект метанола развивается на протяжении нескольких часов, и эффективные антидоты способны уменьшить наносимый вред. Опасен для жизни не только чистый метанол, но и жидкости, содержащие этот яд даже в сравнительно небольшом количестве.
В США максимальное допустимое суточное употребление метанола (референтная доза), подразумевая несвязанное с какими-либо эффектами на здоровье, установлено в размере 2 мг на кг веса тела (с 1988 года).
Предельно допустимая концентрация метанола в воздухе рабочей зоны равна 5 мг/м³ (у изопропилового спирта 10 мг/м³, у этанола — 1000 мг/м³), ПДК в воздухе населенных мест равна 1,0 мг/м³ (у изопропилового спирта 0,6 мг/м³, у этанола — 5 мг/м³).
Наиболее легкая форма отравления характеризуется наличием головной боли, общей слабостью, недомоганием, ознобом, тошнотой, рвотой.
Токсичность метанола состоит в том, что при попадании в организм он с течением времени окисляется до ядовитого формальдегида, который вызывает слепоту, вредно влияет на нервную систему, вступает в реакции с белками. Происходит так называемый летальный синтез.
Особая опасность метанола связана с тем, что по запаху и вкусу он неотличим от этилового спирта, из-за чего и происходят случаи его употребления внутрь. Йодоформная реакция: с этиловым спиртом выпадет йодоформ жёлтого цвета, а с метанолом ничего не выпадает (реакция не подходит для определения содержания метанола в растворе этанола).
Как указано в руководстве для врача скорой медицинской помощи, при отравлении метанолом антидотом является этанол, который вводится внутривенно в форме 10 % раствора капельно или 30—40 % раствора перорально из расчёта 1—2 грамма раствора на 1 кг веса в сутки. Полезный эффект в этом случае обеспечивается отвлечением фермента АДГ I на окисление экзогенного этанола.
Следует учесть, что при недостаточно точном диагнозе за отравление метанолом можно принять алкогольную интоксикацию, отравление 1,2-дихлорэтаном или четырёххлористым углеродом — в этом случае введение дополнительного количества этилового спирта опасно.
Отравления метанолом довольно часты. Так, в США в течение 2013 года зафиксировано 1747 случаев.
Массовые отравления метанолом
Известно множество массовых отравлений метанолом. Источником метанола могут быть фальсифицированные незамерзающие жидкости для автомобилей, контрафактный алкоголь, метанол, выдаваемый за этиловый спирт.
- Массовое отравление метанолом в Испании в начале 1963 года; официальное число погибших 51 человек, однако существуют оценки в диапазоне от 1000 до 5000 человек.
- Массовое отравление метанолом в Бангалоре (Индия) в июле 1981 года. Число погибших — 308 человек.
- Массовое отравление вином с добавкой метанола в Италии весной 1986 года; погибли 23 человека.
- Массовое отравление метанолом в Сальвадоре в октябре 2000 года вызвало смерть 122 человек. Власти подозревали теракт, поскольку в спиртных напитках на заводах-производителях метанол при расследовании инцидента не был выявлен.
- Массовое отравление метанолом 9—10 сентября 2001 года в городе Пярну (Эстония); 68 человек погибли.
- Массовое отравление метанолом в Чехии , Польше и Словакии в сентябре 2012 года; 51 человек погиб.
- Массовое отравление метанолом 17-20 декабря 2016 года в Иркутске (Россия). Число погибших — 78 человек.