Этан C2H6 – это предельный углеводород, содержащий два атома углерода в углеродной цепи. Бесцветный газ без вкуса и запаха, нерастворим в воде и не смешивается с ней.
- Гомологический ряд этана
- Строение этана
- Изомерия этана
- Химические свойства этана
- 1. Реакции замещения
- 1.1. Галогенирование
- 1.2. Нитрование этана
- 2. Дегидрирование этана
- 3. Окисление этана
- 3.1. Полное окисление – горение
- Получение этана
- 1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
- 2. Декарбоксилирование солей карбоновых кислот (реакция Дюма)
- 3. Гидрирование алкенов и алкинов
- 4. Синтез Фишера-Тропша
- 5. Получение этана в промышленности
- Уравнение реакции получения этана гидрированием этиленового углеводорода
- Получение этилена из этана является реакцией
- Цели разработки альтернативных методов получения этилена
- Окислительное дегидрирование этана
- Дегидратация биоэтанола
- Выводы
Гомологический ряд этана
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Самый первый представитель гомологического ряда алканов – метан CH4. , или Н–СH2–H.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Строение этана
В молекулах алканов встречаются химические связи C–H и С–С.
Связь C–H ковалентная слабополярная, связь С–С – ковалентная неполярная. Это одинарные σ-связи. Атомы углерода в алканах образуют по четыре σ-связи. Следовательно, гибридизация атомов углерода в молекулах алканов – sp 3 :
При образовании связи С–С происходит перекрывание sp 3 -гибридных орбиталей атомов углерода:
При образовании связи С–H происходит перекрывание sp 3 -гибридной орбитали атома углерода и s-орбитали атома водорода:
Четыре sp 3 -гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109 о 28′ друг к другу:
Это соответствует тетраэдрическому строению молекулы.
| Например, в молекуле этана C2H6 атомы водорода располагаются в пространстве в вершинах двух тетраэдров, центрами которых являются атомы углерода |
Изомерия этана
Для этана не характерно наличие изомеров – ни структурных (изомерия углеродного скелета, положения заместителей), ни пространственных.
Химические свойства этана
Этан – предельный углеводород, поэтому он не может вступать в реакции присоединения.
Для метана характерны реакции:
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для этана характерны радикальные реакции.
Этан устойчив к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагирует с концентрированными кислотами, щелочами, бромной водой.
1. Реакции замещения
В молекулах алканов связи С–Н более доступны для атаки другими частицами, чем менее прочные связи С–С.
1.1. Галогенирование
Этан реагирует с хлором и бромом на свету или при нагревании.
При хлорировании этана сначала образуется хлорэтан:
Хлорэтан может взаимодействовать с хлором и дальше с образованием дихлорэтана, трихлорэтана, тетрахлорметана и т.д.
1.2. Нитрование этана
Этан взаимодействует с разбавленной азотной кислотой по радикальному механизму, при нагревании и под давлением. Атом водорода в этане замещается на нитрогруппу NO2.
Например. При нитровании этана образуется преимущественно нитроэтан:2. Дегидрирование этанаДегидрирование – это реакция отщепления атомов водорода. В качестве катализаторов дегидрирования используют никель Ni, платину Pt, палладий Pd, оксиды хрома (III), железа (III), цинка и др. При дегидрировании алканов, содержащих от 2 до 4 атомов углерода в молекуле, разрываются связи С–Н у соседних атомов углерода и образуются двойные и тройные связи.
3. Окисление этанаЭтан – слабополярное соединение, поэтому при обычных условиях он не окисляется даже сильными окислителями (перманганат калия, хромат или дихромат калия и др.). 3.1. Полное окисление – горениеЭтан горит с образованием углекислого газа и воды. Реакция горения этана сопровождается выделением большого количества теплоты. Уравнение сгорания алканов в общем виде: При горении этана в недостатке кислорода может образоваться угарный газ СО или сажа С. Получение этана1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)Это один из лабораторных способов получения этана из хлорметана или бромметана. При этом происходит удвоение углеродного скелета.
Задание 1
Задание 2
Задание 3 Задание 4 Задание 5 Получение этилена из этана является реакциейэтан > этилен получение этана из этилена Этилен из этана можно получить дегидрированием: СН3-СН3 ——> СН2=СН2 + Н2. Самое смешное, что я сам бывший химик, но конкретных условий проведения такой реакции не знаю. Ведь различных химических реакций и процессов — миллионы, и реально химики хорошо знают только ту область, в которой работают. На практике (в лабораторной практике или в промышленности) такой процесс не проводится. Наверное нужно нагревание, градусов этак до 500 (Цельсия) и использование каких-либо катализаторов (металлов наподобие меди, никеля, платины, палладия). Этан из этилена получают по обратной реакции, называется гидрирование. СН2=СН2 + Н2 ——> СН3-СН3. Условия проведения примерно те же, что и для дегидрирования, разве что отличается тем, что гидрирование проводится под избыточным давлением водорода, возможно даже достаточно большим. Разделы: Химия Класс: Цель: изучить строение, свойства, получение и применение этенов. Оборудование и реактивы. Компьютер, проектор, экран, штатив с пробирками, спиртовка, лабораторный штатив, спички, этиловый спирт, Н2SO4 (конц.), кипелка (прокаленный песок), бромная вода, раствор KMnO4, образцы полиэтиленовой пленки, гранулированный полиэтилен. Ознакомление учащихся с целью урока. Урок начинается с повторения строения молекулы этилена и гомологического ряда этиленовых углеводородов. Затем учащиеся выполняют задания: 1. Сопоставьте названия и состав предельных и непредельных углеводородов. Предельные углеводороды ряда метана Непредельные углеводороды ряда этилена
2.Данное вещество является изомером пентена-1. Определите вид изомерии данного вещества: Ученики выполняют задание, озвучивают с места ответ, обсуждают возможные ошибки. II.Изучение нового материала 1. Лабораторный опыт. Изучение свойств полиэтилена. Учитель формулирует цель лабораторного опыта: изучить явление пластичности и химические свойства полимера. Учащиеся работают в парах. На экране появляется инструкция проведения лабораторного опыта. 1. Изучение явления пластичности. Кусочек полиэтилена закрепите в держателе, подержите его над пламенем спиртовки. Стеклянной палочкой измените форму размягченного полимера, затем дайте ему остыть. Попытайтесь изменять его форму при обычной температуре. 2. Изучение химических свойств полимера. Гранулы полиэтилена поместите в пробирку с раствором перманганата калия. Происходит ли изменение окраски раствора? Поместите кусочки полимера в пробирки, содержащие 1 миллилитр растворов серной кислоты и гидроксида натрия. Наблюдаются ли химические реакции? На основе проделанных опытов учащиеся делают выводы о свойствах полимера. Учитель объясняет, что свойства полимера размягчаться при нагревании и в этом состоянии легко изменять свою форму, а затем сохранять ее при охлаждении называют термопластичностью. 2. История открытия непредельных углеводородов. Учащиеся готовят к уроку сообщения об истории открытия этиленовых углеводородов. На экране появляются тезисы. 1669г. Немецкий ученый Иоганн Бехер, нагревая этиловый спирт с серной кислотой, получил неизвестный ранее газ, названный “газ Бехера” 1795г. Голландский химик И. Дейман подробно изучил “газ Бехера”. Его состав: углерод и водород, при взаимодействии с хлором превращается в маслянистую жидкость – 1,2 дихлорэтан. Так произошло название ОЛЕФИНЫ, что означает МАСЛОРОДНЫЙ. 3. Получение этилена в лаборатории. Доказательство наличия этена. Учитель демонстрирует опыт по получению этилена в лаборатории. На экране — уравнение реакции дегидратации этанола: Для доказательства наличия этилена полученный газ пропускают через раствор перманганата калия, фиолетовый раствор KMnO4 обесцвечивается, при этом образуется двухатомный спирт этиленгликоль. При пропускании этилена через бромную воду красно-бурый бром быстро обесцвечивается. Это качественные реакции на непредельные углеводороды. 4. Получение алкенов в промышленности. Этилен и его гомологи получают в промышленности в результате реакции дегидрирования: 5. Решение экологической задачи. Перед учениками ставится экологическая задача: какое влияние оказывают отходы полиэтилена и его производные на окружающую среду? Дети делают свои предположения, в результате дискуссии учащиеся приходят к выводу: отходы полиэтилена и его производные отрицательно влияют на окружающую среду, отравляя природу продуктами сгорания, вызывают гибель морских животных (зубатых китов и др.) при попадании полиэтилена внутрь организма, не разлагаются почвенными бактериями. 6.Применение этилена и его производных. Исходя из жизненного опыта, учащимся предлагается привести примеры применения этилена и его производных. Учащиеся приводят примеры. Затем учитель подводит итог: этилен и его производные используют для ускоренного созревания плодов (помидоров, груш, дынь, лимонов и т.д.), изготовления разовой посуды, синтетического каучука, антифризов, взрывчатых веществ, пластмасс, растворителей, пакетов, полиэтиленовой пленки, получения горючего. III. Закрепление нового материала. Самопроверка качества усвоения материала учащимися. По материалу урока учащимся предлагается выполнить тест. (Вопросы теста на экране). 1.В гомологическом ряду алкенов нормального строения четвертый по счету гомолог называется: 2.Укажите формулу пентена-2: 3. Пропен из пропилового спирта СН3-СН2-СН2-ОН можно получить в результате реакции: 4. Качественной реакцией на непредельные углеводороды является: а) реакция горения; б) взаимодействие с водородом; в) реакция гидратации; г) обесцвечивание бромной воды. 5. Этилен можно получить из этана в результате реакции: Затем на экране учитель показывает правильные ответы. Учащиеся проводят самоконтроль и выставляют оценки. IV.Подведение итогов урока 1.Этиленовые углеводороды отличаются от предельных по составу, строению и свойствам. 2.Экспериментальным путем установлено, что этилен химически активен, а полиэтилен — инертен. 3.Изучены способы получения этилена и его гомологов. 4.Отходы полиэтилена и его производные отрицательно влияют на окружающую среду. V. Домашнее задание Решите экологическую проблему утилизации отходов полиэтилена и его производных.
Опубликовано в журнале Химическая техника №11/2016 В последнее время все чаще стал возникать вопрос о малотоннажных установках производства этилена. Зачастую это связано с потребностью в обеспечении сырьем производств сопоплимеров. Большая удаленность потребителей и производств этилена друг от друга, сложности при транспортировке этилена все чаще заставляют большие компании задумываться об самостоятельных установках получения этилена. В таких случаях, как правило, рассматривают целесообразность строительства производства этилена путем пиролиза углеводородного сырья. При пиролизе углеводородов, кроме этилена, продуктами термической обработки являются метан, ацетилен, углеводородные фракции С3, С4, С5, С6+ и др. компоненты. Даже при пиролизе этана селективность по основному продукту – этилену, составляет не более 80% при конверсии этана 60-65 %. Наличие вышеуказанных продуктов требует их дальнейшей переработки, реализации, или утилизации. Выделение этилена полимеризационной чистоты из такой смеси продуктов требует высоких эксплуатационных и капитальных затрат. Для предприятий, нуждающихся исключительно в небольших количествах этилена и не имеющих потребности в побочных продуктах пиролиза (такие как производства полимеров/сополимеров) строительство установки пиролиза углеводородного сырья может быть крайне невыгодно по следующим причинам:
Спрос на этилен со стороны производств сополимеров гарантирует переработку этилена в более дорогие продукты. Переработка дешевого сырья в этилен и впоследствии в сополимеры в рамках одного промышленного комплекса позволит достичь наименьших значений себестоимости товарной продукции, и, следовательно, высокой прибыли от ее реализации.
В связи с вышеуказанными причинами все чаще в качестве способов малотоннажного производства этилена рассматриваются альтернативные методы получения этилена. Среди таких методов: выделение этилена из отходящих газов каталитического крекинга (при наличии поблизости НПЗ, эксплуатирующего каталитический крекинг), окислительное дегидрирование этана, окислительная димеризация метана, получение этилена из низших спиртов – этанола и метанола (рис. 1). ООО «ВНИИОС-наука» уже много лет работает в области промышленного производства этилена, пропилена и других продуктов нефтехимии. Компания участвует в модернизациях и разработках технологий различных методов получения этилена: как основного способа получения этилена – пиролиза, так и альтернативных методов получения этилена, в том числе выделение этилена из отходящих газов каталитического крекинга, окислительное дегидрирование этана, окислительная димеризация метана, получение этилена из этанола. По данным процессам имеются патенты и готовые разработки. Цели разработки альтернативных методов получения этиленаВ данной статье более подробно остановимся на двух альтернативных методах получения этилена: окислительном дегидрировании этана и дегидратации биоэтанола. С учетом указанных недостатков пиролиза в условиях низкой производительности, требования к данным альтернативным процессам очевидны:
Окислительное дегидрирование этанаРеакция окислительного дегидрирования этана (ОДЭ) производится по следующей формуле: C2H6 + 1/2O2 = C2H4 + H2O (1) В качестве окислителя может применяться как концентрированный кислород, так и кислород в составе воздуха. Последние опыты по окислительному дегидрированию этана показали следующие результаты (в качестве окислителя применялся кислород с концентрацией 99,5 %):
С использованием полученных данных была разработана схема выделения этилена из контактного газа окислительного дегидрирования этана, основанная на абсорбционном методе извлечении этан-этиленовой фракции. Принципиальная схема получения этилена путем ОДЭ представлена на рис. 2.
Схема включает реакционный узел Р-1, узел водной отмывки К-1, стадию предварительного удаления СО2 путем аминовой хемосорбции К-2, компримирования М-1, осушку С-1, колонны абсорбции и десорбции ЭЭФ (соответственно К-3 и К-4), колонну выделения товарного этилена К-5. Разработанная технология является достаточно гибкой, чтобы проводить окислительное дегидрирование как концентрированным кислородом, так и кислородом воздуха или какой-либо промежуточной смесью воздухкислород. Для любого случая в зависимости от применяемого окислителя в представленной технологии решена проблема образования взрывоопасных смесей кислород-углеводороды-монооксид углерода, что делает технологию простой и безопасной. Кроме того, гибкость технологии позволяет использовать различные катализаторы окислительного дегидрирования этана, т.е. при появлении новых катализаторов, являющихся по тем или иным характеристикам лучше ныне существующих, их также можно применять в данной технологической схеме. Благодаря разработанной технологии, а также применению абсорбционной технологии выделения ЭЭФ из контактного газа, исключающей использование хладагентов с температурой ниже минус 37 °С, удалось достичь приемлемых для промышленной установки показателей эксплуатационных параметров. При моделировании технологии были получены следующие результаты: Расходный коэффициент по сырью, т этана/т этилена 1,29 Расход электроэнергии, МВт⋅ч/т этилена 0,60 Степень извлечения этилена, % 98,5 Моделирование технологии ОДЭ с применением концентрированного кислорода показало значительно более низкие эксплуатационные затраты по сравнению с пиролизом этана (в качестве примера: потребление электроэнергии составляет соответственно 0,6 и 1,0). Кроме того, технология ОДЭ имеет значительно более простую схему выделения этилена: отсутствуют узлы каталитического удаления ацетилена, низкотемпературного (до минус 100 °С) удаления метана и водорода и другие. В связи с этим данный способ получения этилена претендует на получение высоких результатов при дальнейших более подробных оценках экономической целесообразности реализации данного проекта. Дегидратация биоэтанолаРеакция дегидратации этанола производится по следующей формуле: C2H5OH = C2H4 + H20 (2) Последние опыты по окислительному дегидрированию этилена показали следующие результаты:
Таким образом, была разработана технология выделения этилена из реакционных газов, принципиальная схема технологии представлена на рис. 3.
Схема включает узел конденсации реакционной воды Т-1, предварительную осушку С-1, узел удаления кислородсодержащих примесей А-1, компримирования М-1, колонну выделения товарного этилена К-1 и стадию доочистки этилена от остаточных примесей А-2. Благодаря высокой селективности процесса, а также отсутствию стадии удаления «легких» компонентов, технология выделения этилена из реакционных газов дегидратации биоэтанола при моделировании показала весьма привлекательные коэффициенты эксплуатационных параметров. Например, потребление электроэнергии составило 0,35 МВт/т. этилена. Учитывая простоту разделения газов дегидратации биоэтанола, низкий расходный коэффициент по сырью, а также низкие эксплуатационное параметры, можно сделать следующие выводы:
В РФ имеется большой потенциал для производства биоэтанола как для нужд нефтехимии, так и для использования в качестве присадок к жидкому топливу, однако из-за акцизной политики государства биоэтанол не может быть реализован как продукт, так как это повлечет за собой высокую себестоимость биоэтанола ввиду попадания под акциз (доля акциза достигает значений до 90 %). Данный фактор затрудняет возможность использования биоэтанола в качестве сырья для получения этилена, так как требует реализацию такого процесса в рамках предприятия, также производящего биоэтанол, что влечет за собой дополнительные трудности, связанные с различной спецификой аграрных и нефтехимических производств. ВыводыРазработанные технологии получения этилена позволяют достичь выгодных эксплуатационных параметров при достаточно простом конструктивном оформлении, являются гибкими и безопасными при эксплуатации. ООО «ВНИИОС-наука» может провести работы как по описанным в статье процессам, так и по другим альтернативным методам получения этилена: выделение этилена из сухого газа, окислительная димеризация метана. Проводится весь цикл работ по разработке и реализации технологии до этапа пуска установки. |










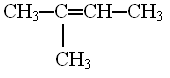
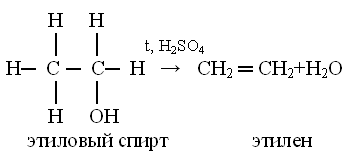
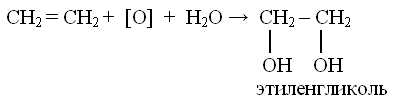
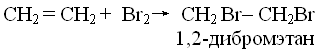
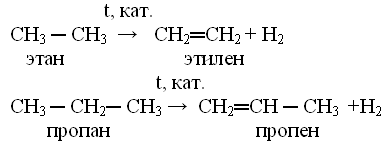
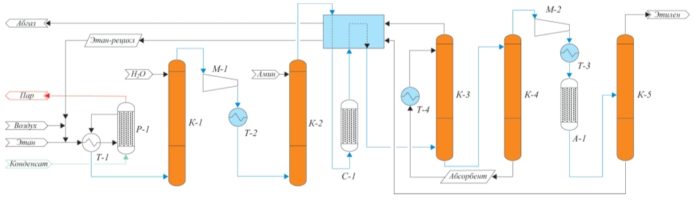
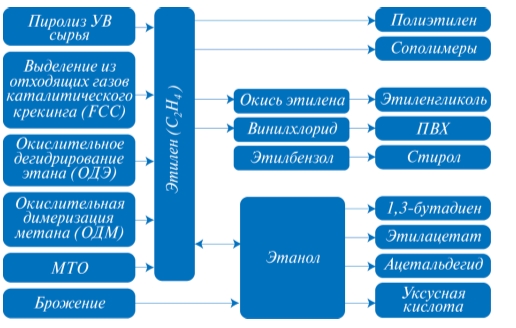 Рис. 1. Способы получения и использования этилена в промышленности
Рис. 1. Способы получения и использования этилена в промышленности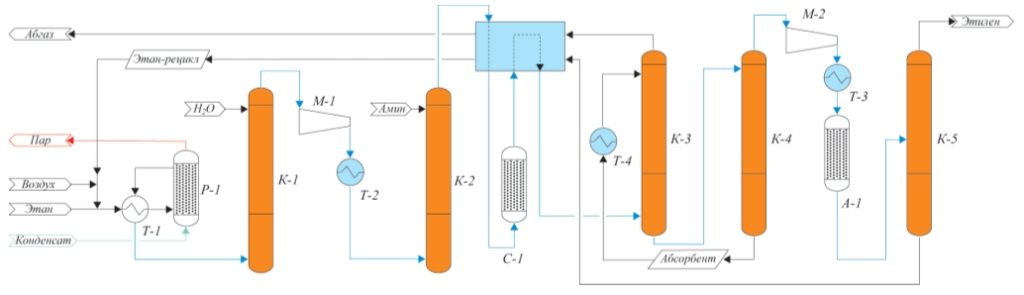
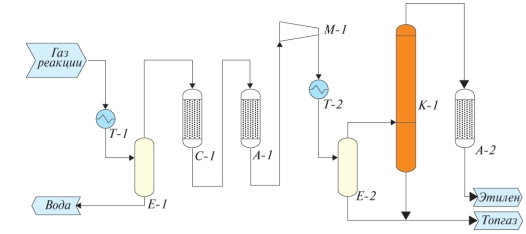 Рис. 3. Принципиальная схема технологии выделения этилена из реакционных газов дегидратации биоэтанола
Рис. 3. Принципиальная схема технологии выделения этилена из реакционных газов дегидратации биоэтанола