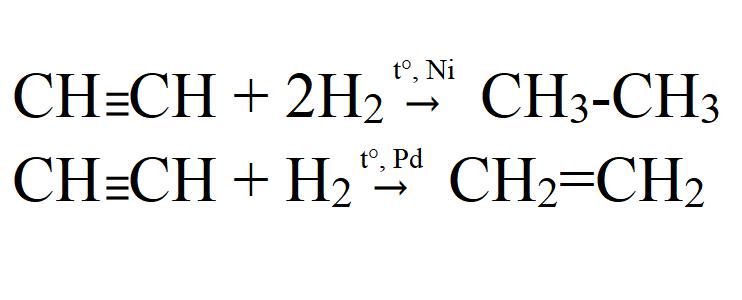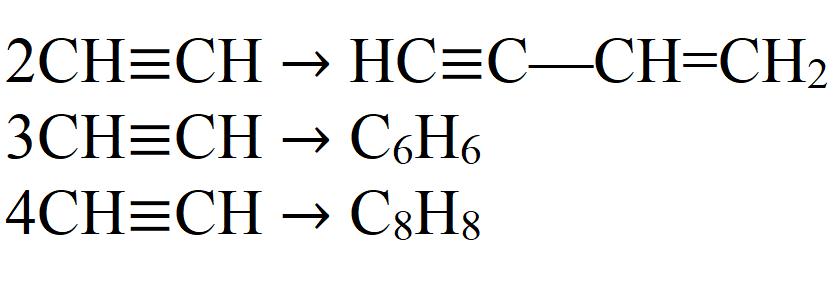- Содержание
- История получения ацетилена
- Получение ацетилена
- Применение ацетилена
- Горение ацетилена
- Хранение и транспортировка ацетилена
- Физические свойства ацетилена
- Коэффициенты перевода объема и массы С2Н2 при Т=15°С и Р=0,1 МПа
- Коэффициенты перевода объема и массы С2Н2 при Т=0°С и Р=0,1 МПа
- Ацетилен в баллоне
- Ацетилен — формула, свойства, получение, преимущества
- Ацетилен
- Меры безопасности при работе с ацетиленом
- Получение
- В лаборатории
- В промышленности
- Получение пиролизом
- Карбидный метод
- Как синтезировался ацетилен
- Химические свойства ацетилена
- Ацетилен сегодня: способы получения
- Применение ацетилена при сварке
- Преимущества
- Химические и физические свойства
- Состав
- Технология и режимы сварки
- Заключение
- Взрывоопасность ацетилена и безопасность при обращении с ним:
- Acetyl
Содержание
При нормальном давлении и температуре от -82,4°С (190,6 К) до -84,0°С (189 К) переходит в жидкое состояние, а при температуре -85°С (188 К) затвердевает, образуя кристаллы плотностью 0,76 кг/м 3 . Жидкий и твердый ацетилен легко взрывается от трения, механического или гидравлического удара и действия детонатора. Технический ацетилен при нормальных давлении и температуре представляет собой бесцветный газ с резким специфическим чесночным запахом из-за содержащихся в нем примесей в виде сернистого водорода, аммиака, фосфористого водорода и др.
История получения ацетилена
В 1836 г. в Бристоле на заседании Британской ассоциации Эдмунд Дэви (Edmund Davy), профессор химии Дублинского Королевского общества и двоюродный брат Гемфри Дэви (Humphry Davy), сообщил:
. При попытке получить калий, сильно нагревая смесь прокаленного винного камня с древесным углем в большом железном сосуде, я получил черное вещество, которое легко разлагалось водой и образовывало газ, оказавшийся новым соединением углерода и водорода. Этот газ горит на воздухе ярким пламенем, более густым и светящимся даже сильнее, чем пламя маслородного газа (этилена). Если подача воздуха ограничена, горение сопровождается обильным отложением сажи. В контакте с хлором газ мгновенно взрывается, причем взрыв сопровождается большим красным пламенем и значительными отложениями сажи. Дистиллированная вода поглощает около одного объема нового газа, однако при нагревании раствора газ выделяется, по-видимому, не изменяясь. Для полного сгорания нового газа необходимо 2,5 объема кислорода. При этом образуются два объема углекислого газа и вода, которые являются единственными продуктами горения. Газ содержит столько же углерода, что и маслородный газ, но вдвое меньше водорода. Он удивительно подойдет для целей искусственного освещения, если только его удастся дешево получать.
Дэви получил карбид калия К2С2 и обработал его водой.
В статье о получении карбида кальция мы писали о том, что его «двууглеродистый водород» впервые был назван ацетиленом французским химиком Пьером Эженом Марселеном Бертло (Marcellin Berthelot) в 1860 г. Только через 60 лет после открытия Дэви предсказанное им использование ацетилена для освещения явилось первым толчком для его промышленного получения.
Получение ацетилена
Получение ацетилена производится двумя основными способами:
- в результате реакции карбида кальция и воды
- из метана путем сжигания в смеси с кислородом в специальных реакторах при температуре 1300-1500°C
А вот какой способ сейчас более распространён можно узнать из статьи о получении ацетилена.
Применение ацетилена
Применение ацетилена при газовой сварке обусловлено тем, что у него самая большая температуры горения. Но он также нашел свое применение в химической отрасли для получения пластмасс, синтетического каучука, уксусной кислоты и растворителей. Более подробный ответ по данному вопросу можно найти в статье о применении ацетилена.
Горение ацетилена
Для полного сгорания 1 м 3 ацетилена по вышеуказанной реакции теоретически требуется 2,5 м 3 кислорода или = 11,905 м 3 воздуха. При этом выделяется тепло Q1 ? 312 ккал/моль. Высшая теплотворная способность 1 м 3 С2Н2 при 0°C и 760 мм рт. ст., определенная в газовом калориметре, составляет QВ = 14000 ккал/м 3 (58660 кДж/м 3 ), что соответствует расчетной:
312?1,1709?1000/26,036 = 14000 ккал/м 3
Низшая теплотворная способность при тех же условиях может быть принята QH = 13500 ккал/м 3 (55890 кДж/м 3 ).
Практически для горения в горелках при восстановительном пламени в горелку подается не 2,5 м 3 кислорода на 1 м 3 ацетилена, а всего лишь от 1 до 1,2 м 3 , что примерно соответствует неполному сгоранию по реакции:
где Q2 ? 60 ккал/моль или 2300 ккал/кгС2H2. Остальные 1,5-1,3 м 3 кислорода поступают в пламя из окружающего воздуха, в результате чего в наружной оболочке пламени протекает реакция:
Реакция неполного горения ацетилена протекает на внешней оболочке светящегося внутреннего конуса пламени, причем под влиянием высокой температуры на внутренней поверхности конуса происходит распад С2Н2 на его составляющие по реакции:
где Q4?54 ккал/моль или 2070 ккал/кг С2H2.
Таким образом, общая полезная теплопроизводительность пламени применительно к сварочным процессам представляет собой сумму тепла, выделяемого при распаде С2Н2, и тепла, выделяемого при неполном сгорании, что составляет Q4 + Q2 = 2070 + 2300 = 4370 ккал/кг или 4370?1,1709 ? 5120 ккал/м 3 .
При содержании С2Н2 в смеси около 45% (т. е. при отношении кислорода к ацетилену, примерно равном 1,25) достигается максимальная температура горения ацетилена, которая составляет 3200°С.
Следовательно, температура пламени изменяется в зависимости от состава смеси.
При содержании 27% С2Н2 достигается максимальная скорость воспламенения ацетилено-кислородной смеси, которая равна 13,5 м/сек.
Следовательно, в зависимости от состава смеси также изменяется и скорость воспламенения.
Данные зависимостей скорости воспламенения и температуры пламени и от содержания в ней ацетилена представлены ниже в таблице.
| Содержание С2Н2 в смеси в объемных процентах | 12 | 15 | 20 | 25 | 27 | 30 | 32 | 35 | 40 | 45 | 50 | 55 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Максимальная температура горения ацетилена, °С | — | 2920 | 2940 | 2960 | 2970 | 2990 | 3010 | 3060 | 3140 | 3200 | 3070 | 2840 |
| Скорость воспламенения смеси, м/сек | 8,0 | 10,0 | 11,8 | 13,3 | 13,5 | 13,1 | 12,5 | 11,3 | 9,3 | 7,8 | 6,7 | — |
Необходимо понимать, что полное сгорание ацетилено-воздушной смеси достигается при наличии в ней не более 1?100/(1+11,905)=7,75% ацетилена (так называемая стехиометрическая смесь). При этом продуктами реакции являются только углекислый газ (СО2) и вода (H2О). При содержании ацетилена более 17,37% в виде сажи выделяется свободный углерод.
С увеличение процентного содержание ацетила выделение сажи также возрастает (коптящее пламя), а при 81% С2Н2 — процесс горения прекращается или не возникает.
Хранение и транспортировка ацетилена
Ацетилен выпускают по ГОСТ 5457 растворенным и газообразным. Хранят и транспортируют его в растворенном состоянии в специальных стальных баллонах по ГОСТ 949, заполненных пористой, пропитанной ацетоном массой. Ацетилен, растворенный в ацетоне не склонен к взрывчатому распаду.
Баллоны окрашены в серый цвет и надписью красными буквами «АЦЕТИЛЕН» на верхней цилиндрической части.
Максимальное давление ацетилена при заполнении баллона составляет 2,5 МПа (25 кгс/см 2 ), при отстое и охлаждении баллона до 20°С оно снижается до 1,9 МПа (19 кгс/см 2 ). При этом давлении в 40-литровый баллон вмещается 5-5,8 кг С2Н2 по массе (4,6-5,3 м 3 газа при 20°С и 760 мм рт. ст.).
Давление ацетилена в полностью наполненном баллоне изменяется при изменении температуры следующим образом:
| Температура, °С | -5 | 0 | 5 | 10 | 15 | 20 | 30 | 40 |
|---|---|---|---|---|---|---|---|---|
| Давление, МПа | 1,3 | 1,4 | 14 | 1,7 | 1,8 | 12 | 2,4 | 3,0 |
Другие требования техники безопасности можно узнать из статьи о классе опасности и мерах безопасности при работе с ацетиленом
Физические свойства ацетилена
Физические свойства ацетилена представлены в таблицах ниже.
Коэффициенты перевода объема и массы С2Н2 при Т=15°С и Р=0,1 МПа
| Масса, кг | Объем газа, м 3 |
|---|---|
| 1,109 | 1 |
| 1 | 0,909 |
Коэффициенты перевода объема и массы С2Н2 при Т=0°С и Р=0,1 МПа
| Масса, кг | Объем газа, м 3 |
|---|---|
| 1,176 | 1 |
| 1 | 0,850 |
Ацетилен в баллоне
| Наименование | Объем баллона, л | Масса газа в баллоне, кг | Объем газа (м 3 ) при Т=15°С, Р=0,1 МПа |
|---|---|---|---|
| С2Н2 | 40 | 5 | 4,545 |
Благодаря информации в таблице можно дать ответы на часто задаваемые вопросы:
- Сколько ацетилена в одном баллоне?
Ответ: в 40 л баллоне 5 кг или 4,545 м 3 ацетилена - Сколько весит баллон ацетилена?
Ответ:
58,5 кг — масса пустого баллона из углеродистой стали согласно ГОСТ 949;
18-20 кг — масса пористого материала, пропитанного ацетоном;
5,0 — кг масса С2Н2 в баллоне;
Итого: 58,5 + 20,0 + 5,0= 83,5 кг вес баллона с ацетиленом. - Сколько м 3 ацетилена в баллоне
Ответ: 4,545 м 3
Ацетилен — формула, свойства, получение, преимущества
Ацетилен (или по международной номенклатуре — этин) — это непредельный углеводород, принадлежащий к классу алкинов. Химическая формула ацетилена — C2H2. Атомы углерода в молекуле соединены тройной связью. Он является первым в своем гомологическом ряду. Представляет собой бесцветный газ. Очень огнеопасен.
Ацетилен
Название этого вещества связано со словом «уксус». Сегодня это единственный широко используемый в промышленности газ, горение и взрыв которого возможны в отсутствие кислорода или других окислителей. Сгорая в кислоте, он дает очень горячее пламя — до 3100°С.
Меры безопасности при работе с ацетиленом
- содержание ацетилена в воздухе рабочей зоны необходимо непрерывно контролировать автоматическими приборами, сигнализирующими о превышении допустимой взрывобезопасной концентрации ацетилена в воздухе, равной 0,46%;
- при работе с ацетиленовыми баллонами поблизости не должно быть открытого пламени или отопительной системы; запрещается работать с баллонами, находящимися в горизонтальном положении, с незакрепленными баллонами, с неисправными баллонами; необходимо использовать неискрящийся инструмент, освещение и электрическое оборудование только во взрывобезопасном исполнении;
- в случае обнаружения утечки ацетилена из баллона (по запаху и звуку) необходимо по возможности быстро закрыть вентиль баллона специальным неискрящимся ключом;
- при нагреве баллон с ацетиленом может взорваться с крайне разрушительными последствиями; в случае пожара необходимо по возможности удалить из опасной зоны холодные баллоны с ацетиленом, оставшиеся баллоны постоянно охлаждать водой или специальными составами до полного остывания; при загорании ацетилена, выходящего из баллона, необходимо по возможности быстро закрыть вентиль баллона специальным неискрящимся ключом и поливать баллон водой до полного остывания; при сильном возгорании пожаротушение необходимо производить с безопасного расстояния; при пожаротушении рекомендуется применять огнетушители с содержанием флегматизирующей концентрации азота 70% по объему, диоксида углерода 57% по объему, водяные струи, песок, сжатый азот, асбестовое полотно, токораспыленную пену и воду; при тушении сильного пожара используются огнезащитные костюмы, противогазы и т.п.
Получение
В лаборатории
В лаборатории, а также в газосварочном оборудовании, ацетилен получают действием воды на карбид кальция (Ф. Вёлер, 1862 год):
а также при дегидрировании двух молекул метана при температуре свыше 1400 °C:
В промышленности
В промышленности ацетилен получают гидролизом карбида кальция и пиролизом углеводородного сырья — метана или пропана с бутаном. В последнем случае ацетилен получают совместно с этиленом и примесями других углеводородов. Карбидный метод позволяет получать очень чистый ацетилен, но требует высокого расхода электроэнергии. Пиролиз существенно менее энергозатратен, т.к. для нагрева реактора используется сгорание того же рабочего газа во внешнем контуре, но в газовом потоке продуктов концентрация самого ацетилена низка. Выделение и концентрирование индивидуального ацетилена в таком случае представляет сложную задачу. Экономические оценки обоих методов многочисленны, но противоречивы.
Получение пиролизом
Электрокрекинг
Метан превращают в ацетилен и водород в электродуговых печах (температура 2000—3000 °С, напряжение между электродами 1000 В). Метан при этом разогревается до 1600 °С. Расход электроэнергии составляет около 13000 кВт•ч на 1 тонну ацетилена, что относительно много (примерно равно затрачиваемой энергии по карбидному методу) и потому является недостатком процесса. Выход ацетилена составляет 50 %.
Регенеративный пиролиз
Иное название — Вульф-процесс. Сначала разогревают насадку печи путём сжигания метана при 1350—1400 °С. Далее через разогретую насадку пропускают метан. Время пребывания метана в зоне реакции очень мало и составляет доли секунды. Процесс реализован в промышленности, но экономически оказался не таким перспективным, как считалось на стадии проектирования.
Окислительный пиролиз
Метан смешивают с кислородом. Часть сырья сжигают, а образующееся тепло расходуют на нагрев остатка сырья до 1600 °С. Выход ацетилена составляет 30—32 %. Метод имеет преимущества — непрерывный характер процесса и низкие энергозатраты. Кроме того, с ацетиленом образуется еще и синтез-газ. Этот процесс (Заксе-процесс или BASF-процесс) получил наиболее широкое внедрение.
Гомогенный пиролиз
Является разновидностью окислительного пиролиза. Часть сырья сжигают с кислородом в топке печи, газ нагревается до 2000 °С. Затем в среднюю часть печи вводят остаток сырья, предварительно нагретый до 600 °С. Образуется ацетилен. Метод характеризуется большей безопасностью и надёжностью работы печи.
Пиролиз в струе низкотемпературной плазмы
Процесс разрабатывается с 1970-х годов, но, несмотря на перспективность, пока не внедрён в промышленности. Сущность процесса состоит в нагреве метана ионизированным газом. Преимущество метода заключается в относительно низких энергозатратах (5000—7000 кВт•ч) и высоких выходах ацетилена (87 % в аргоновой плазме и 73 % в водородной).
Карбидный метод
Этот способ известен с XIX века, но не потерял своего значения до настоящего времени. Сначала получают карбид кальция, сплавляя оксид кальция и кокс в электропечах при 2500—3000 °С:
Известь получают из карбоната кальция:
Далее карбид кальция обрабатывают водой:
Получаемый ацетилен имеет высокую степень чистоты 99,9 %. Основным недостатком процесса является высокий расход электроэнергии: 10000—11000 кВт•ч на 1 тонну ацетилена.
Как синтезировался ацетилен
Впервые ацетилен получил в 1836 Эдмунд Дэви, двоюродный брат знаменитого Гемфри Дэви. Он подействовал водой на карбид калия: К2С2 + 2Н2О=С2Н2 + 2КОН и получил новый газ, который назвал двууглеродистым водородом. Этот газ был, в основном, интересен химикам с точки зрения теории строения органических соединений. Один из создателей так называемой теории радикалов Юстус Либих назвал группу атомов (т.е. радикал) С2Н3ацетилом.
На латыни acetum – уксус; молекула уксусной кислоты (С2Н3О+О+Н, как записывали тогда ее формулу) рассматривалась как производное ацетила. Когда французский химик Марселен Бертло в 1855 сумел получить «двууглеродистый водород» сразу несколькими способами, он назвал его ацетиленом. Бертло считал ацетилен производным ацетила, от которого отняли один атом водорода: С2Н3 – Н = С2Н2. Сначала Бертло получал ацетилен, пропуская пары этилена, метилового и этилового спирта через раскаленную докрасна трубку. В 1862 он сумел синтезировать ацетилен из элементов, пропуская водород через пламя вольтовой дуги между двумя угольными электродами. Все упомянутые методы синтеза имели только теоретическое значение, и ацетилен был редким и дорогим газом, пока не был разработан дешевый способ получения карбида кальция прокаливанием смеси угля и негашеной извести: СаО + 3С = СаС2 + СО. Это произошло в конце XIX века.
Тогда ацетилен стали использовать для освещения. В пламени при высокой температуре этот газ, содержащий 92,3% углерода (это своеобразный химический рекорд), разлагается с образованием твердых частичек углерода, которые могут иметь в своем составе от нескольких до миллионов атомов углерода. Сильно накаливаясь во внутреннем конусе пламени, эти частички обуславливают яркое свечение пламени — от желтого до белого, в зависимости от температуры (чем горячее пламя, тем ближе его цвет к белому).
Ацетиленовые горелки давали в 15 раз больше света, чем обычные газовые фонари, которыми освещали улицы. Постепенно они были вытеснены электрическим освещением, но еще долго использовались в небольших фонарях на велосипедах, мотоциклах, в конных экипажах.
В течение длительного времени ацетилен для технических нужд (например, на стройках) получали «гашением» карбида водой. Полученный из технического карбида кальция ацетилен имеет неприятный запах из-за примесей аммиака, сероводорода, фосфина, арсина.
Химические свойства ацетилена
Исходя из тройной связи ацетилена, для него будут характерны реакции присоединения и реакции полимеризации. Атомы водорода в молекуле ацетилена могут замещаться другими атомами или группами. Поэтому можно сказать, что ацетилен проявляет кислотные свойства. Разберем химические свойства ацетилена на конкретных реакциях.
- Гидрирование. Осуществляется при высокой температуре и в присутствии катализатора (Ni, Pt, Pd). На палладиевом катализаторе возможно неполное гидрирование.
- Галогенирование. Может быть как частичным, так и полным. Идет легко даже без катализаторов или нагревания. На свету хлорирование идет с взрывом. При этом ацетилен полностью распадается до углерода.
- Присоединение к уксусной кислоте и этиловому спирту. Реакции идут только в присутствии катализаторов.
- Присоединение синильной кислоты.
CH≡CH + HCN → CH2=CH-CN
- Взаимодействие ацетилена с металл-органическими соединениями.
CH≡CH + 2C2H5MgBr → 2C2H6 + BrMgC≡CMgBr
- Взаимодействие с металлическим натрием. Необходима температура 150 °C или предварительное растворение натрия в аммиаке.
2CH≡CH + 2Na → 2CH≡CNa + H2
- Взаимодействие с комплексными солями меди и серебра.
- Взаимодействие с амидом натрия.
CH≡CH + 2NaNH2 → NaC≡CNa + 2NH3
- Димеризация. При этой реакции две молекулы ацетилена объединяются в одну. Необходим катализатор — соль одновалентной меди.
- Тримеризация. В этой реакции три молекулы ацетилена образуют бензол. Необходим нагрев до 70 °C, давление и катализатор.
- Тетрамеризация. В результате реакции получается восьмичленный цикл — циклооктатетраен. Для этой реакции также требуется небольшой нагрев, давление и соответствующий катализатор. Обычно это комплексные соединения двухвалентного никеля.
Это далеко не все химические свойства ацетилена.
Ацетилен сегодня: способы получения
В промышленности ацетилен часто получают действием воды на карбид кальция.
Сейчас широко применяются методы получения ацетилена из природного газа – метана:
электрокрекинг (струю метана пропускают между электродами при температуре 1600°С и быстро охлаждают, чтобы предотвратить разложение ацетилена);
термоокислительный крекинг (неполное окисление), где в реакции используют теплоту частичного сгорания ацетилена.
Применение ацетилена при сварке
Ацетилен – основной горючий газ, используемый при газовой сварке, а также широко применяется для газовой резки (кислородной резки). Температура ацетилено-кислородного пламени может достигать 3300°C. Благодаря этому ацетилен по сравнению с более доступными горючими газами (пропан-бутаном, природным газом и др.) обеспечивает более высокое качество и производительность сварки.
Снабжение постов ацетиленом для газовой сварки и резки может осуществляться
- от баллонов с ацетиленом и
- от ацетиленового генератора.
Для хранения ацетилена обычно используются стандартные баллоны емкостью 40 л, окрашенные в белый цвет, с надписью «Ацетилен» красного цвета (ПБ 10-115-96, ГОСТ 949-73). Согласно ГОСТ 5457-75 для газопламенной обработки металлов применяется технический ацетилен растворенный марки Б и газообразный.
Таблица. Характеристики марок технического ацетилена (ГОСТ 5457-75), используемого при сварке и резке.
| Параметр | Ацетилен технический | ||
| растворенный марки Б | газообразный | ||
| первого сорта | второго сорта | ||
| Объемная доля ацетилена C2H2, %, не менее | 99,1 | 98,8 | 98,5 |
| Объемная доля воздуха и других газов, малорастворимых в воде, %, не более | 0,8 | 1,0 | 1,4 |
| Объемная доля фосфористого водорода PH3, %, не более | 0,02 | 0,05 | 0,08 |
| Объемная доля сероводорода H2S, %, не более | 0,005 | 0,05 | 0,05 |
| Массовая концентрация водяных паров при давлении 101,3 кПа (760 мм рт. ст.) и температуре 20°С, г/м3, не более | 0,5 | 0,6 | не нормируется |
| что соответствует температуре насыщения, не выше (°C) | -24 | -22 | |
Баллоны заполнены пористой массой, пропитанной ацетоном. Ацетилен хорошо растворяется а ацетоне: при нормальной температуре и давлении в 1 л ацетона растворяется 23 л ацетилена (в 1 л бензина растворяется 5,7 л ацетилена, в 1 л воды – 1,15 л ацетилена). Пористая масса выполняет следующие функции:
- повышает безопасность при работе с баллоном – за счет пористой массы общий объем ацетилена разделен на отдельные ячейки; таким образом, вероятность распространения общего фронта горения и взрыва значительно уменьшается;
- позволяет повысить количество ацетилена в баллоне, ускорить процесс его растворения при заполнении баллона и выделении при отборе газа – поскольку при использовании пористой массы, пропитанной ацетоном, обеспечивается большая поверхность взаимного контакта между газом и ацетоном.
В качестве пористых масс могут применяться активированный уголь, пемза, волокнистый асбест.
Таблица. Допустимое давление газа в баллоне в зависимости от температуры (при номинальном давлении 1,9 МПа / +20°С) (ГОСТ 5457-75)
| Температура, °С | -5 | 0 | +5 | +10 | +15 | +20 | +25 | +30 | +35 | +40 | |
| Давление в баллоне, не более | МПа | 1,34 | 1,4 | 1,5 | 1,65 | 1,8 | 1,9 | 2,15 | 2,35 | 2,6 | 3 |
| кгс/см2 | 13,4 | 14 | 15 | 16,5 | 18 | 19 | 21,5 | 23,5 | 26 | 30 | |
Таблица. Остаточное давление газа в баллоне, поступающем от потребителя (ГОСТ 5457-75)
| Температура, °С | до 0 | от 0 до +15 | от +15 до +25 | от +25 до +35 | |
| Остаточное давление в баллоне, не менее | МПа | 0,05 | 0,1 | 0,2 | 0,3 |
| кгс/см2 | 0,5 | 1 | 2 | 3 | |
40-литровые баллоны с максимальным давлением газа 1,9 МПа при температуре 20°С обычно заполняют 5–5,8 кг ацетилена (4,6–5,3 м3 газа при температуре 20°С и давлении 760 мм рт. ст.). Масса ацетилена в баллоне определяется по разности масс баллона до и после наполнения газом. Объем ацетилена равен отношению его массы и плотности. Так, объем 5,5 кг ацетилена при температуре 20°С и давлении 760 мм рт. ст. составляет 5,5/1,09 = 5,05 м3.
Таблица. Сравнительные характеристики ацетилена, пропана и метилацетилен-алленовой фракции (МАФ)
| Параметр | ацетилен | пропан | МАФ |
| Чувствительность к удару, безопасность | нестабилен | стабилен | стабилен |
| Токсичность | незначительная | ||
| Предел взрываемости в воздухе (%) | 2,2–81 | 2,0–9,5 | 3,4–10,8 |
| Предел взрываемости в кислороде (%) | 2,3–93 | 2,4–57 | 2,5–60 |
| Температура пламени (°С) | 3087 | 2526 | 2927 * |
| Реакции с обычными металлами | избегать сплавов, содержащих более 70% меди | незначительные ограничения | избегать сплавов, содержащих более 65–67% меди |
| Склонность к обратному удару | значительная | незначительная | незначительная |
| Скорость сгорания в кислороде (м/с) | 6,10 | 3,72 | 4,70 |
| Плотность газа (кг/м3) | 1,17 (при 0°С) 1,09 (при 20°С) | 2,02 (при 0°С) | 1,70 (при 0°С) * |
| Плотность в жидком состоянии при 15,6°С (кг/м3) | – | 513 | 575 |
| Отношение расхода кислорода к горючему газу (м3/м3) при нормальном пламени | 1–1,2 | 3,50 | 2,3–2,5 |
Преимущества
Газ является непредельным углеводородом, который обладает тройной связью атомов углерода. Формула ацетилена – С2Н2. При этом структурная формула ацетилена выглядит следующим образом Н-С=С-Н, так как связь идет между атомами углерода.
Химические и физические свойства
В нормальных условиях газ является бесцветным. Он легче воздуха. В техническом ацетилене имеются добавки, которые придают ему резкий запах, но в чистом виде он ни чем не пахнет. Лучше всего газ растворяется в ацетоне, но в воде он мало растворим. Температура кипения достигает -83,6 градусов Цельсия.
Газ требует очень аккуратного обращения. Баллон может взорваться от обыкновенного удара при падении или при нагреве около 500 градусов Цельсия. Воспламениться струя может даже от статического электричества от пальца человеческой руки. Молярная масса ацетилена составляет 26 г/моль. Температура горения ацетилена в ядре пламени может составлять более 2600 градусов Цельсия.
Химические свойства ацетилена показывают, в какие реакции может вступать субстанция с другими веществами. В присутствии катализаторов, в частности солей ртути, газ образует уксусный альдегид. Благодаря наличию тройной связи, молекулы вещества имеют большой запас энергии. Это обеспечивает ей высокую теплоту сгорания, которая составляет 14 000 ккал/м3. Если при сгорании добавить струю кислорода, то температура пламени достигнет более 3100 градусов Цельсия. Газ может полимеризироваться в такое вещество как бензол и прочие органические соединения, к примеру, винилацетилен или полиацетилен. Полимеризация в бензол происходит при температуре в 500 градусов Цельсия и при наличии графита. Если в качестве катализатора использоваться трикарбонил никеля, то данная реакция может пройти при температуре в 65 градусов Целься. Ацетилен обладает очень сильными кислотными свойствами. Атомы водорода могут легко отщепиться в качестве протонов. В эфирном растворе металмагнийбромида данный газ вытесняет метан. В сочетании с солями одновалентной меди и серебра ацетилен образует взрывчатый нерастворимый осадок.
Состав
Горение ацетилена и прочие его практические свойства во многом зависят от состава. Даже небольшие отклонения от нормы могут привести к тому, что газ поменяет свои характеристики. Поэтому, выделяют несколько основных сортов, отличающихся друг от друга по своему составу.
Состав ацетилена газообразного технического:
- Основной газ – 98,5%;
- Воздух – 1,4%;
- Фосфорный водород – 0,08%;
- Сероводород – 0,05%.
Растворенное вещество первого сорта марки Б должно обладать следующим составом:
- Основной газ – 99,1%;
- Воздух – 0,8%;
- Фосфорный водород – 0,02%;
- Сероводород – 0,005%.
Растворенное вещество второго сорта марки Б должно обладать следующим составом:
- Основной газ – 98,8%;
- Воздух – 1%;
- Фосфорный водород – 0,05%;
- Сероводород – 0,05%.
Растворенное вещество марки А должно обладать следующим составом:
- Основной газ – 99,5%;
- Воздух – 0,5%;
- Фосфорный водород – 0,005%;
- Сероводород – 0,002%.
Технология и режимы сварки
Перед началом сварки нужно подобрать баллон с ацетиленом и понять саму его конструкцию.
Конструкция баллона с ацетиленом
Потом подбирается горелка требуемого размера от 0 до 5. Толщина этого инструмента определяет расход газа, а также ширину образуемого шва. Чтобы проверить готовность изделия к работе, ее нужно продуть ацетиленом до тех пор, чтобы почувствовать его запах.
Поджог газа осуществляется еще до добавления кислорода. После загорания можно добавить понемногу струю кислорода, пока не образуется устойчивое пламя. Выходное давление основного газа должно быть до 4 атмосфер, а дополнительного – до 2 атмосфер. Затем подбирается мощность пламени согласно толщине свариваемого металла.
Заранее очищенные заготовки предварительно прогреваются пламенем горелки до нужной температуры. После этого добавляется сварочная проволока, которая вместе с основным металлом образует сварочную ванну. Процесс сварки может проводиться как правым, так и левым способом. После окончания процедуры горение ацетилена поможет постепенному охлаждению шва с подогревом.
Заключение
Разбираясь, для чего нужен ацетилен в сварочной области, в первую очередь нужно думать о безопасности. Отличные практические качества и низкая стоимость газа не позволяют отказаться от него полностью из-за взрывоопасности. Любой специалист может оценить все преимущества работы с ним, но сложности хранения затрудняют его применение в домашних условиях.
Взрывоопасность ацетилена и безопасность при обращении с ним:
Ацетилен обладает взрывоопасными свойствами.
Поэтому обращение с ацетиленом требует строгого соблюдения правил техники безопасности.
Ацетилен горит и взрывается даже в отсутствии кислорода и других окислителей.
Смеси ацетилена с воздухом взрывоопасны в очень широком диапазоне концентраций.
Струя ацетилена, выпущенная на открытый воздух, может загореться от малейшей искры, в том числе от разряда статического электричества с пальца руки.
Взрываемость ацетилена зависит от множества факторов: давления, температуры, чистоты ацетилена, содержания в нем влаги, наличия катализаторов и пр. веществ и ряда других причин.
Температура самовоспламенения ацетилена при нормальном – атмосферном давлении колеблется в пределах 500-600 °C. При повышении давления существенно уменьшается температура самовоспламенения ацетилена. Так, при давлении 2 кгс/см2 (0,2 МПа, 1,935682 атм.) температура самовоспламенения ацетилена равна 630 °C. А при давлении 22 кгс/см2 (2,2 МПа, 21,292502 атм.) температура самовоспламенения ацетилена равна 350 °С.
Присутствие в ацетилене частиц различных веществ увеличивают поверхность его контакта и тем самым снижает температуру самовоспламенения при атмосферном давлении. Например, активированный уголь снижает температуру самовоспламенения ацетилена до 400 °С, гидрат оксида железа (ржавчина) – до 280-300 °С, железная стружка – до 520 °С, латунная стружка – до 500-520 °С, карбид кальция – до 500 °С, оксид алюминия – до 490 °С, медная стружка – 460 °С, оксид железа – 280 °С, оксид меди – до 250 °С.
Взрывоопасность ацетилена уменьшается при разбавлении ацетилена другими газами, например азотом, метаном или пропаном.
При определенных условиях ацетилен реагирует с медью, серебром и ртутью образуя взрывоопасные соединения. Поэтому при изготовлении ацетиленового оборудования (например, вентилей баллонов) запрещается применять сплавы, содержащие более 70 % Cu.
Для хранения и перевозки ацетилена используются специальные стальные баллоны белого цвета (с красной надписью «А»), заполненные инертным пористым материалом (например, древесным углём). При этом ацетилен хранится и перевозится в указанных баллонах в виде раствора ацетилена в ацетоне под давлением 1,5-2,5 МПа.



карта сайта
как получить ацетилен реакция ацетилен этен 1 2 вещество кислород водород связь является углекислый газ бромная вода
уравнение реакции масса объем полное сгорание моль молекула смесь превращение горение получение ацетилена
напишите уравнение реакций ацетилен
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. |