Второе название яблочной кислоты – оксиянтарная. Это представитель класса гидрокси-дикарбоновых кислот. Впервые соединение было получено Карлом Шееле (шведским ученым-химиком) из незрелых яблок (что и определило его название) в 1785 году. Также в природе оно встречается в винограде, барбарисе, рябине, малине и т.д. В виде солей, называемых малатами, вещество содержится в табаке. Максимальное содержание оксиянтарной кислоты совместно с лимонной в незрелых зеленых яблоках доходит до 1.2 %.
- Яблочная кислота: формула
- Получение
- Яблочная кислота. Реакции взаимодействия
- Биологическая роль
- Сферы использования
- Яблочная кислота: формула, реакции, применение, полезные свойства
- Что такое яблочная кислота?
- Формула яблочной кислоты и ее свойства
- История открытия и использования яблочной кислоты
- Методы получения яблочной кислоты
- Химические реакции с яблочной кислотой
- Допустимые нормы приема яблочной кислоты
- Сферы применения яблочной кислоты
- Яблочная кислота в пищевой промышленности
- Яблочная кислота в медицине
- Яблочная кислота в косметологии
- Влияние яблочной кислоты на организм человека
- Польза яблочной кислоты
- Вред яблочной кислоты
- Противопоказания к употреблению яблочной кислоты
- Яблочный пилинг и его особенности
- Тип яблочной кислоты как пищевой добавки и правила ее хранения
- Где можно приобрести яблочную кислоту и сколько она стоит
- Заключение
- Acetyl
Яблочная кислота: формула
Данное химическое соединении имеет следующую формулу:
В обычных условиях яблочная кислота – это бесцветный кристаллический порошок, который хорошо растворяется в спирте (в 100 мл – 35,9 г) и в воде (в 100 мл – 144 г). Молекулярная масса соединения равна 134,1 г/моль.
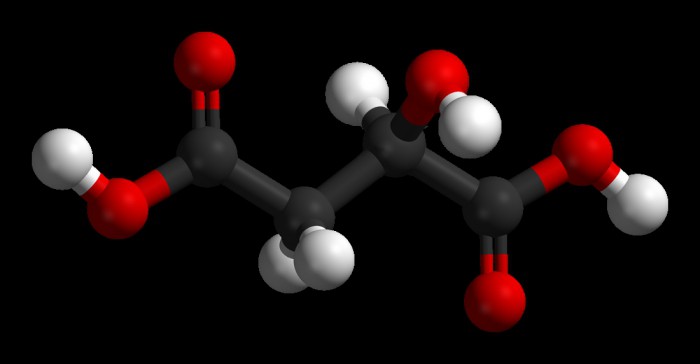
На картинке ниже показано пространственное строение молекулы яблочной кислоты. Атомы углерода обозначены черным цветом, кислорода – красным, водорода – белым.
Яблочная кислота существует в виде рацемата (оптически неактивное соединение) и двух стереоизомеров. Последние представляют собой такие соединения, в молекулах которых между атомами наблюдается одинаковая последовательность химических связей, но имеются отличия в их расположении в пространстве относительно друг друга. Подробно данным вопросом занимается стереохимия. У яблочной кислоты стереоизомера два, именно на их примере П.Вальден в 1896 году первым показал, что возможны взаимопревращения энантиомеров. Изучение этого явления выступило в роли фундамента для последующего создания теории реакции так называемого нуклеофильного замещения у атома углерода (насыщенного).
Получение
Вещество получают двумя способами: естественным и химическим. Первый предлагает экстракцию из фруктов и ягод. Синтетическую яблочную кислоту получают в результате нескольких реакций:
1. Гидратация малеиновой или фумаровой кислоты. Обязательное условие – это температура 100-150 °С. Уравнение реакции следующее:
HOOCCH= CHCOOH + H2O → НООС-СН2-СН (ОН) – СООН
2. Гидролиз бромо- или хлороянтарной кислоты. Яблочная кислота добывается с использованием эфира. При этом используется растительный материал.
Яблочная кислота. Реакции взаимодействия
1. Окисление серной концентрированной кислотой (H2SO4) с образованием кумалиновой кислоты. Реакция проходит в два этапа:
В результате образуется альдегидомалоновая и муравьиная кислоты. Последнее соединение разлагается с образованием угарного газа и воды:
Альдегидомалоновая кислота сразу же трансформируется в кумалиновую.
НООС-СН2-СН (ОН) – СООН + HCl → HOOC-CH2-CHCl-COOH
Образующееся вещество носит название 2-хлорянтарного.
3. Яблочная кислота поддается окислению (в частности, при использовании KMnO4):
НООС-СН2-СН (ОН) – СООН + KMnO4 → HOOC-CH2-CO-COOH
Образующаяся кислота называется 2-оксоянтарной (оксалилуксусной).
4. Взаимодействие с ацетилхлоридом с образованием 2-ацетоксиянтарной кислоты:
НООС-СН2-СН (ОН) – СООН + CH3COCl → HOOC-CH2-CH(OCOCH3)-COOH
При постепенном нагревании яблочная кислота разлагается с образованием ряда промежуточных продуктов. При температуре в 100°С происходит образование ангидридов (они подобны лактидам). При повышении до 140-150 °С происходит их преобразование в фумаровую кислоту. При быстром увеличении температуры до 180°С получают малеиновый ангидрид.
Обобщая все данные, можно сказать, что химические свойства яблочной кислоты те же, что и у остальных оксикислот.
Биологическая роль
Яблочная кислота участвует в цикле Кребса. Он представляет собой главный этап в дыхании всех клеток, которые используют кислород и является промежуточным звеном между гликолизом и электротранспортной цепью. Основная роль цикла трикарбоновых кислот (Кребса) – это синтез восстановленных коферментов ФАД*Н2 и НАД*Н. Они впоследствии используются для получения АТФ, АДФ и фосфатов. Оксиянтарная кислота образуется в результате гидратации фумаровой. Ее последующее окисление при помощи НАД + завершает цикл Кребса. Катализирующий фермент при этом – малатдегидрогеназа.
Сферы использования
Получаемая в промышленных масштабах яблочная кислота находит достаточно широкое применение:
- В пищевой отрасли она известна под кодом Е296. Вещество используется в качестве консерванта, усилителя вкуса и регулятора кислотности. Основное применение: газированные напитки, фруктовые соки, кондитерские изделия, вино, консервы. Стоит подчеркнуть, что в малых количествах яблочная кислота оказывает на организм положительное воздействие.
- В косметологии. Оксиянтарная кислота обладает антиоксидантными, отбеливающими, отшелущивающими и увлажняющими свойствами, что позволяет использовать ее в составе антицеллюлитных и отбеливающих средств для кожи, пилингах. Кроме того, она добавляется в зубные пасты и средства, ухаживающие за полостью рта.
- В фармакологии яблочная кислота (формула приведена выше) используется в составе отхаркивающих и слабительных средств.
Яблочная кислота: формула, реакции, применение, полезные свойства
Яблочная кислота – это органическое соединение, основным источником которого, как несложно догадаться, служат яблоки, пищевая добавка Е296. В меньших количествах вещество содержится и в других плодах: грушах, натуральном березовом соке, крыжовнике, томатах и ревене. Внешне пищевая добавка представляет собой лишенный цвета мелкокристаллический порошок, частички которого имеют насыщенный кислый вкус.
Яблочную кислоту в разных источниках именуют по-разному. Она известна как оксиянтарная и малановая кислота, в перечне пищевых добавок его обозначают под индексом Е296.
Оксиянтарная кислота активно применяется в производстве безалкогольных напитков, сладостей и некоторых вин. Кроме того, яблочная кислота применяется при производстве лекарственных препаратов и косметологических средств.
Что такое яблочная кислота?
Яблочная кислота – это соединение, принадлежащее к классу органических веществ. С химической точки зрения она представляет собой двухосновную гидроксикислоту, принадлежащую к классу оксикарбоновых кислот. Химические соединения такого рода имеют в своей структуре гидроксильную (функциональную группу ОН, в которой атомы водорода и кислорода соединены между собой ковалентной связью) и карбоксильную группы (функциональную группу СООН, определяющую кислотные свойства соединений).
Яблочная кислота способна активно проявлять свои кислотные свойства и с легкостью образует соли и сложные эфиры при взаимодействии с другими веществами. Помимо кислотных свойств, проявляет свойства спиртов: способность образования простых эфиров, высокая склонность к окислению.
Соли, приготовленные на основе яблочной кислоты, достигли широкого распространения в пищевой промышленности: их применяют в качестве добавок, улучшающих вкус готовых продуктов.
Наибольшее количество яблочной кислоты содержится в спелых яблоках, ей также богаты кислые ягоды, в частности – крыжовник, виноград, рябина, малина и некоторые цитрусовых. Обнаружить яблочную кислоту можно также в составе мякоти груш.
Формула яблочной кислоты и ее свойства
Формула яблочной кислоты записывается следующим образом:
Химический состав данной кислоты представлен четырьмя атомами углерода, шестью атомами водорода и пятью атомами кислорода.
Из химической формулы можно высчитать молярную массу вещества: она составляет 134 г/моль.
Температура плавления яблочной кислоты составляет 130,8 ˚С.
Степень растворимости соединения определяется типом применяемого растворителя. На 100 г растворителя растворимость данной кислоты составляет:
- в воде (при температуре 26 ˚C) – 144 г;
- в воде (при температуре 80 ˚C) – 411 г;
- в этаноле (при температуре 20 ˚C) – 35,9 г;
- в диэтиловом эфире (при температуре 20 ˚C) – 0,6 г;
- в бензоле – не растворяется.
Яблочной кислоте характерны химические свойства оксикислот (органических соединений, содержащих одновременно одну или несколько карбоксильных и гидроксильных групп).
При нагревании реагента до 100 ˚C происходит образование агидрида, а при продолжении повышения температуры до 140-150 ˚C – образование фумаровой кислоты.
При попадании в человеческий организм в чистом виде, окисянтарная кислота преобразуется в малаты – соли яблочной кислоты, оказывающие огромное влияние на правильность протекания обменных реакций.
История открытия и использования яблочной кислоты
Впервые оксиянтарная кислота была обнаружена в конце 18 века, а именно – в 1785 году. Открытие совершил Карл Шелле – известный ученый родом из Швеции. Он вывел вещество из состава неспелых яблок. Исследование химический свойств обнаруженного вещества показало его высокую эффективность в косметологии, пищевой индустрии и фармакологии.
Разумеется, пищевая добавка Е296 на основе яблочной кислоты появилась далеко не сразу – сперва вещество претерпело массу опытов и исследований, в ходе которых было установлено, что вещество способно выступать в роли оздоровительного компонента, который может увеличивать активность человека, насыщать его организм энергией, а также оказывать регенерирующее воздействие на клетки печени. Эти свойства обусловили высокую популярность яблочной кислоты в фармакологии и медицине.
Первую яблочную кислоту получали посредством переработки растительного сырья: зелени, кислых ягод, яблок и груш. В настоящее время для получения вещества применяется химическая реакция аспаргиновой кислоты с азотистой кислотой при температуре 130 ˚C.
Методы получения яблочной кислоты
Первым методом, который применялся для выделения яблочной кислоты, как уже было сказано выше, был метод переработки природного сырья – ягод, фруктов и зелени. Однако, у него была масса недостатков, главным из которых было уменьшение концентрации оксиянтарной кислоты в продуктах с увеличением степени их зрелости. То есть, производство яблочной кислоты становилось сезонной работой, возможной только в период наличия большого количества незрелых плодов.
С ходом развития химической промышленности появились и другие, более удобные, методы производства яблочной кислоты. Так, большой популярностью пользуется синтетический способ, предполагающий гидратацию малеиновой кислоты. Проще говоря, к малеиновой кислоте добавляют воду и нагревают реагенты до 170-200 ˚C:
Альтернативной данному методу служит способ ферментации. Он подразумевает воздействие обездвиженных клеток в присутствии фермента фумараза. В ферментативном методе вместо малеиновой кислоты применяется фумаровая: она присоединяет к себе воду, образуя яблочную кислоту:
Ежегодно в мире производится более 600 000 тонн яблочной кислоты.
Химические реакции с яблочной кислотой
Для оксиянтарной кислоты характерны те же свойства, что и для других оксикислот.
Так, при смешивании яблочной кислоты с концентрированной серной кислотой происходит образование кумалиновой кислоты. Реакция состоит из двух основных этапов: сперва образуются альдегидомалоновая и муравьиная кислота. Последняя на второй ступени разлагается на угарный газ и воду. Альдегидомалоновая кислота в результате реакции преобразуется в кумалиновую:
Кроме того, яблочная кислота легко поддается окислению (в особенности в присутствии перманганата калия). По завершении реакции образуется щавелевоуксусная кислота:
Яблочная кислота вступает в реакцию с ацетилхлоридом, образуя 2-ацетоксиянтарную кислоту:
При медленном нагревании яблочная кислота разлагается на составляющие с образованием промежуточных продуктов.
Допустимые нормы приема яблочной кислоты
Яблочная кислота разрешена к применению практически во всех странах. Несмотря на такое широкое распространение, конкретных рекомендаций относительно объема употребления нет. Специалисты обычно советуют есть по 2-4 яблока среднего размера в сутки при обнаружении у себя следующих симптомов:
- быстрой утомляемости;
- замедлении метаболизма;
- закислении организма;
- заболеваниях пищеварительной системы;
- сильных кожных высыпаниях.
Сократить употребление яблок и уменьшить количество потребляемой яблочной кислоты рекомендуется при высокой кислотности желудка, тяжелых внутренних кровотечениях и расстройствах пищеварения. Также не стоит объедаться фруктами беременным и кормящим женщинам и маленьким детям (до 10 лет).
Сферы применения яблочной кислоты
Наибольшей популярности яблочная кислота достигла в пищевой промышленности: она регулирует показатель кислотности и выступает в роли консерванта, препятствующего образованию грибков и бактерий.
Яблочная кислота применяется и косметологи: соединение часто вводят в состав пилингов и отшелушивающих масок, растворяющих мертвые клетки. Кроме того, данная кислота в составе косметических средств отвечает за поддержание липидного баланса кожи, не давая ей пересыхать.
Яблочная кислота применяется и в медицине. Добавку применяют для производства длинного перечня медикаментов, действие которых направлено на улучшение состояния организма при нарушениях в работе органов ЖКТ и дыхательной системы.
Яблочная кислота в пищевой промышленности
В производстве продуктов питания и напитков оксиянтарная кислота известна как пищевая добавка Е296. В сочетании с другими ингредиентами она выполняет роль регулятора кислотности и консерванта, препятствующего развитию патогенных микроорганизмов.
Наиболее часто пищевую добавка яблочная кислота применяется в производстве:
- молока и продуктов на его основе;
- фруктовых соков и других безалкогольных напитков;
- варенье и желе;
- карамельных конфетах;
- консервированных фруктах и овощах;
- водки;
- детского питания.
Пищевая добавка Е296 (яблочная кислота) применяется также для производства всевозможных сладостей и алкогольных напитков.
Встретить оксиянтарную кислоту можно практически во всех кислых плодах: так, ее много в неспелых яблоках, зеленом крыжовнике и белом винограде. Соединение может содержаться также в плодах рябины, ревене, барбарисе и малине. Совсем небольшое количество яблочной кислоты содержится в листьях табака.
Яблочная кислота в медицине
Как уже было сказано выше, соединение входит в состав многих лекарств. Наиболее часто яблочная кислота применяется в производстве слабительных средств и аминокислотных инъекционных препаратов.
Кроме того, в медицинском деле кислота необходима для:
- обеспечения защиты печени;
- предотвращения развития заболеваний почек;
- лечения повышенного давления;
- лечения уремии;
- улучшения общего состояния организма;
- обеспечения правильного протекания пищеварительных процессов.
Яблочная кислота в косметологии
В составе уходовой косметики оксиянтарная кислота отвечает сразу за несколько процессов: она очищает кожу, увлажняет ее и оказывает противовоспалительный эффект. Добавка применяется для производства средств для пилингов и масок, находится в составе отбеливающих зубных паст, антивозрастных кремов и сывороток, лаков для волос и антицеллюлитных средств.
Как компонент кремов и сывороток яблочная кислота помогает в избавлении от морщин и повышении эластичности кожи. Кроме того, соединение хорошо справляется с омертвевшими частичками, отшелушивая их и питая кожу. Отбеливающие свойства яблочной кислоты используют для устранения пигментных пятен и борьбы с веснушками.
Влияние яблочной кислоты на организм человека
Яблочная кислота не является незаменимым для человека соединением, но это не значит, что она не приносит пользу. Вещество является сильнодействующим оздоровительным компонентом, способным обеспечивать организм энергией, улучшать состояние печени и почек, бороться с повышенным давлением.
Польза яблочной кислоты
Оксиянтарная (яблочная) кислота играет важную роль в поддержании метаболической активности клеток: она нормализует выработку энергии, обеспечивая человеку нормальное самочувствие, защищает мышечные ткани от истощения.
При попадании в иммунную систему яблочная кислота обеспечивает здоровье полости рта, правильное функционирование сердечной мышцы, нервов и мышечного каркаса, улучшает общее состояние кожи.
Часто кислоту используют спортсмены для улучшения своих результатов и снятия мышечной усталости.
Так, яблочная кислота оказывает положительное влияние на многие системы человеческого организма:
- улучшает кровообращение;
- помогает в избавлении от отеков;
- нормализует работу пищеварительной системы;
- улучшает обмен веществ;
- улучшает качество крови;
- усиливает защитную функцию организма, защищая его от вирусных и простудных заболеваний;
- оказывает противовоспалительный эффект;
- улучшает состояние печени и очищает ее от токсинов;
- выполняет роль мягкого слабительного;
- нормализует работу почек;
- улучшает аппетит;
- поддерживает кислотно-щелочной баланс.
Вред яблочной кислоты
При нормальном состоянии здоровья яблочная кислота не может нанести вред организму, однако ее не рекомендуют принимать при наличии определенных заболеваний, поскольку веществол способно ухудшить состояние здоровья.
Так, при наличии проблем с органами желудочного-кишечного тракта не рекомендуется употреблять в пищу большое количество продуктов, включающих в свой состав яблочную кислоту.
Употребление чрезмерного количества кислых фруктов способно вызвать язву желудка, образование опухолей, в том числе и злокачественных, появление внутренних кровотечений и развитие кожных заболеваний.
Противопоказания к употреблению яблочной кислоты
Как таковых противопоказаний к употреблению оксиянтарной кислоты нет, однако существуют случаи, в которых ее дозировку рекомендуется снизить. Так, сократить объем потребляемой яблочной кислоты специалисты рекомендуют при:
- заболеваниях желудочно-кишечного тракта, связанных с повышенной кислотностью;
- кишечном колите;
- панкреатите;
- повышенной чувствительности зубов;
- индивидуальной непереносимости;
- беременности.
Яблочный пилинг и его особенности
Главной задачей яблочного пилинга является глубокая очистка кожи с последующим ее увлажнением. При нанесении косметического средства на кожу происходит расщепление связей между омертвевшими клетками и здоровым эпидермисом. Яблочная кислота при этом проникает вглубь кожи, стимулируя выработку естественного коллагена.
После яблочного пилинга выравнивается тон кожи лица, пропадают покраснения и пигментные пятна, повышается эластичность кожи, исчезают маленькие мимические морщинки, сужаются поры и повышается влагоудерживающая способность кожи. При нанесении на проблемные зоны (руки, бедра, живот) яблочный пилинг помогает в устранении целлюлита.
Стоит отметить, что после использования яблочного пилинга значительно улучшается реакция кожи на применение кремов и сывороток.
Показаниями к применению яблочного пилинга являются:
- акне и постакне;
- нарушение липидного баланса;
- сильная пигментация кожи;
- мимические морщины на коже;
- купероз;
- потеря упругости кожи.
Тип яблочной кислоты как пищевой добавки и правила ее хранения
По степени воздействия на человеческий организм яблочная кислота принадлежит к 3 классу опасности. Он абсолютно не токсична, пожаро- и взрывобезопасна.
При работе с веществом рекомендуется использовать средства индивидуальной защиты и соблюдать правила личной гигиены. Все помещения, в которых производятся работы с большими объемами яблочной кислоты, должны быть оборудованы системой приточно-вытяжной вентиляции.
Хранить оксиянтарную кислоту необходимо в упаковке изготовителя, в сухих хорошо проветриваемых складских помещениях. Срок годности – 2 года со дня изготовления.
Где можно приобрести яблочную кислоту и сколько она стоит
Найти яблочную кислоту в обычном магазине или аптеке достаточно проблематично – искать ее необходимо в специализированных магазинах. 50 г добавки обойдутся примерно в 150-200 рублей.
Заключение
Яблочная кислота – это соединение, содержащееся в больших количествах в неспелых яблоках и грушах, цитрусовых и ягодах. Вещество полностью безопасно для человека: оно применяется в производстве продуктов питания, уходовой косметики и лекарств. В пищевой промышленности яблочная кислота выполняет роль консерванта, увеличивающего срок хранения производимой продукции и известна как пищевая добавка Е296. В косметологии отвечает за степень увлажненности кожи, ее мягкость и упругость. В составе лекарственных средств оксиянтарная кислота оказывает влияние на состояние органов желудочно-кишечного тракта и почек, состав крови, скорость обмена веществ и другие параметры. Несмотря на длинный перечень положительных характеристик, существуют определенные ограничения в использовании яблочной кислоты: строго контролировать ее объем рекомендуется людям с отклонениями в состоянии здоровья.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. |