Химия | 10 — 11 классы
Написать уравнение реакции образования сложного эфира из яблочной кислоты и пропанол — 2.
HCOO — CH(OH) — CH2 — COOH + 2CH3 — CH(OH) — CH3 — > ; CH3 — CH(CH3) — OOC — CH(OH) — CH2 — COOCH(CH3) — CH3.
- Напишите структурные формулы сложных эфиров, образующихся из а) уксусной кислоты и 2 — пропанола ; б) уксусной кислоты и 1 — пропанола ; в) муравьиной кислоты и этанола?
- Образование каких простых эфиров можно ожидать при действии серной кислоты на пропанол 1(решение)?
- . написать уравнение реакции а)получение пропилового эфира муравьиной кислоты Б)метилового эфира валериановой кислоты?
- 1. Какая реакция лежит в основе получения сложных эфиров?
- Напишите уравнение реакции между уксусной кислоты и пропанолом — 1 с образованием сложного эфира?
- Напишите уравнения реакций образования простого и сложного эфиров при взаимодействии β — оксимасляной кислоты с метиловым спиртом?
- Реакция взаимодействия глюкозы с карбоновыми кислотами с образованием сложных эфиров обусловлена наличием функциональной группы?
- Пожалуйста помогите ?
- Напишите уравнение реакции образования сложного эфира из уксусной кислоты и пропанол — 2?
- Какую формулу имеет яблочная кислота и как ее получают?
- Яблочная кислота: формула
- Получение
- Яблочная кислота. Реакции взаимодействия
- Биологическая роль
- Сферы использования
- Уравнение реакции образования сложного эфира из яблочной кислоты и
- 💡 Видео
Видео:Опыты по химии. Получение сложного эфираСкачать

Напишите структурные формулы сложных эфиров, образующихся из а) уксусной кислоты и 2 — пропанола ; б) уксусной кислоты и 1 — пропанола ; в) муравьиной кислоты и этанола?
Напишите структурные формулы сложных эфиров, образующихся из а) уксусной кислоты и 2 — пропанола ; б) уксусной кислоты и 1 — пропанола ; в) муравьиной кислоты и этанола.
Видео:Простые эфиры. Получение. Все 4 реакции ЕГЭ.Скачать

Образование каких простых эфиров можно ожидать при действии серной кислоты на пропанол 1(решение)?
Образование каких простых эфиров можно ожидать при действии серной кислоты на пропанол 1(решение).
Видео:РЕАКЦИИ ИОННОГО ОБМЕНА, ИОННОЕ УРАВНЕНИЕ - Урок Химия 9 класс / Подготовка к ЕГЭ по ХимииСкачать

. написать уравнение реакции а)получение пропилового эфира муравьиной кислоты Б)метилового эфира валериановой кислоты?
. написать уравнение реакции а)получение пропилового эфира муравьиной кислоты Б)метилового эфира валериановой кислоты?
Видео:Химические уравнения // Как Составлять Уравнения Реакций // Химия 9 классСкачать

1. Какая реакция лежит в основе получения сложных эфиров?
1. Какая реакция лежит в основе получения сложных эфиров?
Привести 2 примера образования сложных эфиров и дать названия 2.
Составить уравнения реакций для превращений : а)Пропанол + Уксусная Кислота — > ; б)Бутанол + натрий — > ; в)Фармальдегид + водород — > ; 3.
Вычеслить сколько сгорело этанола, если образовалось 56л углекислого газа.
Напишите уравнение реакций образования простого и сложного эфиров из салициловой кислоты и этанола.
Видео:Простые эфиры. Химические свойства. Все 3 реакции ЕГЭ.Скачать

Напишите уравнение реакции между уксусной кислоты и пропанолом — 1 с образованием сложного эфира?
Напишите уравнение реакции между уксусной кислоты и пропанолом — 1 с образованием сложного эфира.
Видео:Сложные эфиры за 45 минут | Химия ЕГЭ 10 класс | УмскулСкачать

Напишите уравнения реакций образования простого и сложного эфиров при взаимодействии β — оксимасляной кислоты с метиловым спиртом?
Напишите уравнения реакций образования простого и сложного эфиров при взаимодействии β — оксимасляной кислоты с метиловым спиртом.
Видео:РЕАКЦИЯ ЭТЕРИФИКАЦИИСкачать

Реакция взаимодействия глюкозы с карбоновыми кислотами с образованием сложных эфиров обусловлена наличием функциональной группы?
Реакция взаимодействия глюкозы с карбоновыми кислотами с образованием сложных эфиров обусловлена наличием функциональной группы.
Видео:13.2. Сложные эфиры: Способы полученияСкачать

Пожалуйста помогите ?
Запишите реакцию образования сложного эфира, в которой участвует уксусная кислота и изоамиловый спирт, назовите появившийся сложный эфир.
Видео:Карбоновые кислоты и сложные эфиры | Демонеделя по химии | ЕГЭ 2024Скачать

Напишите уравнение реакции образования сложного эфира из уксусной кислоты и пропанол — 2?
Напишите уравнение реакции образования сложного эфира из уксусной кислоты и пропанол — 2.
Вы находитесь на странице вопроса Написать уравнение реакции образования сложного эфира из яблочной кислоты и пропанол — 2? из категории Химия. Уровень сложности вопроса рассчитан на учащихся 10 — 11 классов. На странице можно узнать правильный ответ, сверить его со своим вариантом и обсудить возможные версии с другими пользователями сайта посредством обратной связи. Если ответ вызывает сомнения или покажется вам неполным, для проверки найдите ответы на аналогичные вопросы по теме в этой же категории, или создайте новый вопрос, используя ключевые слова: введите вопрос в поисковую строку, нажав кнопку в верхней части страницы.
Дано : D (СnH2n) по Н₂ = 21 общая формула алкенов — СnH2n M(СnH2n) = 14 n D (СnH2n) по Н₂ = M(СnH2n) / M(Н₂) M(СnH2n) = 21 * 2 = 42 г / моль 14n = 42 n = 3 C₃H₆ CH₃ — CH = CH₂ — пропен.
А) 4 — метилпентин — 2 б) 3 — метилпентен — 1 в) 3 — метилбутин — 1.
—так как кислород тяжелее воздуха, то для того, чтобы перелить из одного сосуда в другой кислород, необходимо сосуд с кислородом расположить сверху, а пустой — снизу.
Cr хром 1s ^ 2, 2s ^ 2, 2p ^ 6, 3s ^ 2, 3p ^ 6, 3d ^ 4, 4s ^ 2.
Пишем реакцию 2Al + 3Cl2 = 2AlCl3 По уравнению реакции n(Cl2) = 3 / 2n(Al) = 3 / 2 * 0. 24 = 0. 36 моль Считаем объем хлора V = n * Vm = 0. 36 * 22. 4 = 8. 064 л.
Вот такая формула : C5H12.
1) С + O2 = СO2 2)CO2 + H2 = H2CO2 3) H2CO3 + Ca(OH)2 = CaCO3 + 2H20 4) CaCO3 + 2HCl = CaCl2 + H2O + CO2 C — УГЛЕРОД O — кислород H — водород CA — кальций Cl — ХЛОР.
А) 2HNO3 + CuO — Cu(NO3)2 + H2O б) H2SO4 + 2NaOH — Na2SO4 + 2H2O в) 2HCl + K2CO3 — 2KCl + H2CO3.
Последнее не знаю точно.
2) и 6) если 2 варианта надо, если один то только 6).
Видео:Сложные эфиры и мыла. 1 часть. 11 класс.Скачать

Какую формулу имеет яблочная кислота и как ее получают?
Второе название яблочной кислоты – оксиянтарная. Это представитель класса гидрокси-дикарбоновых кислот. Впервые соединение было получено Карлом Шееле (шведским ученым-химиком) из незрелых яблок (что и определило его название) в 1785 году. Также в природе оно встречается в винограде, барбарисе, рябине, малине и т.д. В виде солей, называемых малатами, вещество содержится в табаке. Максимальное содержание оксиянтарной кислоты совместно с лимонной в незрелых зеленых яблоках доходит до 1.2 %.
Видео:Вся теория по карбоновым кислотам для ЕГЭ | Химия ЕГЭ для 10 класса | УмскулСкачать

Яблочная кислота: формула
Данное химическое соединении имеет следующую формулу:
В обычных условиях яблочная кислота – это бесцветный кристаллический порошок, который хорошо растворяется в спирте (в 100 мл – 35,9 г) и в воде (в 100 мл – 144 г). Молекулярная масса соединения равна 134,1 г/моль.
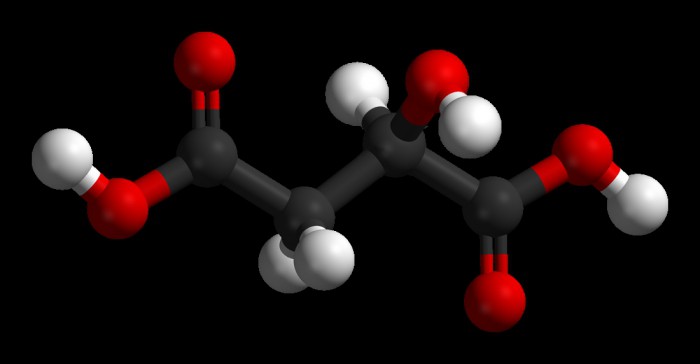
На картинке ниже показано пространственное строение молекулы яблочной кислоты. Атомы углерода обозначены черным цветом, кислорода – красным, водорода – белым.
Яблочная кислота существует в виде рацемата (оптически неактивное соединение) и двух стереоизомеров. Последние представляют собой такие соединения, в молекулах которых между атомами наблюдается одинаковая последовательность химических связей, но имеются отличия в их расположении в пространстве относительно друг друга. Подробно данным вопросом занимается стереохимия. У яблочной кислоты стереоизомера два, именно на их примере П.Вальден в 1896 году первым показал, что возможны взаимопревращения энантиомеров. Изучение этого явления выступило в роли фундамента для последующего создания теории реакции так называемого нуклеофильного замещения у атома углерода (насыщенного).
Видео:47. Простые и сложные эфиры (часть 1)Скачать

Получение
Вещество получают двумя способами: естественным и химическим. Первый предлагает экстракцию из фруктов и ягод. Синтетическую яблочную кислоту получают в результате нескольких реакций:
1. Гидратация малеиновой или фумаровой кислоты. Обязательное условие – это температура 100-150 °С. Уравнение реакции следующее:
HOOCCH= CHCOOH + H2O → НООС-СН2-СН (ОН) – СООН
2. Гидролиз бромо- или хлороянтарной кислоты. Яблочная кислота добывается с использованием эфира. При этом используется растительный материал.
Видео:Сложные эфиры | Химия 10 класс #34 | ИнфоурокСкачать

Яблочная кислота. Реакции взаимодействия
1. Окисление серной концентрированной кислотой (H2SO4) с образованием кумалиновой кислоты. Реакция проходит в два этапа:
В результате образуется альдегидомалоновая и муравьиная кислоты. Последнее соединение разлагается с образованием угарного газа и воды:
Альдегидомалоновая кислота сразу же трансформируется в кумалиновую.
НООС-СН2-СН (ОН) – СООН + HCl → HOOC-CH2-CHCl-COOH
Образующееся вещество носит название 2-хлорянтарного.
3. Яблочная кислота поддается окислению (в частности, при использовании KMnO4):
НООС-СН2-СН (ОН) – СООН + KMnO4 → HOOC-CH2-CO-COOH
Образующаяся кислота называется 2-оксоянтарной (оксалилуксусной).
4. Взаимодействие с ацетилхлоридом с образованием 2-ацетоксиянтарной кислоты:
НООС-СН2-СН (ОН) – СООН + CH3COCl → HOOC-CH2-CH(OCOCH3)-COOH
При постепенном нагревании яблочная кислота разлагается с образованием ряда промежуточных продуктов. При температуре в 100°С происходит образование ангидридов (они подобны лактидам). При повышении до 140-150 °С происходит их преобразование в фумаровую кислоту. При быстром увеличении температуры до 180°С получают малеиновый ангидрид.
Обобщая все данные, можно сказать, что химические свойства яблочной кислоты те же, что и у остальных оксикислот.
Видео:Реакции кислот-окислителей со сложными веществами: как понять? | Химия ЕГЭ 2022 | УмскулСкачать

Биологическая роль
Яблочная кислота участвует в цикле Кребса. Он представляет собой главный этап в дыхании всех клеток, которые используют кислород и является промежуточным звеном между гликолизом и электротранспортной цепью. Основная роль цикла трикарбоновых кислот (Кребса) – это синтез восстановленных коферментов ФАД*Н2 и НАД*Н. Они впоследствии используются для получения АТФ, АДФ и фосфатов. Оксиянтарная кислота образуется в результате гидратации фумаровой. Ее последующее окисление при помощи НАД + завершает цикл Кребса. Катализирующий фермент при этом – малатдегидрогеназа.
Видео:Сложные эфирыСкачать

Сферы использования
Получаемая в промышленных масштабах яблочная кислота находит достаточно широкое применение:
- В пищевой отрасли она известна под кодом Е296. Вещество используется в качестве консерванта, усилителя вкуса и регулятора кислотности. Основное применение: газированные напитки, фруктовые соки, кондитерские изделия, вино, консервы. Стоит подчеркнуть, что в малых количествах яблочная кислота оказывает на организм положительное воздействие.
- В косметологии. Оксиянтарная кислота обладает антиоксидантными, отбеливающими, отшелущивающими и увлажняющими свойствами, что позволяет использовать ее в составе антицеллюлитных и отбеливающих средств для кожи, пилингах. Кроме того, она добавляется в зубные пасты и средства, ухаживающие за полостью рта.
- В фармакологии яблочная кислота (формула приведена выше) используется в составе отхаркивающих и слабительных средств.
Видео:Химия | Тепловой эффект химической реакции (энтальпия)Скачать

Уравнение реакции образования сложного эфира из яблочной кислоты и
Опубликовано 09.06.2017 по предмету Химия от Гость >>
Ответ оставил Гость
НООС-СН=СН-СООН + СН3-СН(СН3)-ОН ——> СН3-СН(СН3)-ООС-СН=СН-СООН + Н2О, моноизопропилфумарат.
СН3-СН(СН3)-ООС-СН=СН-СООН + СН3-СН(СН3)-ОН——> СН3-СН(СН3)-ООС-СН=СН-СОО-СН(СН3)-СН3 + Н2О, диизопропилфумарат.
💡 Видео
Сложные эфиры | Органическая химия ЕГЭ, ЦТСкачать

13.3. Сложные эфиры: Химические свойстваСкачать

Химические уравнения - Как составлять уравнения реакций // Составление Уравнений Химических РеакцийСкачать

Самые красивые химические реакции - образование Сu(OH)₂Скачать