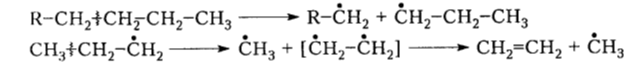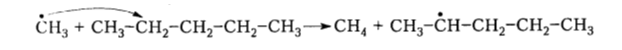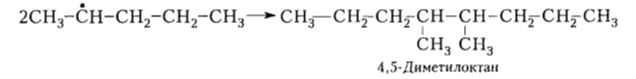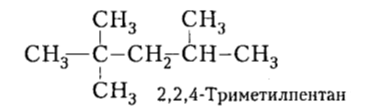Вопрос по химии:
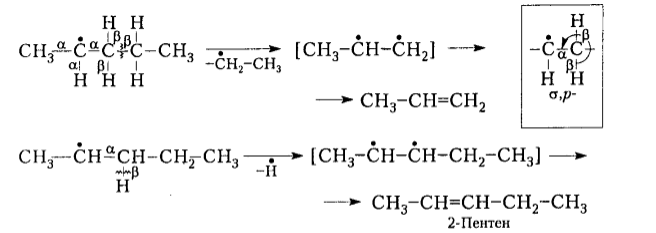
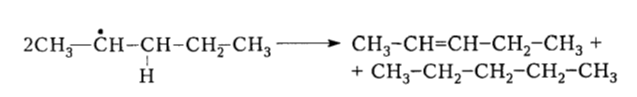
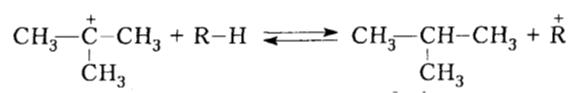
Правильно ли записан крекинг пентана? Как написать крекинг 2-метилпентана?
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок — бесплатно!
- Как написать хороший ответ?
- Крекинг алканов
- Виды и особенности крекинга
- Готовые работы на аналогичную тему
- Термический крекинг
- Каталитический крекинг
- Алканы в топливе
- Правильно ли записан крекинг пентана?
- Напишите уравнение реакции :● Крекинг гептана?
- Проведите крекинг октана?
- В чем преимущество термического и каталитического крекинга?
- При крекинге пентана массой 108 грамм получили пропан объемом 22, 4 литра?
- Уравнение реакций крекинга для C40H82?
- Составить уравнение крекинга с18н38?
- Запишите уравнение реакции крекинга декана?
- 1. Допишите уравнения реакций : а) взаимодействие пропана с бромом б) дегидрирование пентана в)крекинг гексана г) разложение этана?
- ПОМОГИТЕ СРОЧНО НАПИСАТЬ : КРЕКИНГ НОНАНА?
- Крекинг это , помогите?
Ответы и объяснения 1
Первое абсолютно верно
вообще при крекинге разрывается наиболее замещенная цепь
поэтому во втором случае будет образовываться пропан и пропилен
Знаете ответ? Поделитесь им!
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете правильный ответ;
- Писать подробно, чтобы ответ был исчерпывающий и не побуждал на дополнительные вопросы к нему;
- Писать без грамматических, орфографических и пунктуационных ошибок.
Этого делать не стоит:
- Копировать ответы со сторонних ресурсов. Хорошо ценятся уникальные и личные объяснения;
- Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не знаю» и так далее;
- Использовать мат — это неуважительно по отношению к пользователям;
- Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
Крекинг алканов
Вы будете перенаправлены на Автор24
Крекингом называется термическое превращение алканов при температурах 470-540 $^circ$С.
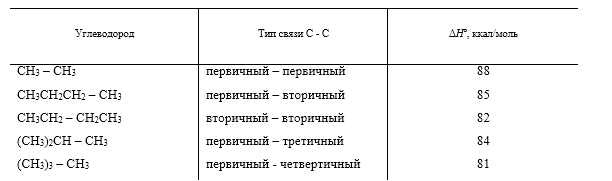
При более высоких температурах (700-1000 $^circ$ С) алканы подвергаются пиролитическому разложению с образованием сложной смеси продуктов, состав и соотношение которых зависят от температуры и времени реакции. При пиролизе происходит расщепление углерод-углеродных связей с образованием алкильных радикалов. Энергия углерод-углеродных связей в алканах близки по величине для первичных, вторичный, третичных и четвертичных атомов углерода (табл. 1) и в жестких условиях пиролиза расщепление любой связи $CH_2 — CH_2$ в нормальных алканах равновероятно.
Для разветвленных углеводородов преимущественно происходит разрыв связи у третичного или четвертичного атома углерода.
Виды и особенности крекинга
Различают термическое и каталитический крекинг. Главным объектом при крекинге является расщепление (деструкция) углеродной цепи по связям С-С с одновременным дегидрированием, изомеризацией и циклизацией. При этом образуются главным образом ненасыщенные углеводороды. Строение продуктов крекинга определяется:
- природой исходного алкана
- условиями проведения процесса (температурой, давлением, природой катализатора).
Начальная температура крекинга алканов зависит от их моле кулярный массы. Чем больше молекулярная масса, тем легче расщепляются алканы. В зависимости от длины углеродной цепи относительная скорость крекинга, например по отношению к пентана, равна:
- Количество атомов углерода 5, 6, 7, 8, 10, 20
- Относительная скорость крекинга 1, 4, 9, 10, 32, 120
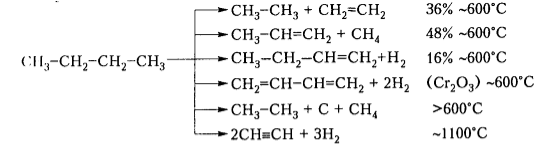
Существуют такие тенденции разрыва связи С-С: с повышением температуры наблюдается смещение места разрыва к краю молекулы, с повышением давления углеродная цепь расщепляется ближе к середине. Так, из бутана при различных условиях могут образовываться следующие соединения:
Готовые работы на аналогичную тему
Рисунок 2. Виды и особенности крекинга. Автор24 — интернет-биржа студенческих работ
Термический крекинг
Термический крекинг — свободнорадикальное процесс, в результате которого образуются главным образом ненасыщенные углеводороды (мономеры). При температурах 450-550 $^circ$С алканы расщепляются на свободные радикалы, способны дальше распадаться на более простые метильные и этильные радикалы, например:
Рисунок 3. Термический крекинг. Автор24 — интернет-биржа студенческих работ
Активные метильные радикалы отщепляют атомы водорода от молекул других алканов с образованием новых свободных радикалов:
Рисунок 4. Термический крекинг. Автор24 — интернет-биржа студенческих работ
Для таких свободных радикалов при крекинге наиболее характерные реакции, которые в целом формируют природу конечных продуктов, а именно:
Реакции $beta $-распада:
Реакции обрыва (рекомбинации):
$beta $-Распад и диспропорционирование свободных радикалов практически всегда проходят по $beta $-связям относительно неспаренного электрона. Это происходит потому, что $beta $-связь в известной степени разрыхлена вследствие уменьшения степени перекрывания соответствующих атомных орбиталей. Электронные облака таких $sigma $-связей С-Н взаимодействуют с неспаренным электроном благодаря эффекту гиперконьюгации ($sigma $-р-сопряжению).
В условиях пиролиза (высокие температуры) наблюдается глубокий распад алканов с образованием ацетиленовых углеводородов, сажи или кокса, водорода и др.
Каталитический крекинг
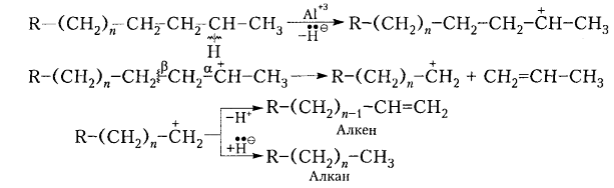
Каталитический крекинг применяют главным образом с целью получения разветвленных алканов (моторного топлива) и ненасыщенных углеводородов. В промышленных условиях процесс проходит в присутствии алюмосиликатных катализаторов или кислот Льюиса при 450-530 $^circ$С и примерно атмосферном давлении. Реакция начинается с отщепления гидрид-иона от алкана с образованием карбокатионов, которые благодаря $beta $-распаду притерпевают дальнейшие изменения:
Рисунок 8. Каталитический крекинг. Автор24 — интернет-биржа студенческих работ
Параллельно процессу образования олефинов происходит реакция изомеризации, которая чрезвычайно важна для получения разветвленных алканов, особенно изобутана и изопентана.
Изомеризация алканов в присутствии сильных кислот Льюиса или суперкислот проходит с образованием карбокатионов. Сильная кислота необходима потому, что алканы проявляют малое родство с протоном, поскольку не содержат $pi $- или n-электронов.
Сначала образуется протонированный алкан с трицентровой двуэлектронной связью у атома углерода, по месту условного присоединения протона, поскольку конкретное место присоединения, как правило, неизвестно. Протонованый алкан быстро превращается в карбокатион, которые путем гидридного и метиланионного перемещений изомеризуются в третичные карбокатионы, то есть в разветвленные алканы:
Рисунок 9. Каталитический крекинг. Автор24 — интернет-биржа студенческих работ
Образованные с помощью каталитического крекинга разветвленные алканы — ценные высокооктановые бензины и сырье для получения каучуков.
Алканы в топливе
В двигателе внутреннего сгорания при сжатии бензиновой паров с воздухом алканы нормального строения образуют перекиси, которые вызывают преждевременное возгорание углеводородной смеси. Это явление называется детонацией и наносит вред двигателю.
Разветвленные алканы лишены этого недостатка. Ценные углеводороды с неоструктурой или структурой, подобной структуре изооктана (последнему условно присвоено октановое число 100, а для н-гептана октановое число составляет 0):
Рисунок 10. Алканы в топливе. Автор24 — интернет-биржа студенческих работ
Итак, если бензин имеет марку, например, 76, то это означает, что ему соответствует октановое число 76 и он проявляет такую же детонационную стойкость, как смесь 76% изооктана и 24% н-гептана. Выше октановое число (130> имеет 2,2,3-триметилбутан (триптан).
Топливо для дизельных двигателей характеризуется другим показателем — цетановым числом. Ценные топлива при этом, наоборот, состоят из алканов нормального, неразветвленного строения. Стандартом для дизельного топлива принят цетан $C_H_$ (цетановое число 100).
Правильно ли записан крекинг пентана?
Химия | 10 — 11 классы
Правильно ли записан крекинг пентана?
Как написать крекинг 2 — метилпентана?
1) это один из возможных вариантов.
Напишите уравнение реакции :● Крекинг гептана?
Напишите уравнение реакции :
● Хлорирование цикла пентана на свету.
Проведите крекинг октана?
Проведите крекинг октана.
В чем преимущество термического и каталитического крекинга?
В чем преимущество термического и каталитического крекинга?
При крекинге пентана массой 108 грамм получили пропан объемом 22, 4 литра?
При крекинге пентана массой 108 грамм получили пропан объемом 22, 4 литра.
Найти объемную долю выхода пропана.
Уравнение реакций крекинга для C40H82?
Уравнение реакций крекинга для C40H82.
Составить уравнение крекинга с18н38?
Составить уравнение крекинга с18н38.
Запишите уравнение реакции крекинга декана?
Запишите уравнение реакции крекинга декана.
1. Допишите уравнения реакций : а) взаимодействие пропана с бромом б) дегидрирование пентана в)крекинг гексана г) разложение этана?
1. Допишите уравнения реакций : а) взаимодействие пропана с бромом б) дегидрирование пентана в)крекинг гексана г) разложение этана.
ПОМОГИТЕ СРОЧНО НАПИСАТЬ : КРЕКИНГ НОНАНА?
ПОМОГИТЕ СРОЧНО НАПИСАТЬ : КРЕКИНГ НОНАНА.
Крекинг это , помогите?
Крекинг это , помогите.
Если вам необходимо получить ответ на вопрос Правильно ли записан крекинг пентана?, относящийся к уровню подготовки учащихся 10 — 11 классов, вы открыли нужную страницу. В категории Химия вы также найдете ответы на похожие вопросы по интересующей теме, с помощью автоматического «умного» поиска. Если после ознакомления со всеми вариантами ответа у вас остались сомнения, или полученная информация не полностью освещает тематику, создайте свой вопрос с помощью кнопки, которая находится вверху страницы, или обсудите вопрос с посетителями этой страницы.
1) NaOH + H2 2) ZnS 3) ZnO 4) ZnCl2 + H2 5) ZnCl2 + Fe 6) Mg(OH)2 + H2 7) Mg3P2 8) — 9) MgCl2 10) — 11) MgSO4 + Ni 12) AlBr3 13) Al2(SO4)3 + Fe 14) AlI3 + H2.
FeO + P = Fe + P2O5 1)восстановитель Fe (в степени — 2) – 2е = Fe (в нулевой степени) 2)окислитель Р (в нулевой степени) + 5е = P (в степени + 5).
Химия используется при уборке в доме , мытьё посуды . В сельской хозяйственности для орошения полей от вредителей . В медецине для создания лекарств .
Ba — металлическая BaBr2 — ионная HBr — ковалентная полярная Br2 — ковалентная не полярная.
Ba — металлическая HBr — Ковалентная полярная Br2 — ковалентная не полярная BaBr2 — ионная.
Ми знаємо формулу знаходження масової частки елемента в речовині і у цю формулу підставляємо значення, знаходимо скількі атомів Оксигена у формулі .
В этих местах останутся желтые пятна, а потом они станут оранжевые.
2Al(OH)3 = Al2O3 + 3H2O H2CO3 = CO2 + H2O CACO3 = CAO + CO2( газ) CU(OH)2 = CUO + H2O Zn + 2HCl = ZnCl2 + H°2(газ) Ca° + H2SO4 = CaSO4 + H°2(газ) 3Mg° + 2H3PO4 = Mg3(PO4)2 + H°2(газ) 2Al° + Fe2O3 = Al2O3 + 2Fe° Cu(No3) + NaOH = Cu(OH) (осадок) + NaNo..
2Al(OH)3 — — >Al2O3 + 3H2O H2CO3 — — >CO2 + H2O CaCO3 — — >CaO + CO2 Cu(OH)2 — — >CuO + H2O Zn + 2HCL — — >ZnCL2 + H2 Ca + H2SO4 — — >CaSO4 + H2 3Mg + 2H3PO4 — — >Mg3(PO4)2 + 3H2 2Al + Fe2O3 — — >2Fe + Al2O3 Cu(NO3)2 + 2NaOH — — >Cu(OH)2 + 2NaNO3 HNO..
Вещества : вода, медь Тела : льдина , ваза, труба, гвоздь, сосулька.