Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Содержание Фосфид калия
Фосфид калия (фосфористый калий) — бинарное неорганическое соединение калия и фосфора с формулой K3P. Зелёные кристаллы. СодержаниеПолучение
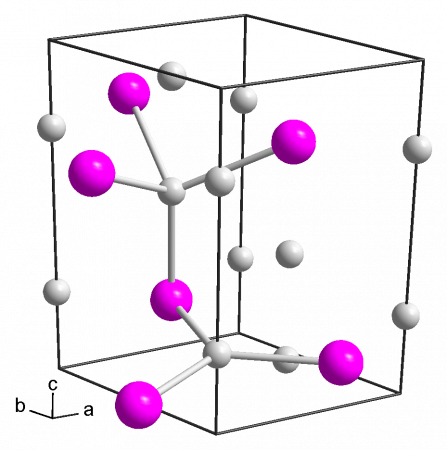
3K + P → 700oC K3P Физические свойстваФосфид калия образует кристаллы гексагональной сингонии, пространственная группа P 63/mmc, параметры ячейки a = 0,5691 нм , c = 1,005 нм , Z = 2 . Химические свойстваСильный восстановитель. Реагирует с водой и влагой воздуха с выделением высокотоксичного и легковоспламеняющегося газообразного фосфина: Калий: способы получения и химические свойстваКалий К — это щелочной металл. Серебристо-белый, мягкий, легкоплавкий. Относительная молекулярная масса Mr = 39,098; относительная плотность для твердого состояния d = 0,8629; относительная плотность для жидкого состояния d = 0,83; tпл = 63, 51º C; tкип = 760º C. Способ получения1. Калий получают в промышленности путем разложения гидрида калия при температуре 400º С в вакууме, при этом образуются калий и водород : 2KH = 2K + H2 2. В результате электролиза жидкого гидроксида калия образуются калий, кислород и вода : 4KOH → 4K + O2↑ + 2H2O Качественная реакцияКачественная реакция на калий — окрашивание пламени солями калия в фиолетовый цвет . Химические свойства1. Калий — сильный восстановитель . Поэтому он реагирует почти со всеми неметаллами : 1.1. Калий легко реагирует с водородом при 200–350º C образованием гидрида калия: 2K + H2 = 2KH 1.2. Калий сгорает в кислороде с образованием надпероксида калия: 1.3. Калий активно реагирует при комнатной температуре с фтором, хлором, бромом и йодом . При этом образуются фторид калия, хлорид калия, бромид калия, йодид калия : 2K + F2 = 2KF 2K + Cl2 = 2KCl 2K + Br2 = 2KBr 2K + I2 = 2KI 1.4. С серой, теллуром и селеном реагирует при температуре 100–200º C с образованием сульфида калия, селенида калия и теллурид калия : 2K + S = K2S 2K + Se = K2Se 2K + Te = K2Te 1.5. Калий реагирует с фосфором при 200º C в атмосфере аргона с образованием фосфида калия: 3K + P = K3P 2. Калий активно взаимодействует со сложными веществами: 2.1. Калий реагирует с водой . Взаимодействие натрия с водой приводит к образованию щелочи и газа водорода: 2K 0 + 2 H2 O = 2 K + OH + H2 0 2.2. Калий взаимодействует с кислотами . При этом образуются соль и водород. 2.2.1. Ка лий реагирует с разбавленной соляной кислотой, при этом образуются хлорид калия и водород : 2K + 2HCl = 2KCl + H2 ↑ 2.2.2. При взаимодействии с разбавленной с ерной кислотой образуется сульфат калия, сероводород и вода: 2.2.3. Реагируя с азотной кислотой калий образует нитрат калия, можно образовать газ оксид азота (II), газ оксид азота (I), газ азот и воду. 2.2.4. В результате реакции насыщенной сероводородной кислоты и калия в бензоле образуется осадок гидросульфид калия и газ водород: 2K + 2H2S = 2KHS↓ + H2↑ 2.3. Калий при температуре 65–105º C может реагировать с аммиаком , при этом образуются амид натрия и водород: 2.4. Калий может взаимодействовать с гидроксидами: Например , Калий взаимодействует с гидроксидом калия при температуре 450º С, при этом образуется оксид калия и водород: 2K + 2KOH = 2K2O + H2 | |||||||||||||||||||||||||