Видео:Гидролиз солей. 1 часть. 11 класс.Скачать

We are checking your browser. gomolog.ru
Видео:Гидролиз солей. Классификация солей. Решение примеров.Скачать

Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
Видео:Гидролиз солей. 9 класс.Скачать

What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e27070f2e167597 • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Видео:Химические уравнения // Как Составлять Уравнения Реакций // Химия 9 классСкачать

Гидролиз солей Методические указания (стр. 6 )
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 5 6 |
Кг,1 = Kw / 
Для 2-й ступени гидролиза
ZnOH+ + НОН 
аналогичный расчет дает: Кг,2 = 1,1 ⋅ 10–9, β2 ≈ 0,01, [H+]2 = 1,03 ⋅ 10–7 М, или ≈ 1% суммы [H+]1 и [H+]2, рН = 4,975.
Таким образом, для расчета рН 0,01 М ZnCl2 достаточно учесть первую ступень гидролиза.
Кислотную диссоциацию амфотерного гидроксида Zn(OH)2 не учитываем, так как Ка Кг,2.
Вторую ступень гидролиза следует учитывать при расчете рН растворов некоторых сильно гидролизующихся солей, например, 0,1 и 0,01 М нитратов олова (II), ртути (II) и железа (III), а также образующих малорастворимые (SbOCl, BiOCl) или летучие продукты (H2S).
4. ВЛИЯНИЕ УСЛОВИЙ
НА СТЕПЕНЬ ГИДРОЛИЗА СОЛЕЙ
4.1. Разбавление растворов солей
С уменьшением концентрации растворов гидролиз усиливается. Как было показано ранее, понижение концентрации соли, гидролизующейся по катиону (аниону), приводит к увеличению степени гидролиза β.
Экспериментальным подтверждением этого обстоятельства может служить, например, помутнение растворов некоторых солей, в частности, нитрата висмута (III) или хлорида сурьмы (III) по мере их разбавления. Прибавление воды приводит к образованию малорастворимого нитрата висмутила BiONO3 или оксохлорида сурьмы (III) SbOCl.
4.2. Нагревание растворов
Константа диссоциации воды увеличивается с ростом температуры в большей степени, чем константа диссоциации продуктов гидролиза (слабых кислот и оснований). Поэтому при нагревании степень гидролиза возрастает. К этому выводу можно придти и иначе: так как реакция нейтрализации экзотермична, то гидролиз будучи противоположным ей процессом эндотермичен; поэтому, в соответствии с принципом Ле-Шателье, нагревание вызывает усиление гидролиза.
Например, при комнатной температуре гидролиз соли FeCl3 идет по уравнению:
FeCl3 + HOH 
При нагревании и разбавлении раствора гидролиз идет до образования Fe(OH)2Cl и даже FeO(OH) (т)
FeOHCl2 + HOH 
Fe(OH)2Cl + HOH 
Fe(OH)3 (p) → FeO(OH) ↓ + H2O.
Степень гидролиза 0,1 М раствора CrCl3 возрастает от 4,6% при 0° С до 40% при 100° С.
4.3. Изменение рН растворов
Поскольку при обратимом гидролизе устанавливается динамическое равновесие, то в соответствии с принципом Ле-Шателье можно сместить это равновесие в ту или иную сторону введением в раствор кислоты или основания. Этим часто пользуются для усиления или подавления процесса гидролиза, в частности, с целью поддержания постоянной концентрации ионов водорода в растворе.
Прибавление сильной кислоты вызывает усиление гидролиза по аниону (смещение равновесия вправо в результате связывания ионов ОН– в воду); гидролиз по катиону усиливается в присутствии щелочи.
Если к раствору тетрабората натрия добавить соляную кислоту, т. е. связать гидроксид-ионы, то гидролиз:
Na2B4O7 + 7H2O 
усилится; если же добавить щелочь NaOH, то равновесие сместится влево – гидролиз будет подавлен.
Видео:РЕАКЦИИ ИОННОГО ОБМЕНА, ИОННОЕ УРАВНЕНИЕ - Урок Химия 9 класс / Подготовка к ЕГЭ по ХимииСкачать

Опыт 2. Смещение равновесия гидролиза при разбавлении раствора
Налить в пробирку 1–2 мл раствора нитрата висмута Bi(NO3)3 и постепенно разбавлять водой до выпадения осадка. Прибавить в пробирку с осадком несколько капель концентрированной азотной кислоты. Наблюдать растворение осадка.
Требования к результатам опыта
1. Составить сокращенные, полные ионные и молекулярные уравнения реакции гидролиза нитрата висмута по первой и второй ступени.
2. Сделать вывод о смещении равновесия при разбавлении раствора и добавлении кислоты.
Опыт 3. Смещение равновесия гидролиза при изменении температуры
В пробирку налить 5–6 мл раствора ацетата натрия CH3COONa и добавить 1–2 капли фенолфталеина. Содержимое пробирки разделить на 2 части, одну из них оставьте для сравнения, другую – нагреть до кипения. Сравнить окраску индикатора в обеих пробирках. Дать пробирке охладиться и снова сравнить окраску индикатора в обеих пробирках.
Требования к результатам опыта
1. Составить сокращенное, полное ионное и молекулярное уравнение реакции гидролиза CH3COONa.
2. Сделать вывод о смещении равновесия при изменении температуры.
Опыт 4. Реакции обмена, сопровождаемые гидролизом
В одну пробирку налить 2–3 мл раствора сульфата меди (II), в другую – столько же хлорида железа (III). Затем в каждую пробирку добавить по 2–3 мл раствора карбоната натрия. Отметить выделение углекислого газа в обеих пробирках и выпадение осадков. В первой пробирке в осадок выпадает карбонат гидроксомеди (II), во второй – гидроксид железа (III).
Требования к результатам опыта
1. Закончить уравнения реакций в молекулярном и ионном виде:
2. Объяснить, почему не получились карбонаты меди и железа.
Примеры решения задач
Пример 9.1.Какие продукты получатся при смешивании растворов AlCl3 и Na2S? Составить ионно-молекулярные и молекулярное уравнение реакции.
Решение. Соль AlCl3 гидролизуется по катиону, а Na2S – по аниону:
Al 3+ + H2O ↔ AlOH 2+ + H + ,
S 2− + H2O ↔ HS ‾ + OH ‾ .
Гидролиз приведенных солей обычно ограничиваются первой ступенью. При смешивании растворов этих солей ионы H + и OH ‾ связываются в молекулы слабого электролита H2O, сдвигая гидролитическое равновесие вправо. Это приводит к тому, что усиливается гидролиз каждой из солей до образования Al(OH)3 и H2S. Ионно-молекулярные и молекулярное уравнения имеют следующий вид:
2Al 3+ + 6Cl − + 6Na + +3S 2− + 6H2O = 2Al(OH)3↓ + 3H2S↑ + 6Na + + 6Cl −
Таким образом, продуктами гидролиза являются Al(OH)3 и H2S.
Пример 9.2. К раствору Na2CO3 добавили следующие вещества: а) HCl;
б) NaOH; в) Cu(NO3)2; г) K2S. В каких случаях гидролиз карбоната натрия усилится? Почему? Составить ионно-молекулярные уравнения гидролиза соответствующих солей.
Решение. Карбонат натрия Na2CO3 – соль слабой кислоты и сильного основания гидролизуется по аниону: СО3 2− + Н2О 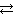
Чтобы усилить гидролиз соли, нужно удалить ионы ОН − и таким образом сместить равновесие (1) вправо. Этого можно достигнуть добавлением в раствор Na2CO3 веществ, растворы которых содержат ионы Н + . Ионы Н + свяжут ионы ОН − из (1) в молекулы слабого электролита Н2О, в результате чего равновесие (1) смесится вправо и гидролиз усилится. В нашей задаче такими веществами являются кислота HCl (HCl → Н + + Cl − ) и соль Cu(NO3)2, содержащая ионы Н + вследствие ее гидролиза по катиону Cu 2+ + H2O 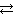
Задачи и упражнения для самостоятельного решения
9.1. Какие из перечисленных ниже солей подвергаются гидролизу: NaCN, KNO3, CuCl2, ZnSO4? Cоставить ионно-молекулярные и молекулярные уравнения реакций, указать рН среды.
9.2. К раствору Cr2(SO4)3 добавили раствор K2S. Объяснить причину образования осадка и выделения газа. Составить молеклярное и ионно-молекулярные уравнения реакции.
9.3. Какие из солей: Na2SO4, К2SO3, NH4CN, LiCl, Fe2(SO4)3 подвергаются гидролизу? Составить ионно-молекулярные и молекулярные уравнения гидролиза этих солей. Какое значение pH (> 7 3+ +H2O 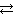
б) S 2− + H2O 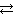
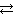
9.6. Подобрать по два уравнения в молекулярном виде к каждому из трех ионно-молекулярных уравнений: а) Fe 3+ + 2H2O 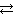
б) CO3 2- + H2O 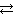
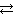
9.7. Составить ионно-молекулярные и молекулярные уравнения реакций для солей, подвергающихся гидролизу, указать реакцию среды: K2SO3, Cr(NO3)3, NaNO2, NiSO4.
9.8. В какой цвет будет окрашен лакмус в водных растворах: K2S, (NH4)2SO4, Na2CO3, Li2SO4? Ответ обосновать ионно-молекулярными и молекулярными уравнениями реакций гидролиза солей.
9.9. Составить ионно-молекулярные и молекулярные уравнения реакций для солей, подвергающихся гидролизу, указать реакцию среды: KI, Cu(NO3)2, K2SiO3, ZnSO4.
9.10. Какие из приведенных солей подвергаются гидролизу по катиону, по аниону, по катиону и аниону: BaS, Mn(NO3)2, AlCl3, Cr2S3? Указать pH среды для водных растворов солей. Составить ионно-молекулярные и молекулярные уравнения гидролиза.
9.11. Какие из солей NaI, CrCl3, NH4NO3, NH4NO2 подвергаются гидролизу? Составить ионно-молекулярные и молекулярные уравнения гидролиза этих солей, указать реакцию среды.
9.12. К раствору Al2(SO4)3 добавили следующие вещества: а) H2SO4; б) KOH;
в) Na2SO3; г) ZnSO4. В каких случаях гидролиз сульфата алюминия усилится? Почему? Составить ионно-молекулярные уравнения гидролиза соответствующих солей.
9.13. Какие из веществ: Na2CO3, Li2SO3, CuCl2, MgSO4, BaS создадут избыток гидроксид-ионов в растворе своей соли? Почему? Составить ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
9.14. При сливании растворов солей CrCl3 и Na2CO3 образуется осадок Cr(OH)3 и выделяется газ СО2. Объяснить причину и написать молекулярное и ионно-молекулярные уравнения реакции.
9.15. Написать уравнения реакций гидролиза в ионно-молекулярном и молекулярном виде: ацетата лития CH3COOLi, хлорида алюминия NH4Cl, цианида аммония NH4CN, сульфида бария BaS.
9.16. Объяснить, почему водные растворы NaNO2, Li2CO3, Na3PO4 имеют щелочную реакцию. Ответ подтвердить уравнениями реакций в ионно-молекулярном и молекулярном виде.
9.17. К раствору FeCl3 добавили следующие вещества: а) HCl; б) KOH; в) CuCl2; г) Na2CO3. В каких случаях гидролиз хлорида железа усилится? Почему? Составить ионно-молекулярные уравнения гидролиза соответствующих солей.
9.18. При смешивании растворов Fe2(SO4)3 и K2S образуется осадок и выделяется газ. Написать молекулярное и ионно-молекулярные уравнения совместного гидролиза солей.
9.19. Составить ионно-молекулярные и молекулярные уравнения гидролиза cолей: NH4CH3COO, Ca(NO2)2, К3PO4, MnCl2.
9.20. Почему при добавлении горячей воды к водному раствору хлорида железа (III) выпадает осадок? Подтвердить это уравнениями реакций в ионно-молекулярном и молекулярном виде.
Лабораторная работа 10
Коллоидные растворы
Цель работы: изучить основные понятия коллоидной химии «дисперсность, коллоидный раствор, дисперсная фаза, дисперсионная среда, коллоидная частица, мицелла, коагуляция, седиментация, пептизация»; получение коллоидных растворов; научиться составлять схемы мицелл.
Задание: получить коллоидные растворы гидроксида железа (III) методоми конденсации и диспергирования осадка Fe(OH)3. Выполнить требования к результатам опытов, оформить отчет, решить задачу.
Теоретическое введение
Системы, в которых одно вещество распределено в мелкораздробленном состоянии в среде другого, называются дисперсными. Раздробленное (распределенное вещество) называется дисперсной фазой, а среда, в которой распределена дисперсная фаза – дисперсионной средой.Дисперсные системы с размером частиц дисперсной фазы от 1 до 100 нм называются коллоидными растворамиили золями.
Дисперсная фаза в коллоидном растворе (или золе) представлена коллоидными частицами, в состав которых входят ядро, зарядообразующие ионы и противоионы. Зарядообразующие ионы могут быть положительно или отрицательно заряженными, поэтому и коллоидные частицы имеют либо положительный, либо отрицательный заряд. Заряженные коллоидные частицы притягивают к себе молекулы Н2О из дисперсионной среды; так создается гидратная оболочка, окружающая коллоидную частицу.
Примерный состав коллоидных частиц золей Sb2S3 и Fe(OH)3 можно выразить следующими формулами:
Противоионы Н + или Cl — , которые входят в состав коллоидных частиц, называют связанными. Свободные противоионы остаются в дисперсионной среде.
Коллоидную частицу и эквивалентную ей часть дисперсионной среды (гидратированных свободных противоионов) называют мицеллой. Мицеллу считают структурной единицей коллоидного раствора. Формулы
выражают примерный состав мицелл золей сульфида сурьмы и гидроксида
железа.
Коллоидная дисперсность вещества является промежуточной между группой дисперсности, характерной для взвеси и молекулярной, характерной для истинных растворов. Поэтому коллоидные растворы получают либо из истинных растворов путем укрупнения частиц молекулярной дисперсности до определенного предела (максимум до 100 нм), либо из взвеси путем дробления грубодисперсных частиц также до определенного предела (минимум до 1 нм). В этой связи различают конденсационные методы (укрупнение частиц) и метод диспергирования(дробление частиц).
Конденсация частиц молекулярной дисперсности может происходить в процессе гидролиза солей некоторых поливалентных металлов, например, FeCl3. Гидролиз иона Fe 3+ протекает по ступеням:
Fe 3+ + H2O = FeOH 2+ + H +
Гидроксид железа Fe(OH)3 не выпадает в осадок, т.к. степень гидролиза FeCl3 по третьей ступени мала.
Зарядообразующими ионами в процессе образования золя могут быть Fe 3+ , FeOH 2+ , Fe(OH)2 + , а противоионами − Cl − .
Примером получения золей методом диспергирования может служить получение коллоидного раствора Fe(OH)3 путем химического дробления осадка гидроксида железа (III), называемого пептизацией. Пептизатором может быть электролит с одноименным ионом, входящим в состав осадка, например, FeCl3.
Добавление пептизатора к небольшому количеству осадка в водной среде приводит к тому, что ионы Fe 3+ проникают в глубь осадка и разрыхляют его, постепенно дробя до коллоидной дисперсности. Дробление называют химическим потому, что ионы непросто проникают в осадок, а, взаимодействуя с его частицами, образуют дисперсную фазу положительного заряда. Ионы Fe 3+ являются зарядообразующими в составе коллоидных частиц получающегося золя, а ионы Cl − противоионами.
Коллоидные растворы обладают специфическими оптическими, кинетическими и электрическими свойствами (специфика связана с размерами и зарядом коллоидных частиц) и характеризуются высокой кинетической и агрегативной устойчивостью.
Устойчивость коллоидного раствора можно нарушить. Потеря агрегативной устойчивости золя приводит к укрупнению частиц дисперсной фазы, их слипанию. Этот процесс называют коагуляцией. Коагуляция вызывает нарушение кинетической устойчивости системы, которая приводит к образованию осадка (коагулята). Этот процесс называют седиментацией.
Примерный состав коагулята золей сульфида сурьмы и гидроксида железа выражают формулами:
Выполнение работы
Опыт 1. Получение золя гидроксида железа (III) методом конденсации
Пробирку заполнить водой (примерно до половины ее объема) и поставить в горячую водяную баню. Через 5–7 минут внести в пробирку 2–3 капли концентрированного раствора FeCl3. Наблюдать образование краснооранжевого золя Fe(OH)3. Раствор сохранить для опыта 3.
Требование к результатам опыта
Указать состав ядра коллоидной частицы полученного золя, состав коллоидной частицы, состав мицеллы.
Опыт 2. Получение золя гидроксида железа (III) методом диспергирования осадка Fe(OH)3
В стакан объемом 50 мл налить 25 мл воды и добавить 10 капель 20 %-го раствора хлорида железа FeCl3. Перемешать содержимое стакана и после этого добавить по каплям раствор гидроксида аммония NH4OH до полного осаждения гидроксида Fe(OH)3.
После того как осадок уплотнится на дне стакана, осторожно слить с него избыток раствора. Осадок промыть 2–3 раза, добавляя к нему небольшие порции воды и сливая эту воду после того, как между ними и осадком четко обозначится граница раздела.
К осадку гидроксида железа (III) прилить 25 мл H2O и 3 капли 20 %-го раствора FeCl3. Смесь хорошо перемешать. Для ускорения процесса пептизации нагреть раствор на водяной бане. Прекратить нагревание, когда раствор приобретет устойчивую краснооранжевую окраску.
Требование к результатам опыта
Составить схему строения мицеллы золя гидроксида железа (III) в растворе хлорида железа FeCl3.
Опыт 3. Коагуляция золя гидроксида железа электролитами
Разлить в три пробирки золь гидроксида железа, полученный в опыте 1. По каплям прибавить в первую пробирку NaCl , во вторую – Na2SO4 , в третью – Na2HPO4. Считать число капель до изменения вида раствора (появления мути и осадка).
Требования к результатам опыта
1. Написать формулу мицеллы золя гидроксида железа.
2. Объяснить влияние заряда коагулирующего иона на время, проходящее до начала коагуляции.
Примеры решения задач
Пример 10.1. Золь иодида серебра получен при добавлении к раствору AgNO3 избытка KI. Определить заряд частиц полученного золя и написать формулу его мицеллы.
Решение. При смешивании растворов AgNO3 и KI протекает реакция
Ядро коллоидной частицы золя иодида серебра состоит из агрегата молекул (mAgI) и зарядообразующих ионов I ‾ , которые находятся в растворе в избытке и обеспечивают коллоидным частицам отрицательный заряд. Противоионами являются гидратированные ионы калия. Формула мицеллы иодида серебра имеет вид <[(mAgI)·nI ‾ ·(n-x)К + ·yH2O] x − + xК + ∙zH2O> 0 .
Пример 10.2.Золь кремневой кислоты был получен при взаимодействии растворов K2SiO3 и HCl. Написать формулу мицеллы золя и определить, какой из электролитов был взят в избытке, если противоионы в электрическом поле движутся к катоду.
Решение. Образование золя кремневой кислоты происходит по реакции
Чтобы двигаться к катоду (отрицательному электроду) противоионы должны иметь положительный заряд, а коллоидные частицы золя должны быть заряжены отрицательно. На электронейтральном агрегате частиц (mH2SiO3) адсорбируются ионы элемента, входящего в состав ядра. Таковыми являются ионы HSiO3 ‾ , которые образуются в результате гидролиза соли K2SiO3:
K2SiO3 + H2O 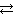
SiO3 2− + H2O 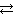
Ионы HSiO3 ‾ , адсорбируясь на поверхности частиц золя кремниевой кислоты, сообщают им отрицательный заряд. Противоионами являются гидратированные ионы водорода H + . Формула мицеллы золя кремневой кислоты
Так как коллоидные частицы золя кремневой кислоты заряжены отрицательно за счет ионов HSiO3 ‾ , то, следовательно, в избытке был взят K2SiO3.
Пример 10.3. Какого из веществ, K2SO4 или KCl, потребуется меньше, чтобы вызвать коагуляцию коллоидного раствора гидроксида железа (II), полученного по реакции FeCl2 + 2NaOH = Fe(OH)2 + 2NaCl?
Решение. Из формулы коллоидной частицы золя гидроксида железа (II) [(mFe(OH)2·nFe 2+ 2(n-x)Cl ‾ ∙yH2O] 2 x + видно, что частицы золя имеют положительный заряд. Коагуляцию золя вызывает тот из ионов прибавленного электролита, заряд которого противоположен заряду коллоидной частицы. В данной задаче – это ионы SO4 2− и Cl‾. Коагулирующая способность иона определяется его зарядом – чем больше заряд иона, тем больше его коагулирующая способность. Заряд иона SO4 2− больше заряда иона Cl‾, поэтому, чтобы вызвать коагуляцию коллоидного раствора гидроксида железа (II), раствора K2SO4 потребуется меньше, чем раствора KCl.
Пример 10.4. Составить схему строения мицеллы золя гидроксида меди (II) в растворе хлорида меди.
Решение. В состав мицеллы гидроксида меди входят: агрегат молекул (mCu(OH)2), адсорбированный слой, состоящий из зарядообразующих ионов меди Cu 2+ и гидратированных противоионов хлора, и диффузный слой гидратированных противоионов хлора. Схема строения мицеллы гидроксида меди
Задачи и упражнения для самостоятельного решения
10.1. Составить схему строения мицеллы золя сульфида мышьяка As2S3 в растворе сульфида натрия.
10.2.Какой из солей: Ca(NO3)2, NaNO3 или Al(NO3)3 потребуется меньше для коагуляции золя хлорида серебра?
10.3. Составить схему строения мицеллы золя сульфата бария в растворе сульфата натрия.
10.4. Образование золя сульфата бария происходит по реакции
Написать формулу мицеллы золя BaSO4 и определить, какой из электролитов был в избытке, если противоионы в электрическом поле движутся к аноду.
10.5. Составить схему строения мицеллы золя кремниевой кислоты в растворе силиката натрия.
10.6. При пропускании избытка сероводорода в раствор AsCl3 получили золь сульфида мышьяка As2S3. Определить знак заряда частиц золя и написать формулу мицеллы золя сульфида мышьяка.
10.7. Золь иодида свинца был получен по реакции
Составить формулу мицеллы золя иодида свинца и определить, какой из электролитов был взят в избытке, если при электрофорезе противоионы двигались к аноду (положительному электроду).
10.8. Составить схему строения мицеллы золя кремниевой кислоты в растворе соляной кислоты.
10.9. Какого электролита, FeCl3 или AgNO3, нужно взять в избытке, чтобы частицы золя хлорида серебра в электрическом поле двигались к аноду? Написать формулу мицеллы золя.
10.10. Составить схему строения мицеллы гидроксида железа (III) в растворе соляной кислоты.
10.11. Составить схему строения мицеллы оловянной кислоты H2SnO3 в растворе станната калия K2SnO3.
10.12. Какой из солей, NaCl, Na2SO4 или Na3PO4, потребуется больше для коагуляции золя гидроксида железа (III), частицы золя которого заряжены положительно?
10.13. Золь бромида серебра был получен по реакции
Составить формулу мицеллы золя и определить, какой из электролитов был взят в избытке, если при электрофорезе частицы золя двигались к катоду.
10.14. Составить схему строения мицеллы гидроксида железа (III) в растворе хлорида железа (III).
10.15. Какого из веществ, хлорида алюминия AlCl3, нитрата бария Ba(NO3)2 или сульфата калия K2SO4, потребуется меньше для коагуляции золя кремниевой кислоты, частицы которого заряжены отрицательно?
10.16. Составить схему строения мицеллы сульфида сурьмы (III) в растворе сульфата калия.
10.17. Золь сульфида кадмия был получен по реакции
Составить формулу мицеллы золя сульфида кадмия и определить, какой из электролитов был взят в избытке, если при электрофорезе противоионы двигались к аноду.
10.18. Золь хлорида свинца был получен по реакции
Составить формулу мицеллы золя и определить, какой из электролитов был взят в избытке, если при электрофорезе частицы золя двигались к катоду (отрицательному электроду).
10.19. При пропускании избытка сероводорода в раствор SbCl3 получили золь сульфида сурьмы Sb2S3. Определить знак заряда частиц золя и написать формулу мицеллы золя сульфида сурьмы.
10.20. Представить строение мицеллы оксида олова (IV) в растворе K2SnO3.
🔥 Видео
ГИДРОЛИЗ СОЛЕЙ | 9 класс | Кратко и понятноСкачать

ГИДРОЛИЗ СОЛЕЙ. Теория + практикаСкачать

Химия 9 класс (Урок№8 - Гидролиз солей.)Скачать

ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ХИМИЯ 8 класс // Подготовка к ЕГЭ по Химии - INTENSIVСкачать

Ступенчатый гидролиз по катиону. Слабое основание + сильная кислотаСкачать

Все об электролизе и задании 20 за 20 минут | Химия ЕГЭ 2023 | УмскулСкачать

Всё про ГИДРОЛИЗ для ЕГЭ ПО ХИМИИ. с ЭКСПЕРИМЕНТАМИ!Скачать

Ступенчатый гидролиз солей по аниону. Решаем примеры.Скачать

Гидролиз солейСкачать

Летучка: все реакции гидролиза | Химия ЕГЭ 2023 | УмскулСкачать

Химия 11 класс (Урок№7 - Гидролиз органических и неорганических соединений.)Скачать

Гидролиз солей | ХимияСкачать

Гидролиз | Химия ЕГЭ | УмскулСкачать

Гидролиз солей. Опыт 1. Окраска индикаторов в различных средахСкачать

Гидролиз солей.ПримерыСкачать


