Вопрос по химии:
Реакцию присоединения воды называют реакцией гидратации, а как следует назвать реакцию присоединения водорода? Напишите уравнения реакций присоединения водорода для этилена и для пропилена.
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок — бесплатно!
- Как написать хороший ответ?
- Гидратация пропилена: уравнение реакции
- История
- Выделение пропилена
- Особенности строения пропилена
- Теория гидратации
- Механизм гидратации
- Реакция: как она происходит
- Как записать реакцию?
- Где это применяется?
- Реакция получения ацетона
- Уравнение реакции
- Заключение
- Химические свойства алкенов
- Химические свойства алкенов
- 1. Реакции присоединения
- 1.1. Гидрирование
- 1.2. Галогенирование алкенов
- 1.3. Гидрогалогенирование алкенов
- 1.4. Гидратация
- 1.5. Полимеризация
- 2. Окисление алкенов
- 2.1. Каталитическое окисление
- 2.2. Мягкое окисление
- 2.2. Жесткое окисление
- 2.3. Горение алкенов
- 3. Замещение в боковой цепи
- 4. Изомеризация алкенов
Ответы и объяснения 1
Реакция присоединения водорода — гидрирование.
СН₂=СН₂ + Н₂ → СН₃-СН₃
этилен этан
СН₃-СН=СН₂ + Н₂ → СН₃-СН₂-СН₃
пропилен пропан
Реакции гидрирования идут при нагревании и повышенном давлении.
Знаете ответ? Поделитесь им!
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете правильный ответ;
- Писать подробно, чтобы ответ был исчерпывающий и не побуждал на дополнительные вопросы к нему;
- Писать без грамматических, орфографических и пунктуационных ошибок.
Этого делать не стоит:
- Копировать ответы со сторонних ресурсов. Хорошо ценятся уникальные и личные объяснения;
- Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не знаю» и так далее;
- Использовать мат — это неуважительно по отношению к пользователям;
- Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
Гидратация пропилена: уравнение реакции
Органические вещества занимают важное место в нашей жизни. Они являются основной составляющей полимеров, которые окружают нас повсюду: это и полиэтиленовые пакеты, и резина, а также множество других материалов. Полипропилен занимает в этом ряду не последнюю ступень. Он также входит в состав различных материалов и применяется в ряде отраслей, таких как строительство, имеет бытовое применение в качестве материала для пластиковых стаканчиков и прочих мелких (но не по масштабам производства) нужд. Прежде чем поговорить о таком процессе, как гидратация пропилена (благодаря которому, кстати, мы можем получить изопропиловый спирт), обратимся к истории открытия этого необходимого для промышленности вещества.
История
Как таковой даты открытия пропилен не имеет. Однако его полимер — полипропилен -был фактически открыт в 1936 году известным немецким химиком Отто Байером. Конечно, теоретически было известно, как можно получить столь важный материал, но практически сделать это не удавалось. Удалось это только в середине двадцатого века, когда немецкий и итальянский химики Циглер и Натт открыли катализатор полимеризации непредельных углеводородов (имеющих одну и более кратных связей), который впоследствии так и назвали: катализатор Циглера-Натта. До этого момента решительно невозможно было сделать так, чтобы реакция полимеризации таких веществ пошла. Были известны реакции поликонденсации, когда без воздействия катализатора вещества соединялись в полимерную цепь, образуя при этом побочные вещества. Но с непредельными углеводородами это сделать не удавалось.
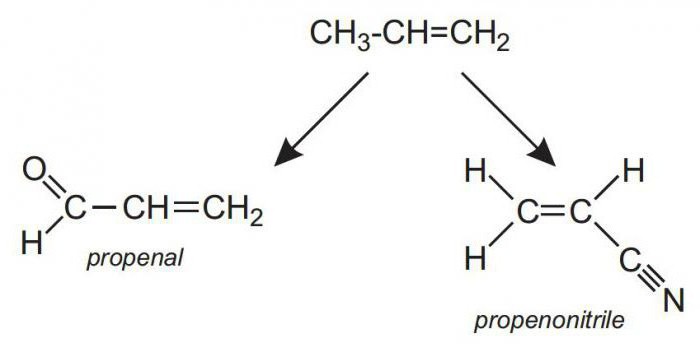
Ещё одним важным процессом, связанным с этим веществом, была его гидратация. Пропилена в годы начала его применения было достаточно много. И всё это благодаря изобретённым разными нефте- и газоперерабатывающими компаниями способам излечения пропена (так иногда тоже называют описываемое вещество). При крекинге нефти он был побочным продуктом, а когда оказалось, что его производное, изопропиловый спирт, является основой для синтеза множества полезных для человечества веществ, многие фирмы, такие как BASF, запатентовали свой способ его производства и начали массовую торговлю этим соединением. Гидратация пропилена была опробована и применена раньше полимеризации, именно поэтому ацетон, пероксид водорода, изопропиламин начали производить раньше полипропилена.
Очень интересен процесс выделения пропена из нефти. Именно к нему мы сейчас и обратимся.
Выделение пропилена
На самом деле в теоретическом понимании основным способом является лишь один процесс: пиролиз нефти и попутных газов. Но вот технологических реализаций — просто море. Дело в том, что каждая компания стремится получить уникальный способ и защитить его патентом, а другие такие же компании также ищут свои способы, чтобы всё-таки производить и продавать пропен как сырьё или же превращать его в различные продукты.
Пиролиз («пиро» — огонь, «лиз» — разрушение) — химический процесс распада сложной и большой молекулы на более мелкие под действием высокой температуры и катализатора. Нефть, как известно, представляет собой смесь углеводородов и состоит из лёгких, средних и тяжёлых фракций. Из первых, самых низкомолекулярных, и получают пропен и этан при пиролизе. Проводят этот процесс в специальных печах. У самых передовых фирм-производителей этот процесс технологически различается: одни используют песок в качестве теплоносителя, другие — кварц, третьи — кокс; можно также разделить печи по их строению: бывают трубчатые и обычные, как их называют, реакторы.
Но процесс пиролиза позволяет получить недостаточно чистый пропен, так как, кроме него, там образуется огромное множество углеводородов, которые потом приходится разделять достаточно энергозатратными способами. Поэтому для получения более чистого вещества для последующей гидратации применяют также дегидрирование алканов: в нашем случае — пропана. Так же, как и полимеризация, вышеописанный процесс просто так не происходит. Отщепление водорода от молкулы предельного углеводорода происходит под действием катализаторов: оксида трёхвалентного хрома и оксида алюминия.
Ну а прежде чем перейти к рассказу о том, как происходит процесс гидратации, обратимся к строению нашего непредельного углеводорода.
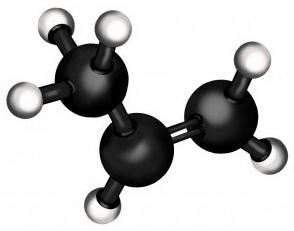
Особенности строения пропилена
Пропен сам по себе — лишь второй член ряда алкенов (углеводороды с одной двойной связью). По лёгкости он уступает лишь этилену (из которого, как можно догадаться, делают полиэтилен — самый массовый полимер в мире). В обычном состоянии пропен — газ, как и его «родственник» из семейства алканов, пропан.
Но существенное отличие пропана от пропена — в том, что последний имеет в своём составе двойную связь, которая коренным образом меняет его химические свойства. Она позволяет присоединять к молекуле непредельного углеводорода другие вещества, в результате чего получаются соединения с совершенно другими свойствами, зачастую очень важными для промышленности и быта.
Пришло время поговорить о теории реакции, которой, собственно, и посвящена эта статья. В следующем разделе вы узнаете, что при гидратации пропилена образуется один из самых промышленно важных продуктов, а также то, как происходит эта реакция и какие в ней есть нюансы.
Теория гидратации
Для начала обратимся к более общему процессу — сольватации, — который включает в себя также и описанную выше реакцию. Это химическое превращение, которое заключается в присоединении молекул растворителя к молекулам растворённого вещества. При этом они могут образовывать новые молекулы, или же так называемые сольваты, — частицы, состоящие из молекул растворённого вещества и растворителя, связанных электростатическим взаимодействием. Нас интересует только первый вид веществ, ведь при гидратации пропилена преимущественно образуется именно такой продукт.
При сольватации вышеописанным способом молекулы растворителя присоединяются к растворённому веществу, получается новое соединение. В органической химии при гидратации преимущественно образуются спирты, кетоны и альдегиды, однако есть и несколько других случаев, например образование гликолей, но их мы касаться не будем. На самом деле этот процесс очень прост, но в то же время достаточно сложен.
Механизм гидратации
Двойная связь, как известно, состоит из двух видов соединения атомов: пи- и сигма-связей. Пи-связь при реакции гидратации разрывается всегда первой, так как она менее прочная (обладает меньшей энергией связи). При её разрыве образуются две вакантные орбитали у двух соседних атомов углерода, которые могут образовать новые связи. Молекула воды, существующая в растворе в виде двух частиц: гидроксид-иона и протона, способна присоединяться по разорвавшейся двойной связи. При этом гидроксид-ион присоединяется к центральному атому углерода, а протон — ко второму, крайнему. Таким образом, при гидратации пропилена преимущественно образуется пропанол 1, или изопропиловый спирт. Это очень важное вещество, так как при его окислении можно получить ацетон, массово используемый в нашем мире. Мы сказали, что он образуется преимущественно, однако это не совсем так. Надо сказать так: единственный продукт образуется при гидратации пропилена, и это — изопропиловый спирт.
Это, конечно, всё тонкости. На самом деле всё можно описать гораздо проще. И сейчас мы узнаем, как же в школьном курсе записывают такой процесс, как гидратация пропилена.
Реакция: как она происходит
В химии всё принято обозначать просто: с помощью уравнений реакций. Вот и химическое превращение обсуждаемого вещества можно описать таким способом. Гидратация пропилена, уравнение реакции которой очень простое, проходит в две стадии. Сначала разрывается пи-связь, входящая в состав двойной. Затем молекула воды в виде двух частиц, гидроксид-аниона и катиона водорода, подходит к молекуле пропилена, имеющей на данный момент два вакантных места для образования связей. Гидроксид-ион образует связь с менее гидрогенизированным атомом углерода (то есть с таким, к которому присоединено меньшее количество атомов водорода), а протон, соответственно, — с оставшимся крайним. Таким образом, получается один-единственный продукт: предельный одноатомный спирт изопропанол.
Как записать реакцию?
Сейчас мы узнаем, как химическим языком записать реакцию, отражающую такой процесс, как гидратация пропилена. Формула, которая нам пригодится: CH2 = CH — CH3. Это формула исходного вещества — пропена. Как можно видеть, у него есть двойная связь, обозначенная знаком «=», и именно в это место будет присоедняться вода, когда будет происходить гидратация пропилена. Уравнение реакции можно записать так: CH2 = CH — CH3 + H2O = CH3 — CH(OH) — CH3. Гидроксильная группа в скобочках означает, что эта часть находится не в плоскости формулы, а ниже или выше. Тут мы не можем показать углы между тремя группами, отходящими от среднего атома углерода, но скажем, что они примерно равны между собой и составляют по 120 градусов.
Где это применяется?
Мы уже говорили, что получаемое в ходе реакции вещество активно используется для синтеза других жизненно важных нам веществ. Оно очень похоже по строению на ацетон, от которого отличается только тем, что вместо гидроксогруппы там стоит кетогруппа (то есть атом кислорода, соединённый двойной связью с атомом азота). Как известно, сам ацетон находит применение в растворителях и лаках, но, кроме этого, он применяется в качестве реагента для дальнейшего синтеза более сложных веществ, таких как полиуретаны, эпоксидные смолы, уксусный ангидрид и так далее.
Реакция получения ацетона
Думаем, нелишним будет описать превращение изопропилового спирта в ацетон, тем более что реакция эта не так сложна. Для начала пропанол испаряют и при 400-600 градусах по Цельсию оксиляют кислородом на специальном катализаторе. Очень чистый продукт получается при проведении реакции на серебряной сетке.
Уравнение реакции
Не будем вдаваться в подробности механизма реакции окисления пропанола в ацетон, так как он очень сложен. Ограничимся обычным уравнением химического превращения: CH3 — CH(OH) — CH3 + O2 = CH3 — C(O) — CH3 + H2O. Как видно, на схеме всё достаточно просто, но стоит углубиться в процесс, и мы столкнёмся с рядом трудностей.
Заключение
Вот мы и разобрали процесс гидратации пропилена и изучили уравнение реакции и механизм её протекания. Рассмотренные технологические принципы лежат в основе реальных процессов, происходящих в производстве. Как оказалось, они не очень сложны, однако имеют реальную пользу для нашей повседневной жизни.
Химические свойства алкенов
Алкены – это непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствует одна двойная связь между атомами углерода С=С.
Наличие двойной связи между атомами углерода очень сильно меняет свойства углеводородов.
Химические свойства алкенов
Алкены – непредельные углеводороды, в молекулах которых есть одна двойная связь. Строение и свойства двойной связи определяют характерные химические свойства алкенов.
Двойная связь состоит из σ-связи и π-связи. Рассмотрим характеристики одинарной связи С-С и двойной связи С=С:
| Энергия связи, кДж/моль | Длина связи, нм | |
| С-С | 348 | 0,154 |
| С=С | 620 | 0,133 |
Можно примерно оценить энергию π-связи в составе двойной связи С=С:
Таким образом, π-связь — менее прочная, чем σ-связь. Поэтому алкены вступают в реакции присоединения, сопровождающиеся разрывом π-связи. Присоединение к алкенам может протекать по ионному и радикальному механизмам.
Для алкенов также характерны реакции окисления и изомеризации. Окисление алкенов протекает преимущественно по двойной связи, хотя возможно и жесткое окисление (горение).
1. Реакции присоединения
Для алкенов характерны реакции присоединения по двойной связи С=С, при которых протекает разрыв пи-связи в молекуле алкена.
1.1. Гидрирование
Алкены реагируют с водородом при нагревании и под давлением в присутствии металлических катализаторов (Ni, Pt, Pd и др.).
| Например, при гидрировании бутена-2 образуется бутан. |
| Реакция протекает обратимо. Для смещения равновесия в сторону образования бутана используют повышенное давление. |
1.2. Галогенирование алкенов
Присоединение галогенов к алкенам происходит даже при комнатной температуре в растворе (растворители — вода, CCl4).
| При взаимодействии с алкенами красно-бурый раствор брома в воде (бромная вода) обесцвечивается. Это качественная реакция на двойную связь. |
| Например, при бромировании пропилена образуется 1,2-дибромпропан, а при хлорировании — 1,2-дихлорпропан. |
Реакции протекают в присутствии полярных растворителей по ионному (электрофильному) механизму.
1.3. Гидрогалогенирование алкенов
Алкены присоединяют галогеноводороды. Реакция идет по механизму электрофильного присоединения с образованием галогенопроизводного алкана.
| Например, при взаимодействии этилена с бромоводородом образуется бромэтан. |
При присоединении полярных молекул к несимметричным алкенам образуется смесь изомеров. При этом выполняется правило Марковникова.
| Правило Марковникова: при присоединении полярных молекул типа НХ к несимметричным алкенам водород преимущественно присоединяется к наиболее гидрогенизированному атому углерода при двойной связи. |
| Например, при присоединении хлороводорода HCl к пропилену атом водорода преимущественно присоединяется к атому углерода группы СН2=, поэтому преимущественно образуется 2-хлорпропан. |
1.4. Гидратация
Гидратация (присоединение воды) алкенов протекает в присутствии минеральных кислот. При присоединении воды к алкенам образуются спирты.
| Например, при взаимодействии этилена с водой образуется этиловый спирт. |
Гидратация алкенов также протекает по ионному (электрофильному) механизму.
Для несимметричных алкенов реакция идёт преимущественно по правилу Марковникова.
| Например, при взаимодействии пропилена с водой образуется преимущественно пропанол-2. |
1.5. Полимеризация
Полимеризация — это процесс многократного соединения молекул низкомолекулярного вещества (мономера) друг с другом с образованием высокомолекулярного вещества (полимера).
nM → Mn (M – это молекула мономера)
| Например, при полимеризации этилена образуется полиэтилен, а при полимеризации пропилена — полипропилен. |
2. Окисление алкенов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на каталитическое, мягкое и жесткое.
2.1. Каталитическое окисление
Каталитическое окисление протекает под действием катализатора.
| Взаимодействие этилена с кислородом в присутствии солей палладия протекает с образованием этаналя (уксусного альдегида) |
| Взаимодействие этилена с кислородом в присутствии серебра протекает с образованием эпоксида |
2.2. Мягкое окисление
Мягкое окисление протекает при низкой температуре в присутствии перманганата калия. При этом раствор перманганата обесцвечивается.
В молекуле алкена разрывается только π-связь и окисляется каждый атом углерода при двойной связи.
При этом образуются двухатомные спирты (диолы).
| Например, этилен реагирует с водным раствором перманганата калия при низкой температуре с образованием этиленгликоля (этандиол-1,2) |
2.2. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) происходит полный разрыв двойной связи С=С и связей С-Н у атомов углерода при двойной связи. При этом вместо разрывающихся связей образуются связи с кислородом.
Так, если у атома углерода окисляется одна связь, то образуется группа С-О-Н (спирт). При окислении двух связей образуется двойная связь с атомом углерода: С=О, при окислении трех связей — карбоксильная группа СООН, четырех — углекислый газ СО2.
Поэтому можно составить таблицу соответствия окисляемого фрагмента молекулы и продукта:
| Окисляемый фрагмент | KMnO4, кислая среда | KMnO4, H2O, t |
| >C= | >C=O | >C=O |
| -CH= | -COOH | -COOK |
| CH2= | CO2 | K2CO3 |
При окислении бутена-2 перманганатом калия в среде серной кислоты окислению подвергаются два фрагмента –CH=, поэтому образуется уксусная кислота:
При окислении метилпропена перманганатом калия в присутствии серной кислоты окислению подвергаются фрагменты >C= и CH2=, поэтому образуются углекислый газ и кетон:
При жестком окислении алкенов в нейтральной среде образующаяся щелочь реагирует с продуктами реакции окисления алкена, поэтому образуются соли (кроме реакций, где получается кетон — кетон со щелочью не реагирует).
| Например, при окислении бутена-2 перманганатом калия в воде при нагревании окислению подвергаются два фрагмента –CH=, поэтому образуется соль уксусной кислоты – ацетат калия: |
| Например, при окислении метилпропена перманганатом калия в воде при нагревании окислению подвергаются фрагменты >C= и CH2=, поэтому образуются карбонат калия и кетон: |
Взаимодействие алкенов с хроматами или дихроматами протекает с образованием аналогичных продуктов окисления.
2.3. Горение алкенов
Алкены, как и прочие углеводороды, горят в присутствии кислорода с образованием углекислого газа и воды.
В общем виде уравнение сгорания алкенов выглядит так:
| Например, уравнение сгорания пропилена: |
3. Замещение в боковой цепи
Алкены с углеродной цепью, содержащей более двух атомов углерода, могут вступать в реакции замещения в боковой цепи, как алканы.
При взаимодействии алкенов с хлором или бромом при нагревании до 500 о С или на свету происходит не присоединение, а радикальное замещение атомов водорода в боковой цепи. При этом хлорируется атом углерода, ближайший к двойной связи.
| Например, при хлорировании пропилена на свету образуется 3-хлорпропен-1 |
4. Изомеризация алкенов
При нагревании в присутствии катализаторов (Al2O3) алкены вступают в реакцию изомеризации. При этом происходит либо перемещение двойной связи, либо изменение углеродного скелета. При изомеризации из менее устойчивых алкенов образуются более устойчивые. Как правило, двойная связь перемещается в центр молекулы.