Оксид серы (IV) – это кислотный оксид . Бесцветный газ с резким запахом, хорошо растворимый в воде.
- Cпособы получения оксида серы (IV)
- Химические свойства оксида серы (IV)
- SO2 — кислотный оксид
- Взаимодействие с основными оксидами и щелочами
- SO2 — активный восстановитель
- SO2 — окислитель
- H2SO3 — сернистая кислота
- Сульфиты и гидросульфиты
- Гидролиз сульфитов
- Химические свойства сульфитов
- I. Не окислительно-восстановительные реакции
- II. Окислительно-восстановительные реакции
- Please wait.
- We are checking your browser. gomolog.ru
- Why do I have to complete a CAPTCHA?
- What can I do to prevent this in the future?
- 🔥 Видео
Видео:8 класс. ОВР. Окислительно-восстановительные реакции.Скачать

Cпособы получения оксида серы (IV)
1. Сжигание серы на воздухе :
2. Горение сульфидов и сероводорода:
2CuS + 3O2 → 2SO2 + 2CuO
3. Взаимодействие сульфитов с более сильными кислотами:
Например , сульфит натрия взаимодействует с серной кислотой:
4. Обработка концентрированной серной кислотой неактивных металлов.
Например , взаимодействие меди с концентрированной серной кислотой:
Видео:Учимся составлять электронный баланс/овр/8классСкачать
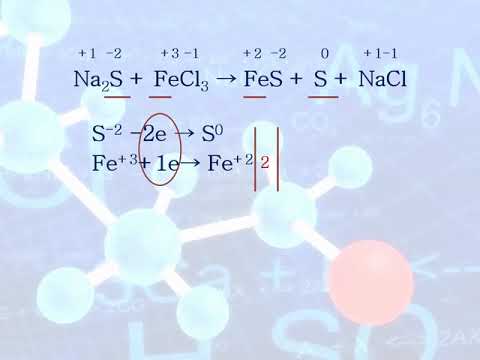
Химические свойства оксида серы (IV)
Оксид серы (IV) – это типичный кислотный оксид. За счет серы в степени окисления +4 проявляет свойства окислителя и восстановителя .
1. Как кислотный оксид, сернистый газ реагирует с щелочами и оксидами щелочных и щелочноземельных металлов .
Например , оксид серы (IV) реагирует с гидроксидом натрия. При этом образуется либо кислая соль (при избытке сернистого газа), либо средняя соль (при избытке щелочи):
SO2(изб) + NaOH → NaHSO3
Еще пример : оксид серы (IV) реагирует с основным оксидом натрия:
2. При взаимодействии с водой S O2 образует сернистую кислоту. Реакция обратимая, т.к. сернистая кислота в водном растворе в значительной степени распадается на оксид и воду.
3. Наиболее ярко выражены восстановительные свойства SO2. При взаимодействии с окислителями степень окисления серы повышается.
Например , оксид серы окисляется кислородом на катализаторе в жестких условиях. Реакция также сильно обратимая:
Сернистый ангидрид обесцвечивает бромную воду:
Азотная кислота очень легко окисляет сернистый газ:
Озон также окисляет оксид серы (IV):
Качественная реакция на сернистый газ и на сульфит-ион – обесцвечивание раствора перманганата калия:
Оксид свинца (IV) также окисляет сернистый газ:
4. В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства.
Например , при взаимодействии с сероводородом сернистый газ восстанавливается до молекулярной серы:
Оксид серы (IV) окисляет угарный газ и углерод:
SO2 + 2CO → 2СО2 + S
Видео:ОВР и Метод Электронного Баланса — Быстрая Подготовка к ЕГЭ по ХимииСкачать

SO2 — кислотный оксид
При растворении SO2 в воде происходит его частичное соединение с молекулами воды — об разуется слабая сернистая кислота.
Видео:Окислительно-восстановительные реакции. 1 часть. 9 класс.Скачать

Взаимодействие с основными оксидами и щелочами
Видео:Окислительно-восстановительные реакции в кислой среде. Упрощенный подход.Скачать

SO2 — активный восстановитель
SO2 + СаО = CaSO3 сульфит кальция
SO2 + NaOH = NaHSO3 гидросульфит натрия
Диоксид серы окисляется в газовой фазе до SO3:
На свету легко окисляется хлором:
В водных растворах при окислении SO2 образуется серная кислота H2SO4:
Обесцвечивание окрашенных окислителей (КМпO4 и Вr2) — качественная реакция для распознавания SO2 (например, отличие его от СO2, СО, СН4 и многих других газов):
Видео:ОВР для чайников — Как определить Окислитель и Восстановитель #shorts #youtubeshortsСкачать

SO2 — окислитель
Продуктом восстановления SO2 чаще всего является свободная сера.
H2SO3 — сернистая кислота
В свободном состоянии не выделена. Очень непрочное соединение. Образуется при растворении SO2 в воде. Обладает свойствами слабой кислоты.
Сульфиты и гидросульфиты
2-х основная сернистая кислота образует при взаимодействии со щелочами 2 ряда солей: нормальные (средние) — сульфиты Mex(SO3)y и кислые — гидросульфиты Me(HSO3)x.
Сульфиты щелочных Me и аммония растворимы в воде. Сульфиты остальных Me нерастворимы в воде (или не существуют).
Гидросульфиты Me хорошо растворимы в Н2O, некоторые из них существуют только в растворе, например, Ca(HSO3)2.
Видео:Составление ур-й окислительно-восст. реакций методом ионно-электронного баланса. 1ч. 10 класс.Скачать

Гидролиз сульфитов
Водные растворы сульфитов вследствие гидролиза имеют щелочную среду (окрашивают лакмус в синий цвет).
Химические свойства сульфитов
Видео:ЭТОТ метод поможет на уроках ХИМИИ / Химия 9 классСкачать

I. Не окислительно-восстановительные реакции
1. Взаимодействие с сильными кислотами:
Оба типа солей разлагаются сильными кислотами, при этом слабая сернистая кислота вытесняется в виде SO2 и Н2O.
2. Термическое разложение сульфитов:
3. Нормальные сульфиты в водных растворах, содержащих избыток SO2, превращаются в гидросульфиты
Благодаря этой реакции нерастворимые в воде сульфиты превращаются в растворимые гидросульфиты
4. Ионно-обменные реакции с другими солями, приводящие к образованию нерастворимых сульфитов:
Видео:Химические уравнения // Как Составлять Уравнения Реакций // Химия 9 классСкачать

II. Окислительно-восстановительные реакции
I. Сульфиты как восстановители.
Сульфиты, подобно SO2, могут быть и восстановителями, и окислителями, поскольку атомы серы в анионах SO3 находятся в промежуточной С.О. +4
В водных растворах и сульфиты, и гидросульфиты легко окисляются до сульфатов. Примеры реакций:
Даже твердые сульфиты при хранении на воздухе медленно окисляются до сульфатов:
II. Сульфиты как окислители.
Эти реакции не столь многочисленны. При нагревании сухих сульфитов с такими активными восстановителями, как С, Mg, Al, Zn, они переходят в сульфиды:
III. Диспропорционирование сухих сульфитов.
При нагревании до высоких температур сульфиты медленно превращаются в смесь сульфатов и сульфидов:
Видео:89. Как расставить коэффициенты реакции методом электронного баланса (закрепление)Скачать

Please wait.
Видео:РЕАКЦИИ ИОННОГО ОБМЕНА, ИОННОЕ УРАВНЕНИЕ - Урок Химия 9 класс / Подготовка к ЕГЭ по ХимииСкачать

We are checking your browser. gomolog.ru
Видео:Окислительно-восстановительные реакции. 3 часть. 9 класс.Скачать

Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
Видео:Химия, 9 класс, тема "Окислительно-восстановительные реакции" (учитель Швецова Елена Евгеньевна)Скачать

What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6de8d9b3dae49767 • Your IP : 85.95.188.35 • Performance & security by Cloudflare
🔥 Видео
Окислительно-восстановительные реакции. Видеоурок по химии 9 классСкачать

Окислительно-восстановительные реакции с нуля!| Екатерина Строганова | 100балльный репетиторСкачать

8 класс. Составление уравнений химических реакций.Скачать

Расстановка Коэффициентов в Химических Реакциях // Подготовка к ЕГЭ по ХимииСкачать

Составление уравнений химических реакций. 1 часть. 8 класс.Скачать

Химические Цепочки — Решение Цепочек Химических Превращений // Химия 8 классСкачать

Химия 9 класс — Как определять Степень Окисления?Скачать
