| Фторид меди (II) | |
|---|---|
   | |
| Систематическое наименование | меди (II) фторид |
| Сокращения | фторомедь (II) |
| Традиционные названия | дифторид меди |
| Хим. формула | CuF2 |
| Состояние | |
| Молярная масса | |
| Температура | |
| • плавления | (безводный) 950 °C, (дигидрат) 130 |
| • кипения | (безводный) 1676 °C |
| Мол. теплоёмк. | (при 298,15 K) 65.815 Дж/(моль·К) |
| Энтальпия | |
| • образования | −538.9 ± 1.3 кДж/моль |
| Растворимость | |
| • в воде | в хол. воде 0,08 г/100 мл |
| • в других веществах | растворяется в аммиаке, фтороводородной, хлороводородной и азотной кислотах; пиридине, этилацетате |
| Рег. номер CAS | 7789-19-7, 13454-88-1 (дигидрат) |
| PubChem | 522688 |
| Рег. номер EINECS | 232-147-3 |
| SMILES | |
| ChemSpider | 74214 и 455944 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
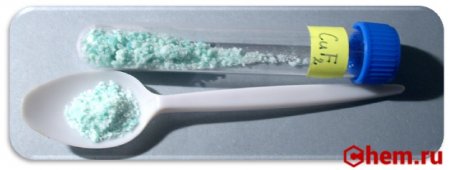
Фторид меди (II) — это неорганическое бинарное химическое соединение. Химическая формула CuF2.
- Содержание
- Физические свойства
- Получение
- Химические свойства
- Применение
- Acetyl
- Реакция термического разложения фторида меди (II)
- Реакция термического разложения фторида меди (II)
- Реакция взаимодействия гидросульфита натрия и цинка
- Реакция взаимодействия оксида молибдена (VI), серной кислоты и воды
- Реакция термического разложения тетрагидрата ортофосфата цинка
- Выбрать язык
- Популярные записи
- Предупреждение.
Содержание
- 1 Физические свойства
- 2 Получение
- 3 Химические свойства
- 4 Применение
Физические свойства
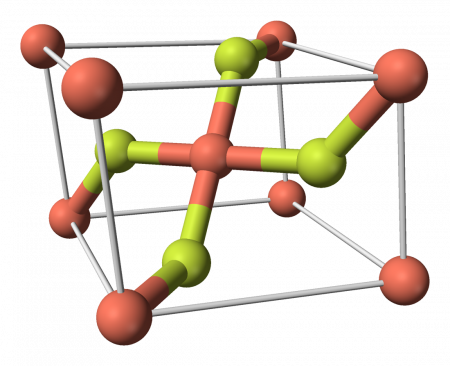
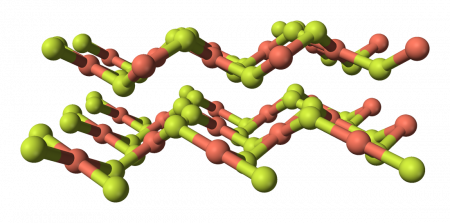
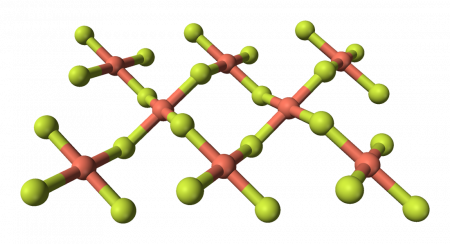
Безводный фторид меди это белые гигроскопические кристаллы кубической сингонии, пространственная группа Fm3m, a = 0,5417 нм, Z=4, структура типа CaF2.
Образует кристаллогидрат CuF2·2H2O — светло-голубые кристаллы, при нагревании плавится в собственной воде.
Получение
Фторид меди (II) можно получить из гидроокиси меди:
Фторид меди(I) при нагревании диспропорционирует:
2CuF → to CuF2 + Cu
Фторид меди (II) можно синтезировать непосредственно из элементов:
При температуре в 400 °C фтор вытесняет из хлорида меди (II) хлор:
При температуре в 375 °C фторид азота (III) с медью реагирует с образованием тетрафторгидразина и фторида меди (II):
Химические свойства
Восстанавливается до меди водородом:
Разлагается парами воды.
Взаимодействует с щелочами:
Соединение теряет фтор будучи расплавленным в температурах выше 950 °C:
В растворах, содержащих фторид-ион F − , образует комплексные анионы, например, CuF3 − , CuF4 2− и CuF6 4− :
Применение
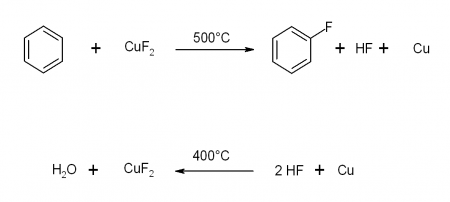
Было выяснено, что ароматические углеводороды реагируют со фторидом меди (II) в кислородсодержащей атмосфере при температурах выше 450 °C, образуя фторированные ароматические углеводороды.
Данная реакция, показанная на рисунке слева, является более простой, чем реакция Сандмайера, но применима только для соединений, которые являются достаточно стабильными при высоких температурах.
Применяется в качестве инсектицида и в производстве керамики.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Реакция термического разложения фторида меди (II)Реакция термического разложения фторида меди (II)Уравнение реакции термического разложения фторида меди (II): Реакция термического разложения фторида меди (II). В результате реакции образуются медь и фтор. Реакция протекает при условии: при температуре выше 950 °C. Формула поиска по сайту: CuF2 → Cu + F2. Реакция взаимодействия гидросульфита натрия и цинкаРеакция взаимодействия оксида молибдена (VI), серной кислоты и водыРеакция термического разложения тетрагидрата ортофосфата цинкаВыбрать языкПопулярные записиПредупреждение.Все химические реакции и вся информация на сайте предназначены для использования исключительно в учебных целях — только для решения письменных, учебных задач. Мы не несем ответственность за проведение вами химических реакций. Химические реакции и информация на сайте |