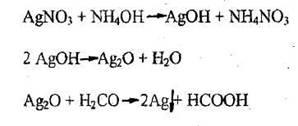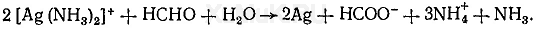В книжной версии
Том 28. Москва, 2015, стр. 338-339
Скопировать библиографическую ссылку:
РЕЗОРЦИ́НО-ФОРМАЛЬДЕГИ́ДНЫЕ СМО́ЛЫ, олигомерные продукты поликонденсации формальдегида с резорцином; относятся к группе фенольных смол синтетических. Общая формула:
Формальдегид. Химико-токсикологический анализ.
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Формальдегид
Формальдегид (от лат. formica «муравей») — бесцветный газ с резким запахом, хорошо растворимый в воде, спиртах и полярных растворителях. Ирритант, токсичен.
Формальдегид НСНО (муравьиный альдегид, метаналь) представляет собой бесцветный газ с резким раздражающим запахом. Хорошо растворим в воде, спиртах и других полярных растворителях. Чистый газообразный формальдегид относительно стабилен при 80-100 °С, при температурах ниже 80 °С полимеризуется; процесс ускоряется в присутствии полярных растворителей, в том числе воды.
Формалин – водный раствор формальдегида (обычно 37 – 40 %), содержащий 6-15 % метанола (ингибитор полимеризации формальдегида). Представляет собой бесцветную жидкость с характерным острым запахом.
Формальдегид используют в органическом синтезе, в производстве синтетических смол и пластмасс, для синтеза многих лекарственных средств и красителей, для дубления кож, как дезинфицирующее, антисептическое и дезодорирующее средство.
При вдыхании воздуха, содержащего большое количество формальдегида, развиваются явления острого отравления со слезотечением, резким кашлем, чувством стеснения в груди.
При приёме внутрь (в большинстве случаев ошибочном) в результате всасывания формальдегида наблюдается потеря сознания, судороги, угнетение нервных центров, раздражение почек.
Качественное обнаружение
- Реакция с резорцином в щелочной среде
Появляется розовая или малиновая окраска.
Реакция не специфична (дают алкилгалогениды и др.).
Чувствительность 0,03 мкг.
- Реакция с реактивом Фелинга
В пробирку вносят 1 мл исследуемого раствора, прибавляют 1–2 кап. 10% раствора гидроксида натрия до щелочной реакции (по лакмусу), а затем добавляют 2-3 кап. реактива Фелинга (готовится перед употреблением путем смешивания равных количеств растворов Фелинга №1 и №2).
Жидкость сильно взбалтывают и нагревают. При охлаждении на дне пробирки виден желтый или красный осадок оксида меди (I).
Реакция не специфична (дают алкилгалогениды и другие). Имеет отрицательное судебно-химическое значение.
3. Реакция с фуксинсернистой кислотой (реактив Шиффа)
Появляется сине- или красно-фиолетовая окраска, иногда не сразу, а через 10-15 мин.
Чувствительность реакции 0,03 мкг.
4. Реакция с кодеином и концентрированной серной кислотой
Через 5-10 мин. появляется сине – или красно-фиолетовое окрашивание.
Реакция специфична, имеет положительное судебнохимическое значение.
Чувствительность реакции 0,02 мкг.
- Реакция с хромотроповой кислотой (1,8-диоксинафталтн-3,6-дисульфокислота) в присутствии концентрированной серной кислоты
В фарфоровую чашку вносят 1 мл исследуемого раствора, а затем прибавляют 5 мл концентрированной кислоты серной и несколько кристаллов кислоты хромотроповой. Наблюдается фиолетовая или красно-фиолетовая окраска.
Реакция специфична, имеет положительное судебно-химическое значение. Чувствительность 1 мкг.
- Реакция восстановления ионов серебра (реакция «серебряного зеркала»)
Реакция не специфична, имеет отрицательное судебно-химическое значение.
Чувствительность реакции – сотые доли микрограмма.
§ 7. ФОРМАЛЬДЕГИД
Формальдегид (альдегид муравьиной кислоты)—газ, хорошо растворимый в воде, обладающий острым специфическим запахом. Водный раствор, содержащий 36,5—37,5 % формальдегида, называется формалином. Формальдегид образуется при неполном сгорании метана, при окислении метилового спирта и т. д. Газообразный формальдегид при комнатной температуре легко полимеризуется с образованием параформальдегида. Известно несколько продуктов полимеризации газообразного формальдегида. Один из полимеров формальдегида называется триоксиметилен (СН 2 О) 3. Он имеет температуру плавления 63—64°С. В водных растворах также образуется параформальдегид, относящийся к полиоксиметиленам, которые являются продуктами полимеризации значительно большего числа молекул формальдегида. ПараформаЛьдегид при нагревании, особенно в присутствии кислот, частично деполимеризуется с образованием газообразного формальдегида.
Формальдегид изолируют из биологического материала путем перегонки с водяным паром. Однако этим методом перегоняется только незначительная часть формальдегида. Считают, что формальдегид в водных растворах находится в виде гидрата (метиленгликоля), который трудно отгоняется с водяным паром:
Применение. Действие на организм. Формальдегид широко используется в промышленности для получения пластических масс и фенолоформальдегидных смол, дубления кож, консервирования анатомических препаратов, получения гексаметилентетрамина, синтетического каучука, протравливания зерна, обработки помещений, тары с целью дезинфекции.
Формальдегид проявляет дубящее, антисептическое и дезодорирующее действие., При вдыхании небольших количеств формальдегида он раздражает верхние дыхательные пути. При вдыхании больших концентраций формальдегида может наступить внезапная смерть в результате отека и спазма голосовой щели. При попадании формальдегида в организм через рот могут наступить некротические поражения слизистой оболочки рта, пищевого канала, появляется слюнотечение, тошнота, рвота, понос. Формальдегид угнетает центральную нервную систему, в результате этого может произойти потеря сознания, появляются судороги. Под влиянием формальдегида развиваются дегенеративные поражения печени, почек, сердца и головного мозга. Формальдегид оказывает влияние на некоторые ферменты. 60—90 мл формалина являются смертельной дозой.
В химико-токсикологическом анализе для обнаружения формальдегида Η—СНО применяют реакции с хромотроповой кислотой, фуксинсернистой кислотой, с раствором кодеина в серной кислоте, с резорцином и др.
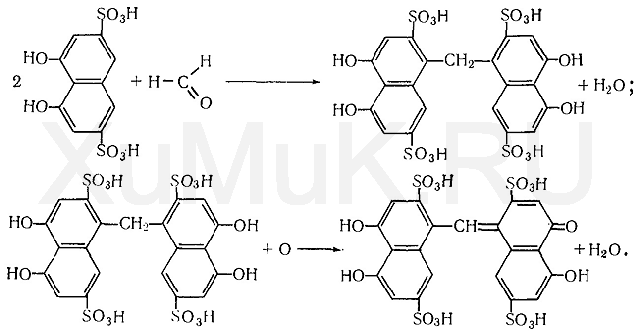
Реакция с хромотроповой кислотой. Хромотроповая кислота (1,8-диоксинафталин-3,6-дисульфокислота) с формальдегидом в присутствии серной кислоты дает фиолетовую окраску. При взаимодействии формальдегида с хромотроповой кислотой концентрированная серная кислота одновременно является водо-
отнимающим средством и окислителем. Вначале серная кислота вызывает конденсацию формальдегида с хромотроповой кислотой, а затем окисляет образовавшийся продукт конденсации:
Для успешного протекания указанной выше реакции требуется серная кислота, концентрация которой должна быть не ниже 72 %.
Выполнение реакции. В пробирку вносят 3—5 капель исследуемого раствора или дистиллята, 4 мл 12 н. раствора серной кислоты и несколько кристалликов хромотроповой кислоты, а затем пробирку нагревают в течение 10 мин на водяной бане до 60 °С. При наличии формальдегида в пробе появляется фиолетовая окраска.
Второй вариант реакции. В пробирку вносят 1 мл исследуемого раствора, 0,2 мл 1 %-го раствора хромотроповой кислоты в концентрированной серной кислоте, а затем прибавляют 5 мл концентрированной серной кислоты и взбалтывают. Появление фиолетовой или красно-фиолетовой окраски указывает на наличие формальдегида в исследуемом растворе.
Предел обнаружения: 1 мкг формальдегида в пробе.
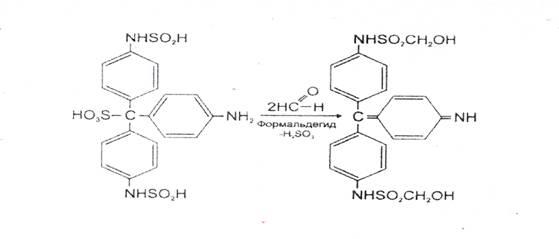
Реакция с фуксинсернистой кислотой. Фуксинсернистая кислота (реактив Шиффа) с формальдегидом дает синюю или сине-фиолетовую окраску.
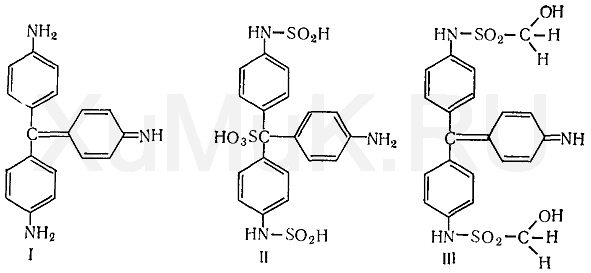
Для приготовления фуксинсернистой кислоты берут раствор парафуксина (I), имеющий красную окраску, прибавляют водный раствор оксида серы (IV) или пропускают газообразный SO 2. При этом образуется фуксинсернистая кислота (II), не имеющая окраски. Эта кислота с альдегидами образует хиноидный краситель (III) розового цвета:
Выполнение реакции. В пробирку вносят 1 мл исследуемого раствора и 2—3 капли концентрированной серной кислоты. Содержимое пробирки взбалтывают и охлаждают проточной водой, затем прибавляют 1 мл раствора фуксинсернистой кислоты. Появление сине-фиолетовой или красно-фиолетовой окраски указывает на наличие формальдегида.
Раствор иногда окрашивается не сразу, а через 10—15 мин. Окраска может появляться не только под влиянием формальдегида, но и под влиянием окислителей (хлор, оксиды азота, кислород воздуха и др.). Поэтому появление окраски через 30 мин после прибавления реактивов не должно рассматриваться как положительный результат реакции на формальдегид.
Эта реакция не специфична для обнаружения формальдегида. Ее дают ацетальдегид, нитробензальдегид и др. Не дает указанной окраски хлоралгидрат. В сильно кислой среде (рН = 0,7) с фуксинсернистой кислотой реагирует только формальдегид. При рН >= 2,7 с фуксинсернистой кислотой реагирует ацетальдегид, фурфурол и др.
Приготовление реактива (см. Приложение 1, реактив 56).
Выполнение реакции. В пробирку вносят 1 мл исследуемого раствора и 0,5 мл 10 %-го раствора серной кислоты, а затем прибавляют такой же объем раствора метилового фиолетового, обесцвеченного сульфитом или гидросульфитом натрия. При наличии формальдегида в пробе появляется сине-фиолетовая окраска. Эта реакция не специфична для обнаружения формальдегида. Ее дают и некоторые другие альдегиды.
Приготовление реактива (см. Приложение 1, реактив 21).
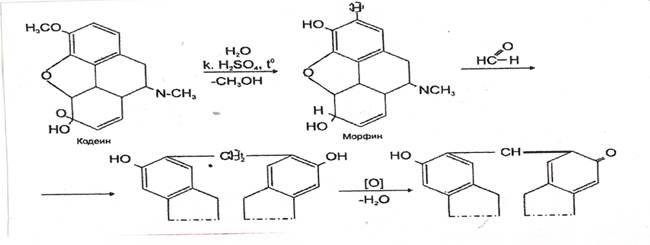
Реакция с кодеином и серной кислотой. При нагревании формальдегида с кодеином в присутствии концентрированной серной кислоты появляется синяя окраска. Эта реакция основана на том, что под влиянием концентрированной серной кислоты от кодеина отщепляется метоксильная группа, в результате чего
образуется морфин, содержащий фенольную группу. При взаимодействии морфина с формальдегидом появляется синяя окраска.
Выполнение реакции. В фарфоровую чашку вносят 1 мл исследуемого раствора и прибавляют 5 мл концентрированной серной кислоты. После охлаждения жидкости прибавляют 0,02— 0,03 г кодеина. При наличии формальдегида сразу или через 5—10 мин появляется сине-фиолетовая или красно-фиолетовая окраска.
Предел обнаружения: 0,02 мкг формальдегида.
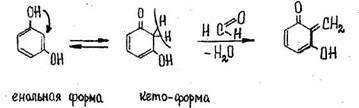
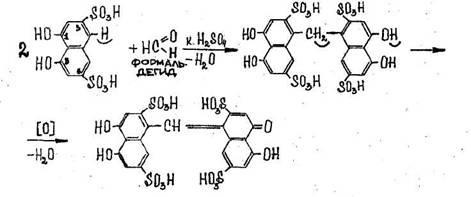
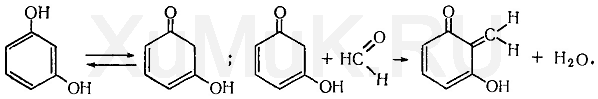
Реакция с резорцином. Альдегиды реагируют с резорцином в его таутомерной форме (кетоформе) с образованием окрашенного соединения:
Выполнение реакции. В пробирку вносят 1 мл исследуемого раствора и 1 мл 1 %-го раствора резорцина в 10 %-м растворе гидроксида натрия. Смесь нагревают в течение 3—5 мин на водяной бане. Появление розовой или малиновой окраски указывает на наличие формальдегида. Эту реакцию дают уксусный альдегид, акролеин, фурфурол и др.
Выполнение реакции. В хорошо очищенную от жира пробирку вносят 5 капель 1 %-го раствора нитрата серебра и по каплям прибавляют 10%-й раствор аммиака до растворения образовавшегося осадка гидроксида серебра. К полученному раствору прибавляют 1 мл исследуемого раствора, а затем смесь осторожно нагревают на пламени горелки. При наличии формальдегида происходит реакция образования «серебряного зеркала». Эта реакция успешно протекает при рН = 8. 9. Нагревание пробирки должно быть умеренным. При высокой температуре «серебряное зеркало» не образуется, а выпадает бурый осадок серебра.
Кроме формальдегида эту реакцию дают и некоторые другие восстанавливающие вещества.
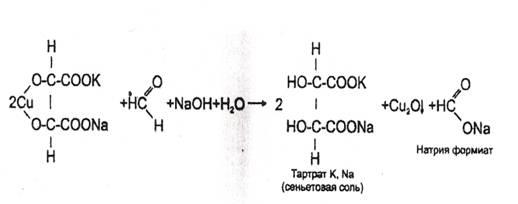
Реакция с реактивом Фелинга. При нагревании реактива Фелинга с формальдегидом выпадает осадок оксида или гидроксида меди. Оксид меди (I) имеет черную окраску. Окраска гидроксида меди (I) зависит от размера частиц. Очень мелкие частицы имеют голубовато-зеленую окраску, а крупные — красную. Поэтому при взаимодействии реактива Фелинга с восстановителями в большинстве случаев выпадает желтый или красный осадок.
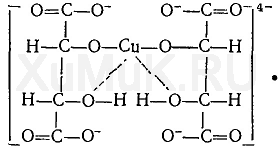
В реактиве Фелинга, который представляет собой смесь сульфата меди, щелочи и сегнетовой соли, медь входит в состав комплексного иона:
Выполнение реакции. 1 мл исследуемого раствора вносят в пробирку, в которую прибавляют 1—2 капли 10 %-го раствора гидроксида натрия до щелочной реакции (по лакмусу), а затем прибавляют 2—3 капли реактива Фелинга. Жидкость интенсивно взбалтывают и нагревают на пламени газовой горелки. Образование желтого или красного осадка указывает на наличие формальдегида в исследуемом растворе.
Эта реакция не специфична. Кроме формальдегида ее дают и другие альдегиды алифатического ряда, восстанавливающие сахара и др.
Приготовление реактива (см. Приложение 1, реактив 42).