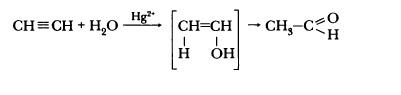Он хорошо растворим в воде, спирте и эфире.
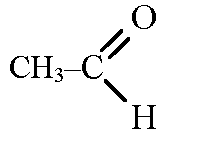
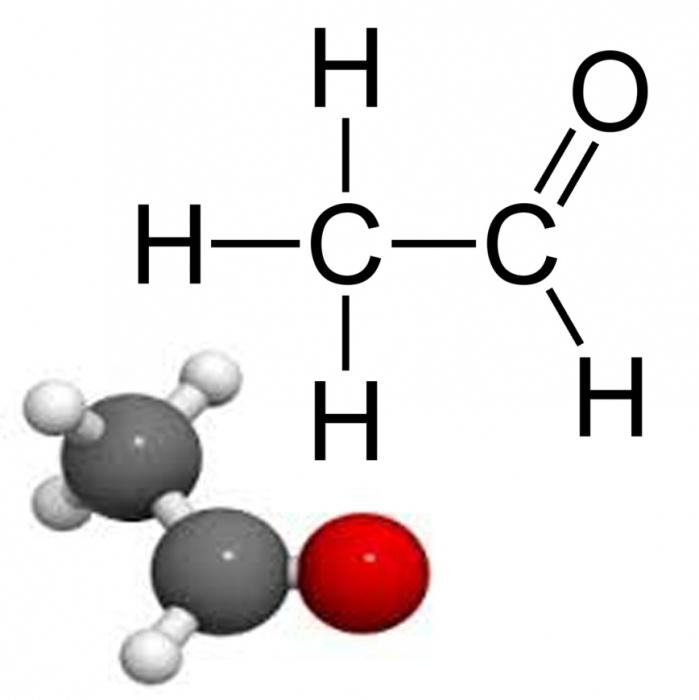
Рис. 1. Строение молекулы этаналя.
Таблица 1. Физические свойства этаналя.
Плотность (0 o С), г/см 3
Температура плавления, o С
Температура кипения, o С
Получение этаналя
Наиболее популярным способом получения этаналя является окисление этанола:
Кроме этого используются и другие реакции:
- пиролиз кальциевый (бариевых) солей карбоновых кислот:
- гидратация ацетилена и его гомологов (реакция Кучерова)
- каталитическое окисление ацетилена
Химические свойства этаналя
Типичные реакции, характерные для этаналя – реакции нуклеофильного присоединения. Все они протекают преимущественно с расщеплением:
- p-связи в карбонильной группе
— присоединение синильной кислоты
— присоединение гидросульфита натрия
- связи С-Н в карбонильной группе
— окисление аммиачным раствором оксида серебра (реакция «серебряного зеркала») – качественная реакция
— окисление гидроксидом меди (II)
Применение этаналя
Этаналь используется в основном для производства уксусной кислоты и в качестве исходного сырья для синтеза многих органических соединений. Кроме этого этаналь и его производные идут на изготовление некоторых лекарств.
Примеры решения задач
| Задание | Эквимолекулярная смесь ацетилена и этаналя полностью реагирует с 69,6 г Ag2O, растворенного в аммиаке. Определите состав исходной смеси. |
| Решение | Запишем уравнения реакций, указанных в условии задачи: |
Рассчитаем количество вещества оксида серебра (I):
n(Ag2O) = 69,6 / 232 = 2,6 моль.
По уравнению (2) количество вещества этаналя будет равно 0,15 моль. По условию задачи смесь эквимолекулярна, следовательно, ацетилена тоже будет 0,15 моль.
Найдем массы веществ, составляющих смесь:
M(HC≡CH) = 26 г/моль;
m(HC≡CH) = 0,15× 26 = 3,9 г;
| Задание | При каталитическом гидрировании 55 г этаналя образовалась карбоновая кислота. Рассчитайте какая масса кислоты была получена. |
| Решение | Запишем уравнение реакции каталитического окисления этаналя: |
Вычислим количество вещества этаналя (молярная масса равна 44 г/моль):
n(CH3-C(O)H) = 55 / 44 = 1,25 моль.
Согласно уравнению реакции n(CH3-C(O)H) : n(CH3-COOH) = 1:1, т.е.
Тогда масса уксусной кислоты будет равна (молярная масса – 60 г/моль):
На сегодняшний день известны миллионы химических соединений. И большинство из них относится к органическим. Эти вещества делят на несколько больших групп, название одной из них — альдегиды. Сегодня мы рассмотрим представителя этого класса — уксусный альдегид.
Определение
Уксусный альдегид является органическим соединением класса альдегидов. Его могут называть и по-другому: ацетальдегидом, этаналем или метилформальдегидом. Формула уксусного альдегида — CH3-CHO.
Свойства
Получение
В основном уксусный альдегид получают с помощью окисления этилена (процесс Вакера). В роли окислителя выступает хлорид палладия. Еще данное вещество можно получить во время гидратации ацетилена, в которой присутствуют соли ртути. Продуктом реакции является енол, который изомеризуется в искомое вещество. Еще один способ получения уксусного альдегида, который был наиболее популярным задолго до того, как стал известен процесс Вакера, — окисление или дегидратация этанола в присутствии медного или серебряного катализаторов. При дегидратации, помимо искомого вещества, образуется водород, а во время окисления — вода.
Применение
С помощью обсуждаемого соединения получают бутадиен, альдегидные полимеры и некоторые органические вещества, в том числе и одноименную кислоту. Она образуется при его окислении. Реакция выглядит так: «кислород + уксусный альдегид = уксусная кислота». Этаналь — важный прекурсор ко многим производным, и это свойство широко применяется в синтезе
многих веществ. В организмах человека, животных и растений ацетальдегид является участником некоторых сложных реакций. Также он входит в состав сигаретного дыма.
Заключение
Ацетальдегид может приносить как пользу, так и вред. Он плохо воздействует на кожу, является ирритантом и, возможно, канцерогеном. Поэтому его присутствие в организме нежелательно. Но некоторые люди сами провоцируют появление ацетальдегида, куря сигареты и употребляя алкоголь. Подумайте над этим!
Общая характеристика
Уксусный альдегид имеет несколько названий: ацетальдегид, этаналь, метилформальдегид. Это соединение является альдегидом уксусной кислоты и этанола. Его структурная формула выглядит следующим образом: CH3-CHO.
Рис. 1. Химическая формула уксусного альдегида.
Особенностью этого альдегида является то, что он встречается как в природе, так и производится искусственным путем. В промышленности объем производства этого вещества может составлять до 1 миллиона тонн в год.
Этаналь встречается в пищевых продуктах, таких как кофе, хлеб, а также это вещество синтезируют растения в процессе метаболизма.
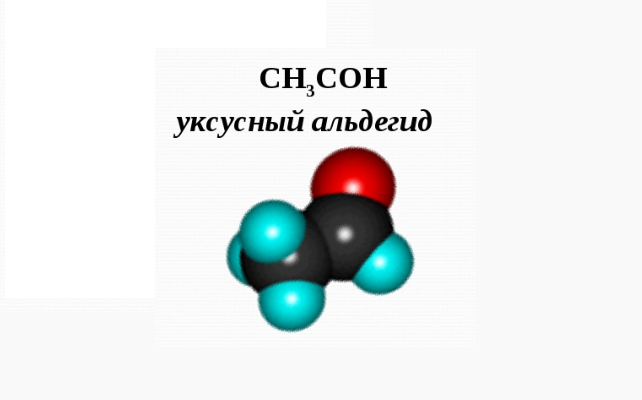
Уксусный альдегид представляет собой жидкость без цвета, но отличающуюся резким запахом. Растворим в воде, спирте и эфире. Является ядовитым.
Рис. 2. Уксусный альдегид.
Жидкость закипает при достаточно низкой температуре – 20,2 градуса по Цельсию. Из-за этого возникают проблемы с ее хранением и транспортировкой. Поэтому хранят вещество в виде паральдегида, а ацетальдегид из него получают в случае необходимости путем нагревания с серной кислотой (либо с любой другой минеральной кислотой). Паральдегид – это циклический тример уксусной кислоты.
Способы получения
Получить уксусный альдегид можно несколькими способами. Самый распространенный вариант – окисление этилена или, как еще называют этот способ, процесс Вакера:
Окислителем в данной реакции выступает хлорид палладия.
Также уксусный альдегид можно получить пр взаимодействии ацетилена с солями ртути. Данная реакция носит имя русского ученого и называется реакцией Кучерова. В результате химического процесса образуется енол, который изомеризуется в альдегид
Рис. 3. М. Г. Кучеров портрет.
До открытия метода Вакера в 60-ые годы уксусный альдегид получали при помощи этилового спирта. Этиловый спирт окисляли или дегидрировали. В качестве катализатора выступали медь или серебро:
По химическим свойствам ацетальдегид является типичным представителем альдегидов.
Применяют в промышленности данное вещество для получения уксусной кислоты, бутадиена и различных органических веществ.
Что мы узнали?
Уксусный альдегид – жидкость, имеющая несколько названий. Это вещество имеет свойство кипеть уже при температуре 20,2 градуса. Существуют два основных способа с помощью которых получают этот альдегид: реакция Вакера и реакция Кучерова.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Уравнение реакции этаналь уксусная кислотаВопрос по химии: Как из этаналя получить уксусную кислоту. Уравнение реакции,пожалуйста. Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ? Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок — бесплатно! Ответы и объяснения 2СН3СОН+Аg2О->СН3СООН+2Аg Существует куча методов, но все они сводятся к окислению этаналя: Например: Знаете ответ? Поделитесь им!Как написать хороший ответ?Чтобы добавить хороший ответ необходимо:
Этого делать не стоит:
Есть сомнения?Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия. Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы! Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются. |