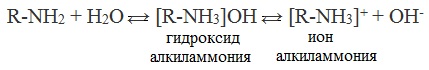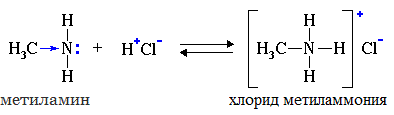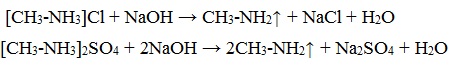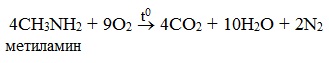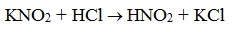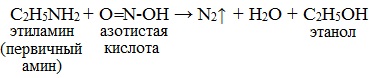Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
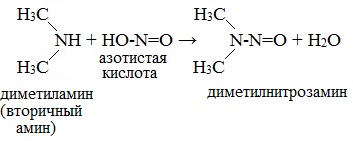
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Опыты по химии. АминыБромирование анилина Аминогруппа влияет на свойства бензольного кольца. Она делает его более реакционноактивным. К насыщенному водному раствору анилина прильем бромную воду. Раствор мутнеет. Выпадает белый осадок 2,4,6-триброманилина. С6Н5NH2 + 3 Br2 = C6H2Br3 + 3HBr Оборудование: пробирки, штатив для пробирок. Техника безопасности. Соблюдать правила работы с ядовитыми веществами и бромом. Постановка опыта и текст – к.п.н. Павел Беспалов. Взаимодействие анилина с соляной кислотой Анилин – слабое основание. С сильными кислотами анилин способен образовывать соли. Приготовим смесь анилина с водой. Прибавим к смеси соляную кислоту. Происходит растворение анилина. В растворе образуется солянокислый анилин или хлорид фениламмония С6Н5NH2 + HCI = [C6H5NH3] CI Оборудование: пробирки, штатив для пробирок. Техника безопасности. Соблюдать правила работы с ядовитыми веществами и кислотами. Постановка опыта и текст – к.п.н. Павел Беспалов. Изучение среды раствора анилина Анилин мало растворим в воде. При 18 о С в 100 мл воды растворяется 3,6г. анилина. Раствор анилина не изменяет окраски индикаторов. Возьмем пробу раствора анилина. Добавим в пробирку лакмус. Окраска индикатора не изменяется, это значит, что раствора анилина имеет нейтральную реакцию среды. Оборудование: пробирка, штатив для пробирок. Оборудование: пробирка, штатив для пробирок. Техника безопасности. Соблюдать правила работы с ядовитыми веществами и кислотами. Постановка опыта и текст – к.п.н. Павел Беспалов. Изучение физических свойств анилина Анилин – бесцветная маслянистая жидкость. При хранении анилин постепенно окисляется и приобретает вначале желтую, затем бурую окраску. Изучим растворимость анилина в воде. Прибавим анилин к воде и перемешаем раствор. Анилин мало растворим в воде. При 18 о С в 100 мл воды растворяется всего 3,6г. анилина. Раствор анилина не изменяет окраски индикаторов. Оборудование: пробирки, штатив для пробирок. Техника безопасности. Соблюдать правила работы с ядовитыми веществами. Постановка опыта и текст – к.п.н. Павел Беспалов. Качественное определение азота в органических соединениях Очень чувствительным методом определения азота в органических соединениях является сплавление вещества с металлическим натрием. Небольшую порцию анализируемого вещества сплавляем с кусочком металлического натрия. Важно, чтобы весь натрий прореагировал или окислился. Когда весь натрий прореагировал, охлаждаем пробирку, заливаем ее водой и кипятим. К полученному раствору добавляем крупинку сульфата железа (II) и вновь нагреваем. Затем добавляем соляную кислоту. Появление синего окрашивания свидетельствует о наличии азота в исследуемом органическом соединении. При сплавлении натрия с азотсодержащим веществом образуется цианид натрия. С солью двухвалентного железа цианид натрия образует гексацианоферрат (II) натрия. Так как сульфат железа (II) всегда содержит примесь железа (III), то с железом (III) гексацианоферрат натрия образует берлинскую лазурь. Появляется голубое окрашивание. Оборудование: штатив для пробирок, пробирки, горелка, зажим для пробирок, стакан, фильтровальная бумага, скальпель, пинцет. Техника безопасности. Соблюдать правила работы со щелочными металлами. Постановка опыта и текст – к.п.н. Павел Беспалов. Окисление анилина раствором дихромата калия Окисление анилина дихроматом калия позволяет получить важный промышленный краситель – черный анилин. К насыщенному раствору дихромата калия прибавим раствор серной кислоты и эмульсию анилина. Жидкость окрашивается в зеленый цвет, который постепенно переходит в черный. Образуется черный анилин — нерастворимый в воде краситель. Оборудование: пробирки, штатив для пробирок. Техника безопасности. Соблюдать правила работы с ядовитыми веществами и кислотами. Постановка опыта и текст – к.п.н. Павел Беспалов. Окисление анилина раствором хлорной извести Определить наличие анилина в растворе можно с помощью раствора хлорной извести. К сильно разбавленному раствору анилина добавим отфильтрованный раствор хлорной извести. Раствор становится синим. Реакция с хлорной известью – качественная реакция на анилин, она основана на легкой окисляемости анилина. Реакция очень чувствительна и позволяет определить даже следы анилина. Оборудование: пробирки, штатив для пробирок. Техника безопасности. Соблюдать правила работы с ядовитыми веществами. Постановка опыта и текст – к.п.н. Павел Беспалов. Получение гидроксида диметиламмония и изучение его свойств Амины с водой образуют достаточно сильные основания. Приготовим раствор диметиламина в воде. Газ диметиламин хорошо растворяется в воде. При этом образуется гидроксид диметиламмония (гидрат диметиламина) (СН3)2NH + H2O = [(СН3)2NH2]ОН Пробу гидроксида диметиламмония (гидрата диметиламина) испытаем раствором фенолфталеина. Фенолфталеин приобретает малиновую окраску: среда раствора – щелочная. К следующей порции раствора прибавим раствор хлорида железа (III) – выпадает бурый осадок гидроксида железа. 3[(СН3)2NH2]ОН + FeCI3 = Fe(OH)3 ↓+ 3[(СН3)2NH2]CI Вносим палочку, смоченную концентрированной соляной кислотой, в выделяющийся газ диметиламин, образуется густой белый дым. Дым – кристаллы гидрохлорида диметиламина. (СН3)2NH + HCI = [(СН3)2NH2] CI Оборудование: пробирки, штатив для пробирок, горелка. Техника безопасности. Соблюдать правила работы со щелочами, кислотами. Правила работы нагревательными приборами. Постановка опыта и текст – к.п.н. Павел Беспалов. Получение диметиламина и его горение Получим диметиламин действием гидроксида натрия на хлорид диметиламина. Смешаем в пробирке хлорид диметиламина со щелочью и прибавим воды. При легком нагревании выделяется газ диметиламин. [(СН3)2NH2] CI + NaOH = (СН3)2NH + NaCI + H2O При поджигании диметиламин сгорает с образованием углекислого газа, водяных паров и азота. 4(СН3)2NH +15 O2 = 8CO2 + 14H2O + 2N2 Оборудование: штатив для пробирок, пробирки, горелка, зажим для пробирок, газоотводная трубка. Техника безопасности. Соблюдать правила работы со щелочами и нагревательными приборами. Постановка опыта и текст – к.п.н. Павел Беспалов. Уравнение реакции диметиламина с соляной кислотойАмины, являясь производными аммиака, имеют сходное с ним строение и проявляют подобные ему свойства. I. Свойства аминов как оснований Химические свойства алифатических аминов определяются главным образом наличием у атома азота неподеленной пары электронов.За счет неподеленной пары электронов атома азота амины способны присоединять протон, проявляя при этом основные свойства. Связь протона с амином, как и с аммиаком, образуется по донорно-акцепторному механизму. Амины – органические основания. Водные растворы алифатических аминов (алкиламинов) имеют щелочной характер, т.к. при взаимодействии с водой образуются гидроксиды алкиламмония, аналогичные гидроксиду аммония: Механизм реакции Общее уравнение реакции Амины изменяют окраску индикаторов. Видеоопыт «Получение гидроксида диметиламмония и изучение его свойств» 2. Взаимодействие с кислотами (реакция нейтрализации) Алкиламины как основания образуют соли с минеральными кислотами, которые являются аналогами солей аммония: С органическими кислотами возможны аналогичные реакции: Соли аминов – твердые вещества, хорошо растворимые в воде и плохо растворимые в неполярных органических растворителях. Щелочи, как более сильные основания, вытесняют амины из их солей: Способность к образованию растворимых солей с последующим их разложением под действием оснований часто используют для выделения и очистки аминов, не растворимых в воде. II. Окисление аминов Алифатические амины окисляются под действием сильных окислителей. В отличие от аммиака, низшие газообразные амины способны воспламеняться от открытого пламени. Реакция горения (полное окисление) Продуктами горения аминов, как и других азотсодержащих органических соединений, являются углекислый газ, вода и свободный азот: Видеоопыт «Получение диметиламина и его горение» III. Взаимодействие с азотистой кислотой (отличие первичных аминов от вторичных и третичных) Качественная реакция на амины! Азотистая кислота HNO2 — неустойчивое соединение, поэтому ее получают непосредственно в процессе реакции действием сильной минеральной кислоты (НСl, H2SO4) на соль азотистой кислоты (нитрит): Строение продуктов реакции с азотистой кислотой зависит от характера амина. Поэтому данная реакция используется для различения первичных, вторичных и третичных аминов. Важное практическое значение имеет реакция азотистой кислоты с первичными ароматическими аминами. При действии азотистой кислоты на первичные амины выделяется свободный азот и образуются спирты: Вторичные амины с азотистой кислотой дают N-нитрозамины – маслянистые жидкости с характерным запахом: Третичные алифатические амины с азотистой кислотой не реагируют. |

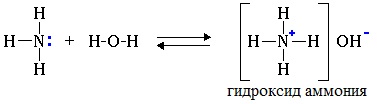
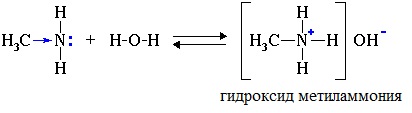
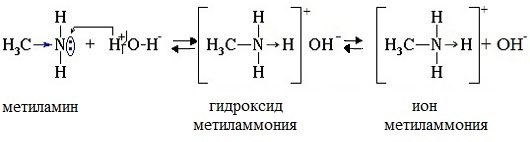
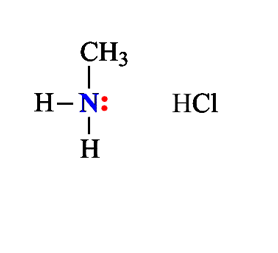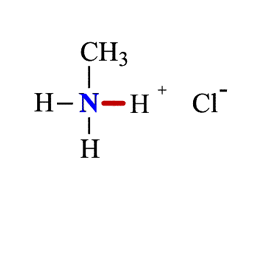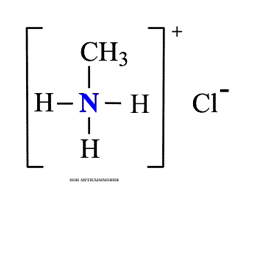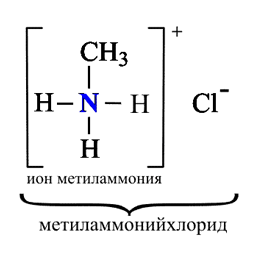 1. Взаимодействие с водой
1. Взаимодействие с водой